2023-2024学年高中化学苏教版2019必修第一册 3.1.2氯气及氯的化合物 课件(共24张PPT)
文档属性
| 名称 | 2023-2024学年高中化学苏教版2019必修第一册 3.1.2氯气及氯的化合物 课件(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 51.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-14 00:00:00 | ||
图片预览







文档简介
(共24张PPT)
专题三第一单元
氯气及氯的化合物
02
氯气的性质及应用
通过视频,氯气有哪些性质?
有刺激性气味
有毒
刺鼻气味
很多学生呕吐
氯气物理性质
黄绿色气体
有刺激性气味
密度比空气大
怎么闻氯气?
用手轻轻地在瓶口扇动,仅使极少量的氯气飘进鼻孔。
氯气物理性质
易液化
液氯是纯净物
储存在钢瓶中
氯气物理性质
能溶于水
(1体积水可溶解2体积氯气)其水溶液称“氯水”
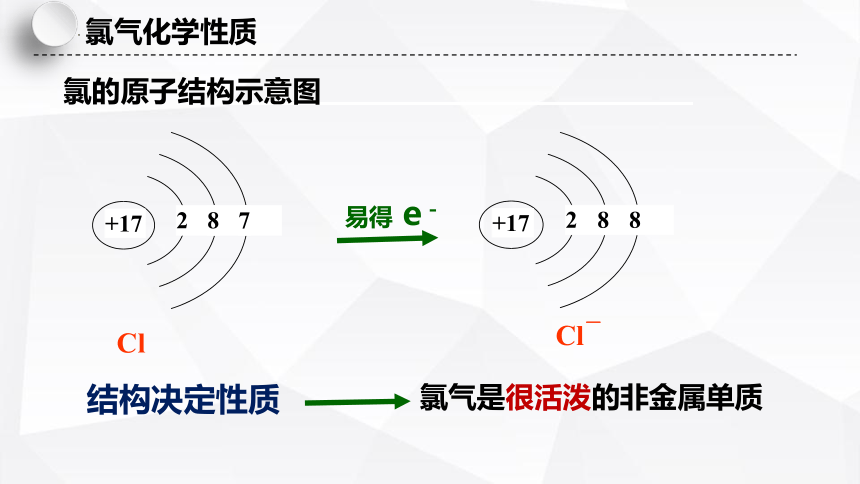
Cl
Cl-
易得 e-
+17
2
8
7
+17
2
8
8
结构决定性质
氯气是很活泼的非金属单质
氯的原子结构示意图
氯气化学性质
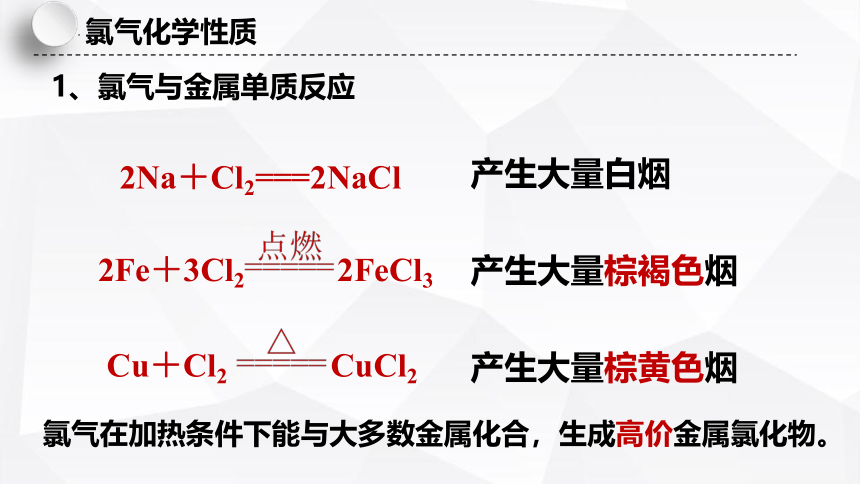
1、氯气与金属单质反应
氯气化学性质
1、氯气与金属单质反应
氯气化学性质
2Na+Cl2===2NaCl
2Fe+3Cl2 2FeCl3
Cu+Cl2 CuCl2
产生大量白烟
产生大量棕褐色烟
产生大量棕黄色烟
氯气在加热条件下能与大多数金属化合,生成高价金属氯化物。
2、氯气与非金属单质反应
氯气化学性质
氯气化学性质
氢气在氯气中安静地燃烧,发出 火焰,集气瓶口上方出现 。
苍白色
白雾
将H2与Cl2混合点燃或强光照射会发生爆炸。
通过H2在Cl2中燃烧的实验,你对燃烧的条件及其本质有什么新的认识
氯气化学性质
燃烧不一定要有氧气参加
燃烧的本质是氧化还原反应
任何发光发热的剧烈的化学反应叫做燃烧
用自来水养鱼前,为什么要先进行曝气处理?
氯气化学性质
除氯
自来水厂用氯气杀菌,消毒。
Cl2 + H2O HCl + HClO
1体积的水能溶解2体积的Cl2,Cl2能溶于水,溶于水中的部分Cl2与水反应。
3、氯气与水反应
可逆反应
次氯酸
氯气化学性质
氯气化学性质
Cl2 + H2O HCl + HClO
实验操作 实验现象 实验结论
_______________ _____________________
____________ ________________
有色布条不褪色
有色布条褪色
干燥氯气不具有漂白性
氯水具有漂白性
湿润的氯气有漂白作用,起漂白作用的是HClO
氯气化学性质
次氯酸的性质:
1.弱酸性 酸性:H2CO3 >HClO
2HClO 2HCl+O2↑
光
3.强氧化性
漂白作用;可用于自来水的杀菌、消毒,可用做漂白剂。
2.不稳定易分解
氯气化学性质
名称 新制氯水 久置氯水
物质类别 混合物 混合物
成分 __________________ ___________ _____________________
颜色 色 色
酸性 pH新 pH久
漂白性 ____ ____
Cl2、HClO、H2O、
H+、Cl-、ClO-、OH-
H2O、
H+、Cl-、OH-
浅黄绿
无
>
有
无
氯水只能现配现用,并盛放在棕色试剂瓶中。
三分四离
氯气化学性质
4、氯气与碱反应
Cl2+2NaOH===NaClO+NaCl+H2O
次氯酸钠
——利用NaOH溶液吸收Cl2尾气
氯气化学性质
工业上常用氯气和石灰乳制成漂白粉
2Ca(OH)2 + 2Cl2 ═ Ca(ClO)2 + CaCl2+ 2H2O
主要成分
有效成分:Ca(ClO)2
Ca(ClO)2+CO2 + 2H2O ═ CaCO3 ↓ + 2HClO
Ca(ClO)2+CO2 + 2H2O ═ CaCO3 ↓ + 2HClO
2HClO 2HCl+O2↑
光照
漂白粉的漂白原理:
漂白粉在空气中久置失效:
氯气化学性质
漂白粉应密封、避光保存,并置于阴凉干燥处。
氯气用途
是合成塑料、橡胶、人造纤维、
农药和药品的重要原料
制取漂白剂
制取盐酸
作消毒剂
氯气
延时符
课堂小结
01
02
氯气物理性质
氯气化学性质
03
氯气用途
课堂练习
C
1.下列有关次氯酸的叙述不正确的是
A.次氯酸不稳定,易分解
B.次氯酸是一种强氧化剂
C.次氯酸是弱酸,但酸性比碳酸强
D.次氯酸能使染料和有机色质褪色
课堂练习
C
2.向盛有氯气的三个集气瓶中,分别注入约五分之一的液体并振荡,观察下图所记录的现象,其中判断各瓶所注入的液体正确的是
A.①中为硝酸银溶液 B.②中为氢氧化钠溶液
C.③中为蒸馏水 D.③中为澄清石灰水
专题三第一单元
氯气及氯的化合物
02
氯气的性质及应用
通过视频,氯气有哪些性质?
有刺激性气味
有毒
刺鼻气味
很多学生呕吐
氯气物理性质
黄绿色气体
有刺激性气味
密度比空气大
怎么闻氯气?
用手轻轻地在瓶口扇动,仅使极少量的氯气飘进鼻孔。
氯气物理性质
易液化
液氯是纯净物
储存在钢瓶中
氯气物理性质
能溶于水
(1体积水可溶解2体积氯气)其水溶液称“氯水”
Cl
Cl-
易得 e-
+17
2
8
7
+17
2
8
8
结构决定性质
氯气是很活泼的非金属单质
氯的原子结构示意图
氯气化学性质
1、氯气与金属单质反应
氯气化学性质
1、氯气与金属单质反应
氯气化学性质
2Na+Cl2===2NaCl
2Fe+3Cl2 2FeCl3
Cu+Cl2 CuCl2
产生大量白烟
产生大量棕褐色烟
产生大量棕黄色烟
氯气在加热条件下能与大多数金属化合,生成高价金属氯化物。
2、氯气与非金属单质反应
氯气化学性质
氯气化学性质
氢气在氯气中安静地燃烧,发出 火焰,集气瓶口上方出现 。
苍白色
白雾
将H2与Cl2混合点燃或强光照射会发生爆炸。
通过H2在Cl2中燃烧的实验,你对燃烧的条件及其本质有什么新的认识
氯气化学性质
燃烧不一定要有氧气参加
燃烧的本质是氧化还原反应
任何发光发热的剧烈的化学反应叫做燃烧
用自来水养鱼前,为什么要先进行曝气处理?
氯气化学性质
除氯
自来水厂用氯气杀菌,消毒。
Cl2 + H2O HCl + HClO
1体积的水能溶解2体积的Cl2,Cl2能溶于水,溶于水中的部分Cl2与水反应。
3、氯气与水反应
可逆反应
次氯酸
氯气化学性质
氯气化学性质
Cl2 + H2O HCl + HClO
实验操作 实验现象 实验结论
_______________ _____________________
____________ ________________
有色布条不褪色
有色布条褪色
干燥氯气不具有漂白性
氯水具有漂白性
湿润的氯气有漂白作用,起漂白作用的是HClO
氯气化学性质
次氯酸的性质:
1.弱酸性 酸性:H2CO3 >HClO
2HClO 2HCl+O2↑
光
3.强氧化性
漂白作用;可用于自来水的杀菌、消毒,可用做漂白剂。
2.不稳定易分解
氯气化学性质
名称 新制氯水 久置氯水
物质类别 混合物 混合物
成分 __________________ ___________ _____________________
颜色 色 色
酸性 pH新 pH久
漂白性 ____ ____
Cl2、HClO、H2O、
H+、Cl-、ClO-、OH-
H2O、
H+、Cl-、OH-
浅黄绿
无
>
有
无
氯水只能现配现用,并盛放在棕色试剂瓶中。
三分四离
氯气化学性质
4、氯气与碱反应
Cl2+2NaOH===NaClO+NaCl+H2O
次氯酸钠
——利用NaOH溶液吸收Cl2尾气
氯气化学性质
工业上常用氯气和石灰乳制成漂白粉
2Ca(OH)2 + 2Cl2 ═ Ca(ClO)2 + CaCl2+ 2H2O
主要成分
有效成分:Ca(ClO)2
Ca(ClO)2+CO2 + 2H2O ═ CaCO3 ↓ + 2HClO
Ca(ClO)2+CO2 + 2H2O ═ CaCO3 ↓ + 2HClO
2HClO 2HCl+O2↑
光照
漂白粉的漂白原理:
漂白粉在空气中久置失效:
氯气化学性质
漂白粉应密封、避光保存,并置于阴凉干燥处。
氯气用途
是合成塑料、橡胶、人造纤维、
农药和药品的重要原料
制取漂白剂
制取盐酸
作消毒剂
氯气
延时符
课堂小结
01
02
氯气物理性质
氯气化学性质
03
氯气用途
课堂练习
C
1.下列有关次氯酸的叙述不正确的是
A.次氯酸不稳定,易分解
B.次氯酸是一种强氧化剂
C.次氯酸是弱酸,但酸性比碳酸强
D.次氯酸能使染料和有机色质褪色
课堂练习
C
2.向盛有氯气的三个集气瓶中,分别注入约五分之一的液体并振荡,观察下图所记录的现象,其中判断各瓶所注入的液体正确的是
A.①中为硝酸银溶液 B.②中为氢氧化钠溶液
C.③中为蒸馏水 D.③中为澄清石灰水
