化学人教版(2019)必修第一册2.2氯及其化合物 课件(共39张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册2.2氯及其化合物 课件(共39张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-16 00:00:00 | ||
图片预览










文档简介
(共39张PPT)
氯及其化合物
华立凤凰城的业主陈女士发现家中的自来水总有一股刺鼻的异味,这是为什么呢?
为什么水质不好的地方自来水有味道?
探究一:水里有什么?
资料卡片:
记者咨询供水部门了解到,为了确保生活饮用水安全,按照国家相关规定供水企业在水处理过程中,必须进行加氯消毒处理,保障居民的生活饮用水安全。
目前,很多自来水厂用氯气来进行杀菌消毒,我们有时候闻到的自来水散发出来的刺激性气味其实是余氯的气味
探究二:为何水中要加氯气,它起什么作用?
请你根据所学知识以及所给提示,推断氯气是以何种原理起到杀菌消毒作用?
并说明理由。
杀菌消毒一般原理:消毒剂能破坏微生物机体细胞中蛋白质的分子结构,使蛋白质变性而失去活性。
双氧水:可与病毒包膜发生氧化反应,迅速杀死病毒,在消毒完成后分解为氧气和水。对病毒及真菌等多种微生物均有很好的杀灭作用。
75%的酒精溶液:能够吸收细菌蛋白的水分,使其脱水变性凝固,从而达到杀灭细菌的且的。
氯气的性质
1.氯元素的原子结构及存在
(1)原子结构
氯原子结构示意图为 ,氯原子容易 1个电子而形成Cl-。
(2)存在
氯在自然界中以 态存在,主要以 、 、 等形式存在于海水中。
得到
化合
NaCl
MgCl2
CaCl2
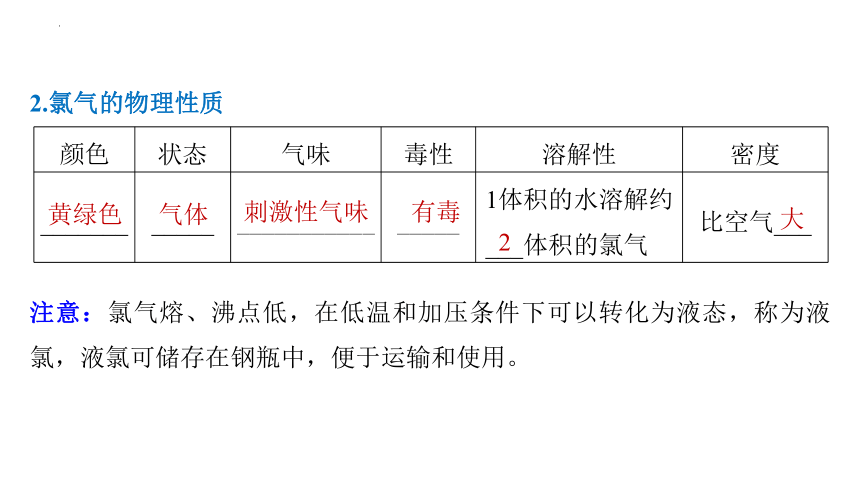
2.氯气的物理性质
有毒
2
黄绿色
气体
刺激性气味
颜色 状态 气味 毒性 溶解性 密度
_______ _____ ___________ _____ 1体积的水溶解约 ___体积的氯气 比空气___
大
注意:氯气熔、沸点低,在低温和加压条件下可以转化为液态,称为液氯,液氯可储存在钢瓶中,便于运输和使用。
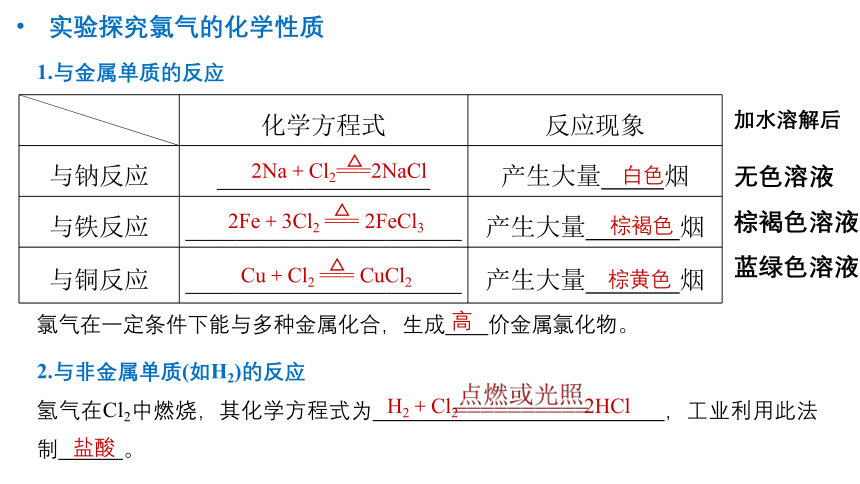
1.与金属单质的反应
化学方程式 反应现象
与钠反应 _________________ 产生大量 烟
与铁反应 ______________________ 产生大量 烟
与铜反应 ______________________ 产生大量 烟
2Na+Cl2===2NaCl
白色
2Fe+3Cl2 === 2FeCl3
棕褐色
Cu+Cl2 === CuCl2
棕黄色
氯气在一定条件下能与多种金属化合,生成 价金属氯化物。
高
实验探究氯气的化学性质
2.与非金属单质(如H2)的反应
氢气在Cl2中燃烧,其化学方程式为 ,工业利用此法制 。
H2+Cl2 2HCl
盐酸
加水溶解后
无色溶液
棕褐色溶液
蓝绿色溶液
氯气溶于水只是简单的溶解吗,有没有其他可能?
H2O + Cl2 —— ???
大胆假设,小心求证!
序号 实验操作 实验现象 实验结论
① 将干燥的有色布条和湿润的有色布条分别放入两瓶干燥的氯气中 干燥的有色布条__ ,湿润的有色布条____ 干燥的氯气无____性,氯水有 性
② 分别用玻璃棒蘸取新制氯水和稀盐酸,滴在pH试纸上 滴有盐酸的试纸变红,滴有氯水的试纸中间变为 ,外圈变____ 氯水中有能使试纸变红的 和能使有色物质 的漂白性物质
氯水的成分探究
(1)探究实验
不
褪色
褪色
漂白
漂白
白色
红
酸
褪色
③ 向1 mL新制氯水中滴加几滴硝酸银溶液和稀硝酸 产生 沉淀 新制氯水中含有___
白色
Cl-
综合分析得结论:(1)氯气溶于水得到的氯水显 性,有 作用,氯水中存在 。
酸
漂白
Cl-
(2)实际上,氯气溶于水得到的氯水具有漂白性是因为______
,反应的化学方程式是 。
(3)氯水中所含的分子有 。
氯水中所含的离子有 。
氯气与
H2O反应生成了HClO
Cl2+H2O ===HCl+HClO
Cl2、H2O、HClO
Cl-、H+、ClO-、OH-
(1)操作:如图,取一支100 mL的针筒抽取80 mL的氯气,再抽取20 mL的水,振荡。
(2)现象:刚开始抽进去氯气的时候针管内为 ,随后 移动,水溶液颜色逐渐变为 ,最终活塞移动至大约60 mL处。
(3)结论:氯气可溶于水,其水溶液叫 ,水溶液呈 ,常温常压下,1体积的水约能溶解2体积的氯气。
黄绿色
氯水
活塞向里
浅黄绿色
浅黄绿色
3. 实验探究氯气与水反应
氯气与水反应除了生成HCl外,还生成了具有漂白性的HClO,漂白杀菌作用是多种物质共同作用的结果,主要是HClO。
次氯酸可可用于棉、麻和纸张的漂白,有很强的氧化性,请大家回忆我们在日常生活中都是使用什么来漂白衣物的?大家在生活中见到过次氯酸吗?为什么
光照
只存在于水溶液中,不稳定,在光照下容易分解放出氧气:
2HClO = 2HCl+O2↑
次氯酸的性质
次氯酸是 于水的弱酸,酸性比碳酸 。
易溶
弱
归纳总结
液氯、新制氯水和久置氯水的区别
液氯 新制氯水 久置氯水
成分 Cl2 Cl2、HClO、H2O、H+、Cl-、ClO-、OH- H+、Cl-、H2O、OH-
分类 纯净物 混合物 混合物
颜色 黄绿色 浅黄绿色 无色
性质 氧化性 酸性、氧化性、漂白性 酸性
漂白液的主要成分:NaClO
从物质分类角度思考,如何制备漂白液?
与氢氧化钠溶液反应——制取漂白液
(1)反应的化学方程式: 。
(2)漂白液的有效成分是 。
与石灰乳反应——制取漂白粉
(1)反应的化学方程式: 。
(2)漂白粉的有效成分是 。
Cl2+2NaOH===NaCl+NaClO+H2O
次氯酸钠
2Ca(OH)2+2Cl2===CaCl2+Ca(ClO)2+2H2O
Ca(ClO)2
4. 氯气与碱反应
当Ca(ClO)2是主要成分时,就得到漂粉精
漂白原理
次氯酸盐溶于水后与空气中的CO2反应生成次氯酸,如漂白液的漂白原理用化学方程式表示为 。
常用含氯消毒剂及其合理使用(P48-6)
(1)具有漂白和消毒作用的含氯化合物有次氯酸、次氯酸盐(次氯酸钙、次氯酸钠)、二氧化氯(ClO2)。二氧化氯的漂白和消毒能力比氯气强,效果更持久,受水体的pH变化影响小,且使用起来更方便、安全。
(2)漂白粉需 保存,以防止变质失效。
(3)含氯漂白剂与洁厕灵(含有盐酸)不能混合使用,否则将产生 。
2NaClO+CO2+H2O===Na2CO3+2HClO
密封
Cl2
如果遭遇氯气泄漏该如何逃生?
发生氯气泄漏事件时,污染区居民切忌惊慌,应向上风向地区转移,并用湿毛巾护住口鼻;到了安全地带要好好休息,避免剧烈运动,以免加重心肺负担,恶化病情
在第一次世界大战期间,有一次德军与英法联军在比利时对峙,黎明时,英法联军前线战壕的士兵突然看到一股黄绿色气体逐渐袭来,很快数百名英法军战士窒息而死。后来人们在打扫战场时发现跑到山坡上的士兵竟幸免于难。
市中环水务水质检测中心主任吴非介绍,饮用水中必须要保持一定的消毒剂余量,才能起到杀灭水中的病原微生物的作用,而国家对生活饮用水中的消毒剂余量含量也有着严格的规定,余氯含量只要在国家标准范围内,市民可以放心饮用。即便水中略带氯味这也属于正常现象,不会影响健康。而中环水务也是严格按照这一标准在执行,绝不存在超标的情况。
把握性质、合理使用!
未知溶液中氯离子的检验:
稀盐酸 NaCl溶液 Na2CO3溶液
AgNO3溶液
少量稀硝酸
白色沉淀 白色沉淀 白色沉淀
仍有沉淀 仍有沉淀 沉淀消失
氯气的实验室制法
氯气的发现
(1)发现:1774年,瑞典化学家舍勒将软锰矿(主要成分是 )与______
混合加热,意外地发现了一种具有强烈 气味的 气体,受当时条件的限制未能确定这种气体。
(2)命名:1810年,英国化学家戴维仔细研究了这种 气体,确认它是一种新元素组成的单质,并将其命名为 。
MnO2
浓盐酸
刺激性
黄绿色
黄绿色
氯气
氯气的实验室制法
1.反应原理
实验室常用MnO2和浓盐酸在加热条件下制备Cl2,化学方程式为:
。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
2.仪器装置如何设计?
固 + 液 气
反应物装置
产物收集装置
反应物装置
如何收集气体?
常见气体收集装置
(1)气体发生装置类型:固+液 气。
(2)发生装置所用仪器A和B的名称为 、 。
分液漏斗
圆底烧瓶
强氧化性物质如高锰酸钾,氯酸钾等和浓盐酸反应不需要加热
实验室制备和图片相比有何不同?这个反应中还有哪些不足?
如何改进装置解决 1.Cl2不纯 2. Cl2有毒
气体净化装置的设计必须同时考虑主要成分和杂质成分的性质,以便选择适当的装置除去杂质。用浓盐酸和二氧化锰制取氯气时,氯气中混有HCl和水蒸气等杂质,除去氯气中的HCl可以用饱和食盐水(如图Ⅰ);除去氯气中的水蒸气可用浓硫酸(如图Ⅱ)或无水CaCl2(如图Ⅲ)。
如何净化氯气?
常见气体除杂装置
尾气处理时,不能用澄清石灰水吸收氯气,因为澄清石灰水中Ca(OH)2的含量少,吸收不完全。
如何进行尾气处理?
有毒气体的处理装置
(1)观察到集气瓶中充满黄绿色气体,则证明已集满。
(2)将湿润的淀粉碘化钾试纸靠近盛氯气的瓶口,观察到试纸立即变蓝,则证明已集满。
(3)将湿润的蓝色石蕊试纸靠近盛氯气的瓶口,观察到试纸立即发生先变红后褪色的变化,则证明已集满。
如何检验氯气收集满?
完整的实验装置:
制备
净化
收集
尾气处理
实验室制备Cl2注意事项
①必须用浓盐酸,MnO2与稀盐酸不反应。
②为了减少制得的Cl2中HCl的含量,所以加热温度不宜过高,减少HCl的挥发。
③实验结束后,先使反应停止并排出装置中残留的Cl2,再拆卸装置,避免污染空气。
④尾气吸收时,不能用澄清石灰水吸收Cl2,因为溶液中Ca(OH)2浓度小,吸收不完全。
3.收集方法
用 排空气法,理由是 。
4.尾气处理
(1)仪器装置图中的烧杯内盛放的液体是 。
(2)该液体的作用是 。
向上
氯气与空气不反应且密度比空气的大
NaOH溶液
吸收过量的氯气,防止污染环境
查阅资料知氯气可溶于水,但在饱和食盐水中几乎不溶,Cl2可以与KI溶液反应置换出I2。
(1)利用MnO2与浓盐酸制取的Cl2中混有的杂质是什么?
提示 HCl、水蒸气。
(2)如何获取纯净的氯气?
提示 先将气体通过饱和食盐水除去HCl,再通过浓硫酸除去水蒸气。
(3)实验室收集Cl2除了用向上排空气法还可以用什么方法?
提示 排饱和食盐水法。
(4)实验室收集Cl2除了观察颜色来验满,也可以用湿润的淀粉-KI试纸置于集气瓶口验满。试用化学方程式和必要的文字说明原因?
提示 Cl2+2KI===2KCl+I2,淀粉遇I2变蓝,若置于集气瓶口的湿润的淀粉-KI试纸变蓝即可验证Cl2已集满。
归纳总结
氯气的实验室制取流程及相应原理
二者不能混用!
洁厕灵能快速除去马桶内污渍和异味
84消毒液则能有效杀灭真菌和细菌
若将二者混合使用
是不是就会达到
“强强联合”的双重效果呢?
84消毒液是一种以次氯酸钠为主的高效消毒剂,主要成分为次氯酸钠(NaClO)。通常为无色或淡黄色液体,被广泛用于宾馆、医院、家庭等的衣物、仪器、餐具的卫生消毒。之所以叫84消毒液,是因为这种消毒液是北京的地坛医院于1984年研制的。
洁厕灵主要成分是盐酸(HCl)。对陶瓷类日用品,如便器、瓷砖、水池表面具有良好去污除垢作用。
两种日用品混用则会产生氯气(Cl2)
吸入少量低浓度氯气可导致咳嗽胸闷,高浓度的氯气则会引起窒息。
氯气还可能引发眼部和皮肤不适或者病变。
吸入的氯气与体内的水反应,生成的次氯酸可以透过细胞膜,破坏细胞完整性。
氯及其化合物
华立凤凰城的业主陈女士发现家中的自来水总有一股刺鼻的异味,这是为什么呢?
为什么水质不好的地方自来水有味道?
探究一:水里有什么?
资料卡片:
记者咨询供水部门了解到,为了确保生活饮用水安全,按照国家相关规定供水企业在水处理过程中,必须进行加氯消毒处理,保障居民的生活饮用水安全。
目前,很多自来水厂用氯气来进行杀菌消毒,我们有时候闻到的自来水散发出来的刺激性气味其实是余氯的气味
探究二:为何水中要加氯气,它起什么作用?
请你根据所学知识以及所给提示,推断氯气是以何种原理起到杀菌消毒作用?
并说明理由。
杀菌消毒一般原理:消毒剂能破坏微生物机体细胞中蛋白质的分子结构,使蛋白质变性而失去活性。
双氧水:可与病毒包膜发生氧化反应,迅速杀死病毒,在消毒完成后分解为氧气和水。对病毒及真菌等多种微生物均有很好的杀灭作用。
75%的酒精溶液:能够吸收细菌蛋白的水分,使其脱水变性凝固,从而达到杀灭细菌的且的。
氯气的性质
1.氯元素的原子结构及存在
(1)原子结构
氯原子结构示意图为 ,氯原子容易 1个电子而形成Cl-。
(2)存在
氯在自然界中以 态存在,主要以 、 、 等形式存在于海水中。
得到
化合
NaCl
MgCl2
CaCl2
2.氯气的物理性质
有毒
2
黄绿色
气体
刺激性气味
颜色 状态 气味 毒性 溶解性 密度
_______ _____ ___________ _____ 1体积的水溶解约 ___体积的氯气 比空气___
大
注意:氯气熔、沸点低,在低温和加压条件下可以转化为液态,称为液氯,液氯可储存在钢瓶中,便于运输和使用。
1.与金属单质的反应
化学方程式 反应现象
与钠反应 _________________ 产生大量 烟
与铁反应 ______________________ 产生大量 烟
与铜反应 ______________________ 产生大量 烟
2Na+Cl2===2NaCl
白色
2Fe+3Cl2 === 2FeCl3
棕褐色
Cu+Cl2 === CuCl2
棕黄色
氯气在一定条件下能与多种金属化合,生成 价金属氯化物。
高
实验探究氯气的化学性质
2.与非金属单质(如H2)的反应
氢气在Cl2中燃烧,其化学方程式为 ,工业利用此法制 。
H2+Cl2 2HCl
盐酸
加水溶解后
无色溶液
棕褐色溶液
蓝绿色溶液
氯气溶于水只是简单的溶解吗,有没有其他可能?
H2O + Cl2 —— ???
大胆假设,小心求证!
序号 实验操作 实验现象 实验结论
① 将干燥的有色布条和湿润的有色布条分别放入两瓶干燥的氯气中 干燥的有色布条__ ,湿润的有色布条____ 干燥的氯气无____性,氯水有 性
② 分别用玻璃棒蘸取新制氯水和稀盐酸,滴在pH试纸上 滴有盐酸的试纸变红,滴有氯水的试纸中间变为 ,外圈变____ 氯水中有能使试纸变红的 和能使有色物质 的漂白性物质
氯水的成分探究
(1)探究实验
不
褪色
褪色
漂白
漂白
白色
红
酸
褪色
③ 向1 mL新制氯水中滴加几滴硝酸银溶液和稀硝酸 产生 沉淀 新制氯水中含有___
白色
Cl-
综合分析得结论:(1)氯气溶于水得到的氯水显 性,有 作用,氯水中存在 。
酸
漂白
Cl-
(2)实际上,氯气溶于水得到的氯水具有漂白性是因为______
,反应的化学方程式是 。
(3)氯水中所含的分子有 。
氯水中所含的离子有 。
氯气与
H2O反应生成了HClO
Cl2+H2O ===HCl+HClO
Cl2、H2O、HClO
Cl-、H+、ClO-、OH-
(1)操作:如图,取一支100 mL的针筒抽取80 mL的氯气,再抽取20 mL的水,振荡。
(2)现象:刚开始抽进去氯气的时候针管内为 ,随后 移动,水溶液颜色逐渐变为 ,最终活塞移动至大约60 mL处。
(3)结论:氯气可溶于水,其水溶液叫 ,水溶液呈 ,常温常压下,1体积的水约能溶解2体积的氯气。
黄绿色
氯水
活塞向里
浅黄绿色
浅黄绿色
3. 实验探究氯气与水反应
氯气与水反应除了生成HCl外,还生成了具有漂白性的HClO,漂白杀菌作用是多种物质共同作用的结果,主要是HClO。
次氯酸可可用于棉、麻和纸张的漂白,有很强的氧化性,请大家回忆我们在日常生活中都是使用什么来漂白衣物的?大家在生活中见到过次氯酸吗?为什么
光照
只存在于水溶液中,不稳定,在光照下容易分解放出氧气:
2HClO = 2HCl+O2↑
次氯酸的性质
次氯酸是 于水的弱酸,酸性比碳酸 。
易溶
弱
归纳总结
液氯、新制氯水和久置氯水的区别
液氯 新制氯水 久置氯水
成分 Cl2 Cl2、HClO、H2O、H+、Cl-、ClO-、OH- H+、Cl-、H2O、OH-
分类 纯净物 混合物 混合物
颜色 黄绿色 浅黄绿色 无色
性质 氧化性 酸性、氧化性、漂白性 酸性
漂白液的主要成分:NaClO
从物质分类角度思考,如何制备漂白液?
与氢氧化钠溶液反应——制取漂白液
(1)反应的化学方程式: 。
(2)漂白液的有效成分是 。
与石灰乳反应——制取漂白粉
(1)反应的化学方程式: 。
(2)漂白粉的有效成分是 。
Cl2+2NaOH===NaCl+NaClO+H2O
次氯酸钠
2Ca(OH)2+2Cl2===CaCl2+Ca(ClO)2+2H2O
Ca(ClO)2
4. 氯气与碱反应
当Ca(ClO)2是主要成分时,就得到漂粉精
漂白原理
次氯酸盐溶于水后与空气中的CO2反应生成次氯酸,如漂白液的漂白原理用化学方程式表示为 。
常用含氯消毒剂及其合理使用(P48-6)
(1)具有漂白和消毒作用的含氯化合物有次氯酸、次氯酸盐(次氯酸钙、次氯酸钠)、二氧化氯(ClO2)。二氧化氯的漂白和消毒能力比氯气强,效果更持久,受水体的pH变化影响小,且使用起来更方便、安全。
(2)漂白粉需 保存,以防止变质失效。
(3)含氯漂白剂与洁厕灵(含有盐酸)不能混合使用,否则将产生 。
2NaClO+CO2+H2O===Na2CO3+2HClO
密封
Cl2
如果遭遇氯气泄漏该如何逃生?
发生氯气泄漏事件时,污染区居民切忌惊慌,应向上风向地区转移,并用湿毛巾护住口鼻;到了安全地带要好好休息,避免剧烈运动,以免加重心肺负担,恶化病情
在第一次世界大战期间,有一次德军与英法联军在比利时对峙,黎明时,英法联军前线战壕的士兵突然看到一股黄绿色气体逐渐袭来,很快数百名英法军战士窒息而死。后来人们在打扫战场时发现跑到山坡上的士兵竟幸免于难。
市中环水务水质检测中心主任吴非介绍,饮用水中必须要保持一定的消毒剂余量,才能起到杀灭水中的病原微生物的作用,而国家对生活饮用水中的消毒剂余量含量也有着严格的规定,余氯含量只要在国家标准范围内,市民可以放心饮用。即便水中略带氯味这也属于正常现象,不会影响健康。而中环水务也是严格按照这一标准在执行,绝不存在超标的情况。
把握性质、合理使用!
未知溶液中氯离子的检验:
稀盐酸 NaCl溶液 Na2CO3溶液
AgNO3溶液
少量稀硝酸
白色沉淀 白色沉淀 白色沉淀
仍有沉淀 仍有沉淀 沉淀消失
氯气的实验室制法
氯气的发现
(1)发现:1774年,瑞典化学家舍勒将软锰矿(主要成分是 )与______
混合加热,意外地发现了一种具有强烈 气味的 气体,受当时条件的限制未能确定这种气体。
(2)命名:1810年,英国化学家戴维仔细研究了这种 气体,确认它是一种新元素组成的单质,并将其命名为 。
MnO2
浓盐酸
刺激性
黄绿色
黄绿色
氯气
氯气的实验室制法
1.反应原理
实验室常用MnO2和浓盐酸在加热条件下制备Cl2,化学方程式为:
。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
2.仪器装置如何设计?
固 + 液 气
反应物装置
产物收集装置
反应物装置
如何收集气体?
常见气体收集装置
(1)气体发生装置类型:固+液 气。
(2)发生装置所用仪器A和B的名称为 、 。
分液漏斗
圆底烧瓶
强氧化性物质如高锰酸钾,氯酸钾等和浓盐酸反应不需要加热
实验室制备和图片相比有何不同?这个反应中还有哪些不足?
如何改进装置解决 1.Cl2不纯 2. Cl2有毒
气体净化装置的设计必须同时考虑主要成分和杂质成分的性质,以便选择适当的装置除去杂质。用浓盐酸和二氧化锰制取氯气时,氯气中混有HCl和水蒸气等杂质,除去氯气中的HCl可以用饱和食盐水(如图Ⅰ);除去氯气中的水蒸气可用浓硫酸(如图Ⅱ)或无水CaCl2(如图Ⅲ)。
如何净化氯气?
常见气体除杂装置
尾气处理时,不能用澄清石灰水吸收氯气,因为澄清石灰水中Ca(OH)2的含量少,吸收不完全。
如何进行尾气处理?
有毒气体的处理装置
(1)观察到集气瓶中充满黄绿色气体,则证明已集满。
(2)将湿润的淀粉碘化钾试纸靠近盛氯气的瓶口,观察到试纸立即变蓝,则证明已集满。
(3)将湿润的蓝色石蕊试纸靠近盛氯气的瓶口,观察到试纸立即发生先变红后褪色的变化,则证明已集满。
如何检验氯气收集满?
完整的实验装置:
制备
净化
收集
尾气处理
实验室制备Cl2注意事项
①必须用浓盐酸,MnO2与稀盐酸不反应。
②为了减少制得的Cl2中HCl的含量,所以加热温度不宜过高,减少HCl的挥发。
③实验结束后,先使反应停止并排出装置中残留的Cl2,再拆卸装置,避免污染空气。
④尾气吸收时,不能用澄清石灰水吸收Cl2,因为溶液中Ca(OH)2浓度小,吸收不完全。
3.收集方法
用 排空气法,理由是 。
4.尾气处理
(1)仪器装置图中的烧杯内盛放的液体是 。
(2)该液体的作用是 。
向上
氯气与空气不反应且密度比空气的大
NaOH溶液
吸收过量的氯气,防止污染环境
查阅资料知氯气可溶于水,但在饱和食盐水中几乎不溶,Cl2可以与KI溶液反应置换出I2。
(1)利用MnO2与浓盐酸制取的Cl2中混有的杂质是什么?
提示 HCl、水蒸气。
(2)如何获取纯净的氯气?
提示 先将气体通过饱和食盐水除去HCl,再通过浓硫酸除去水蒸气。
(3)实验室收集Cl2除了用向上排空气法还可以用什么方法?
提示 排饱和食盐水法。
(4)实验室收集Cl2除了观察颜色来验满,也可以用湿润的淀粉-KI试纸置于集气瓶口验满。试用化学方程式和必要的文字说明原因?
提示 Cl2+2KI===2KCl+I2,淀粉遇I2变蓝,若置于集气瓶口的湿润的淀粉-KI试纸变蓝即可验证Cl2已集满。
归纳总结
氯气的实验室制取流程及相应原理
二者不能混用!
洁厕灵能快速除去马桶内污渍和异味
84消毒液则能有效杀灭真菌和细菌
若将二者混合使用
是不是就会达到
“强强联合”的双重效果呢?
84消毒液是一种以次氯酸钠为主的高效消毒剂,主要成分为次氯酸钠(NaClO)。通常为无色或淡黄色液体,被广泛用于宾馆、医院、家庭等的衣物、仪器、餐具的卫生消毒。之所以叫84消毒液,是因为这种消毒液是北京的地坛医院于1984年研制的。
洁厕灵主要成分是盐酸(HCl)。对陶瓷类日用品,如便器、瓷砖、水池表面具有良好去污除垢作用。
两种日用品混用则会产生氯气(Cl2)
吸入少量低浓度氯气可导致咳嗽胸闷,高浓度的氯气则会引起窒息。
氯气还可能引发眼部和皮肤不适或者病变。
吸入的氯气与体内的水反应,生成的次氯酸可以透过细胞膜,破坏细胞完整性。
