第6节 几种重要的盐 第1课时(课件 22张ppt)
文档属性
| 名称 | 第6节 几种重要的盐 第1课时(课件 22张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-09-16 00:00:00 | ||
图片预览





文档简介
(共22张PPT)
第6节 几种重要的盐
第1课时
一、什么是盐
思考:有人讲,食盐就是盐,盐就是食盐。你认为对吗?
①盐是酸跟碱反应的产物。
②盐的组成:
金属阳离子
或铵根离子
NH4+
酸根阴离子
+
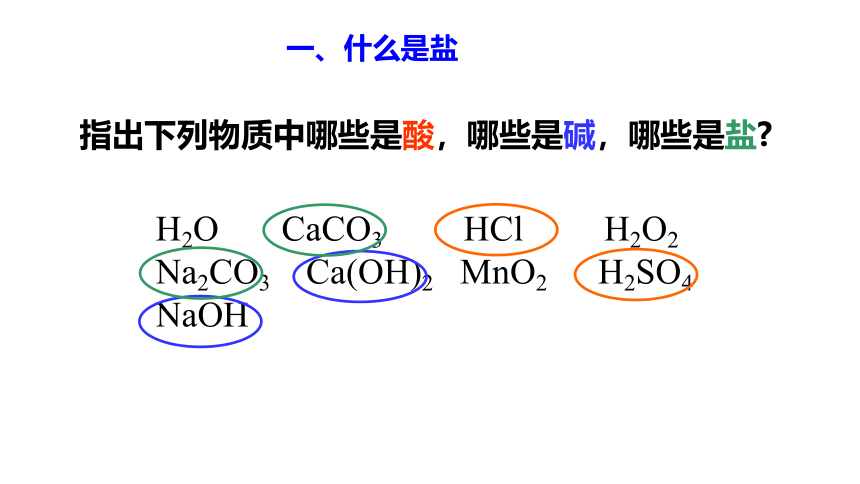
H2O CaCO3 HCl H2O2 Na2CO3 Ca(OH)2 MnO2 H2SO4 NaOH
一、什么是盐
指出下列物质中哪些是酸,哪些是碱,哪些是盐
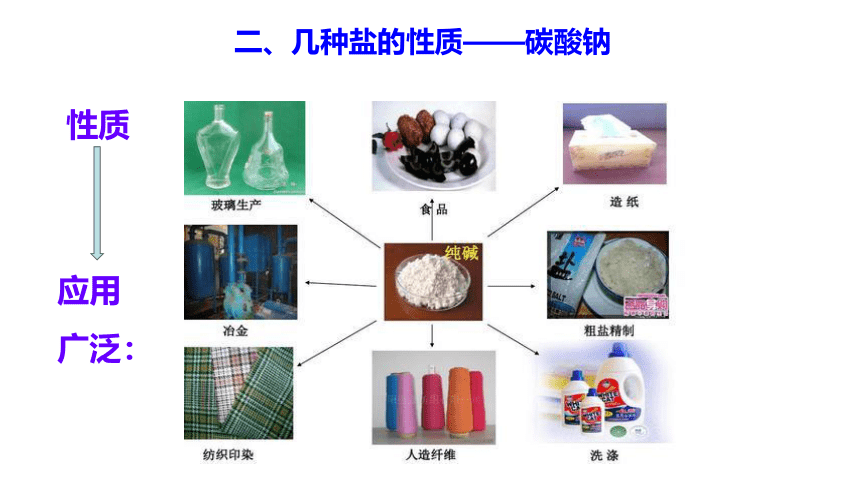
应用
广泛:
二、几种盐的性质——碳酸钠
性质
二、几种盐的性质——碳酸钠
1、碳酸钠
1).是一种__色粉末,__溶于水
白
易
(俗名:纯碱或苏打)
(Na2CO3)
2).从水溶液中析出时,晶体含有结晶水,化学式是_____。
Na2CO3·10H2O
纯净物
像碳酸钠晶体(Na2CO3.10H2O)这样的化合物含有结晶水,这类化合物归为一类——结晶水合物,它是一种纯净物.
结晶水合物在常温下,放在干燥的空气里,逐渐失去结晶水的现象叫风化.
化学变化
Na2CO3.10H2O
Na2CO3
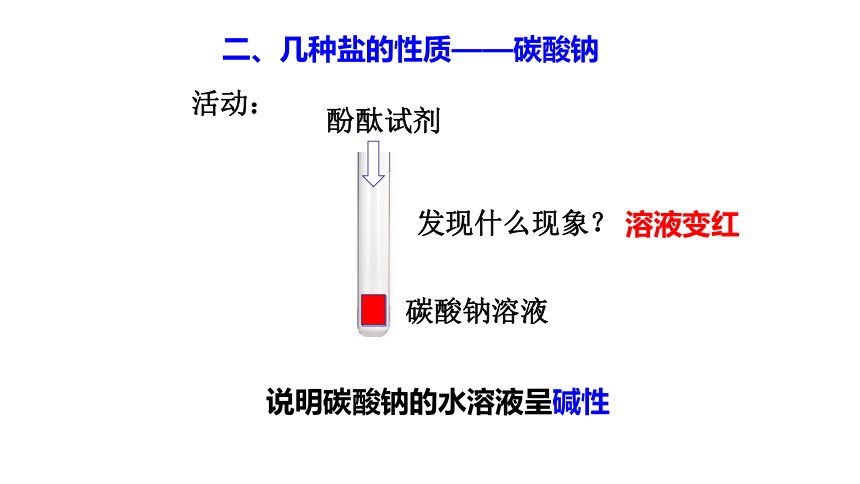
二、几种盐的性质——碳酸钠
发现什么现象?
溶液变红
碳酸钠溶液
酚酞试剂
活动:
说明碳酸钠的水溶液呈碱性
1)、碳酸钠与酸碱指示剂反应
碳酸钠的化学性质
3)、碳酸钠与酸反应:
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
Na2CO3 + 2 HCl===2 NaCl + H2O + CO2↑
2) 能与氢氧化钙反应:
Na2CO3+Ca(OH)2 = CaCO3↓ +2NaOH
二、几种盐的性质——碳酸钙
2、碳酸钙
(CaCO3)
应用
广泛:
性质
汉白玉
石灰石
大理石
二、几种盐的性质——碳酸钙
2、碳酸钙
(CaCO3)
1)白色粉末状
2)难溶于水
物理性质:
碳酸钙的制取:
Ca(OH)2+H2CO3=CaCO3 +2H2O
CaCO3+2HCl=CaCl2+H2O+CO2↑
碳酸钙与酸反应
化学性质
二、几种盐的性质——碳酸钙
制取二氧化碳
思考与讨论:怎样证明一块岩石是碳酸盐?
CO32-检验方法
滴加盐酸,将产生的气体通入澄清石灰水,如果变浑浊,则该物质中含有CO32-
CaCO3 + 2HCl=== CaCl2 + H2O + CO2↑
Na2CO3 + 2 HCl===2 NaCl + H2O + CO2↑
含有CO32-
都加入盐酸
都有气体放出
而且所放出的气体能使澄清的石灰水变浑浊.
食盐有自然中分布广,但主要存在于海水中
思考:汗液为什么是咸味?
实验室用什么化学试剂来证明氯化钠的存在?
二、几种盐的性质——氯化钠
3、氯化钠(俗名:食盐)
化学式:NaCl
白色晶体 易溶于水
物理性质:
氯化钠在生活中有哪些用途?
氯化钠的用途
应用1:生理盐水
二、几种盐的性质——氯化钠
0.9%的氯化钠溶液
应用2:食物佐料
应用3:浓盐水杀菌
因为浓的食盐溶液会使细胞内的水渗出,使蛋白质凝固,所以具有杀菌作用。
NaCl+AgNO3 =AgCl↓+ NaNO3
活动:收集一些汗液(或氯化钠溶液)盛放在试管中,滴入几滴硝酸银溶液,有什么现象产生?
白色沉淀
信息:
检验氯离子的方法--滴加AgNO3溶液,再加稀HNO3
思考与讨论:
为何用食盐腌过的肉类和蔬菜不易腐败?
食盐不仅直接抑制了微生物的活性,而且通过使食物脱水,来抑制微生物的滋生。
下列各组物质的名称、俗称(主要成分)和化学式,表示同一种物质的是( )
A.碳酸钙、生石灰、CaO
B.氯化钠、苏打、NaCl
C.氢氧化钠、烧碱、NaOH
D.氢氧化钙、石灰石、Ca(OH)2
本题试卷
科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,见如图。如果钥匙代表的试剂能够鉴别出门上代表的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
下列关于氯化钠的性质和用途的描述中,不正确的是( )
A.易溶于水
B.能吸收空气中的水分而潮解
C.其溶液能跟硝酸银溶液反应
D.0.9%的氯化钠溶液用作医疗上的生理盐水
现有NaCl、Na2CO3 、CaCO3物质的粉末,请你根据今天所学的知识,设计一种方案,将它们鉴别开来。
实验设计
Na2CO3的水溶液呈碱性,下列说法错误的是( )
A.在Na2CO3水中会电离出OH-
B.向Na2CO3溶液中加稀硫酸后溶液的pH降低
C. Na2CO3溶液中存在OH-
D.向Na2CO3溶液中滴加紫色石蕊试液后溶液显蓝色
第6节 几种重要的盐
第1课时
一、什么是盐
思考:有人讲,食盐就是盐,盐就是食盐。你认为对吗?
①盐是酸跟碱反应的产物。
②盐的组成:
金属阳离子
或铵根离子
NH4+
酸根阴离子
+
H2O CaCO3 HCl H2O2 Na2CO3 Ca(OH)2 MnO2 H2SO4 NaOH
一、什么是盐
指出下列物质中哪些是酸,哪些是碱,哪些是盐
应用
广泛:
二、几种盐的性质——碳酸钠
性质
二、几种盐的性质——碳酸钠
1、碳酸钠
1).是一种__色粉末,__溶于水
白
易
(俗名:纯碱或苏打)
(Na2CO3)
2).从水溶液中析出时,晶体含有结晶水,化学式是_____。
Na2CO3·10H2O
纯净物
像碳酸钠晶体(Na2CO3.10H2O)这样的化合物含有结晶水,这类化合物归为一类——结晶水合物,它是一种纯净物.
结晶水合物在常温下,放在干燥的空气里,逐渐失去结晶水的现象叫风化.
化学变化
Na2CO3.10H2O
Na2CO3
二、几种盐的性质——碳酸钠
发现什么现象?
溶液变红
碳酸钠溶液
酚酞试剂
活动:
说明碳酸钠的水溶液呈碱性
1)、碳酸钠与酸碱指示剂反应
碳酸钠的化学性质
3)、碳酸钠与酸反应:
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
Na2CO3 + 2 HCl===2 NaCl + H2O + CO2↑
2) 能与氢氧化钙反应:
Na2CO3+Ca(OH)2 = CaCO3↓ +2NaOH
二、几种盐的性质——碳酸钙
2、碳酸钙
(CaCO3)
应用
广泛:
性质
汉白玉
石灰石
大理石
二、几种盐的性质——碳酸钙
2、碳酸钙
(CaCO3)
1)白色粉末状
2)难溶于水
物理性质:
碳酸钙的制取:
Ca(OH)2+H2CO3=CaCO3 +2H2O
CaCO3+2HCl=CaCl2+H2O+CO2↑
碳酸钙与酸反应
化学性质
二、几种盐的性质——碳酸钙
制取二氧化碳
思考与讨论:怎样证明一块岩石是碳酸盐?
CO32-检验方法
滴加盐酸,将产生的气体通入澄清石灰水,如果变浑浊,则该物质中含有CO32-
CaCO3 + 2HCl=== CaCl2 + H2O + CO2↑
Na2CO3 + 2 HCl===2 NaCl + H2O + CO2↑
含有CO32-
都加入盐酸
都有气体放出
而且所放出的气体能使澄清的石灰水变浑浊.
食盐有自然中分布广,但主要存在于海水中
思考:汗液为什么是咸味?
实验室用什么化学试剂来证明氯化钠的存在?
二、几种盐的性质——氯化钠
3、氯化钠(俗名:食盐)
化学式:NaCl
白色晶体 易溶于水
物理性质:
氯化钠在生活中有哪些用途?
氯化钠的用途
应用1:生理盐水
二、几种盐的性质——氯化钠
0.9%的氯化钠溶液
应用2:食物佐料
应用3:浓盐水杀菌
因为浓的食盐溶液会使细胞内的水渗出,使蛋白质凝固,所以具有杀菌作用。
NaCl+AgNO3 =AgCl↓+ NaNO3
活动:收集一些汗液(或氯化钠溶液)盛放在试管中,滴入几滴硝酸银溶液,有什么现象产生?
白色沉淀
信息:
检验氯离子的方法--滴加AgNO3溶液,再加稀HNO3
思考与讨论:
为何用食盐腌过的肉类和蔬菜不易腐败?
食盐不仅直接抑制了微生物的活性,而且通过使食物脱水,来抑制微生物的滋生。
下列各组物质的名称、俗称(主要成分)和化学式,表示同一种物质的是( )
A.碳酸钙、生石灰、CaO
B.氯化钠、苏打、NaCl
C.氢氧化钠、烧碱、NaOH
D.氢氧化钙、石灰石、Ca(OH)2
本题试卷
科学兴趣小组在课余时间做了“开门大吉”的游戏,其规则是:每把钥匙代表一种试剂,每扇门代表需要鉴别的两种溶液,见如图。如果钥匙代表的试剂能够鉴别出门上代表的两种溶液,钥匙就能把门打开(每把钥匙只能使用一次),下列能够依次将四扇门打开的钥匙顺序是( )
下列关于氯化钠的性质和用途的描述中,不正确的是( )
A.易溶于水
B.能吸收空气中的水分而潮解
C.其溶液能跟硝酸银溶液反应
D.0.9%的氯化钠溶液用作医疗上的生理盐水
现有NaCl、Na2CO3 、CaCO3物质的粉末,请你根据今天所学的知识,设计一种方案,将它们鉴别开来。
实验设计
Na2CO3的水溶液呈碱性,下列说法错误的是( )
A.在Na2CO3水中会电离出OH-
B.向Na2CO3溶液中加稀硫酸后溶液的pH降低
C. Na2CO3溶液中存在OH-
D.向Na2CO3溶液中滴加紫色石蕊试液后溶液显蓝色
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
