2023-2024学年人教版高中化学选择性必修一 2.4化学反应的调控(共24张PPT)
文档属性
| 名称 | 2023-2024学年人教版高中化学选择性必修一 2.4化学反应的调控(共24张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-17 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
化学反应的调控
一、合成氨反应条件的原理分析
1.反应原理:N2(g)+3H2(g) 2NH3(g) ΔH=-92.2 kJ·mol-1。
2.反应特点:
合成氨 反应
—可逆性:反应为 反应 —体积变化:正反应是气体体积 的反应 —焓变:ΔH 0
可逆
减小
<
一、合成氨反应的特点
思考与讨论:
(1)原理分析
根据合成氨反应的特点,应如何选择反应条件,以增大合成氨的反应速率、提高平衡混合物中氨的含量?
请同学们独立完成课本表格!
二、合成氨反应特点的分析
结论:提高合成氨反应速率和平衡转化率的条件比较
条件 提高反应速率 提高平衡转化率 综合结果
压强
温度
催化剂
浓度
高压
高压
高压
高温
低温
兼顾速率和平衡,且考虑催化剂活性
使用
无影响
使用
增大反应物浓度
增大反应物浓度,降低生成物浓度
增大反应物浓度,且不断减少生成物浓度
核心素养:变化观念与平衡思想
思考与讨论:
(2)数据分析
表2-2中的实验数据是在不同温度、压强下,平衡混合物中氨的含量的变化情况(初始时氮气和氢气的体积比是1:3)。
分析表中数据,结合合成氨反应的特点,讨论应如何选择反应条件,以增大合成氨的反应速率、提高平衡混合物中氨的含量。
实践是检验真理的唯一标准
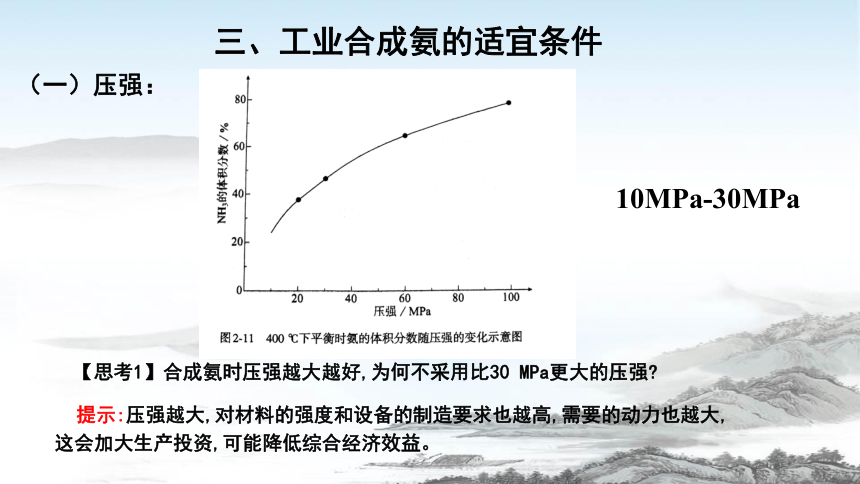
三、工业合成氨的适宜条件
(一)压强:
10MPa-30MPa
【思考1】合成氨时压强越大越好,为何不采用比30 MPa更大的压强
提示:压强越大,对材料的强度和设备的制造要求也越高,需要的动力也越大,这会加大生产投资,可能降低综合经济效益。
(二)温度:
400℃-500℃
【思考2】合成氨采用低温时可提高转化率,但为何未采用更低的温度
提示:温度太低,反应速率太小,达到平衡所需的时间变长,不经济。另外,合成氨所需的催化剂铁触媒的活性在500 ℃左右活性最大。
(三)催化剂:
目前,合成氨工业中普遍使用的是以铁为主体的多成分催化剂,又称铁触媒。铁触媒在500℃左右时的活性最大,这也是合成氨一般选择400—500℃进行的重要原因。
(四)浓度:
采取迅速冷却的方法,使气态氨变成液氨后及时从平衡混合物中分离出去,以促使化学平衡向生成NH3的方向移动。此外,如果让N2和H2的混合气体只一次通过合成塔发生反应也是很不经济的,应将NH3分离后的原料气循环使用,并及时补充N2和H2,使反应物保持一定的浓度,以利于合成氨反应。
总结:工业合成氨的适宜条件
外部条件 工业合成氨的适宜条件
压强
温度
催化剂
浓度
根据反应器可使用的钢材质量及综合指标来选择压强(10~30 MPa)
适宜温度,400~500 ℃
使用铁触媒做催化剂
及时补充N2和H2,并将氨及时从混合气中分离出去
微点拨:
工业生产中,必须从反应限度和反应速率两个角度选择合成氨的适宜条件,既要考虑尽量增大反应物的转化率,充分利用原料,又要选择较快的反应速率,提高单位时间内的产量,同时还要考虑设备的要求、技术条件、经济效益、环境保护等。
核心素养:科学态度与社会责任
合作学习
探究学习
(1)温度越高越利于合成氨反应平衡正向移动。 ( )
(2)合成氨反应中,压强越大越利于增大反应速率和平衡正向移动。 ( )
(3)使用催化剂能提高合成氨反应物的平衡转化率。 ( )
答案: (1)× (2)√ (3)×
小试牛刀
四、工业生产中选择适宜生产条件的原则
(一)影响化学反应进行的因素:参加反应的物质组成、结构和性质等本身因素,还有温度、压强、浓度、催化剂等反应条件。
(二)化学反应的调控需要考虑的因素:在实际生产中常常需要结合设备条件、安全操作、经济成本等情况,综合考虑影响化学反应速率和化学平衡的因素,寻找适宜的生产条件。此外,还要根据环境保护及社会效益等方面的规定和要求做出分析,权衡利弊,才能实施生产。
小结:
核心素养:宏观辨识与微观探析
针对训练
解析:
文质彬彬,然后君子
领袖气质、君子风度科学精神、工匠才干
构建思维导图
科学 技术 社会
.
.
合成氨—实验室研究与工业化生产
教师寄语:
同学们,科学发展的过程是艰辛的,是无数科学家艰苦奋斗的结果。作为新时代青年的我们,更应以他们为榜样,牢记习近平总书记对青年提出的殷切希望,努力学习科学知识,发展自身技能,成长为新时代需要的全能型人才!
化学反应的调控
一、合成氨反应条件的原理分析
1.反应原理:N2(g)+3H2(g) 2NH3(g) ΔH=-92.2 kJ·mol-1。
2.反应特点:
合成氨 反应
—可逆性:反应为 反应 —体积变化:正反应是气体体积 的反应 —焓变:ΔH 0
可逆
减小
<
一、合成氨反应的特点
思考与讨论:
(1)原理分析
根据合成氨反应的特点,应如何选择反应条件,以增大合成氨的反应速率、提高平衡混合物中氨的含量?
请同学们独立完成课本表格!
二、合成氨反应特点的分析
结论:提高合成氨反应速率和平衡转化率的条件比较
条件 提高反应速率 提高平衡转化率 综合结果
压强
温度
催化剂
浓度
高压
高压
高压
高温
低温
兼顾速率和平衡,且考虑催化剂活性
使用
无影响
使用
增大反应物浓度
增大反应物浓度,降低生成物浓度
增大反应物浓度,且不断减少生成物浓度
核心素养:变化观念与平衡思想
思考与讨论:
(2)数据分析
表2-2中的实验数据是在不同温度、压强下,平衡混合物中氨的含量的变化情况(初始时氮气和氢气的体积比是1:3)。
分析表中数据,结合合成氨反应的特点,讨论应如何选择反应条件,以增大合成氨的反应速率、提高平衡混合物中氨的含量。
实践是检验真理的唯一标准
三、工业合成氨的适宜条件
(一)压强:
10MPa-30MPa
【思考1】合成氨时压强越大越好,为何不采用比30 MPa更大的压强
提示:压强越大,对材料的强度和设备的制造要求也越高,需要的动力也越大,这会加大生产投资,可能降低综合经济效益。
(二)温度:
400℃-500℃
【思考2】合成氨采用低温时可提高转化率,但为何未采用更低的温度
提示:温度太低,反应速率太小,达到平衡所需的时间变长,不经济。另外,合成氨所需的催化剂铁触媒的活性在500 ℃左右活性最大。
(三)催化剂:
目前,合成氨工业中普遍使用的是以铁为主体的多成分催化剂,又称铁触媒。铁触媒在500℃左右时的活性最大,这也是合成氨一般选择400—500℃进行的重要原因。
(四)浓度:
采取迅速冷却的方法,使气态氨变成液氨后及时从平衡混合物中分离出去,以促使化学平衡向生成NH3的方向移动。此外,如果让N2和H2的混合气体只一次通过合成塔发生反应也是很不经济的,应将NH3分离后的原料气循环使用,并及时补充N2和H2,使反应物保持一定的浓度,以利于合成氨反应。
总结:工业合成氨的适宜条件
外部条件 工业合成氨的适宜条件
压强
温度
催化剂
浓度
根据反应器可使用的钢材质量及综合指标来选择压强(10~30 MPa)
适宜温度,400~500 ℃
使用铁触媒做催化剂
及时补充N2和H2,并将氨及时从混合气中分离出去
微点拨:
工业生产中,必须从反应限度和反应速率两个角度选择合成氨的适宜条件,既要考虑尽量增大反应物的转化率,充分利用原料,又要选择较快的反应速率,提高单位时间内的产量,同时还要考虑设备的要求、技术条件、经济效益、环境保护等。
核心素养:科学态度与社会责任
合作学习
探究学习
(1)温度越高越利于合成氨反应平衡正向移动。 ( )
(2)合成氨反应中,压强越大越利于增大反应速率和平衡正向移动。 ( )
(3)使用催化剂能提高合成氨反应物的平衡转化率。 ( )
答案: (1)× (2)√ (3)×
小试牛刀
四、工业生产中选择适宜生产条件的原则
(一)影响化学反应进行的因素:参加反应的物质组成、结构和性质等本身因素,还有温度、压强、浓度、催化剂等反应条件。
(二)化学反应的调控需要考虑的因素:在实际生产中常常需要结合设备条件、安全操作、经济成本等情况,综合考虑影响化学反应速率和化学平衡的因素,寻找适宜的生产条件。此外,还要根据环境保护及社会效益等方面的规定和要求做出分析,权衡利弊,才能实施生产。
小结:
核心素养:宏观辨识与微观探析
针对训练
解析:
文质彬彬,然后君子
领袖气质、君子风度科学精神、工匠才干
构建思维导图
科学 技术 社会
.
.
合成氨—实验室研究与工业化生产
教师寄语:
同学们,科学发展的过程是艰辛的,是无数科学家艰苦奋斗的结果。作为新时代青年的我们,更应以他们为榜样,牢记习近平总书记对青年提出的殷切希望,努力学习科学知识,发展自身技能,成长为新时代需要的全能型人才!
