1.3常见的酸 同步练习(含解析)
图片预览




文档简介
1.3 常见的酸
一 、选择题
1.分析下列实验操作正确的是( )
A.稀释浓硫酸 B.称量氢氧化钠固体
C.测定溶液的 pH D.a 处进气收集 O2
2.下列物质能与盐酸反应, 但不产生气体的是( )
A.Fe B.Cu C.CuO D.CaCO3
3.鸡蛋壳的主要成分是碳酸钙。某同学决定利用厨房里常见的物品制作一个“无壳鸡蛋 ”。他可将鸡
蛋泡入( )。
A.白醋 B.黄酒 C.酱油 D.植物油
4.下列物质敞口放置在空气中,质量会 增加但不发生化学反应的是( )
A.浓盐酸 B.氢氧化钠固体
C.熟石灰 D.浓硫酸
5.一瓶没有塞瓶塞的浓盐酸和一瓶没有盖瓶塞的浓硫酸, 一段时间后,下列关于两者溶质质量分数说
法正确的是(不考虑水分蒸发)( )
A.都变大 B.都变小
C.浓盐酸变小,浓硫酸变大 D.浓盐酸变大,浓硫酸变小
6.向稀盐酸中加入 Z 物质, 其 pH 变化情况如图所示,则 Z 物质是( )
A.H2O B.AgNO3 固体 C.浓盐酸 D.NaOH 固体
第 1 页(共 10 页)
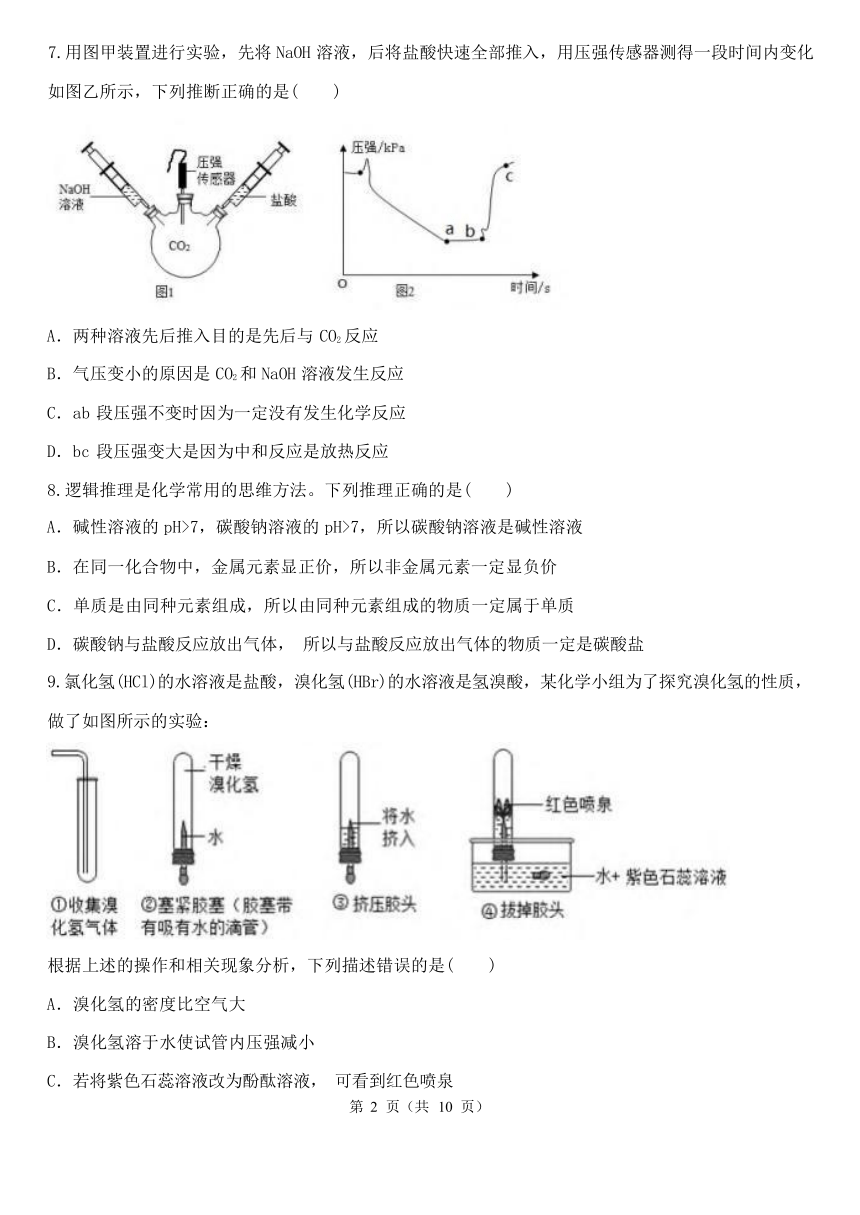
7.用图甲装置进行实验,先将 NaOH 溶液,后将盐酸快速全部推入,用压强传感器测得一段时间内变化
如图乙所示,下列推断正确的是( )
A.两种溶液先后推入目的是先后与 CO2 反应
B.气压变小的原因是 CO2 和 NaOH 溶液发生反应
C.ab 段压强不变时因为一定没有发生化学反应
D.bc 段压强变大是因为中和反应是放热反应
8.逻辑推理是化学常用的思维方法。下列推理正确的是( )
A.碱性溶液的 pH>7,碳酸钠溶液的 pH>7,所以碳酸钠溶液是碱性溶液
B.在同一化合物中,金属元素显正价,所以非金属元素一定显负价
C.单质是由同种元素组成,所以由同种元素组成的物质一定属于单质
D.碳酸钠与盐酸反应放出气体, 所以与盐酸反应放出气体的物质一定是碳酸盐
9.氯化氢(HCl)的水溶液是盐酸,溴化氢(HBr)的水溶液是氢溴酸,某化学小组为了探究溴化氢的性质,
做了如图所示的实验:
根据上述的操作和相关现象分析,下列描述错误的是( )
A.溴化氢的密度比空气大
B.溴化氢溶于水使试管内压强减小
C.若将紫色石蕊溶液改为酚酞溶液, 可看到红色喷泉
第 2 页(共 10 页)
D.试管内液体的 pH<7
10.往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量 y 随加入锌粒的质量变化的图像。
由此可知, y 不可能表示( ) 。
A.硫酸的质量分数 B.生成硫酸锌的质量
C.溶液的 pH D.生成氢气的质量
二 、填空题
11.实验室化学试剂常需要密封保存.比如长期敞口放置浓硫酸, 会因为其具有 而导致
浓度减小, 而浓盐酸会因为具有 也导致浓度减小。
12.由 CO2 和和 CO 组成的混合气体, 为了将它们分开,有同学设计了如图所示的实验装置。图中烧瓶中
盛的是 NaOH 溶液, 分液漏斗中盛的是稀盐酸。
(1)实验开始时关闭活塞 B,让混合气体从导管口进入,所得纯净气体从导管 C 逸出(假设反应完全
进行),此时逸出的气体是 。
(2)混合气体通往完毕后,再关闭活塞 A,打开活塞 B,使分液漏斗中的稀盐酸进入 烧 瓶 ,这时逸
出的气体是 。
13.生活中处处有科学, 根据所学知识回答:
(1)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是 ; (填
字母)
A.食醋 B.食盐水
C.肥皂水 D.氢氧化钠溶液
第 3 页(共 10 页)
(2)公共场所常用“84 消毒液”(NaClO 溶液)进行环境杀菌,NaClO 中 Cl 元素的化合价是 。
(3)驱动氢能汽车的能量来源于氢气燃烧,其反应的基本类型为 。
(4)某同学拆开家中使用过的“暖宝宝 ”,发现内有褐色固体,查阅后得知:“暖宝宝 ”成分中有铁 粉、食盐和水等物质;使用后形成的褐色固体主要是氧化铁和氢氧化铁:其中氢氧化铁受热会分解成
氧化铁和水。据上信息, 你认为该褐色固体可能是“暖宝宝 ”中的物质跟空气中的 发生反应
形成的。
三 、实验题
14.实验室常用锌和稀硫酸来制取氢气, 向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。
(1)写出该反应的化学方程式 。
(2)如图的“ ”“〇 ”“●”表示溶液中由溶质电离产生的不同离子, 则“●”表示 。
(离子符号)
四 、解答题
15.实验室有盐酸、白醋、柠檬酸三种溶液,回答下列问题:
(1)向三氧化二铁(红棕色固体)中放入足量盐酸,充分反应后,观察到的现
象 ;反应的化学方程式是 。 (2)白醋、柠檬酸溶液也能与三氧化二铁发生类似反应,说明白醋、柠檬酸溶液和盐酸中都含有的离
子是 。
(3)理论上溶解 3.2g 三氧化二铁,需要 36.5%的盐酸多少克? (列式计算)
第 4 页(共 10 页)
1.3 常见的酸答案解析
一 、选择题
1.D
【解析】A.根据浓硫酸稀释要“酸入水 ”中分析;
B.根据氢氧化钠有腐蚀性,易潮解分析;
C.根据 pH 试纸的使用方法分析;
D.根据氧气密度小于水分析。
A.稀释浓硫酸时要将浓硫酸沿器壁缓缓倒入水中, 并有玻璃棒搅拌散热,符合题意;
B、氢氧化钠有腐蚀性, 易潮解, 不能放纸上称量, 不符合题意;
C、测溶液 pH 时不能将试纸浸入待测液中,应用玻璃棒蘸取少量液体滴在试纸上测定, 不符合题意;
D、氧气密度小于水,收集氧气时应短导管 a 端进气,符合题意;
故选 D。
2.C
【解析】根据金属活动性顺序中排在氢前的金属能与酸反应产生氢气,排在氢后的金属不能与酸反应,
碳酸盐与酸反应产生二氧化碳气体, 金属氧化物与酸反应生成盐和水分析。
A.铁与盐酸反应会产生氢气,不符合题意;
B、铜不能与盐酸反应, 不符合题意;
C、氧化铜能与盐酸反应生成氯化铜和水, 不产生气体,符合题意;
D、碳酸钙与盐酸反应会产生二氧化碳气体,不符合题意;
故选 C。
3.A
【解析】根据碳酸盐能与酸反应分析。
A.白醋中含有醋酸,醋酸可与碳酸钙反应生成可溶的氯化钙、水和二氧化碳,符合题意;
B、黄酒中成分不能与碳酸钙反应,不符合题意;
C、酱油中成分不能与碳酸钙反应,不符合题意;
D、植物油中成分不能与碳酸钙反应, 不符合题意;
故选 A.
第 5 页(共 10 页)
4.D
【解析】根据浓盐酸的挥发性、氢氧化钠和氢氧化钙与空气中二氧化碳反应的性质、浓硫酸的吸水性
分析。
A.浓盐酸具有挥发性, 敞口放置在空气中质量会减少, 不符合题意;
B、氢氧化钠具有潮解性和与二氧化碳反应的性质,敞口放置在空气中质量会增加,但发生了化学变化 ,
不符合题意;
C、 熟石灰敞口放置在空气中与空气中二氧化碳反应,质量会增加, 发生了化学变化 ,不符合题意;
D、浓硫酸具有吸水性, 敞口放置在空气中,质量会增大, 且发生的是物理变化 ,符合题意;
故选 D。
5.B
【解析】根据浓盐酸有挥发性、浓硫酸的吸水性分析。
浓盐酸有挥发性,敞口放置时会挥发出溶质氯化氢,使溶质质量分数变小, 浓硫酸的吸水性,敞口放
置时会吸收空气中水份而使溶液质量增加,溶质质量分数变小;
故选 B。
6.B
【解析】盐酸是酸性 pH<7,pH=7 是中性,pH>7 是碱性。
A.稀盐酸中加水是稀释导致酸性减小,pH 会变大,A 错误;
B.盐酸会与硝酸银反应:AgNO3+HCl=AgCl↓+HNO3,反应后生成了氯化银沉淀和
硝酸使溶液还是酸性,B 正确;
C.向稀盐酸中加入浓盐酸,溶液酸性变强 pH 会变小,C 错误;
D.向稀盐酸中加入氢氧化钠会发生化学反应, 生成氯化钠和水,导致 pH 值会
变大, D 错误;
故答案为:B
7.B
【解析】根据图像乙可知,先将氢氧化钠溶液全部推入, 由于容器中二氧化碳受到挤压,因此会有小 段时间压强增大;随着氢氧化钠溶液和二氧化碳的反应生成碳酸钠和水,使容器内气压迅速减小。当
到达 a 点时,二氧化碳全部反应完毕,由于这时稀盐酸还没有推入, 所以 ab 段容器内气压保持不变。
第 6 页(共 10 页)
b 点时,由于稀盐酸的推入,它先与容器中的氢氧化钠溶液发生中和反应并放出热量,再与生成的碳酸
钠反应生成二氧化碳气体,所以 bc 段容器内的气压不断增大。
A.稀盐酸不能与二氧化碳气体反应, 故 A 错误;
B.气压变小的原因是 CO2 和 NaOH 溶液发生反应, 故 B 正确;
C.ab 段压强不变时,说明二氧化碳和氢氧化钠的反应结束,但是氢氧化钠与盐酸反应压强也是不变的,
因此不能说明此时没有发生化学反应,故 C 错误;
D.bc 段压强变大是因为碳酸钠和稀盐酸反应生成二氧化碳,故 D 错误。
故选 B。
8.A
【解析】A.根据碱性溶液 pH 大于 7 分析;
B.根据非金属元素可能显正价可能显负价分析;
C.根据单质是同种元素组成的纯净物分析;
D.根据活泼金属和碳酸盐都能与酸反应产生气体分析。
A.碱性溶液的 pH>7,碳酸钠溶液的 pH>7,所以碳酸钠溶液是碱性溶液 ,符合题意;
B. 在同一化合物中,金属元素显正价,非金属元素可能显负价可能显正价 ,
不符合题意;
C. 由同种元素组成的物质不一定属于单质, 也可能是混合物 ,不符合题意;
D. 与盐酸反应放出气体的物质不一定是碳酸盐也可能是活泼金属 ,不符合
题意;
故选 A.
9.C
【解析】常用气体的发生装置和收集装置,酸的化学性质, 溶液的酸碱性与 pH 值的关系。据此回答。
A.收集装置为向上排空气法收集装置,所以可知溴化氢密度比空气大, 选项 A 正确。
B、根据②③④现象可知, 内部压强减小, 说明溴化氢溶于水, 使内部气体减小, 外界大气压将水压入
试管, 形成喷泉,选项 B 正确。
C.酚酞在酸性溶液中不变色,不会看到蓝色喷泉, 选项 C 错误。
D.溴化氢溶于水, 形成酸性溶液,溶液 pH<7,选项 D 正确。
第 7 页(共 10 页)
故选 C。
10.A
【解析】根据锌与硫酸反应生成硫酸锌和氢气,反应物质量会减少,生成物质量会增加,至反应结束
不再改变, 溶液 pH 会从小于 7 增加至等于 7 分析。
A.硫酸的质量会随着锌的加入发生反应而减少,符合题意;
B.生成硫酸锌的质量会随锌的加入而增加,至硫酸反应结束后不再改变,不
符合题意;
C.盐酸为酸, 溶液 pH 小于 7,产生硫酸锌为中性溶液, pH 等于 7,加入锌后,溶液的 pH 会从小于 7
增加至反应结束后不再发生改变 ,不符合题意;
D.生成氢气质量会随锌的加入而增加,至硫酸反应结束后不再改变,不符合
题意;
故选 A.
二 、填空题
11.吸水性;挥发性
【解析】根据浓硫酸具有吸水性,浓盐酸具有挥发性分析。
浓硫酸具有吸水性, 敞口放置会因吸水使溶剂质量增加, 浓度减小,浓盐酸具有挥发性,敞口放置会
因挥发出氯化氢使溶质质量减小,浓度减小。
故答案为: 吸水性; 挥发性。
12.(1)CO
(2)CO2
【解析】根据二氧化碳与氢氧化钠反应生成碳酸钠和水, 一氧化碳不与氢氧化钠反应, 碳酸钠与盐酸
反应生成二氧化碳分析。
(1)二氧化碳能与氢氧化钠溶液反应,所以关闭活塞 b,让混合气体从导管口进入,二氧化碳与氢氧
化钠反应生成碳酸钠和水,一氧化碳气体从导管 C 逸出;
(2) 混合气体通往完毕后,再关闭活塞 A,打开活塞 B,使分液漏斗中的稀盐酸进入烧瓶 ,盐酸与
碳酸钠反应生成二氧化碳;
故答案为:(1)CO;(2) CO2 。
13.(1)C
第 8 页(共 10 页)
(2)+1
(3)化合
(4)氧气
【解析】(1)根据酸碱中和反应分析;
(2)根据化合物中元素化合价代数和为 0 分析;
(3)根据多变一的为化合反应分析;
(4)根据铁与氧气、水等反应可生锈分析。
(1) 蚊虫分泌出蚁酸 ,要减轻疼痛可涂抹碱性物质, 食醋呈酸性,A 错误;食盐水呈中性,B 错误;
肥皂水呈碱性, C 正确; 氢氧化钠溶液呈碱性,但具有腐蚀性,D 错误;
(2) NaClO 中钠元素为+1 价, 氧元素为-2 价, 根据化合物中元素化合价代数和为 0 可知, Cl 元素
的化合价是+1;
(3)氢气燃烧是氢气与氧气反应生成水, 属于化合反应;
(4) “暖宝宝”中有铁粉,根据质量守恒定律可知,要生成氧化铁或氢氧化铁, 可能是铁与氧气、
水等物质发生的反应;
故答案为:(1)C;(2)+1;(3)化合;(4)氧气。
三 、实验题
14.(1)Zn+H2SO4 =ZnSO4 +H2 ↑
(2)SO -
【解析】实验室制取氢气的化学方程式: Zn+H2SO4 =ZnSO4 +H2 ↑
(1)该反应的化学方程式为: Zn+H2SO4 =ZnSO4 +H2 ↑
(2)图中是由溶质电离产生的不同离子, “ ”表示SO4 (2) ; “〇 ”表示 H+ ;“●” 表示 Zn2+
故答案为:(1) Zn+H2SO4 =ZnSO4 +H2 ↑ (2)SO4 (2)
四 、解答题
15.(1)红色固体溶解,溶液由无色变为黄色;Fe2O3+6HCl=2FeCl3+3H2O
(2)H+
(3)12
【解析】(1)依据氧化铁与盐酸的反应情况进行分析书写即可;(2)依据白醋、柠檬酸溶液也能与三 第 9 页(共 10 页)
氧化二铁发生类似反应可知:这两种物质均呈酸性,据此回答即可;(3)根据化学方程式的计算,据 氧化铁质量求盐酸的质量即可; 此题是对金属氧化物与酸的反应的考查,解题的关键是掌握酸性的实
质以及相关的化学方程式的计算,题型基础能强化对基础知识的掌握.
解:(1)氧化铁与盐酸的反应可生成氯化铁和水, 氯化铁的溶液呈黄色,其方程式为:
Fe2O3+6HCl=2FeCl3+3H2O;(2)由于白醋、柠檬酸溶液也能与三氧化二铁发生类似反应,所以这两种物
质的溶液均呈酸性, 从而可说明白醋、柠檬酸溶液和盐酸中都含有的离子是氢离子;(3)设理论上溶
解 3.2g 三氧化二铁,需要 36.5%的盐酸质量是 x
Fe2O3+6HCl=2FeCl3+3H2O
56×2+16×3 6×(1+35.5)
3.2g x×36.5%
160 3.2g
=
219 x × 36.5%
x=12g
故答案为:(1)红色固体溶解, 溶液由无色变为黄色; Fe2O3+6HCl=2FeCl3+3H2O;(2)H+ ;(3)12.
第 10 页(共 10 页)
一 、选择题
1.分析下列实验操作正确的是( )
A.稀释浓硫酸 B.称量氢氧化钠固体
C.测定溶液的 pH D.a 处进气收集 O2
2.下列物质能与盐酸反应, 但不产生气体的是( )
A.Fe B.Cu C.CuO D.CaCO3
3.鸡蛋壳的主要成分是碳酸钙。某同学决定利用厨房里常见的物品制作一个“无壳鸡蛋 ”。他可将鸡
蛋泡入( )。
A.白醋 B.黄酒 C.酱油 D.植物油
4.下列物质敞口放置在空气中,质量会 增加但不发生化学反应的是( )
A.浓盐酸 B.氢氧化钠固体
C.熟石灰 D.浓硫酸
5.一瓶没有塞瓶塞的浓盐酸和一瓶没有盖瓶塞的浓硫酸, 一段时间后,下列关于两者溶质质量分数说
法正确的是(不考虑水分蒸发)( )
A.都变大 B.都变小
C.浓盐酸变小,浓硫酸变大 D.浓盐酸变大,浓硫酸变小
6.向稀盐酸中加入 Z 物质, 其 pH 变化情况如图所示,则 Z 物质是( )
A.H2O B.AgNO3 固体 C.浓盐酸 D.NaOH 固体
第 1 页(共 10 页)
7.用图甲装置进行实验,先将 NaOH 溶液,后将盐酸快速全部推入,用压强传感器测得一段时间内变化
如图乙所示,下列推断正确的是( )
A.两种溶液先后推入目的是先后与 CO2 反应
B.气压变小的原因是 CO2 和 NaOH 溶液发生反应
C.ab 段压强不变时因为一定没有发生化学反应
D.bc 段压强变大是因为中和反应是放热反应
8.逻辑推理是化学常用的思维方法。下列推理正确的是( )
A.碱性溶液的 pH>7,碳酸钠溶液的 pH>7,所以碳酸钠溶液是碱性溶液
B.在同一化合物中,金属元素显正价,所以非金属元素一定显负价
C.单质是由同种元素组成,所以由同种元素组成的物质一定属于单质
D.碳酸钠与盐酸反应放出气体, 所以与盐酸反应放出气体的物质一定是碳酸盐
9.氯化氢(HCl)的水溶液是盐酸,溴化氢(HBr)的水溶液是氢溴酸,某化学小组为了探究溴化氢的性质,
做了如图所示的实验:
根据上述的操作和相关现象分析,下列描述错误的是( )
A.溴化氢的密度比空气大
B.溴化氢溶于水使试管内压强减小
C.若将紫色石蕊溶液改为酚酞溶液, 可看到红色喷泉
第 2 页(共 10 页)
D.试管内液体的 pH<7
10.往一定量的稀硫酸中加入过量的锌粒,如图是反应过程中某种量 y 随加入锌粒的质量变化的图像。
由此可知, y 不可能表示( ) 。
A.硫酸的质量分数 B.生成硫酸锌的质量
C.溶液的 pH D.生成氢气的质量
二 、填空题
11.实验室化学试剂常需要密封保存.比如长期敞口放置浓硫酸, 会因为其具有 而导致
浓度减小, 而浓盐酸会因为具有 也导致浓度减小。
12.由 CO2 和和 CO 组成的混合气体, 为了将它们分开,有同学设计了如图所示的实验装置。图中烧瓶中
盛的是 NaOH 溶液, 分液漏斗中盛的是稀盐酸。
(1)实验开始时关闭活塞 B,让混合气体从导管口进入,所得纯净气体从导管 C 逸出(假设反应完全
进行),此时逸出的气体是 。
(2)混合气体通往完毕后,再关闭活塞 A,打开活塞 B,使分液漏斗中的稀盐酸进入 烧 瓶 ,这时逸
出的气体是 。
13.生活中处处有科学, 根据所学知识回答:
(1)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是 ; (填
字母)
A.食醋 B.食盐水
C.肥皂水 D.氢氧化钠溶液
第 3 页(共 10 页)
(2)公共场所常用“84 消毒液”(NaClO 溶液)进行环境杀菌,NaClO 中 Cl 元素的化合价是 。
(3)驱动氢能汽车的能量来源于氢气燃烧,其反应的基本类型为 。
(4)某同学拆开家中使用过的“暖宝宝 ”,发现内有褐色固体,查阅后得知:“暖宝宝 ”成分中有铁 粉、食盐和水等物质;使用后形成的褐色固体主要是氧化铁和氢氧化铁:其中氢氧化铁受热会分解成
氧化铁和水。据上信息, 你认为该褐色固体可能是“暖宝宝 ”中的物质跟空气中的 发生反应
形成的。
三 、实验题
14.实验室常用锌和稀硫酸来制取氢气, 向盛有稀硫酸溶液的烧杯中加入足量的锌至反应完全。
(1)写出该反应的化学方程式 。
(2)如图的“ ”“〇 ”“●”表示溶液中由溶质电离产生的不同离子, 则“●”表示 。
(离子符号)
四 、解答题
15.实验室有盐酸、白醋、柠檬酸三种溶液,回答下列问题:
(1)向三氧化二铁(红棕色固体)中放入足量盐酸,充分反应后,观察到的现
象 ;反应的化学方程式是 。 (2)白醋、柠檬酸溶液也能与三氧化二铁发生类似反应,说明白醋、柠檬酸溶液和盐酸中都含有的离
子是 。
(3)理论上溶解 3.2g 三氧化二铁,需要 36.5%的盐酸多少克? (列式计算)
第 4 页(共 10 页)
1.3 常见的酸答案解析
一 、选择题
1.D
【解析】A.根据浓硫酸稀释要“酸入水 ”中分析;
B.根据氢氧化钠有腐蚀性,易潮解分析;
C.根据 pH 试纸的使用方法分析;
D.根据氧气密度小于水分析。
A.稀释浓硫酸时要将浓硫酸沿器壁缓缓倒入水中, 并有玻璃棒搅拌散热,符合题意;
B、氢氧化钠有腐蚀性, 易潮解, 不能放纸上称量, 不符合题意;
C、测溶液 pH 时不能将试纸浸入待测液中,应用玻璃棒蘸取少量液体滴在试纸上测定, 不符合题意;
D、氧气密度小于水,收集氧气时应短导管 a 端进气,符合题意;
故选 D。
2.C
【解析】根据金属活动性顺序中排在氢前的金属能与酸反应产生氢气,排在氢后的金属不能与酸反应,
碳酸盐与酸反应产生二氧化碳气体, 金属氧化物与酸反应生成盐和水分析。
A.铁与盐酸反应会产生氢气,不符合题意;
B、铜不能与盐酸反应, 不符合题意;
C、氧化铜能与盐酸反应生成氯化铜和水, 不产生气体,符合题意;
D、碳酸钙与盐酸反应会产生二氧化碳气体,不符合题意;
故选 C。
3.A
【解析】根据碳酸盐能与酸反应分析。
A.白醋中含有醋酸,醋酸可与碳酸钙反应生成可溶的氯化钙、水和二氧化碳,符合题意;
B、黄酒中成分不能与碳酸钙反应,不符合题意;
C、酱油中成分不能与碳酸钙反应,不符合题意;
D、植物油中成分不能与碳酸钙反应, 不符合题意;
故选 A.
第 5 页(共 10 页)
4.D
【解析】根据浓盐酸的挥发性、氢氧化钠和氢氧化钙与空气中二氧化碳反应的性质、浓硫酸的吸水性
分析。
A.浓盐酸具有挥发性, 敞口放置在空气中质量会减少, 不符合题意;
B、氢氧化钠具有潮解性和与二氧化碳反应的性质,敞口放置在空气中质量会增加,但发生了化学变化 ,
不符合题意;
C、 熟石灰敞口放置在空气中与空气中二氧化碳反应,质量会增加, 发生了化学变化 ,不符合题意;
D、浓硫酸具有吸水性, 敞口放置在空气中,质量会增大, 且发生的是物理变化 ,符合题意;
故选 D。
5.B
【解析】根据浓盐酸有挥发性、浓硫酸的吸水性分析。
浓盐酸有挥发性,敞口放置时会挥发出溶质氯化氢,使溶质质量分数变小, 浓硫酸的吸水性,敞口放
置时会吸收空气中水份而使溶液质量增加,溶质质量分数变小;
故选 B。
6.B
【解析】盐酸是酸性 pH<7,pH=7 是中性,pH>7 是碱性。
A.稀盐酸中加水是稀释导致酸性减小,pH 会变大,A 错误;
B.盐酸会与硝酸银反应:AgNO3+HCl=AgCl↓+HNO3,反应后生成了氯化银沉淀和
硝酸使溶液还是酸性,B 正确;
C.向稀盐酸中加入浓盐酸,溶液酸性变强 pH 会变小,C 错误;
D.向稀盐酸中加入氢氧化钠会发生化学反应, 生成氯化钠和水,导致 pH 值会
变大, D 错误;
故答案为:B
7.B
【解析】根据图像乙可知,先将氢氧化钠溶液全部推入, 由于容器中二氧化碳受到挤压,因此会有小 段时间压强增大;随着氢氧化钠溶液和二氧化碳的反应生成碳酸钠和水,使容器内气压迅速减小。当
到达 a 点时,二氧化碳全部反应完毕,由于这时稀盐酸还没有推入, 所以 ab 段容器内气压保持不变。
第 6 页(共 10 页)
b 点时,由于稀盐酸的推入,它先与容器中的氢氧化钠溶液发生中和反应并放出热量,再与生成的碳酸
钠反应生成二氧化碳气体,所以 bc 段容器内的气压不断增大。
A.稀盐酸不能与二氧化碳气体反应, 故 A 错误;
B.气压变小的原因是 CO2 和 NaOH 溶液发生反应, 故 B 正确;
C.ab 段压强不变时,说明二氧化碳和氢氧化钠的反应结束,但是氢氧化钠与盐酸反应压强也是不变的,
因此不能说明此时没有发生化学反应,故 C 错误;
D.bc 段压强变大是因为碳酸钠和稀盐酸反应生成二氧化碳,故 D 错误。
故选 B。
8.A
【解析】A.根据碱性溶液 pH 大于 7 分析;
B.根据非金属元素可能显正价可能显负价分析;
C.根据单质是同种元素组成的纯净物分析;
D.根据活泼金属和碳酸盐都能与酸反应产生气体分析。
A.碱性溶液的 pH>7,碳酸钠溶液的 pH>7,所以碳酸钠溶液是碱性溶液 ,符合题意;
B. 在同一化合物中,金属元素显正价,非金属元素可能显负价可能显正价 ,
不符合题意;
C. 由同种元素组成的物质不一定属于单质, 也可能是混合物 ,不符合题意;
D. 与盐酸反应放出气体的物质不一定是碳酸盐也可能是活泼金属 ,不符合
题意;
故选 A.
9.C
【解析】常用气体的发生装置和收集装置,酸的化学性质, 溶液的酸碱性与 pH 值的关系。据此回答。
A.收集装置为向上排空气法收集装置,所以可知溴化氢密度比空气大, 选项 A 正确。
B、根据②③④现象可知, 内部压强减小, 说明溴化氢溶于水, 使内部气体减小, 外界大气压将水压入
试管, 形成喷泉,选项 B 正确。
C.酚酞在酸性溶液中不变色,不会看到蓝色喷泉, 选项 C 错误。
D.溴化氢溶于水, 形成酸性溶液,溶液 pH<7,选项 D 正确。
第 7 页(共 10 页)
故选 C。
10.A
【解析】根据锌与硫酸反应生成硫酸锌和氢气,反应物质量会减少,生成物质量会增加,至反应结束
不再改变, 溶液 pH 会从小于 7 增加至等于 7 分析。
A.硫酸的质量会随着锌的加入发生反应而减少,符合题意;
B.生成硫酸锌的质量会随锌的加入而增加,至硫酸反应结束后不再改变,不
符合题意;
C.盐酸为酸, 溶液 pH 小于 7,产生硫酸锌为中性溶液, pH 等于 7,加入锌后,溶液的 pH 会从小于 7
增加至反应结束后不再发生改变 ,不符合题意;
D.生成氢气质量会随锌的加入而增加,至硫酸反应结束后不再改变,不符合
题意;
故选 A.
二 、填空题
11.吸水性;挥发性
【解析】根据浓硫酸具有吸水性,浓盐酸具有挥发性分析。
浓硫酸具有吸水性, 敞口放置会因吸水使溶剂质量增加, 浓度减小,浓盐酸具有挥发性,敞口放置会
因挥发出氯化氢使溶质质量减小,浓度减小。
故答案为: 吸水性; 挥发性。
12.(1)CO
(2)CO2
【解析】根据二氧化碳与氢氧化钠反应生成碳酸钠和水, 一氧化碳不与氢氧化钠反应, 碳酸钠与盐酸
反应生成二氧化碳分析。
(1)二氧化碳能与氢氧化钠溶液反应,所以关闭活塞 b,让混合气体从导管口进入,二氧化碳与氢氧
化钠反应生成碳酸钠和水,一氧化碳气体从导管 C 逸出;
(2) 混合气体通往完毕后,再关闭活塞 A,打开活塞 B,使分液漏斗中的稀盐酸进入烧瓶 ,盐酸与
碳酸钠反应生成二氧化碳;
故答案为:(1)CO;(2) CO2 。
13.(1)C
第 8 页(共 10 页)
(2)+1
(3)化合
(4)氧气
【解析】(1)根据酸碱中和反应分析;
(2)根据化合物中元素化合价代数和为 0 分析;
(3)根据多变一的为化合反应分析;
(4)根据铁与氧气、水等反应可生锈分析。
(1) 蚊虫分泌出蚁酸 ,要减轻疼痛可涂抹碱性物质, 食醋呈酸性,A 错误;食盐水呈中性,B 错误;
肥皂水呈碱性, C 正确; 氢氧化钠溶液呈碱性,但具有腐蚀性,D 错误;
(2) NaClO 中钠元素为+1 价, 氧元素为-2 价, 根据化合物中元素化合价代数和为 0 可知, Cl 元素
的化合价是+1;
(3)氢气燃烧是氢气与氧气反应生成水, 属于化合反应;
(4) “暖宝宝”中有铁粉,根据质量守恒定律可知,要生成氧化铁或氢氧化铁, 可能是铁与氧气、
水等物质发生的反应;
故答案为:(1)C;(2)+1;(3)化合;(4)氧气。
三 、实验题
14.(1)Zn+H2SO4 =ZnSO4 +H2 ↑
(2)SO -
【解析】实验室制取氢气的化学方程式: Zn+H2SO4 =ZnSO4 +H2 ↑
(1)该反应的化学方程式为: Zn+H2SO4 =ZnSO4 +H2 ↑
(2)图中是由溶质电离产生的不同离子, “ ”表示SO4 (2) ; “〇 ”表示 H+ ;“●” 表示 Zn2+
故答案为:(1) Zn+H2SO4 =ZnSO4 +H2 ↑ (2)SO4 (2)
四 、解答题
15.(1)红色固体溶解,溶液由无色变为黄色;Fe2O3+6HCl=2FeCl3+3H2O
(2)H+
(3)12
【解析】(1)依据氧化铁与盐酸的反应情况进行分析书写即可;(2)依据白醋、柠檬酸溶液也能与三 第 9 页(共 10 页)
氧化二铁发生类似反应可知:这两种物质均呈酸性,据此回答即可;(3)根据化学方程式的计算,据 氧化铁质量求盐酸的质量即可; 此题是对金属氧化物与酸的反应的考查,解题的关键是掌握酸性的实
质以及相关的化学方程式的计算,题型基础能强化对基础知识的掌握.
解:(1)氧化铁与盐酸的反应可生成氯化铁和水, 氯化铁的溶液呈黄色,其方程式为:
Fe2O3+6HCl=2FeCl3+3H2O;(2)由于白醋、柠檬酸溶液也能与三氧化二铁发生类似反应,所以这两种物
质的溶液均呈酸性, 从而可说明白醋、柠檬酸溶液和盐酸中都含有的离子是氢离子;(3)设理论上溶
解 3.2g 三氧化二铁,需要 36.5%的盐酸质量是 x
Fe2O3+6HCl=2FeCl3+3H2O
56×2+16×3 6×(1+35.5)
3.2g x×36.5%
160 3.2g
=
219 x × 36.5%
x=12g
故答案为:(1)红色固体溶解, 溶液由无色变为黄色; Fe2O3+6HCl=2FeCl3+3H2O;(2)H+ ;(3)12.
第 10 页(共 10 页)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
