第一章 第一节 第1课时 根据物质的组成和性质分类 (62张PPT)
文档属性
| 名称 | 第一章 第一节 第1课时 根据物质的组成和性质分类 (62张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-17 00:00:00 | ||
图片预览









文档简介
(共62张PPT)
第一章 第一节
第1课时 根据物质的组成和性质分类
1.了解分类的意义、常用的分类方法,并将其运用到物质的分类上。
2.能从元素组成(宏观)和构成微粒(微观)的角度分析认识物质,根据物质的组成
和性质对物质进行分类,培养宏观辨识与微观探析的意识和能力。
核心素养
发展目标
一、根据物质的组成分类
二、根据物质的性质分类
课时对点练
内容索引
随堂演练 知识落实
根据物质的组成分类
一
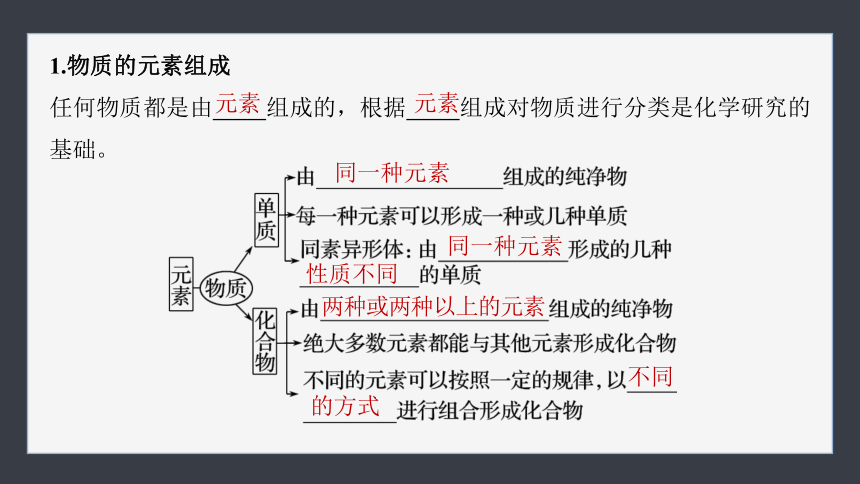
1.物质的元素组成
任何物质都是由 组成的,根据 组成对物质进行分类是化学研究的基础。
元素
元素
同一种元素
同一种元素
性质不同
两种或两种以上的元素
不同
的方式
【思考1】 氧元素形成的同素异形体有 ,碳元素形成的同素异形体有 ,磷元素形成的同素异形体有
。
(1)金刚石与石墨的物理性质相同吗?化学性质相同吗?
(2)O2可以转化为O3,这个转化属于化学变化吗?
提示 物理性质不同,化学性质相同。
提示 属于化学变化。
氧气、臭氧
金刚石、石墨、C60
白磷、红磷
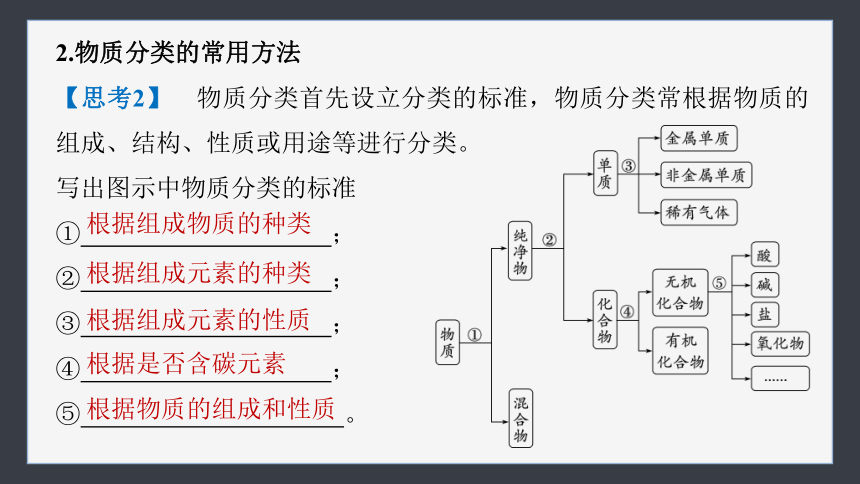
2.物质分类的常用方法
【思考2】 物质分类首先设立分类的标准,物质分类常根据物质的组成、结构、性质或用途等进行分类。
写出图示中物质分类的标准
① ;
② ;
③ ;
④ ;
⑤ 。
根据组成物质的种类
根据组成元素的种类
根据组成元素的性质
根据是否含碳元素
根据物质的组成和性质
(1)树状分类法:对同类事物按照某种标准进行再分类的分类方法。
特点:同一层次的物质类别间一般是相互独立的,没有交叉。
【思考3】 对于Na2CO3,从其组成的阳离子来看,它属于什么盐?从阴离子来看,又属于什么盐?
提示 对于Na2CO3,从其组成的阳离子来看,它属于钠盐;从阴离子来看,属于碳酸盐。
(2)交叉分类法:依据物质的不同属性从不同的角度对物质进行分类的方法。
特点:物质类别之间有部分交叉。
应用体验
1.判断正误
(1)纯净物一定由同种分子构成
(2)只含一种元素的物质一定是单质
(3)氯化钠属于盐,也属于化合物
(4)树状分类法各级之间存在包含关系,如氧化物属于化合物
×
×
√
√
应用体验
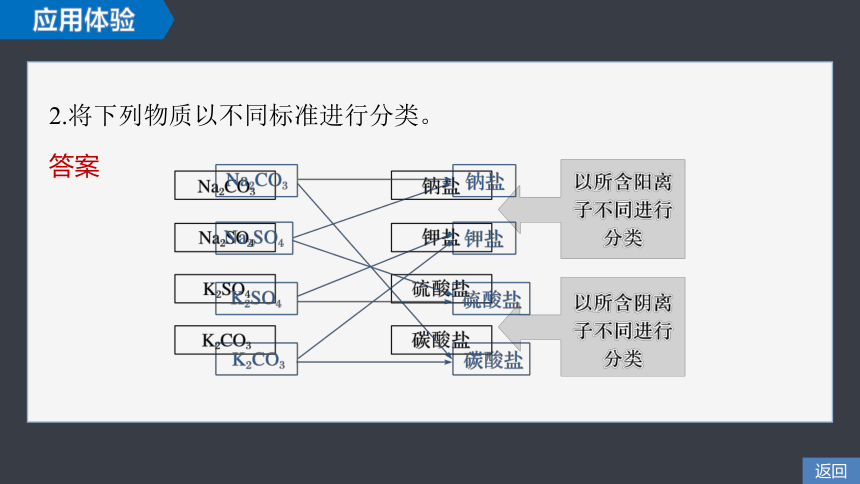
2.将下列物质以不同标准进行分类。
答案
返回
根据物质的性质分类
二
【思考1】 写出CO2与足量澄清石灰水,SO2与足量NaOH溶液,MgO与硫酸,Fe2O3与盐酸反应的化学方程式。体会氧化物的性质。
提示 CO2+Ca(OH)2===CaCO3↓+H2O
SO2+2NaOH===Na2SO3+H2O
MgO+H2SO4===MgSO4+H2O
Fe2O3+6HCl===2FeCl3+3H2O
1.概念
酸性氧化物:和 反应只生成盐和水。
碱性氧化物:和 反应只生成盐和水。
碱
酸
2.氧化物分类
氧化物
按组成元素
金属氧化物:CuO、Fe2O3、Na2O等
非金属氧化物:CO、P2O5、H2O等
按性质
成盐氧化物
酸性氧化物:CO2、Mn2O7等
碱性氧化物:CaO等
两性氧化物:Al2O3等
不成盐氧化物:CO、NO等
【思考2】 举例说明下列说法是否正确。
(1)非金属氧化物一定是酸性氧化物吗? 酸性氧化物一定是非金属氧化物吗?
提示 非金属氧化物大多是酸性氧化物,但不一定全是,如NO、CO不是酸性氧化物;酸性氧化物也不一定是非金属氧化物,如Mn2O7是酸性氧化物,但却是金属氧化物。
(2)金属氧化物一定是碱性氧化物吗?碱性氧化物一定是金属氧化物吗?
提示 金属氧化物大多是碱性氧化物,但不一定全是,如Al2O3是金属氧化物,却是两性氧化物;碱性氧化物一定是金属氧化物。
归纳总结
应用体验
1.判断正误
(1)Na2CO3含有氧元素,所以属于氧化物
(2)CuSO4·5H2O属于混合物
(3)酸性氧化物能溶于水,和水化合生成酸
(4)CH3COOH是多元酸
×
×
×
×
应用体验
2.采用不同的分类方法,可将非金属氧化物分为不同的类别。根据某种共性,可将CO2、P2O5、SO2、SO3归为一类,下列物质中,完全符合此共性而能归为此类物质的是
A.CaO B.CO
C.SiO2 D.H2O
√
CO2、P2O5、SO2、SO3都属于酸性氧化物,CaO属于碱性氧化物,CO和H2O既不属于酸性氧化物,也不属于碱性氧化物。
返回
随堂演练 知识落实
1
2
3
4
1.经测定,一瓶气体中只含有C、O两种元素,通常情况下这瓶气体不可能是
A.一种化合物
B.一种单质和一种化合物的混合物
C.两种化合物
D.两种单质
√
随堂演练
由题意知,瓶中气体中含C、O两种元素,在通常情况下,含C元素的单质为固体,故不能是两种单质。
2.(2022·广西北海教育教学研究室高一质检)下列物质的分类不正确的是
A.水、二氧化硫和干冰都属于氧化物
B.NaHSO4、CuSO4·5H2O和KMnO4都属于盐
C.H2SO4、HNO3、H2CO3都属于酸
D.烧碱、纯碱、熟石灰都属于碱
√
随堂演练
1
2
3
4
随堂演练
1
2
3
4
水、二氧化硫和干冰都是含有两种元素且有一种元素为氧元素的纯净物,都是氧化物,A正确;
NaHSO4、CuSO4·5H2O和KMnO4都是由金属阳离子和酸根阴离子构成的纯净物,都属于盐,B正确;
H2SO4、HNO3、H2CO3为三种含氧酸,C正确;
纯碱为Na2CO3,属于盐,D不正确。
3.化学概念在逻辑上存在如下关系:
下列说法正确的是
A.化合物与纯净物属于重叠关系
B.金属氧化物与碱性氧化物属于交叉关系
C.分解反应与复分解反应属于并列关系
D.钠盐与碳酸盐属于并列关系
√
随堂演练
1
2
3
4
4.下列五组物质,每组中有一种物质从某种角度分析与其他三种不同,请找出该物质,并说明理由。
(1)Fe、S、C、P______________。
(2)H2、O2、N2、S__________________。
(3)Fe2O3、Na2CO3、CuO、H2O_____________________。
(4)AgCl、BaSO4、KNO3、CaCO3_________________________________
_______________________。
随堂演练
1
2
3
4
Fe;Fe为金属
S;常温下S为固体
Na2CO3;Na2CO3为盐
KNO3;KNO3易溶于水(或AgCl;
AgCl酸根离子中不含氧)
返回
课时对点练
1
2
3
4
5
6
7
8
9
题组一 根据物质的组成分类
1.(2022·温州高一期中)航天员王亚平在“天宫课堂”演示了失重条件下水球包裹泡腾片的实验。泡腾片里含有碳酸氢钠,碳酸氢钠属于
A.酸 B.碱 C.盐 D.氧化物
√
10
11
12
13
14
15
对点训练
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
2.(2023·无锡高一检测)下列各组物质,按单质、化合物、混合物顺序排列的是
A.铝、纯碱、盐酸 B.红磷、熟石灰、水
C.石墨、稀硫酸、胆矾 D.石灰水、干冰、空气
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
铝是单质,纯碱是碳酸钠,为化合物,盐酸是混合物,A正确;
红磷是单质,熟石灰是氢氧化钙,为化合物,水是纯净物,B错误;
石墨是单质,稀硫酸是混合物,胆矾是五水硫酸铜,为化合物,C错误;
石灰水是混合物,干冰是二氧化碳,为化合物,空气为混合物,D错误。
2
3.(2022·江西奉新一中高一月考)下列关于同素异形体的说法正确的是
A.红磷转化为白磷属于物理变化
B.石墨导电,金刚石不导电,故二者不互为同素异形体
C.O2和O3的分子式不同,但结构相同
D.S2、S4、S8都是硫元素的同素异形体
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
2
红磷与白磷互为同素异形体,属于不同物质,它们之间的转化属于化学变化,A项错误;
石墨和金刚石互为同素异形体,同素异形体的物理性质一般不同,B项错误;
O2和O3的结构不同,C项错误;
S2、S4、S8为硫元素的不同单质,它们互为同素异形体,D项正确。
4.硝酸钾是一种无氯氮钾复合肥,宜在种植水果、蔬菜、花卉时使用,下列关于KNO3的说法不正确的是
A.从其阳离子看,属于钾盐 B.含有氧元素,属于氧化物
C.它属于正盐 D.从其阴离子看,属于硝酸盐
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
硝酸钾含有钾离子和硝酸根离子,从其阳离子看,属于钾盐,从其阴离子看,属于硝酸盐,故A、D正确;
氧化物只含有两种元素,硝酸钾属于含氧酸盐,故B错误。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
5.(2022·长春第一五一中学高一质检)下列说法正确的是
A.Na2SO4·10H2O是混合物
B.同种分子构成的物质一定是纯净物
C.混合物肯定由两种或两种以上元素组成
D.含有氧元素的化合物都是氧化物
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
Na2SO4·10H2O由单一物质组成,属于纯净物,故A错误;
纯净物由一种物质组成,所以同种分子构成的物质一定是纯净物,故B正确;
混合物可能由一种元素组成,如氧气和臭氧的混合物,故C错误;
含有氧元素的化合物不一定是氧化物,如含氧酸或含氧酸盐等,故D错误。
2
题组二 根据物质的性质分类
6.下列物质中能与水反应的碱性氧化物是
A.CO2 B.CuO C.Fe2O3 D.CaO
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
CO2是酸性氧化物;CuO、Fe2O3和CaO虽然都是碱性氧化物,但只有CaO能与H2O反应生成Ca(OH)2。
7.科学家通过电解Fe2O3、SiO2、CaO的熔融液(1 600 ℃)制得铁。按照树状分类法对Fe2O3、SiO2、CaO这三种物质进行分类,其中正确的是
A.均属于酸性氧化物
B.均属于金属氧化物
C.均属于纯净物
D.均属于非金属氧化物
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
SiO2是酸性氧化物,Fe2O3、CaO是碱性氧化物,故A错误;
SiO2是非金属氧化物,Fe2O3、CaO是金属氧化物,故B、D错误;
Fe2O3、SiO2、CaO都是化合物,即都是纯净物,故C正确。
2
8.(2022·河南商丘市第一高级中学高一期末)下列物质的分类正确的是
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
2
选项 碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 H2SO4 Cu2(OH)2CO3 CO2 SO3
B Ba(OH)2 HCl NaCl Na2O CO
C 氨水 HClO NaHCO3 MgO CO2
D KOH HNO3 CaCO3 CaO SO2
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
纯碱是碳酸钠,属于盐,CO2是酸性氧化物,故A错误;
CO是不成盐氧化物,故B错误;
氨水是混合物,故C错误。
2
9.(2022·吉林抚松第五中学高一质检)下列图示错误的是
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
FeO能与酸反应生成盐和水,属于碱性氧化物,FeO中Fe元素为+2价,属于+2价铁的化合物,也属于铁的氧化物,且碱性氧化物、铁的氧化物、+2价铁的化合物属于交叉关系,故A正确;
Na2SO4只含酸根阴离子和金属阳离子,属于正盐,含有钠离子属于钠盐,含有硫酸根离子属于硫酸盐,且正盐、钠盐、硫酸盐属于交叉关系,故B正确;
2
综合强化
1
3
4
5
6
7
8
9
10
11
12
13
14
15
H2SO4的酸根阴离子中含有O元素,属于含氧酸,硫酸在水溶液中完全电离,属于强酸,一个硫酸分子可以电离出两个氢离子,所以属于二元酸,且含氧酸、强酸、二元酸属于交叉关系,故C正确;
三种物质的类别关系错误,应为 ,故D错误。
2
综合强化
10.某校实验室将试剂分类后放在不同的试剂柜里,已存放的部分试剂如下表:
1
3
4
5
6
7
8
9
10
11
12
13
14
15
2
综合强化
试剂柜号 ① ② ③ ④
试剂 NaOH、Ca(OH)2 盐酸、硫酸 MnO2、CuO NaCl、Na2SO4
该实验室新购进部分氧化钙和纯碱,应将它们分别放在
A.③和① B.④和①
C.①和② D.③和④
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
根据表中信息可判断①中存放的是碱,②中存放的是酸,③中存放的是氧化物,④中存放的是盐。氧化钙属于氧化物,应放在③中;纯碱是碳酸钠,属于盐,应放在④中。
2
综合强化
试剂柜号 ① ② ③ ④
试剂 NaOH、Ca(OH)2 盐酸、硫酸 MnO2、CuO NaCl、Na2SO4
11.酸式盐是盐的一类,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,则下列说法正确的是
A.H3PO2属于二元酸 B.H3PO2属于三元酸
C.NaH2PO2属于酸式盐 D.NaH2PO2属于正盐
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
2
综合强化
由于H3PO2与足量的NaOH反应只生成一种盐NaH2PO2,故H3PO2为一元酸,NaH2PO2属于正盐。
12.已知化学反应:
Ⅰ.Na2O+H2O===2NaOH
Ⅱ.2Na2O2+2H2O===4NaOH+O2↑
Ⅲ.N2O5+H2O===2HNO3
Ⅳ.3NO2+H2O===2HNO3+NO
下列说法错误的是
A.Na2O是碱性氧化物
B.N2O5是酸性氧化物
C.Na2O2是一种金属氧化物,它跟水的反应是置换反应
D.Ⅰ和Ⅲ是没有元素化合价变化的反应,Ⅱ和Ⅳ是有元素化合价变化的反应
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
A对,Na2O跟酸反应只生成盐和水,它是碱性氧化物;
D对,Ⅱ中Na2O2、NaOH、O2所含氧元素的化合价依次为-1、-2、0,则该反应是有元素化合价变化的反应;Ⅳ中NO2、HNO3、NO所含氮元素的化合价依次为+4、+5、+2,则该反应是有元素化合价变化的反应。
13.分类是一种重要的方法,阅读下列材料并填空。
由于①煤和②石油通常都含有硫元素,燃烧时会生成③SO2。当SO2溶于④H2O时,会形成⑤H2SO3,H2SO3在PM2.5存在的条件下,在空气中会迅速生成⑥H2SO4(酸雨的主要成分)。
石灰法是目前应用最广泛的工业脱硫方法,过程如下:通过煅烧⑦CaCO3得到⑧CaO,再与废气中的SO2反应生成CaSO3,最后与⑨O2作用生成
⑩CaSO4而将硫固定,生成的产物可作建筑材料。
(1)在上述材料中标有序号的物质中,属于混合物的是________(填序号,下同);属于氧化物的是________;属于酸的是______。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
①②
③④⑧
⑤⑥
(2)从物质组成角度来看,CaCO3、CaSO3、CaSO4都属于______。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
从物质组成角度来看,CaCO3、CaSO3、CaSO4都是由金属阳离子与酸根阴离子组成的化合物,因此三种物质都属于盐。
盐
(3)从物质类别角度来看,SO2属于________(填 “酸性”“碱性”或“两性”)氧化物,写出其与CaO发生反应的化学方程式:_________________,属于四种基本反应类型中的__________。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
从物质类别角度来看,SO2与水反应生成H2SO3,因此属于酸性氧化物;SO2与CaO反应生成CaSO3,化学方程式为SO2+CaO===CaSO3,该反应的反应物是两种,生成物是一种,因此反应类型属于化合反应。
酸性
SO2+CaO===CaSO3
化合反应
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
14.无机化合物可根据其组成和性质进行分类。
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
(1)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②④⑥⑧⑩后面。
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ②______ ③NaOH ④______ ⑤Na2SO4 ⑥______ ⑦SO2 ⑧____ ⑨NH3
⑩____
HNO3
KOH
K2SO4
SO3
H2S
答案 其他合理答案均可
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
H、O、N组成的硝酸或H、O、S组成的亚硫酸属于酸;K、H、O组成的KOH或H、O、N组成的一水合氨属于碱;K、O、N组成的硝酸钾或Na、O、N组成的硝酸钠等属于盐;K、Na、H、S、N分别可与O组成氧化物;K、Na、O、S、N分别可与H组成氢化物。
2
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ②HNO3 ③NaOH ④KOH ⑤Na2SO4 ⑥K2SO4 ⑦SO2 ⑧SO3 ⑨NH3
⑩H2S
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
(2)SO2和CO2都属于酸性氧化物,在化学性质上有很多相似的地方,请写出少量的⑦与③反应的化学方程式:___________________________。
SO2+2NaOH===Na2SO3+H2O
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ②HNO3 ③NaOH ④KOH ⑤Na2SO4 ⑥K2SO4 ⑦SO2 ⑧SO3 ⑨NH3
⑩H2S
少量的SO2与NaOH反应生成亚硫酸钠和水,反应的化学方程式为SO2+2NaOH===Na2SO3+H2O。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
(3)只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称为氢化物。下列物质不属于氢化物的是_____(填字母)。
A.H2SO4 B.HCl
C.NaH D.H2O
A
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
15.根据物质的分类方法,回答下列问题。
(1)现有两组单质:(Ⅰ)氧气、氢气、硫、氯气;(Ⅱ)铁、钠、铝、硅。
试从不同角度对每组单质进行分类,则每组单质中均有一种单质与其他单质属于不同“类”。请将该单质(写化学符号)和分类依据填在下列表格中。
2
组别 第(Ⅰ)组 第(Ⅱ)组
不同“类”单质 Si
分类依据
S
物质状态
金属与非金属
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
第(Ⅰ)组中四种单质,除硫外其余均为气体,第(Ⅱ)组中四种单质,除硅外其余均为金属。
组别 第(Ⅰ)组 第(Ⅱ)组
不同“类”单质 Si
分类依据
S
物质状态
金属与非金属
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
(2)观察下列物质变化(有的化学方程式未配平),有同学将反应①③划为一类,②划为另一类。则将①和③划为一类的依据是________________
_______________。
①NO+NO2―→N2O3
②NH3+HNO3―→NH4NO3
③NH3+NO2―→N2+H2O
2
反应中都有元素
化合价发生变化
①和③划为一类的依据是反应中都有元素化合价发生变化,而②没有。
氢溴酸(HBr)与HCl化学性质相似,因为HCl不能与银发生反应,所以HBr也不能与银发生反应。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
(3)某同学根据性质划分,把氢溴酸(HBr)与HCl划为一类,其理由是它们的化学性质十分相似。据此判断下列反应不会发生的是______(填字母)。
A.2HBr+Na2CO3===2NaBr+H2O+CO2↑
B.HBr+AgNO3===AgBr↓+HNO3
C.HBr+NaOH===NaBr+H2O
D.2HBr+2Ag===2AgBr+H2↑
D
2
返回
本课结束
第一章 第一节
第1课时 根据物质的组成和性质分类
1.了解分类的意义、常用的分类方法,并将其运用到物质的分类上。
2.能从元素组成(宏观)和构成微粒(微观)的角度分析认识物质,根据物质的组成
和性质对物质进行分类,培养宏观辨识与微观探析的意识和能力。
核心素养
发展目标
一、根据物质的组成分类
二、根据物质的性质分类
课时对点练
内容索引
随堂演练 知识落实
根据物质的组成分类
一
1.物质的元素组成
任何物质都是由 组成的,根据 组成对物质进行分类是化学研究的基础。
元素
元素
同一种元素
同一种元素
性质不同
两种或两种以上的元素
不同
的方式
【思考1】 氧元素形成的同素异形体有 ,碳元素形成的同素异形体有 ,磷元素形成的同素异形体有
。
(1)金刚石与石墨的物理性质相同吗?化学性质相同吗?
(2)O2可以转化为O3,这个转化属于化学变化吗?
提示 物理性质不同,化学性质相同。
提示 属于化学变化。
氧气、臭氧
金刚石、石墨、C60
白磷、红磷
2.物质分类的常用方法
【思考2】 物质分类首先设立分类的标准,物质分类常根据物质的组成、结构、性质或用途等进行分类。
写出图示中物质分类的标准
① ;
② ;
③ ;
④ ;
⑤ 。
根据组成物质的种类
根据组成元素的种类
根据组成元素的性质
根据是否含碳元素
根据物质的组成和性质
(1)树状分类法:对同类事物按照某种标准进行再分类的分类方法。
特点:同一层次的物质类别间一般是相互独立的,没有交叉。
【思考3】 对于Na2CO3,从其组成的阳离子来看,它属于什么盐?从阴离子来看,又属于什么盐?
提示 对于Na2CO3,从其组成的阳离子来看,它属于钠盐;从阴离子来看,属于碳酸盐。
(2)交叉分类法:依据物质的不同属性从不同的角度对物质进行分类的方法。
特点:物质类别之间有部分交叉。
应用体验
1.判断正误
(1)纯净物一定由同种分子构成
(2)只含一种元素的物质一定是单质
(3)氯化钠属于盐,也属于化合物
(4)树状分类法各级之间存在包含关系,如氧化物属于化合物
×
×
√
√
应用体验
2.将下列物质以不同标准进行分类。
答案
返回
根据物质的性质分类
二
【思考1】 写出CO2与足量澄清石灰水,SO2与足量NaOH溶液,MgO与硫酸,Fe2O3与盐酸反应的化学方程式。体会氧化物的性质。
提示 CO2+Ca(OH)2===CaCO3↓+H2O
SO2+2NaOH===Na2SO3+H2O
MgO+H2SO4===MgSO4+H2O
Fe2O3+6HCl===2FeCl3+3H2O
1.概念
酸性氧化物:和 反应只生成盐和水。
碱性氧化物:和 反应只生成盐和水。
碱
酸
2.氧化物分类
氧化物
按组成元素
金属氧化物:CuO、Fe2O3、Na2O等
非金属氧化物:CO、P2O5、H2O等
按性质
成盐氧化物
酸性氧化物:CO2、Mn2O7等
碱性氧化物:CaO等
两性氧化物:Al2O3等
不成盐氧化物:CO、NO等
【思考2】 举例说明下列说法是否正确。
(1)非金属氧化物一定是酸性氧化物吗? 酸性氧化物一定是非金属氧化物吗?
提示 非金属氧化物大多是酸性氧化物,但不一定全是,如NO、CO不是酸性氧化物;酸性氧化物也不一定是非金属氧化物,如Mn2O7是酸性氧化物,但却是金属氧化物。
(2)金属氧化物一定是碱性氧化物吗?碱性氧化物一定是金属氧化物吗?
提示 金属氧化物大多是碱性氧化物,但不一定全是,如Al2O3是金属氧化物,却是两性氧化物;碱性氧化物一定是金属氧化物。
归纳总结
应用体验
1.判断正误
(1)Na2CO3含有氧元素,所以属于氧化物
(2)CuSO4·5H2O属于混合物
(3)酸性氧化物能溶于水,和水化合生成酸
(4)CH3COOH是多元酸
×
×
×
×
应用体验
2.采用不同的分类方法,可将非金属氧化物分为不同的类别。根据某种共性,可将CO2、P2O5、SO2、SO3归为一类,下列物质中,完全符合此共性而能归为此类物质的是
A.CaO B.CO
C.SiO2 D.H2O
√
CO2、P2O5、SO2、SO3都属于酸性氧化物,CaO属于碱性氧化物,CO和H2O既不属于酸性氧化物,也不属于碱性氧化物。
返回
随堂演练 知识落实
1
2
3
4
1.经测定,一瓶气体中只含有C、O两种元素,通常情况下这瓶气体不可能是
A.一种化合物
B.一种单质和一种化合物的混合物
C.两种化合物
D.两种单质
√
随堂演练
由题意知,瓶中气体中含C、O两种元素,在通常情况下,含C元素的单质为固体,故不能是两种单质。
2.(2022·广西北海教育教学研究室高一质检)下列物质的分类不正确的是
A.水、二氧化硫和干冰都属于氧化物
B.NaHSO4、CuSO4·5H2O和KMnO4都属于盐
C.H2SO4、HNO3、H2CO3都属于酸
D.烧碱、纯碱、熟石灰都属于碱
√
随堂演练
1
2
3
4
随堂演练
1
2
3
4
水、二氧化硫和干冰都是含有两种元素且有一种元素为氧元素的纯净物,都是氧化物,A正确;
NaHSO4、CuSO4·5H2O和KMnO4都是由金属阳离子和酸根阴离子构成的纯净物,都属于盐,B正确;
H2SO4、HNO3、H2CO3为三种含氧酸,C正确;
纯碱为Na2CO3,属于盐,D不正确。
3.化学概念在逻辑上存在如下关系:
下列说法正确的是
A.化合物与纯净物属于重叠关系
B.金属氧化物与碱性氧化物属于交叉关系
C.分解反应与复分解反应属于并列关系
D.钠盐与碳酸盐属于并列关系
√
随堂演练
1
2
3
4
4.下列五组物质,每组中有一种物质从某种角度分析与其他三种不同,请找出该物质,并说明理由。
(1)Fe、S、C、P______________。
(2)H2、O2、N2、S__________________。
(3)Fe2O3、Na2CO3、CuO、H2O_____________________。
(4)AgCl、BaSO4、KNO3、CaCO3_________________________________
_______________________。
随堂演练
1
2
3
4
Fe;Fe为金属
S;常温下S为固体
Na2CO3;Na2CO3为盐
KNO3;KNO3易溶于水(或AgCl;
AgCl酸根离子中不含氧)
返回
课时对点练
1
2
3
4
5
6
7
8
9
题组一 根据物质的组成分类
1.(2022·温州高一期中)航天员王亚平在“天宫课堂”演示了失重条件下水球包裹泡腾片的实验。泡腾片里含有碳酸氢钠,碳酸氢钠属于
A.酸 B.碱 C.盐 D.氧化物
√
10
11
12
13
14
15
对点训练
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
2.(2023·无锡高一检测)下列各组物质,按单质、化合物、混合物顺序排列的是
A.铝、纯碱、盐酸 B.红磷、熟石灰、水
C.石墨、稀硫酸、胆矾 D.石灰水、干冰、空气
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
铝是单质,纯碱是碳酸钠,为化合物,盐酸是混合物,A正确;
红磷是单质,熟石灰是氢氧化钙,为化合物,水是纯净物,B错误;
石墨是单质,稀硫酸是混合物,胆矾是五水硫酸铜,为化合物,C错误;
石灰水是混合物,干冰是二氧化碳,为化合物,空气为混合物,D错误。
2
3.(2022·江西奉新一中高一月考)下列关于同素异形体的说法正确的是
A.红磷转化为白磷属于物理变化
B.石墨导电,金刚石不导电,故二者不互为同素异形体
C.O2和O3的分子式不同,但结构相同
D.S2、S4、S8都是硫元素的同素异形体
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
2
红磷与白磷互为同素异形体,属于不同物质,它们之间的转化属于化学变化,A项错误;
石墨和金刚石互为同素异形体,同素异形体的物理性质一般不同,B项错误;
O2和O3的结构不同,C项错误;
S2、S4、S8为硫元素的不同单质,它们互为同素异形体,D项正确。
4.硝酸钾是一种无氯氮钾复合肥,宜在种植水果、蔬菜、花卉时使用,下列关于KNO3的说法不正确的是
A.从其阳离子看,属于钾盐 B.含有氧元素,属于氧化物
C.它属于正盐 D.从其阴离子看,属于硝酸盐
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
硝酸钾含有钾离子和硝酸根离子,从其阳离子看,属于钾盐,从其阴离子看,属于硝酸盐,故A、D正确;
氧化物只含有两种元素,硝酸钾属于含氧酸盐,故B错误。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
5.(2022·长春第一五一中学高一质检)下列说法正确的是
A.Na2SO4·10H2O是混合物
B.同种分子构成的物质一定是纯净物
C.混合物肯定由两种或两种以上元素组成
D.含有氧元素的化合物都是氧化物
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
Na2SO4·10H2O由单一物质组成,属于纯净物,故A错误;
纯净物由一种物质组成,所以同种分子构成的物质一定是纯净物,故B正确;
混合物可能由一种元素组成,如氧气和臭氧的混合物,故C错误;
含有氧元素的化合物不一定是氧化物,如含氧酸或含氧酸盐等,故D错误。
2
题组二 根据物质的性质分类
6.下列物质中能与水反应的碱性氧化物是
A.CO2 B.CuO C.Fe2O3 D.CaO
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
CO2是酸性氧化物;CuO、Fe2O3和CaO虽然都是碱性氧化物,但只有CaO能与H2O反应生成Ca(OH)2。
7.科学家通过电解Fe2O3、SiO2、CaO的熔融液(1 600 ℃)制得铁。按照树状分类法对Fe2O3、SiO2、CaO这三种物质进行分类,其中正确的是
A.均属于酸性氧化物
B.均属于金属氧化物
C.均属于纯净物
D.均属于非金属氧化物
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
SiO2是酸性氧化物,Fe2O3、CaO是碱性氧化物,故A错误;
SiO2是非金属氧化物,Fe2O3、CaO是金属氧化物,故B、D错误;
Fe2O3、SiO2、CaO都是化合物,即都是纯净物,故C正确。
2
8.(2022·河南商丘市第一高级中学高一期末)下列物质的分类正确的是
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
2
选项 碱 酸 盐 碱性氧化物 酸性氧化物
A 纯碱 H2SO4 Cu2(OH)2CO3 CO2 SO3
B Ba(OH)2 HCl NaCl Na2O CO
C 氨水 HClO NaHCO3 MgO CO2
D KOH HNO3 CaCO3 CaO SO2
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
对点训练
纯碱是碳酸钠,属于盐,CO2是酸性氧化物,故A错误;
CO是不成盐氧化物,故B错误;
氨水是混合物,故C错误。
2
9.(2022·吉林抚松第五中学高一质检)下列图示错误的是
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
FeO能与酸反应生成盐和水,属于碱性氧化物,FeO中Fe元素为+2价,属于+2价铁的化合物,也属于铁的氧化物,且碱性氧化物、铁的氧化物、+2价铁的化合物属于交叉关系,故A正确;
Na2SO4只含酸根阴离子和金属阳离子,属于正盐,含有钠离子属于钠盐,含有硫酸根离子属于硫酸盐,且正盐、钠盐、硫酸盐属于交叉关系,故B正确;
2
综合强化
1
3
4
5
6
7
8
9
10
11
12
13
14
15
H2SO4的酸根阴离子中含有O元素,属于含氧酸,硫酸在水溶液中完全电离,属于强酸,一个硫酸分子可以电离出两个氢离子,所以属于二元酸,且含氧酸、强酸、二元酸属于交叉关系,故C正确;
三种物质的类别关系错误,应为 ,故D错误。
2
综合强化
10.某校实验室将试剂分类后放在不同的试剂柜里,已存放的部分试剂如下表:
1
3
4
5
6
7
8
9
10
11
12
13
14
15
2
综合强化
试剂柜号 ① ② ③ ④
试剂 NaOH、Ca(OH)2 盐酸、硫酸 MnO2、CuO NaCl、Na2SO4
该实验室新购进部分氧化钙和纯碱,应将它们分别放在
A.③和① B.④和①
C.①和② D.③和④
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
根据表中信息可判断①中存放的是碱,②中存放的是酸,③中存放的是氧化物,④中存放的是盐。氧化钙属于氧化物,应放在③中;纯碱是碳酸钠,属于盐,应放在④中。
2
综合强化
试剂柜号 ① ② ③ ④
试剂 NaOH、Ca(OH)2 盐酸、硫酸 MnO2、CuO NaCl、Na2SO4
11.酸式盐是盐的一类,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,则下列说法正确的是
A.H3PO2属于二元酸 B.H3PO2属于三元酸
C.NaH2PO2属于酸式盐 D.NaH2PO2属于正盐
√
1
3
4
5
6
7
8
9
10
11
12
13
14
15
2
综合强化
由于H3PO2与足量的NaOH反应只生成一种盐NaH2PO2,故H3PO2为一元酸,NaH2PO2属于正盐。
12.已知化学反应:
Ⅰ.Na2O+H2O===2NaOH
Ⅱ.2Na2O2+2H2O===4NaOH+O2↑
Ⅲ.N2O5+H2O===2HNO3
Ⅳ.3NO2+H2O===2HNO3+NO
下列说法错误的是
A.Na2O是碱性氧化物
B.N2O5是酸性氧化物
C.Na2O2是一种金属氧化物,它跟水的反应是置换反应
D.Ⅰ和Ⅲ是没有元素化合价变化的反应,Ⅱ和Ⅳ是有元素化合价变化的反应
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
√
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
A对,Na2O跟酸反应只生成盐和水,它是碱性氧化物;
D对,Ⅱ中Na2O2、NaOH、O2所含氧元素的化合价依次为-1、-2、0,则该反应是有元素化合价变化的反应;Ⅳ中NO2、HNO3、NO所含氮元素的化合价依次为+4、+5、+2,则该反应是有元素化合价变化的反应。
13.分类是一种重要的方法,阅读下列材料并填空。
由于①煤和②石油通常都含有硫元素,燃烧时会生成③SO2。当SO2溶于④H2O时,会形成⑤H2SO3,H2SO3在PM2.5存在的条件下,在空气中会迅速生成⑥H2SO4(酸雨的主要成分)。
石灰法是目前应用最广泛的工业脱硫方法,过程如下:通过煅烧⑦CaCO3得到⑧CaO,再与废气中的SO2反应生成CaSO3,最后与⑨O2作用生成
⑩CaSO4而将硫固定,生成的产物可作建筑材料。
(1)在上述材料中标有序号的物质中,属于混合物的是________(填序号,下同);属于氧化物的是________;属于酸的是______。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
①②
③④⑧
⑤⑥
(2)从物质组成角度来看,CaCO3、CaSO3、CaSO4都属于______。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
从物质组成角度来看,CaCO3、CaSO3、CaSO4都是由金属阳离子与酸根阴离子组成的化合物,因此三种物质都属于盐。
盐
(3)从物质类别角度来看,SO2属于________(填 “酸性”“碱性”或“两性”)氧化物,写出其与CaO发生反应的化学方程式:_________________,属于四种基本反应类型中的__________。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
从物质类别角度来看,SO2与水反应生成H2SO3,因此属于酸性氧化物;SO2与CaO反应生成CaSO3,化学方程式为SO2+CaO===CaSO3,该反应的反应物是两种,生成物是一种,因此反应类型属于化合反应。
酸性
SO2+CaO===CaSO3
化合反应
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
14.无机化合物可根据其组成和性质进行分类。
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
(1)以K、Na、H、O、S、N中任两种或三种元素组成合适的物质,分别填在表中②④⑥⑧⑩后面。
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ②______ ③NaOH ④______ ⑤Na2SO4 ⑥______ ⑦SO2 ⑧____ ⑨NH3
⑩____
HNO3
KOH
K2SO4
SO3
H2S
答案 其他合理答案均可
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
H、O、N组成的硝酸或H、O、S组成的亚硫酸属于酸;K、H、O组成的KOH或H、O、N组成的一水合氨属于碱;K、O、N组成的硝酸钾或Na、O、N组成的硝酸钠等属于盐;K、Na、H、S、N分别可与O组成氧化物;K、Na、O、S、N分别可与H组成氢化物。
2
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ②HNO3 ③NaOH ④KOH ⑤Na2SO4 ⑥K2SO4 ⑦SO2 ⑧SO3 ⑨NH3
⑩H2S
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
(2)SO2和CO2都属于酸性氧化物,在化学性质上有很多相似的地方,请写出少量的⑦与③反应的化学方程式:___________________________。
SO2+2NaOH===Na2SO3+H2O
物质类别 酸 碱 盐 氧化物 氢化物
化学式 ①H2SO4 ②HNO3 ③NaOH ④KOH ⑤Na2SO4 ⑥K2SO4 ⑦SO2 ⑧SO3 ⑨NH3
⑩H2S
少量的SO2与NaOH反应生成亚硫酸钠和水,反应的化学方程式为SO2+2NaOH===Na2SO3+H2O。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
(3)只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称为氢化物。下列物质不属于氢化物的是_____(填字母)。
A.H2SO4 B.HCl
C.NaH D.H2O
A
2
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
15.根据物质的分类方法,回答下列问题。
(1)现有两组单质:(Ⅰ)氧气、氢气、硫、氯气;(Ⅱ)铁、钠、铝、硅。
试从不同角度对每组单质进行分类,则每组单质中均有一种单质与其他单质属于不同“类”。请将该单质(写化学符号)和分类依据填在下列表格中。
2
组别 第(Ⅰ)组 第(Ⅱ)组
不同“类”单质 Si
分类依据
S
物质状态
金属与非金属
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
2
第(Ⅰ)组中四种单质,除硫外其余均为气体,第(Ⅱ)组中四种单质,除硅外其余均为金属。
组别 第(Ⅰ)组 第(Ⅱ)组
不同“类”单质 Si
分类依据
S
物质状态
金属与非金属
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
(2)观察下列物质变化(有的化学方程式未配平),有同学将反应①③划为一类,②划为另一类。则将①和③划为一类的依据是________________
_______________。
①NO+NO2―→N2O3
②NH3+HNO3―→NH4NO3
③NH3+NO2―→N2+H2O
2
反应中都有元素
化合价发生变化
①和③划为一类的依据是反应中都有元素化合价发生变化,而②没有。
氢溴酸(HBr)与HCl化学性质相似,因为HCl不能与银发生反应,所以HBr也不能与银发生反应。
1
3
4
5
6
7
8
9
10
11
12
13
14
15
综合强化
(3)某同学根据性质划分,把氢溴酸(HBr)与HCl划为一类,其理由是它们的化学性质十分相似。据此判断下列反应不会发生的是______(填字母)。
A.2HBr+Na2CO3===2NaBr+H2O+CO2↑
B.HBr+AgNO3===AgBr↓+HNO3
C.HBr+NaOH===NaBr+H2O
D.2HBr+2Ag===2AgBr+H2↑
D
2
返回
本课结束
