云南省大理白族自治州民族中学2023-2024学年高一上学期开学考试化学试题(原卷版+解析版)
文档属性
| 名称 | 云南省大理白族自治州民族中学2023-2024学年高一上学期开学考试化学试题(原卷版+解析版) |

|
|
| 格式 | docx | ||
| 文件大小 | 532.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-20 00:00:00 | ||
图片预览




文档简介
大理白族自治州民族中学2023-2024学年高一上学期开学考试
化学试卷
可能用到的相对原子质量:H:1 C:12 O:16
一、选择题(本大题共20个小题,共45分。每题只有一个选项符合题意,1-15题每小题2分,16-20题每小题3分。)
1. 下列关于水的认识正确的是
A. 使用无磷洗衣粉有利于防止水体富营养化
B 生活中通过活性炭吸附、过滤可以使硬水软化
C. 汽车发动机用水来冷却是因为水的比热容小
D. 气压增大,水的沸点会降低
2. 下列化学用语表示正确的是
A. Fe2+—铁离子 B. 镁原子结构示意图—
C. 氯酸钾—KClO3 D. N2—两个氮原子
3. 下图是某反应前后分子种类变化的微观示意图。下列说法正确的是
A. 反应前后分子个数不变
B. 反应中涉及到3种氧化物
C. 丙的中硫元素的化合价为+6
D. 反应中甲、乙分子个数比为2:3
4. 如图所示的实验基本操作正确的是
A.二氧化碳验满 B.点燃酒精灯 C.读取液体体积 D.稀释浓硫酸
A. A B. B C. C D. D
5. 下列反应不属于化学四种基本反应类型的是
A. NH4HCO3NH3↑+CO2↑+H2O B. CaCO3+CO2+H2O=Ca(HCO3)2
C. 2NaCl+2H2O2NaOH+H2↑+Cl2↑ D. 2Mg+CO22MgO+C
6. 节日期间商场里顾客很多,有人会感觉到闷热缺氧,测定出氧气的体积分数可能是
A. 1% B. 19% C. 25% D. 78%
7. 日常生活中,区别下列各组物质所用的方法,错误的是
A. 白酒和白醋——观察颜色
B. 棉线和羊毛线——灼烧,闻气味
C. 黄铜和黄金——灼烧,观察颜色变化
D. 热塑性塑料和热固性塑料——加热,观察外形变化
8. 用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是
A. 隔绝空气 B. 降低可燃物的着火点
C. 清除可燃物 D. 使可燃物温度降到着火点以下
9. 加碘食盐所含的碘酸钾(KIO3)中,碘元素的化合价为
A. +1 B. +3 C. +5 D. +7
10. 下列事实和解释相符的是
A. 干冰用作致冷剂——干冰是冰
B. 纯碱溶液使酚酞试液变红——纯碱是碱
C. 用炭黑墨汁书写的字经久不变色——常温下,碳的化学性质稳定
D. 制糖工业用活性炭脱色制白糖——活性炭和有色物质反应
11. 根据图中的信息判断,下列说法正确的是
A. 硫属于金属元素 B. 硫原子的核电荷数为16
C. 硫原子的相对原子质量为32.07 g D. 在化学反应中,硫原子容易失去电子
12. 下列金属能与硫酸亚铁溶液反应的是
A 锌 B. 银 C. 铜 D. 铅
13. 下列有关乙醇(C2H5OH)的说法,错误的是
A. 乙醇是一种有机物
B. 乙醇由三种元素组成
C. 乙醇分子中,碳、氢、氧原子个数比为2∶6∶1
D. 乙醇中,碳元素的质量分数
14. 下列物质既属于钾盐又属于硫酸盐的是
A. 碳酸钾 B. 硫酸钠 C. 硝酸钠 D. 硫酸钾
15. 按照物质的树状分类和交叉分类,HNO3应属于
①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥一元酸⑦化合物
A. ①②③④⑤⑥⑦ B. ①④⑥⑦
C. ①⑦ D. ①④⑤⑥
16. 下列离子方程式中,正确的是
A. 稀硫酸滴在铜片上:
B. 大理石加入稀盐酸中:
C. 铁粉加入氯化铁溶液中:
D. 氯化钡溶液滴入硫酸钠溶液中:
17. FeCl3溶液、Fe(OH)3胶体共同具备的性质是
A. 都能透过半透膜,都呈红褐色
B. 分散质颗粒直径相同
C 都较稳定,密封保存一段时间都不会产生沉淀
D. 当有光线透过时,都能产生丁达尔效应
18. 下列关于浊液、胶体和溶液的知识,错误的是
A. 胶体区别于溶液的本质是胶体中分散质大小介于1nm和100nm之间
B. 浊液、胶体和溶液中的分散剂可以不一定是水
C. 胶体都可以用来净水
D. 无色溶液和无色的胶体从外观上不能简单区分出来
19. 下列说法中正确的是
A. 熔融的氯化氢不能导电,所以氯化氢是非电解质
B. SO2气体溶于水能导电,所以SO2是电解质
C. 氯化银难溶于水,所以氯化银是非电解质
D. 蔗糖溶液和熔融蔗糖都不能导电,所以蔗糖是非电解质
20. 下列树状分类方法中正确的是( )
A. B.
C. D.
二、填空题(本大题有4个题目,共计55分)
21. 完成下列问题。
(1)写出下列物质的化学式
高锰酸钾___________;二氧化碳___________;氮气___________;双氧水___________;硝酸___________; 氢氧化钠___________;氯化钡___________;硝酸银___________。
(2)写出下列物质在水溶液中的电离方程式:
Al2(SO4)3:___________;
NH4NO3:___________;
(3)根据题中所给信息写出相应反应的化学方程式:
①工业上以Al2O3和冰晶石(Na3AlF6)为原料,在通电的条件下电解熔融氧化铝制取金属铝,同时得到氧气。___________。
②剧烈运动会使人肌肉酸痛。放松一段时间后,血液中的乳酸(化学式为C3H6O3)与吸入的氧气反应生成二氧化碳和水,而使肌肉的酸痛感消失。___________
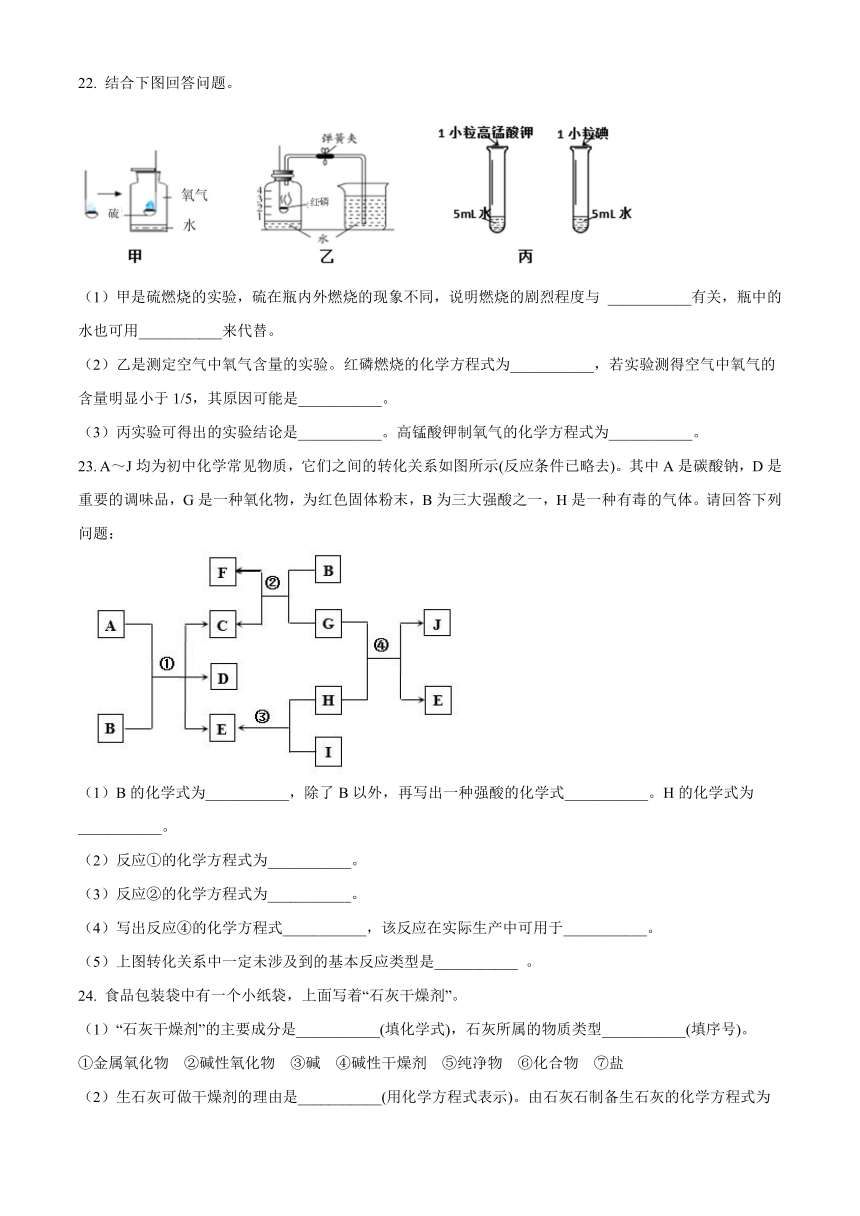
22. 结合下图回答问题。
(1)甲是硫燃烧的实验,硫在瓶内外燃烧的现象不同,说明燃烧的剧烈程度与 ___________有关,瓶中的水也可用___________来代替。
(2)乙是测定空气中氧气含量的实验。红磷燃烧的化学方程式为___________,若实验测得空气中氧气的含量明显小于1/5,其原因可能是___________。
(3)丙实验可得出的实验结论是___________。高锰酸钾制氧气的化学方程式为___________。
23. A~J均为初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中A是碳酸钠,D是重要的调味品,G是一种氧化物,为红色固体粉末,B为三大强酸之一,H是一种有毒的气体。请回答下列问题:
(1)B的化学式为___________,除了B以外,再写出一种强酸的化学式___________。H的化学式为___________。
(2)反应①的化学方程式为___________。
(3)反应②的化学方程式为___________。
(4)写出反应④的化学方程式___________,该反应在实际生产中可用于___________。
(5)上图转化关系中一定未涉及到的基本反应类型是___________ 。
24. 食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分是___________(填化学式),石灰所属的物质类型___________(填序号)。
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂 ⑤纯净物 ⑥化合物 ⑦盐
(2)生石灰可做干燥剂的理由是___________(用化学方程式表示)。由石灰石制备生石灰的化学方程式为___________。
(3)你认为下列内容还必须在这种小纸袋上注明的是___________(填序号)。
①禁止食用 ②可以食用 ③禁止用手拿 ④生产日期
(4)小纸袋中的物质能否长期地作干燥剂?为什么?______________________。
(5)漂白粉可用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为___________。
大理白族自治州民族中学2023-2024学年高一上学期开学考试
化学试卷 答案解析
可能用到的相对原子质量:H:1 C:12 O:16
一、选择题(本大题共20个小题,共45分。每题只有一个选项符合题意,1-15题每小题2分,16-20题每小题3分。)
1. 下列关于水的认识正确的是
A. 使用无磷洗衣粉有利于防止水体富营养化
B. 生活中通过活性炭吸附、过滤可以使硬水软化
C. 汽车发动机用水来冷却是因为水的比热容小
D. 气压增大,水的沸点会降低
【答案】A
【解析】
【分析】
【详解】A.磷使藻类大量繁殖,造成水体的营养化,无磷洗衣粉可以防止水体富营养化,故A正确;
B.通过活性炭吸附作用,可以吸附水中的色素和异味,但是不能减小水中的钙离子、镁离子等,不能使硬水软化,故B错误;
C.与其他物质相比,水的比热容大,在质量相同、升高的温度相同时,水吸收的热量多,所以汽车发动机用水来冷却,故C错误;
D.压强越大水的沸点越高,故D错误;
故选A。
2. 下列化学用语表示正确的是
A. Fe2+—铁离子 B. 镁原子结构示意图—
C. 氯酸钾—KClO3 D. N2—两个氮原子
【答案】C
【解析】
【分析】
【详解】A.Fe2+表示亚铁离子,A错误;
B.Mg是12号元素,原子核外电子排布式是2、8、2,故Mg原子结构示意图为,B错误;
C.氯酸钾化学式为KClO3,C正确;
D.N2表示氮气分子,1个分子中含有两个氮原子,D错误;
故合理选项是C。
3. 下图是某反应前后分子种类变化的微观示意图。下列说法正确的是
A. 反应前后分子个数不变
B. 反应中涉及到3种氧化物
C. 丙的中硫元素的化合价为+6
D. 反应中甲、乙分子个数比为2:3
【答案】D
【解析】
【分析】根据图示,结合质量守恒定律可知发生反应方程式为:2H2S+3O22SO2+2H2O,然后根据问题分析解答。
【详解】A.根据反应方程式可知:反应前后物质分子数不等,A错误;
B.在上述物质中涉及的氧化物只有SO2、H2O两种,B错误;
C.丙是SO2,其中S元素化合价为+4价,C错误;
D.根据方程式可知:在反应中H2S、O2反应的个数比是2:3,D正确;
故合理选项D。
4. 如图所示的实验基本操作正确的是
A.二氧化碳验满 B.点燃酒精灯 C.读取液体体积 D.稀释浓硫酸
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.CO2不能燃烧,也不支持燃烧,其密度比空气大,因此若收集满,集气瓶的瓶口有CO2气体外溢,将燃着的火柴放在集气瓶口,若火柴熄灭,可以证明二氧化碳已经收集满,A正确;
B.不能用燃着的酒精灯去点燃另一个酒精灯,防止酒精洒出,其燃烧引发火灾,B错误;
C.用量筒量取液体物质读数时,应该使视线与凹液面的最低处相切,C错误;
D.浓硫酸溶于水会放出大量热,由于其密度比水大,所以稀释时应该注酸入水,即将浓硫酸沿烧杯内部缓缓加入盛有水的烧杯中,并用玻璃棒不断搅拌,使热迅速扩散,D错误;
故合理选项是A。
5. 下列反应不属于化学四种基本反应类型的是
A. NH4HCO3NH3↑+CO2↑+H2O B. CaCO3+CO2+H2O=Ca(HCO3)2
C. 2NaCl+2H2O2NaOH+H2↑+Cl2↑ D. 2Mg+CO22MgO+C
【答案】C
【解析】
【详解】A .NH4HCO3NH3↑+CO2↑+H2O是由一种物质生成两种物质的反应,属于分解反应,故A不符合题意;
B.CaCO3+CO2+H2O=Ca(HCO3)2是两种或多种物质生成一种物质的反应,属于化合反应,故B不符合题意;
C.2NaCl+2H2O2NaOH+H2↑+Cl2↑不符合四种基本反应类型的特征,故C符合题意;
D.2Mg+CO22MgO+C是一种单质和一种化合物生成另一种单质和另一种化合物的反应,是置换反应,故D不符合题意。
答案选C。
6. 节日期间商场里顾客很多,有人会感觉到闷热缺氧,测定出氧气的体积分数可能是
A. 1% B. 19% C. 25% D. 78%
【答案】B
【解析】
【分析】空气中氧气的体积分数为21%,节日期间的商场里顾客很多,有人会感觉到闷热缺氧,则氧气的体积分数应略小于21%.
【详解】A.氧气的体积分数应略小于21%,空气中氧气的体积分数不可能低至1%,否则人类没法生存,A错误;
B.空气中氧气的体积分数可能为19%,B正确;
C.氧气的体积分数应略小于21%,空气中氧气的体积分数不可能为25%,C错误;
D.氧气的体积分数应略小于21%,空气中氧气的体积分数不可能为78%,D错误;
答案选B。
【点睛】本题难度不大,了解空气中氧气的体积分数(21%)是正确解答本题的关键。
7. 日常生活中,区别下列各组物质所用的方法,错误的是
A. 白酒和白醋——观察颜色
B. 棉线和羊毛线——灼烧,闻气味
C. 黄铜和黄金——灼烧,观察颜色变化
D. 热塑性塑料和热固性塑料——加热,观察外形变化
【答案】A
【解析】
【详解】A.白酒和白醋都是无色的液体,观察颜色无法区分,故A错误;
B.棉线灼烧没有烧焦羽毛的气味,而羊毛灼烧有烧焦羽毛的气味,故B正确;
C.黄铜灼烧其中的铜与氧气反应生成黑色的氧化铜,而黄金灼烧颜色不会改变,故C正确;
D.热固性塑料加热不会形变,而热塑性塑料加热会发生外形变化,故D正确。
答案选A。
8. 用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是
A. 隔绝空气 B. 降低可燃物的着火点
C. 清除可燃物 D. 使可燃物温度降到着火点以下
【答案】D
【解析】
【详解】根据灭火原理分析,灭火的原理:(只要消除燃烧条件的任意一个即可)①撤离可燃物 ②隔绝氧气(或空气)③降温到着火点以下;嘴吹蜡烛时吹走了蜡烛火焰的热量,从而降低了蜡烛的温度,导致可燃物的温度降到了其着火点以下,所以蜡烛熄灭,D符合题意。
答案选D。
9. 加碘食盐所含的碘酸钾(KIO3)中,碘元素的化合价为
A. +1 B. +3 C. +5 D. +7
【答案】C
【解析】
【详解】根据物质碘酸钾的化学式KIO3,利用化合物中各元素化合价代数和为0的原则,由化合物中K、O元素分别为+1、-2价,计算化合物中碘元素的化合价;设化合物中碘元素的化合价为x,依据化合物中各元素化合价代数和为0的原则,有(+1)+x+(-2)×3=0,解得x=+5。
答案选C。
10. 下列事实和解释相符的是
A. 干冰用作致冷剂——干冰冰
B. 纯碱溶液使酚酞试液变红——纯碱是碱
C. 用炭黑墨汁书写的字经久不变色——常温下,碳的化学性质稳定
D. 制糖工业用活性炭脱色制白糖——活性炭和有色物质反应
【答案】C
【解析】
【详解】A.干冰用作致冷剂,干冰不是冰,是固体的二氧化碳,干冰作致冷剂是因为固体二氧化碳汽化时吸热致冷,故A不符合题意;
B.纯碱溶液使酚酞试液变红,但纯碱不是碱,纯碱是碳酸钠的俗称,是由钠离子和碳酸根离子构成的化合物,属于盐,故B不符合题意;
C.墨是用炭黑制成的,炭黑的主要成分是碳,用炭黑墨汁书写的字经久不变色,是因为常温下,碳的化学性质稳定,故C符合题意;
D.制糖工业用活性炭脱色制白糖,是因为活性炭具有吸附性,能吸附异味和色素,故D不符合题意。
答案选C。
11. 根据图中的信息判断,下列说法正确的是
A. 硫属于金属元素 B. 硫原子的核电荷数为16
C. 硫原子的相对原子质量为32.07 g D. 在化学反应中,硫原子容易失去电子
【答案】B
【解析】
【详解】A.硫带“石”字旁,属于固态非金属元素,故A错误;
B.由硫原子的结构示意图,圆圈内的数字是16,表示硫原子的核电荷数为16,故B正确;
C.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,硫原子的相对原子质量为32.07,其单位是1,不是g,故C错误;
D.硫原子的最外层电子数是6,大于4,在化学反应中易得到2个电子而形成阴离子,故D错误。
答案选B
12. 下列金属能与硫酸亚铁溶液反应的是
A. 锌 B. 银 C. 铜 D. 铅
【答案】A
【解析】
【详解】在金属活动性顺序中,锌位于铁的前面,而银、铜、铅位于铁的后面,所以锌与硫酸亚铁溶液反应,所以应选A;
故答案为:A.
13. 下列有关乙醇(C2H5OH)的说法,错误的是
A. 乙醇是一种有机物
B. 乙醇由三种元素组成
C. 乙醇分子中,碳、氢、氧原子个数比为2∶6∶1
D. 乙醇中,碳元素的质量分数
【答案】D
【解析】
【详解】A.乙醇属于常见的有机物,A正确;
B.乙醇由C、H、O三种元素组成,B正确;
C.乙醇的分子式为C2H6O,碳、氢、氧原子个数比为2:6:1,C正确;
D.碳元素的质量分数=,D错误;
答案选D。
14. 下列物质既属于钾盐又属于硫酸盐的是
A. 碳酸钾 B. 硫酸钠 C. 硝酸钠 D. 硫酸钾
【答案】D
【解析】
【分析】盐是指含有金属离子(铵根)和酸根离子的化合物,可根据所含有的金属或酸根去命名,钾盐指由钾离子和酸根离子构成的盐,硫酸盐指金属离子(铵根)和硫酸根离子构成的盐。
【详解】钾盐指由钾离子和酸根离子构成的盐,硫酸钠、硝酸钠属于钠盐,碳酸钾、硫酸钾属于钾盐,硫酸盐指金属离子(铵根)和硫酸根离子构成的盐,硫酸钠、硫酸钾属于硫酸盐,硝酸钠属于硝酸盐,碳酸钾属于碳酸盐,所以既属于钾盐又属于硫酸盐的是硫酸钾。
答案选D。
15. 按照物质的树状分类和交叉分类,HNO3应属于
①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥一元酸⑦化合物
A. ①②③④⑤⑥⑦ B. ①④⑥⑦
C. ①⑦ D. ①④⑤⑥
【答案】B
【解析】
【详解】硝酸是重要的三大强酸之一,它是含氧酸、一元酸、易挥发性酸、化合物,B满足题意。
答案选B。
16. 下列离子方程式中,正确的是
A. 稀硫酸滴在铜片上:
B. 大理石加入稀盐酸中:
C. 铁粉加入氯化铁溶液中:
D. 氯化钡溶液滴入硫酸钠溶液中:
【答案】D
【解析】
【详解】A.铜活泼性弱于氢,与稀硫酸不反应,A错误;
B.大理石成分为CaCO3加入稀盐酸反应生成氯化钙、二氧化碳和水,离子方程式为:,B错误;
C.氯化铁溶液与铁反应生成氯化亚铁,离子方程式为:2Fe3++Fe=3Fe2+,C错误;
D.氯化钡溶液和硫酸钠溶液混合生成硫酸钡和氯化钠,反应的离子方程式:,D正确;
故选:D。
17. FeCl3溶液、Fe(OH)3胶体共同具备的性质是
A. 都能透过半透膜,都呈红褐色
B. 分散质颗粒直径相同
C. 都较稳定,密封保存一段时间都不会产生沉淀
D. 当有光线透过时,都能产生丁达尔效应
【答案】C
【解析】
【分析】
【详解】A.溶液能通过半透膜,胶体不能,FeCl3溶液与Fe(OH)3胶体的颜色分别为棕黄色、红褐色,故A错误;
B.Fe(OH)3胶体的分散质颗粒直径在1~100nm之间,FeCl3溶液的分散质颗粒直径小于1nm,分散质颗粒直径不相同,故B错误;
C.胶体具有介稳性,放置不会产生沉淀,溶液是稳定的,故C正确;
D.只有胶体具有丁达尔效应,所以Fe(OH)3胶体具有丁达尔效应,而FeCl3溶液不具备,故D错误;
故选C。
18. 下列关于浊液、胶体和溶液的知识,错误的是
A. 胶体区别于溶液的本质是胶体中分散质大小介于1nm和100nm之间
B. 浊液、胶体和溶液中的分散剂可以不一定是水
C. 胶体都可以用来净水
D. 无色的溶液和无色的胶体从外观上不能简单区分出来
【答案】C
【解析】
【分析】
【详解】A.胶体区别于溶液的本质是胶体中粒子直径分散质大小介于1nm和100nm之间,故A正确;
B.胶体有气溶胶和固溶胶,分散剂为气体和固体,液溶胶分散剂为液体,但也不一定是水,故B正确;
C.FeCl3等胶体常用于净水,其他的胶体不一定能净水,故C错误;
D.胶体和溶液能用丁达尔效应进行区别,而无色的溶液和无色的胶体从外观上不能简单区分出来,故D正确;
故答案为C。
19. 下列说法中正确的是
A. 熔融的氯化氢不能导电,所以氯化氢是非电解质
B. SO2气体溶于水能导电,所以SO2是电解质
C. 氯化银难溶于水,所以氯化银是非电解质
D. 蔗糖溶液和熔融的蔗糖都不能导电,所以蔗糖是非电解质
【答案】D
【解析】
【分析】
【详解】A.氯化氢气体不能导电,但其水溶液中有自由移动的氯离子和氢离子能够导电,所以氯化氢为电解质,A项错误;
B.SO2常温下为气体,只有SO2分子,没有自由移动的离子,虽SO2在水溶液中与水反应,生成亚硫酸,亚硫酸电离出自由移动的离子,溶液能够导电,但自由移动的离子不是SO2自身电离,SO2是化合物,所以SO2是非电解质,B项错误;
C.化合物为电解质还是非电解质与化合物的溶解性没有关系,氯化银虽难溶于水,但溶解的部分在溶液中却能完全电离,故氯化银为电解质,且为强电解质,C项错误;
D.蔗糖在溶液中以分子形式存在,不能电离,则蔗糖溶液不能导电,蔗糖在熔融状态也不导电,所以蔗糖是非电解质,D项正确;
答案选D。
20. 下列树状分类方法中正确的是( )
A. B.
C. D.
【答案】A
【解析】
【详解】A.纯净物包括单质和化合物两类,单质分为金属单质和非金属单质,A正确;
B.溶液属于混合物,B错误;
C.无机物并不都是化合物,如单质,氧化物、非氧化物并不属于酸,C错误;
D.氧化物属于化合物,两者不是并列关系,D错误;
故答案为:A。
二、填空题(本大题有4个题目,共计55分)
21. 完成下列问题。
(1)写出下列物质的化学式
高锰酸钾___________;二氧化碳___________;氮气___________;双氧水___________;硝酸___________; 氢氧化钠___________;氯化钡___________;硝酸银___________。
(2)写出下列物质在水溶液中的电离方程式:
Al2(SO4)3:___________;
NH4NO3:___________;
(3)根据题中所给信息写出相应反应的化学方程式:
①工业上以Al2O3和冰晶石(Na3AlF6)为原料,在通电的条件下电解熔融氧化铝制取金属铝,同时得到氧气。___________。
②剧烈运动会使人肌肉酸痛。放松一段时间后,血液中的乳酸(化学式为C3H6O3)与吸入的氧气反应生成二氧化碳和水,而使肌肉的酸痛感消失。___________
【答案】(1) ①. KMnO4 ②. CO2 ③. N2 ④. H2O2 ⑤. HNO3 ⑥. NaOH ⑦. BaCl2 ⑧. AgNO3
(2) ①. Al2(SO4)3=2Al3++3 ②. NH4NO3=+
(3) ①. ②. C3H6O3+3O2=3CO2+3H2O
【解析】
【小问1详解】
高锰酸钾的化学式:KMnO4;二氧化碳的化学式:CO2;氮气的化学式:N2;双氧水的化学式:H2O2;硝酸的化学式:HNO3;氢氧化钠的化学式:NaOH;氯化钡的化学式:BaCl2;硝酸银的化学式:AgNO3;故答案为:KMnO4;CO2;N2;H2O2;HNO3;NaOH;BaCl2;AgNO3;
【小问2详解】
硫酸铝在水溶液中完全电离生成铝离子和硫酸根离子,电离方程式为Al2(SO4)3=2Al3++3;硝酸铵在水溶液中完全电离生成铵根离子和硝酸根离子,电离方程式为NH4NO3=+;故答案为:Al2(SO4)3=2Al3++3;NH4NO3=+;
【小问3详解】
①工业上以Al2O3和冰晶石(Na3AlF6)为原料,在通电的条件下电解熔融氧化铝制取金属铝,同时得到氧气,反应的化学方程式为:;故答案为:;
②血液中的乳酸(化学式为C3H6O3)与吸入的氧气反应生成二氧化碳和水,反应的化学方程式为:C3H6O3+3O2=3CO2+3H2O;故答案为:C3H6O3+3O2=3CO2+3H2O。
22. 结合下图回答问题。
(1)甲是硫燃烧的实验,硫在瓶内外燃烧的现象不同,说明燃烧的剧烈程度与 ___________有关,瓶中的水也可用___________来代替。
(2)乙是测定空气中氧气含量的实验。红磷燃烧的化学方程式为___________,若实验测得空气中氧气的含量明显小于1/5,其原因可能是___________。
(3)丙实验可得出的实验结论是___________。高锰酸钾制氧气的化学方程式为___________。
【答案】(1) ①. 氧气的浓度 ②. 氢氧化钠溶
(2) ①. 4P+5O22P2O5 ②. 红磷的量不足(合理均可)
(3) ①. 不同溶质在同种溶剂中的溶解性不同 ②. 2KMnO4K2MnO4+MnO2+O2↑
【解析】
【小问1详解】
甲是硫燃烧的实验,硫在瓶内外燃烧的现象不同,说明燃烧的剧烈程度与氧气的浓度有关,瓶中的水也可用氢氧化钠溶液来代替,因为二氧化硫可溶于氢氧化钠溶液,故答案为:氧气的浓度;氢氧化钠溶液;
【小问2详解】
红磷燃烧化学方程式为4P+5O22P2O5,若实验测得空气中氧气的含量明显小于,其原因可能是红磷的量不足,故答案为:4P+5O22P2O5;红磷的量不足;
【小问3详解】
丙实验发现高锰酸钾完全溶解,碘单质不能完全水解,可得出的实验结论是不同溶质在同种溶剂中的溶解性不同,高锰酸钾制氧气的化学方程式为2KMnO4K2MnO4+MnO2+O2↑;故答案为:不同溶质在同种溶剂中的溶解性不同;2KMnO4K2MnO4+MnO2+O2↑。
23. A~J均为初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中A是碳酸钠,D是重要的调味品,G是一种氧化物,为红色固体粉末,B为三大强酸之一,H是一种有毒的气体。请回答下列问题:
(1)B的化学式为___________,除了B以外,再写出一种强酸的化学式___________。H的化学式为___________。
(2)反应①的化学方程式为___________。
(3)反应②的化学方程式为___________。
(4)写出反应④的化学方程式___________,该反应在实际生产中可用于___________。
(5)上图转化关系中一定未涉及到的基本反应类型是___________ 。
【答案】(1) ①. HCl ②. H2SO4或HNO3 ③. CO
(2)Na2CO3 +2HCl = 2NaCl + H2O+CO2↑
(3)Fe2O3 +6HCl = 2FeCl3 + 3H2O
(4) ①. ②. 炼铁
(5)分解反应、置换反应
【解析】
【分析】A~J均为初中化学常见物质,其中D是重要的调味品,则D为NaCl,A与B反应生成三种物质,其中一种氯化钠,考虑是碳酸钠与盐酸反应,C、E分别为CO2、H2O中一种,A、B分别为盐酸、碳酸钠中的一种,G为红色固体,且G能与盐酸反应生成C与F,推知G为Fe2O3、B为盐酸,则F为FeCl3、C为H2O,故E为CO2、A为Na2CO3,由“G(氧化铁)+H→E(二氧化碳)+J”与“H+I→E(二氧化碳)”,可推知H为CO,则J为Fe、I为O2。
【小问1详解】
由上述分析可知,B为HCl,常见的强酸除了HCl外还有H2SO4或HNO3,H的化学式CO;故答案为:HCl;H2SO4或HNO3;CO;
【小问2详解】
反应①为碳酸钠与盐酸反应,化学方程式为:Na2CO3 +2HCl = 2NaCl + H2O+CO2↑;故答案为:Na2CO3 +2HCl = 2NaCl + H2O+CO2↑;
【小问3详解】
反应②是氧化铁与盐酸反应生成氯化铁与水,化学方程式为Fe2O3+6HCl=2FeCl3+3H2O,故答案为:Fe2O3+6HCl=2FeCl3+3H2O;
【小问4详解】
反应④是氧化铁与一氧化碳反应生成铁与二氧化碳,化学方程式为:;该反应在实际生产中可以冶炼铁,故答案为:;炼铁;
【小问5详解】
反应①是碳酸钠与盐酸反应,反应②是氧化铁与盐酸反应,均属于复分解反应,反应③一氧化碳与氧气反应生成二氧化碳,属于化合反应,反应④可以是一氧化碳与氧化铁反应生成铁与二氧化碳,不属于四种基本类型,转化中不涉及分解反应、置换反应;故答案为:分解反应、置换反应。
24. 食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分是___________(填化学式),石灰所属的物质类型___________(填序号)。
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂 ⑤纯净物 ⑥化合物 ⑦盐
(2)生石灰可做干燥剂的理由是___________(用化学方程式表示)。由石灰石制备生石灰的化学方程式为___________。
(3)你认为下列内容还必须在这种小纸袋上注明的是___________(填序号)。
①禁止食用 ②可以食用 ③禁止用手拿 ④生产日期
(4)小纸袋中的物质能否长期地作干燥剂?为什么?______________________。
(5)漂白粉可用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为___________。
【答案】(1) ①. CaO ②. ①②④⑤⑥
(2) ①. CaO+H2O=Ca(OH)2 ②.
(3)①③④ (4)不能,氧化钙吸收水之后就变成氢氧化钙,失去吸水能力
(5)CO2
【解析】
【小问1详解】
石灰干燥剂的成分是CaO,纯净物包括单质和化合物,化合物包括氧化物、酸、碱、盐,CaO是由钙元素和氧元素组成,属于氧化物,CaO能与水形成的碱,氧化钙为碱性氧化物,能吸收水蒸气,能干燥碱性气体,因此氧化钙为碱性干燥剂,因此石灰所属物质类型为①②④⑤⑥;
【小问2详解】
生石灰能与水反应CaO+H2O=Ca(OH)2,因此生石灰可做干燥剂;工业上常煅烧石灰石制备生石灰,其反应方程式为CaCO3CaO+CO2↑;故答案为CaO+H2O=Ca(OH)2;CaCO3CaO+CO2↑;
【小问3详解】
生石灰不能食用,应注明禁止食用,生石灰与水生成氢氧化钙,氢氧化钙腐蚀皮肤,因此注明禁止用手拿,生石灰能吸收空气中水蒸气、二氧化碳,有一定的使用期限,因此需注明生产日期;故答案为①③④;
【小问4详解】
空气中含有水蒸气,CaO能吸收水蒸气,生成Ca(OH)2,失去吸水能力,因此小纸袋中的物质不能长期作干燥剂;故答案为不能,氧化钙吸收水之后就变成氢氧化钙,失去吸水能力;
【小问5详解】
根据原子守恒、元素守恒,推出X为CO2,故答案为CO2。
化学试卷
可能用到的相对原子质量:H:1 C:12 O:16
一、选择题(本大题共20个小题,共45分。每题只有一个选项符合题意,1-15题每小题2分,16-20题每小题3分。)
1. 下列关于水的认识正确的是
A. 使用无磷洗衣粉有利于防止水体富营养化
B 生活中通过活性炭吸附、过滤可以使硬水软化
C. 汽车发动机用水来冷却是因为水的比热容小
D. 气压增大,水的沸点会降低
2. 下列化学用语表示正确的是
A. Fe2+—铁离子 B. 镁原子结构示意图—
C. 氯酸钾—KClO3 D. N2—两个氮原子
3. 下图是某反应前后分子种类变化的微观示意图。下列说法正确的是
A. 反应前后分子个数不变
B. 反应中涉及到3种氧化物
C. 丙的中硫元素的化合价为+6
D. 反应中甲、乙分子个数比为2:3
4. 如图所示的实验基本操作正确的是
A.二氧化碳验满 B.点燃酒精灯 C.读取液体体积 D.稀释浓硫酸
A. A B. B C. C D. D
5. 下列反应不属于化学四种基本反应类型的是
A. NH4HCO3NH3↑+CO2↑+H2O B. CaCO3+CO2+H2O=Ca(HCO3)2
C. 2NaCl+2H2O2NaOH+H2↑+Cl2↑ D. 2Mg+CO22MgO+C
6. 节日期间商场里顾客很多,有人会感觉到闷热缺氧,测定出氧气的体积分数可能是
A. 1% B. 19% C. 25% D. 78%
7. 日常生活中,区别下列各组物质所用的方法,错误的是
A. 白酒和白醋——观察颜色
B. 棉线和羊毛线——灼烧,闻气味
C. 黄铜和黄金——灼烧,观察颜色变化
D. 热塑性塑料和热固性塑料——加热,观察外形变化
8. 用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是
A. 隔绝空气 B. 降低可燃物的着火点
C. 清除可燃物 D. 使可燃物温度降到着火点以下
9. 加碘食盐所含的碘酸钾(KIO3)中,碘元素的化合价为
A. +1 B. +3 C. +5 D. +7
10. 下列事实和解释相符的是
A. 干冰用作致冷剂——干冰是冰
B. 纯碱溶液使酚酞试液变红——纯碱是碱
C. 用炭黑墨汁书写的字经久不变色——常温下,碳的化学性质稳定
D. 制糖工业用活性炭脱色制白糖——活性炭和有色物质反应
11. 根据图中的信息判断,下列说法正确的是
A. 硫属于金属元素 B. 硫原子的核电荷数为16
C. 硫原子的相对原子质量为32.07 g D. 在化学反应中,硫原子容易失去电子
12. 下列金属能与硫酸亚铁溶液反应的是
A 锌 B. 银 C. 铜 D. 铅
13. 下列有关乙醇(C2H5OH)的说法,错误的是
A. 乙醇是一种有机物
B. 乙醇由三种元素组成
C. 乙醇分子中,碳、氢、氧原子个数比为2∶6∶1
D. 乙醇中,碳元素的质量分数
14. 下列物质既属于钾盐又属于硫酸盐的是
A. 碳酸钾 B. 硫酸钠 C. 硝酸钠 D. 硫酸钾
15. 按照物质的树状分类和交叉分类,HNO3应属于
①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥一元酸⑦化合物
A. ①②③④⑤⑥⑦ B. ①④⑥⑦
C. ①⑦ D. ①④⑤⑥
16. 下列离子方程式中,正确的是
A. 稀硫酸滴在铜片上:
B. 大理石加入稀盐酸中:
C. 铁粉加入氯化铁溶液中:
D. 氯化钡溶液滴入硫酸钠溶液中:
17. FeCl3溶液、Fe(OH)3胶体共同具备的性质是
A. 都能透过半透膜,都呈红褐色
B. 分散质颗粒直径相同
C 都较稳定,密封保存一段时间都不会产生沉淀
D. 当有光线透过时,都能产生丁达尔效应
18. 下列关于浊液、胶体和溶液的知识,错误的是
A. 胶体区别于溶液的本质是胶体中分散质大小介于1nm和100nm之间
B. 浊液、胶体和溶液中的分散剂可以不一定是水
C. 胶体都可以用来净水
D. 无色溶液和无色的胶体从外观上不能简单区分出来
19. 下列说法中正确的是
A. 熔融的氯化氢不能导电,所以氯化氢是非电解质
B. SO2气体溶于水能导电,所以SO2是电解质
C. 氯化银难溶于水,所以氯化银是非电解质
D. 蔗糖溶液和熔融蔗糖都不能导电,所以蔗糖是非电解质
20. 下列树状分类方法中正确的是( )
A. B.
C. D.
二、填空题(本大题有4个题目,共计55分)
21. 完成下列问题。
(1)写出下列物质的化学式
高锰酸钾___________;二氧化碳___________;氮气___________;双氧水___________;硝酸___________; 氢氧化钠___________;氯化钡___________;硝酸银___________。
(2)写出下列物质在水溶液中的电离方程式:
Al2(SO4)3:___________;
NH4NO3:___________;
(3)根据题中所给信息写出相应反应的化学方程式:
①工业上以Al2O3和冰晶石(Na3AlF6)为原料,在通电的条件下电解熔融氧化铝制取金属铝,同时得到氧气。___________。
②剧烈运动会使人肌肉酸痛。放松一段时间后,血液中的乳酸(化学式为C3H6O3)与吸入的氧气反应生成二氧化碳和水,而使肌肉的酸痛感消失。___________
22. 结合下图回答问题。
(1)甲是硫燃烧的实验,硫在瓶内外燃烧的现象不同,说明燃烧的剧烈程度与 ___________有关,瓶中的水也可用___________来代替。
(2)乙是测定空气中氧气含量的实验。红磷燃烧的化学方程式为___________,若实验测得空气中氧气的含量明显小于1/5,其原因可能是___________。
(3)丙实验可得出的实验结论是___________。高锰酸钾制氧气的化学方程式为___________。
23. A~J均为初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中A是碳酸钠,D是重要的调味品,G是一种氧化物,为红色固体粉末,B为三大强酸之一,H是一种有毒的气体。请回答下列问题:
(1)B的化学式为___________,除了B以外,再写出一种强酸的化学式___________。H的化学式为___________。
(2)反应①的化学方程式为___________。
(3)反应②的化学方程式为___________。
(4)写出反应④的化学方程式___________,该反应在实际生产中可用于___________。
(5)上图转化关系中一定未涉及到的基本反应类型是___________ 。
24. 食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分是___________(填化学式),石灰所属的物质类型___________(填序号)。
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂 ⑤纯净物 ⑥化合物 ⑦盐
(2)生石灰可做干燥剂的理由是___________(用化学方程式表示)。由石灰石制备生石灰的化学方程式为___________。
(3)你认为下列内容还必须在这种小纸袋上注明的是___________(填序号)。
①禁止食用 ②可以食用 ③禁止用手拿 ④生产日期
(4)小纸袋中的物质能否长期地作干燥剂?为什么?______________________。
(5)漂白粉可用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为___________。
大理白族自治州民族中学2023-2024学年高一上学期开学考试
化学试卷 答案解析
可能用到的相对原子质量:H:1 C:12 O:16
一、选择题(本大题共20个小题,共45分。每题只有一个选项符合题意,1-15题每小题2分,16-20题每小题3分。)
1. 下列关于水的认识正确的是
A. 使用无磷洗衣粉有利于防止水体富营养化
B. 生活中通过活性炭吸附、过滤可以使硬水软化
C. 汽车发动机用水来冷却是因为水的比热容小
D. 气压增大,水的沸点会降低
【答案】A
【解析】
【分析】
【详解】A.磷使藻类大量繁殖,造成水体的营养化,无磷洗衣粉可以防止水体富营养化,故A正确;
B.通过活性炭吸附作用,可以吸附水中的色素和异味,但是不能减小水中的钙离子、镁离子等,不能使硬水软化,故B错误;
C.与其他物质相比,水的比热容大,在质量相同、升高的温度相同时,水吸收的热量多,所以汽车发动机用水来冷却,故C错误;
D.压强越大水的沸点越高,故D错误;
故选A。
2. 下列化学用语表示正确的是
A. Fe2+—铁离子 B. 镁原子结构示意图—
C. 氯酸钾—KClO3 D. N2—两个氮原子
【答案】C
【解析】
【分析】
【详解】A.Fe2+表示亚铁离子,A错误;
B.Mg是12号元素,原子核外电子排布式是2、8、2,故Mg原子结构示意图为,B错误;
C.氯酸钾化学式为KClO3,C正确;
D.N2表示氮气分子,1个分子中含有两个氮原子,D错误;
故合理选项是C。
3. 下图是某反应前后分子种类变化的微观示意图。下列说法正确的是
A. 反应前后分子个数不变
B. 反应中涉及到3种氧化物
C. 丙的中硫元素的化合价为+6
D. 反应中甲、乙分子个数比为2:3
【答案】D
【解析】
【分析】根据图示,结合质量守恒定律可知发生反应方程式为:2H2S+3O22SO2+2H2O,然后根据问题分析解答。
【详解】A.根据反应方程式可知:反应前后物质分子数不等,A错误;
B.在上述物质中涉及的氧化物只有SO2、H2O两种,B错误;
C.丙是SO2,其中S元素化合价为+4价,C错误;
D.根据方程式可知:在反应中H2S、O2反应的个数比是2:3,D正确;
故合理选项D。
4. 如图所示的实验基本操作正确的是
A.二氧化碳验满 B.点燃酒精灯 C.读取液体体积 D.稀释浓硫酸
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.CO2不能燃烧,也不支持燃烧,其密度比空气大,因此若收集满,集气瓶的瓶口有CO2气体外溢,将燃着的火柴放在集气瓶口,若火柴熄灭,可以证明二氧化碳已经收集满,A正确;
B.不能用燃着的酒精灯去点燃另一个酒精灯,防止酒精洒出,其燃烧引发火灾,B错误;
C.用量筒量取液体物质读数时,应该使视线与凹液面的最低处相切,C错误;
D.浓硫酸溶于水会放出大量热,由于其密度比水大,所以稀释时应该注酸入水,即将浓硫酸沿烧杯内部缓缓加入盛有水的烧杯中,并用玻璃棒不断搅拌,使热迅速扩散,D错误;
故合理选项是A。
5. 下列反应不属于化学四种基本反应类型的是
A. NH4HCO3NH3↑+CO2↑+H2O B. CaCO3+CO2+H2O=Ca(HCO3)2
C. 2NaCl+2H2O2NaOH+H2↑+Cl2↑ D. 2Mg+CO22MgO+C
【答案】C
【解析】
【详解】A .NH4HCO3NH3↑+CO2↑+H2O是由一种物质生成两种物质的反应,属于分解反应,故A不符合题意;
B.CaCO3+CO2+H2O=Ca(HCO3)2是两种或多种物质生成一种物质的反应,属于化合反应,故B不符合题意;
C.2NaCl+2H2O2NaOH+H2↑+Cl2↑不符合四种基本反应类型的特征,故C符合题意;
D.2Mg+CO22MgO+C是一种单质和一种化合物生成另一种单质和另一种化合物的反应,是置换反应,故D不符合题意。
答案选C。
6. 节日期间商场里顾客很多,有人会感觉到闷热缺氧,测定出氧气的体积分数可能是
A. 1% B. 19% C. 25% D. 78%
【答案】B
【解析】
【分析】空气中氧气的体积分数为21%,节日期间的商场里顾客很多,有人会感觉到闷热缺氧,则氧气的体积分数应略小于21%.
【详解】A.氧气的体积分数应略小于21%,空气中氧气的体积分数不可能低至1%,否则人类没法生存,A错误;
B.空气中氧气的体积分数可能为19%,B正确;
C.氧气的体积分数应略小于21%,空气中氧气的体积分数不可能为25%,C错误;
D.氧气的体积分数应略小于21%,空气中氧气的体积分数不可能为78%,D错误;
答案选B。
【点睛】本题难度不大,了解空气中氧气的体积分数(21%)是正确解答本题的关键。
7. 日常生活中,区别下列各组物质所用的方法,错误的是
A. 白酒和白醋——观察颜色
B. 棉线和羊毛线——灼烧,闻气味
C. 黄铜和黄金——灼烧,观察颜色变化
D. 热塑性塑料和热固性塑料——加热,观察外形变化
【答案】A
【解析】
【详解】A.白酒和白醋都是无色的液体,观察颜色无法区分,故A错误;
B.棉线灼烧没有烧焦羽毛的气味,而羊毛灼烧有烧焦羽毛的气味,故B正确;
C.黄铜灼烧其中的铜与氧气反应生成黑色的氧化铜,而黄金灼烧颜色不会改变,故C正确;
D.热固性塑料加热不会形变,而热塑性塑料加热会发生外形变化,故D正确。
答案选A。
8. 用嘴吹灭燃着的生日蜡烛,利用的主要灭火原理是
A. 隔绝空气 B. 降低可燃物的着火点
C. 清除可燃物 D. 使可燃物温度降到着火点以下
【答案】D
【解析】
【详解】根据灭火原理分析,灭火的原理:(只要消除燃烧条件的任意一个即可)①撤离可燃物 ②隔绝氧气(或空气)③降温到着火点以下;嘴吹蜡烛时吹走了蜡烛火焰的热量,从而降低了蜡烛的温度,导致可燃物的温度降到了其着火点以下,所以蜡烛熄灭,D符合题意。
答案选D。
9. 加碘食盐所含的碘酸钾(KIO3)中,碘元素的化合价为
A. +1 B. +3 C. +5 D. +7
【答案】C
【解析】
【详解】根据物质碘酸钾的化学式KIO3,利用化合物中各元素化合价代数和为0的原则,由化合物中K、O元素分别为+1、-2价,计算化合物中碘元素的化合价;设化合物中碘元素的化合价为x,依据化合物中各元素化合价代数和为0的原则,有(+1)+x+(-2)×3=0,解得x=+5。
答案选C。
10. 下列事实和解释相符的是
A. 干冰用作致冷剂——干冰冰
B. 纯碱溶液使酚酞试液变红——纯碱是碱
C. 用炭黑墨汁书写的字经久不变色——常温下,碳的化学性质稳定
D. 制糖工业用活性炭脱色制白糖——活性炭和有色物质反应
【答案】C
【解析】
【详解】A.干冰用作致冷剂,干冰不是冰,是固体的二氧化碳,干冰作致冷剂是因为固体二氧化碳汽化时吸热致冷,故A不符合题意;
B.纯碱溶液使酚酞试液变红,但纯碱不是碱,纯碱是碳酸钠的俗称,是由钠离子和碳酸根离子构成的化合物,属于盐,故B不符合题意;
C.墨是用炭黑制成的,炭黑的主要成分是碳,用炭黑墨汁书写的字经久不变色,是因为常温下,碳的化学性质稳定,故C符合题意;
D.制糖工业用活性炭脱色制白糖,是因为活性炭具有吸附性,能吸附异味和色素,故D不符合题意。
答案选C。
11. 根据图中的信息判断,下列说法正确的是
A. 硫属于金属元素 B. 硫原子的核电荷数为16
C. 硫原子的相对原子质量为32.07 g D. 在化学反应中,硫原子容易失去电子
【答案】B
【解析】
【详解】A.硫带“石”字旁,属于固态非金属元素,故A错误;
B.由硫原子的结构示意图,圆圈内的数字是16,表示硫原子的核电荷数为16,故B正确;
C.根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,硫原子的相对原子质量为32.07,其单位是1,不是g,故C错误;
D.硫原子的最外层电子数是6,大于4,在化学反应中易得到2个电子而形成阴离子,故D错误。
答案选B
12. 下列金属能与硫酸亚铁溶液反应的是
A. 锌 B. 银 C. 铜 D. 铅
【答案】A
【解析】
【详解】在金属活动性顺序中,锌位于铁的前面,而银、铜、铅位于铁的后面,所以锌与硫酸亚铁溶液反应,所以应选A;
故答案为:A.
13. 下列有关乙醇(C2H5OH)的说法,错误的是
A. 乙醇是一种有机物
B. 乙醇由三种元素组成
C. 乙醇分子中,碳、氢、氧原子个数比为2∶6∶1
D. 乙醇中,碳元素的质量分数
【答案】D
【解析】
【详解】A.乙醇属于常见的有机物,A正确;
B.乙醇由C、H、O三种元素组成,B正确;
C.乙醇的分子式为C2H6O,碳、氢、氧原子个数比为2:6:1,C正确;
D.碳元素的质量分数=,D错误;
答案选D。
14. 下列物质既属于钾盐又属于硫酸盐的是
A. 碳酸钾 B. 硫酸钠 C. 硝酸钠 D. 硫酸钾
【答案】D
【解析】
【分析】盐是指含有金属离子(铵根)和酸根离子的化合物,可根据所含有的金属或酸根去命名,钾盐指由钾离子和酸根离子构成的盐,硫酸盐指金属离子(铵根)和硫酸根离子构成的盐。
【详解】钾盐指由钾离子和酸根离子构成的盐,硫酸钠、硝酸钠属于钠盐,碳酸钾、硫酸钾属于钾盐,硫酸盐指金属离子(铵根)和硫酸根离子构成的盐,硫酸钠、硫酸钾属于硫酸盐,硝酸钠属于硝酸盐,碳酸钾属于碳酸盐,所以既属于钾盐又属于硫酸盐的是硫酸钾。
答案选D。
15. 按照物质的树状分类和交叉分类,HNO3应属于
①酸②氢化物③氧化物④含氧酸⑤难挥发性酸⑥一元酸⑦化合物
A. ①②③④⑤⑥⑦ B. ①④⑥⑦
C. ①⑦ D. ①④⑤⑥
【答案】B
【解析】
【详解】硝酸是重要的三大强酸之一,它是含氧酸、一元酸、易挥发性酸、化合物,B满足题意。
答案选B。
16. 下列离子方程式中,正确的是
A. 稀硫酸滴在铜片上:
B. 大理石加入稀盐酸中:
C. 铁粉加入氯化铁溶液中:
D. 氯化钡溶液滴入硫酸钠溶液中:
【答案】D
【解析】
【详解】A.铜活泼性弱于氢,与稀硫酸不反应,A错误;
B.大理石成分为CaCO3加入稀盐酸反应生成氯化钙、二氧化碳和水,离子方程式为:,B错误;
C.氯化铁溶液与铁反应生成氯化亚铁,离子方程式为:2Fe3++Fe=3Fe2+,C错误;
D.氯化钡溶液和硫酸钠溶液混合生成硫酸钡和氯化钠,反应的离子方程式:,D正确;
故选:D。
17. FeCl3溶液、Fe(OH)3胶体共同具备的性质是
A. 都能透过半透膜,都呈红褐色
B. 分散质颗粒直径相同
C. 都较稳定,密封保存一段时间都不会产生沉淀
D. 当有光线透过时,都能产生丁达尔效应
【答案】C
【解析】
【分析】
【详解】A.溶液能通过半透膜,胶体不能,FeCl3溶液与Fe(OH)3胶体的颜色分别为棕黄色、红褐色,故A错误;
B.Fe(OH)3胶体的分散质颗粒直径在1~100nm之间,FeCl3溶液的分散质颗粒直径小于1nm,分散质颗粒直径不相同,故B错误;
C.胶体具有介稳性,放置不会产生沉淀,溶液是稳定的,故C正确;
D.只有胶体具有丁达尔效应,所以Fe(OH)3胶体具有丁达尔效应,而FeCl3溶液不具备,故D错误;
故选C。
18. 下列关于浊液、胶体和溶液的知识,错误的是
A. 胶体区别于溶液的本质是胶体中分散质大小介于1nm和100nm之间
B. 浊液、胶体和溶液中的分散剂可以不一定是水
C. 胶体都可以用来净水
D. 无色的溶液和无色的胶体从外观上不能简单区分出来
【答案】C
【解析】
【分析】
【详解】A.胶体区别于溶液的本质是胶体中粒子直径分散质大小介于1nm和100nm之间,故A正确;
B.胶体有气溶胶和固溶胶,分散剂为气体和固体,液溶胶分散剂为液体,但也不一定是水,故B正确;
C.FeCl3等胶体常用于净水,其他的胶体不一定能净水,故C错误;
D.胶体和溶液能用丁达尔效应进行区别,而无色的溶液和无色的胶体从外观上不能简单区分出来,故D正确;
故答案为C。
19. 下列说法中正确的是
A. 熔融的氯化氢不能导电,所以氯化氢是非电解质
B. SO2气体溶于水能导电,所以SO2是电解质
C. 氯化银难溶于水,所以氯化银是非电解质
D. 蔗糖溶液和熔融的蔗糖都不能导电,所以蔗糖是非电解质
【答案】D
【解析】
【分析】
【详解】A.氯化氢气体不能导电,但其水溶液中有自由移动的氯离子和氢离子能够导电,所以氯化氢为电解质,A项错误;
B.SO2常温下为气体,只有SO2分子,没有自由移动的离子,虽SO2在水溶液中与水反应,生成亚硫酸,亚硫酸电离出自由移动的离子,溶液能够导电,但自由移动的离子不是SO2自身电离,SO2是化合物,所以SO2是非电解质,B项错误;
C.化合物为电解质还是非电解质与化合物的溶解性没有关系,氯化银虽难溶于水,但溶解的部分在溶液中却能完全电离,故氯化银为电解质,且为强电解质,C项错误;
D.蔗糖在溶液中以分子形式存在,不能电离,则蔗糖溶液不能导电,蔗糖在熔融状态也不导电,所以蔗糖是非电解质,D项正确;
答案选D。
20. 下列树状分类方法中正确的是( )
A. B.
C. D.
【答案】A
【解析】
【详解】A.纯净物包括单质和化合物两类,单质分为金属单质和非金属单质,A正确;
B.溶液属于混合物,B错误;
C.无机物并不都是化合物,如单质,氧化物、非氧化物并不属于酸,C错误;
D.氧化物属于化合物,两者不是并列关系,D错误;
故答案为:A。
二、填空题(本大题有4个题目,共计55分)
21. 完成下列问题。
(1)写出下列物质的化学式
高锰酸钾___________;二氧化碳___________;氮气___________;双氧水___________;硝酸___________; 氢氧化钠___________;氯化钡___________;硝酸银___________。
(2)写出下列物质在水溶液中的电离方程式:
Al2(SO4)3:___________;
NH4NO3:___________;
(3)根据题中所给信息写出相应反应的化学方程式:
①工业上以Al2O3和冰晶石(Na3AlF6)为原料,在通电的条件下电解熔融氧化铝制取金属铝,同时得到氧气。___________。
②剧烈运动会使人肌肉酸痛。放松一段时间后,血液中的乳酸(化学式为C3H6O3)与吸入的氧气反应生成二氧化碳和水,而使肌肉的酸痛感消失。___________
【答案】(1) ①. KMnO4 ②. CO2 ③. N2 ④. H2O2 ⑤. HNO3 ⑥. NaOH ⑦. BaCl2 ⑧. AgNO3
(2) ①. Al2(SO4)3=2Al3++3 ②. NH4NO3=+
(3) ①. ②. C3H6O3+3O2=3CO2+3H2O
【解析】
【小问1详解】
高锰酸钾的化学式:KMnO4;二氧化碳的化学式:CO2;氮气的化学式:N2;双氧水的化学式:H2O2;硝酸的化学式:HNO3;氢氧化钠的化学式:NaOH;氯化钡的化学式:BaCl2;硝酸银的化学式:AgNO3;故答案为:KMnO4;CO2;N2;H2O2;HNO3;NaOH;BaCl2;AgNO3;
【小问2详解】
硫酸铝在水溶液中完全电离生成铝离子和硫酸根离子,电离方程式为Al2(SO4)3=2Al3++3;硝酸铵在水溶液中完全电离生成铵根离子和硝酸根离子,电离方程式为NH4NO3=+;故答案为:Al2(SO4)3=2Al3++3;NH4NO3=+;
【小问3详解】
①工业上以Al2O3和冰晶石(Na3AlF6)为原料,在通电的条件下电解熔融氧化铝制取金属铝,同时得到氧气,反应的化学方程式为:;故答案为:;
②血液中的乳酸(化学式为C3H6O3)与吸入的氧气反应生成二氧化碳和水,反应的化学方程式为:C3H6O3+3O2=3CO2+3H2O;故答案为:C3H6O3+3O2=3CO2+3H2O。
22. 结合下图回答问题。
(1)甲是硫燃烧的实验,硫在瓶内外燃烧的现象不同,说明燃烧的剧烈程度与 ___________有关,瓶中的水也可用___________来代替。
(2)乙是测定空气中氧气含量的实验。红磷燃烧的化学方程式为___________,若实验测得空气中氧气的含量明显小于1/5,其原因可能是___________。
(3)丙实验可得出的实验结论是___________。高锰酸钾制氧气的化学方程式为___________。
【答案】(1) ①. 氧气的浓度 ②. 氢氧化钠溶
(2) ①. 4P+5O22P2O5 ②. 红磷的量不足(合理均可)
(3) ①. 不同溶质在同种溶剂中的溶解性不同 ②. 2KMnO4K2MnO4+MnO2+O2↑
【解析】
【小问1详解】
甲是硫燃烧的实验,硫在瓶内外燃烧的现象不同,说明燃烧的剧烈程度与氧气的浓度有关,瓶中的水也可用氢氧化钠溶液来代替,因为二氧化硫可溶于氢氧化钠溶液,故答案为:氧气的浓度;氢氧化钠溶液;
【小问2详解】
红磷燃烧化学方程式为4P+5O22P2O5,若实验测得空气中氧气的含量明显小于,其原因可能是红磷的量不足,故答案为:4P+5O22P2O5;红磷的量不足;
【小问3详解】
丙实验发现高锰酸钾完全溶解,碘单质不能完全水解,可得出的实验结论是不同溶质在同种溶剂中的溶解性不同,高锰酸钾制氧气的化学方程式为2KMnO4K2MnO4+MnO2+O2↑;故答案为:不同溶质在同种溶剂中的溶解性不同;2KMnO4K2MnO4+MnO2+O2↑。
23. A~J均为初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中A是碳酸钠,D是重要的调味品,G是一种氧化物,为红色固体粉末,B为三大强酸之一,H是一种有毒的气体。请回答下列问题:
(1)B的化学式为___________,除了B以外,再写出一种强酸的化学式___________。H的化学式为___________。
(2)反应①的化学方程式为___________。
(3)反应②的化学方程式为___________。
(4)写出反应④的化学方程式___________,该反应在实际生产中可用于___________。
(5)上图转化关系中一定未涉及到的基本反应类型是___________ 。
【答案】(1) ①. HCl ②. H2SO4或HNO3 ③. CO
(2)Na2CO3 +2HCl = 2NaCl + H2O+CO2↑
(3)Fe2O3 +6HCl = 2FeCl3 + 3H2O
(4) ①. ②. 炼铁
(5)分解反应、置换反应
【解析】
【分析】A~J均为初中化学常见物质,其中D是重要的调味品,则D为NaCl,A与B反应生成三种物质,其中一种氯化钠,考虑是碳酸钠与盐酸反应,C、E分别为CO2、H2O中一种,A、B分别为盐酸、碳酸钠中的一种,G为红色固体,且G能与盐酸反应生成C与F,推知G为Fe2O3、B为盐酸,则F为FeCl3、C为H2O,故E为CO2、A为Na2CO3,由“G(氧化铁)+H→E(二氧化碳)+J”与“H+I→E(二氧化碳)”,可推知H为CO,则J为Fe、I为O2。
【小问1详解】
由上述分析可知,B为HCl,常见的强酸除了HCl外还有H2SO4或HNO3,H的化学式CO;故答案为:HCl;H2SO4或HNO3;CO;
【小问2详解】
反应①为碳酸钠与盐酸反应,化学方程式为:Na2CO3 +2HCl = 2NaCl + H2O+CO2↑;故答案为:Na2CO3 +2HCl = 2NaCl + H2O+CO2↑;
【小问3详解】
反应②是氧化铁与盐酸反应生成氯化铁与水,化学方程式为Fe2O3+6HCl=2FeCl3+3H2O,故答案为:Fe2O3+6HCl=2FeCl3+3H2O;
【小问4详解】
反应④是氧化铁与一氧化碳反应生成铁与二氧化碳,化学方程式为:;该反应在实际生产中可以冶炼铁,故答案为:;炼铁;
【小问5详解】
反应①是碳酸钠与盐酸反应,反应②是氧化铁与盐酸反应,均属于复分解反应,反应③一氧化碳与氧气反应生成二氧化碳,属于化合反应,反应④可以是一氧化碳与氧化铁反应生成铁与二氧化碳,不属于四种基本类型,转化中不涉及分解反应、置换反应;故答案为:分解反应、置换反应。
24. 食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分是___________(填化学式),石灰所属的物质类型___________(填序号)。
①金属氧化物 ②碱性氧化物 ③碱 ④碱性干燥剂 ⑤纯净物 ⑥化合物 ⑦盐
(2)生石灰可做干燥剂的理由是___________(用化学方程式表示)。由石灰石制备生石灰的化学方程式为___________。
(3)你认为下列内容还必须在这种小纸袋上注明的是___________(填序号)。
①禁止食用 ②可以食用 ③禁止用手拿 ④生产日期
(4)小纸袋中的物质能否长期地作干燥剂?为什么?______________________。
(5)漂白粉可用水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO)2]。次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O=CaCO3↓+2HClO,则X的化学式为___________。
【答案】(1) ①. CaO ②. ①②④⑤⑥
(2) ①. CaO+H2O=Ca(OH)2 ②.
(3)①③④ (4)不能,氧化钙吸收水之后就变成氢氧化钙,失去吸水能力
(5)CO2
【解析】
【小问1详解】
石灰干燥剂的成分是CaO,纯净物包括单质和化合物,化合物包括氧化物、酸、碱、盐,CaO是由钙元素和氧元素组成,属于氧化物,CaO能与水形成的碱,氧化钙为碱性氧化物,能吸收水蒸气,能干燥碱性气体,因此氧化钙为碱性干燥剂,因此石灰所属物质类型为①②④⑤⑥;
【小问2详解】
生石灰能与水反应CaO+H2O=Ca(OH)2,因此生石灰可做干燥剂;工业上常煅烧石灰石制备生石灰,其反应方程式为CaCO3CaO+CO2↑;故答案为CaO+H2O=Ca(OH)2;CaCO3CaO+CO2↑;
【小问3详解】
生石灰不能食用,应注明禁止食用,生石灰与水生成氢氧化钙,氢氧化钙腐蚀皮肤,因此注明禁止用手拿,生石灰能吸收空气中水蒸气、二氧化碳,有一定的使用期限,因此需注明生产日期;故答案为①③④;
【小问4详解】
空气中含有水蒸气,CaO能吸收水蒸气,生成Ca(OH)2,失去吸水能力,因此小纸袋中的物质不能长期作干燥剂;故答案为不能,氧化钙吸收水之后就变成氢氧化钙,失去吸水能力;
【小问5详解】
根据原子守恒、元素守恒,推出X为CO2,故答案为CO2。
同课章节目录
