人教版化学九年级下册第十单元综合素质评价(含解析)
文档属性
| 名称 | 人教版化学九年级下册第十单元综合素质评价(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 633.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-20 00:00:00 | ||
图片预览




文档简介
第十单元综合素质评价
限时:45分钟 满分:40分
可能用到的相对原子质量: H—1 C—12 O—16 Na—23 Cl—35. 5
一、本大题包括12小题, 每小题1分, 共12分, 每小题的4个选项中只有1个符合题意。
1. 下列变化属于化学变化的是( )
A. 氢氧化钠潮解 B. 熟石灰变质
C. 浓硫酸吸水 D. 浓盐酸挥发
2. 在化学实验中或日常生活中都应强化安全意识, 提高安全素养。下列做法符合安全要求的是( )
A. 不慎将浓硫酸沾到皮肤上, 立即用氢氧化钠溶液冲洗
B. 在一氧化碳还原氧化铁的实验中, 将尾气直接排放
C. 稀释浓硫酸时, 将水慢慢注入浓硫酸中
D. 家中天然气泄漏时, 立即关闭阀门并打开门窗通风
3. 下列图示的实验操作中, 正确的是( )
4. 硼酸(化学式为H3BO3) 常用于治疗小儿湿疹。硼元素的相关信息如图所示, 下列说法正确的是( )
A. 硼属于金属元素
B. 硼酸中硼元素的化合价为+3
C. 硼元素的原子质量是10. 81
D. 氢氧化钠沾到皮肤上可立即涂上硼酸溶液
5. 连花清瘟胶囊源自传统中医名方, 可用于治疗流感, 现代仪器测得其成分之一是没食子酸(化学式为C7H6O5) 。下列有关没食子酸的说法正确的是( )
A. 属于氧化物
B. 碳、氢、氧元素的质量比为12:1:16
C. 1个没食子酸分子中含有3个原子
D. 完全燃烧生成CO2和H2O
6. 中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )
A. 氢氧化铝用于治疗胃酸过多
B. 生石灰用于加热即热食品
C. 熟石灰用于改良酸性土壤
D. 硼酸用于处理皮肤上沾有的碱
7. 蚊虫叮咬人的皮肤时会分泌蚁酸, 使皮肤肿痛。要减轻痛痒, 应在被叮咬处涂抹( )
物质 食醋 牛奶 食盐水 牙膏 肥皂水
pH 2~3 6~7 7 8~9 9~10
A. 食醋 B. 牛奶
C. 食盐水 D. 牙膏或肥皂水
8. 氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图如下。下列说法不正确的是( )
A. 盐酸中存在的微粒有水分子和氯化氢分子
B. 该反应的微观实质是H+和OH-结合生成水分子
C. Na+和Cl-在该反应过程中没有被消耗
D. 恰好完全反应时, 溶液呈中性
9. 构建化学观念是学习化学的基础。下列说法错误的是( )
A. 分类观: 纯碱和火碱都属于碱
B. 微粒观: 稀盐酸、稀硫酸的化学性质相似, 是因为它们的溶液中都含有H+
C. 能量观: 氢氧化钠固体溶于水会放出大量的热
D. 转化观: 烧碱和纯碱在一定条件下可相互转化
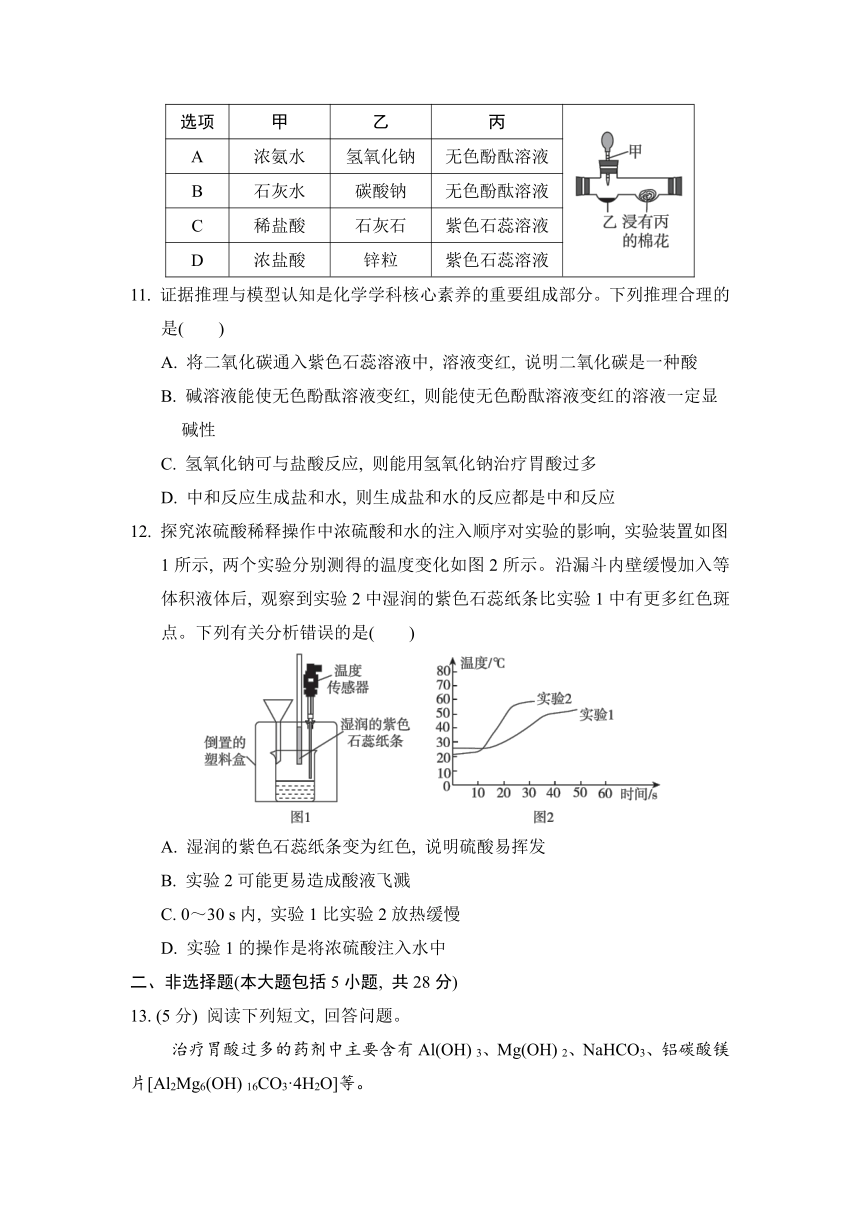
10. 某实验小组用如图所示的装置进行微型实验。按下列表中选项加入试剂, 实验时滴入甲, 浸有丙的棉花不变红的是( )
选项 甲 乙 丙
A 浓氨水 氢氧化钠 无色酚酞溶液
B 石灰水 碳酸钠 无色酚酞溶液
C 稀盐酸 石灰石 紫色石蕊溶液
D 浓盐酸 锌粒 紫色石蕊溶液
11. 证据推理与模型认知是化学学科核心素养的重要组成部分。下列推理合理的是( )
A. 将二氧化碳通入紫色石蕊溶液中, 溶液变红, 说明二氧化碳是一种酸
B. 碱溶液能使无色酚酞溶液变红, 则能使无色酚酞溶液变红的溶液一定显
碱性
C. 氢氧化钠可与盐酸反应, 则能用氢氧化钠治疗胃酸过多
D. 中和反应生成盐和水, 则生成盐和水的反应都是中和反应
12. 探究浓硫酸稀释操作中浓硫酸和水的注入顺序对实验的影响, 实验装置如图1所示, 两个实验分别测得的温度变化如图2所示。沿漏斗内壁缓慢加入等体积液体后, 观察到实验2中湿润的紫色石蕊纸条比实验1中有更多红色斑点。下列有关分析错误的是( )
A. 湿润的紫色石蕊纸条变为红色, 说明硫酸易挥发
B. 实验2可能更易造成酸液飞溅
C. 0~30 s内, 实验1比实验2放热缓慢
D. 实验1的操作是将浓硫酸注入水中
二、非选择题(本大题包括5小题, 共28分)
13. (5分) 阅读下列短文, 回答问题。
治疗胃酸过多的药剂中主要含有Al(OH) 3、Mg(OH) 2、NaHCO3、铝碳酸镁片[Al2Mg6(OH) 16CO3·4H2O]等。
Al(OH) 3难溶于水, 但Al3+在人体内会阻止小肠壁对磷元素的吸收, 使血液和其他组织内磷元素的含量降低, 造成记忆力减退、免疫功能下降。世界卫生组织把铝元素列为食品污染源之一。
Mg(OH)2是一种常用的治疗胃酸过多的药剂, Mg(OH)2与胃酸反应生成Mg2+, 形成的凝胶样的Mg2+对胃酸起到一种隔离的作用, 使胃酸对胃黏膜下组织的刺激作用明显减弱。
NaHCO3是一种白色粉末, 加热至270 ℃完全分解, 遇酸则剧烈反应产生CO2。碳酸氢钠是厨房中常用的面食膨松剂, 医学中常用来治疗胃酸过多。
铝碳酸镁片[Al2Mg6(OH) 16CO3·4H2O]为白色片剂, 成人胃部不适时, 饭后1~2小时可嚼服1~2片。用铝碳酸镁片和碳酸氢钠片治疗胃酸过多时, 药品反应过程中产生CO2的量随时间变化的曲线如图所示。
(1) 从物质类别来看, Mg(OH) 2属于________(填“酸”“碱”或“盐”) 。
(2) 世界卫生组织把铝元素列为食品污染源之一, 原因是________________________________________________________________。
(3) 服用铝碳酸镁片时, 嚼服的目的是________________________________________________________________。
(4) 从安全性和药效时长的角度考虑, 写出由图可得知的信息: ________________________________________________________________。
14. (6分) 下图是实验室制取气体的有关仪器和装置, 据图回答下列问题。
(1) 仪器①的名称是________。
(2) 实验室用稀硫酸与锌粒制取氢气, 为了便于控制反应速率, 组装发生装置时应选择___________(填字母), 反应的化学方程式为______________________________。
(3) 用F装置收集二氧化碳时, 气体应从________(填“a”或“b”) 端通入。收集满二氧化碳后, 用F装置组装G装置, 挤压胶头滴管使NaOH溶液进入烧瓶中, 振荡烧瓶后打开止水夹, 观察到的现象是________________________________________________________________。
15. (6分) 工业上以黄铁矿(主要成分是FeS2) 为原料生产硫酸的流程如图所示:
(1) 将黄铁矿粉碎的目的是___________________________________________。
(2) 沸腾炉中发生反应的化学方程式为_________________________________。
(3) 若硫酸厂产生的废气未经处理就排放到空气中, 可能会形成酸雨, 我们把pH<________的降雨称为酸雨。
(4) 流程图中, 一共有________种氧化物。炉渣(Fe2O3) 在工业上可用于________。
16. (6分) 无明显反应现象的可视化是一项重要的研究课题。某化学兴趣小组以“探究二氧化碳与氢氧化钠是否反应”为主题展开化学反应可视化的项目式学习。
【任务一】证明反应物的减少或消失
实验一: 传统实验
该小组同学利用图1所示装置按照下列步骤展开探究。
步骤1: 关闭K1, 打开K2、K3, 将2 mL稀硫酸迅速全部注入注射器C中。
步骤2: 至不再产生气泡, 拉动注射器B的活塞, 将产生的气体全部抽出后, 关闭K3。
步骤3: 打开K1, 将2 mL氢氧化钠溶液注入注射器B中, 关闭K1后充分振荡, 观察现象。
(1) 上述实验中, 能证明氢氧化钠溶液与二氧化碳反应的现象是____________________________________, 该反应的化学方程式为________________________________________________________________。
实验二: 数字化实验
(2) 按照图2所示装置分别进行两次实验, 所得曲线如图3所示, 则图3中的曲线________(填“A”或“B”) 表示二氧化碳与氢氧化钠溶液的反应; 增加等体积二氧化碳与80 mL蒸馏水进行实验的目的是________________________________________________________________。
【任务二】证明有新物质生成
实验三: 产物转化法实验
(3) 小芳设计并进行实验: 向氢氧化钠溶液中通入二氧化碳, 然后向上述溶液中加入________, 一段时间后有气泡产生, 证明氢氧化钠溶液与二氧化碳发生了反应。
注意: 若答对以下小题奖励3分, 化学总得分不超过40分。
实验四: 创新实验
【查阅资料】气压减小时, 水的沸点会降低。
(4) 用两套图4所示装置进行实验, 在第一套装置中注入3 mL浓氢氧化钠溶液, 在第二套装置中注入3 mL水, 分别振荡试管, 观察到________________________________________________________________________________________的现象, 证明二氧化碳与氢氧化钠发生了反应。
(5) 小雨同学结合“探究藻类植物如何进行生命活动”, 设计了如图5所示的实验装置: 先在水槽内的支架上放两个盛有不同物质的小烧杯(CO2缓冲液能吸收、释放CO2, 使密闭装置内CO2的浓度保持不变) , 再往水槽内注入一定量的水, 最后用一个大烧杯罩住。在光照下实验持续一段时间后, 观察装置内液面变化情况。
①上述实验持续光照一段时间后, 请说出液面的变化情况并做出合理解释: _________________________________________________________________________________________________________________________________。
②若将CO2缓冲液换成NaOH溶液, 重新进行实验, 装置内液面的变化情况是______________________________________________________________。
17. (5分) 某同学做中和反应时, 取20 g 10%的NaOH溶液于烧杯中, 滴入2滴无色酚酞溶液, 然后边滴加稀盐酸边搅拌, 直到溶液恰好由红色变为无色(恰好完全反应) 。
(1) 计算恰好完全反应时, 理论上消耗盐酸中氯化氢的质量。(写出计算过程)
(2) 该同学发现实验过程中溶液里有少量气泡产生, 原因可能是________________________________________________________________。
答案
一、1. B 【点拨】氢氧化钠潮解时吸收水分, 没有新物质生成, 属于物理变化, A不符合; 熟石灰变质是氢氧化钙与二氧化碳发生反应生成了碳酸钙, 属于化学变化, B符合; 浓硫酸具有吸水性, 吸收水分的过程中没有新物质生成, 属于物理变化, C不符合; 浓盐酸具有挥发性, 挥发后溶质质量分数减小, 但没有新物质生成, 属于物理变化, D不符合。故选B。
2. D 【点拨】不慎将浓硫酸沾到皮肤上, 应立即用大量的水冲洗, 再涂上3%~5%的碳酸氢钠溶液, 氢氧化钠溶液具有强腐蚀性, 不能用于冲洗皮肤, A错误; 在一氧化碳还原氧化铁的实验中, 尾气中含有一氧化碳, 一氧化碳有毒, 直接排放会污染空气, B错误; 稀释浓硫酸时, 如果将水注入浓硫酸中, 会造成酸液飞溅, C错误; 家中天然气泄漏时, 为了防止天然气与空气混合后遇明火或电火花发生爆炸, 应立即关闭阀门并打开门窗通风, D正确。故选D。
3. D 【点拨】测定溶液的pH时, 不能将pH试纸直接伸入待测溶液中, 要用玻璃棒蘸取待测溶液滴在pH试纸上, 然后将pH试纸显示的颜色与标准比色卡对照, A错误; 稀释浓硫酸时, 要将浓硫酸沿烧杯内壁慢慢倒入水中, 不能将水倒入浓硫酸中, 防止酸液溅出, B错误; 配制氯化钠溶液时, 溶解操作应在烧杯中进行, 不能在量筒内进行, C错误; D图所示操作正确。故选D。
4. B 【点拨】硼属于非金属元素, A错误; H3BO3中, 氢元素的化合价为+1, 氧元素的化合价为-2, 根据化学式中各元素正、负化合价的代数和为零, 可知硼元素的化合价为+3, B正确; 硼元素的相对原子质量为10. 81, C错误; 氢氧化钠沾到皮肤上, 要立即用大量水冲洗, 然后涂上硼酸溶液, D错误。故选B。
5. D 【点拨】氧化物是由两种元素组成且其中一种为氧元素的化合物, 没食子酸(C7H6O5) 中含有三种元素, 不属于氧化物, A错误; C7H6O5中, 碳、氢、氧元素的质量比为(12×7) :(1×6) :(16×5) =42:3:40, B错误; 1个C7H6O5分子中含有18个原子, C错误; C7H6O5中含有C、H、O元素, 完全燃烧生成CO2和H2O, D正确。故选D。
6. B 【点拨】氢氧化铝用于治疗胃酸过多, 是因为氢氧化铝能与稀盐酸反应生成氯化铝和水, 属于中和反应, A不符合; 生石灰用于加热即热食品, 是因为氧化钙能与水反应生成氢氧化钙, 放出大量的热, 属于化合反应, B符合; 熟石灰用于改良酸性土壤, 是因为氢氧化钙能与土壤中的酸反应生成盐和水, 属于中和反应, C不符合; 硼酸用于处理皮肤上沾有的碱, 是因为硼酸能与碱反应生成盐和水, 属于中和反应, D不符合。故选B。
7. D 【点拨】食醋和牛奶的pH都小于7, 都显酸性, 都不能中和蚁酸, A、B错误; 食盐水的pH等于7, 显中性, 不能中和蚁酸, C错误; 牙膏和肥皂水的pH都大于7, 都显碱性, 都能中和蚁酸, D正确。故选D。
8. A 【点拨】盐酸中存在的微粒有氢离子、氯离子和水分子, A错误; 该反应的微观实质是氢离子和氢氧根离子结合生成水分子, 而钠离子、氯离子未发生变化, B、C正确; 氢氧化钠与稀盐酸恰好完全反应时, 溶液中只含有钠离子、氯离子和水分子, 故溶液显中性, D正确。故选A。
9. A 【点拨】火碱是氢氧化钠的俗称, 属于碱, 纯碱是碳酸钠的俗称, 属于盐, A错误; 稀盐酸、稀硫酸的化学性质相似, 是因为它们的溶液中都含有H+, 都具有酸的通性, B正确; 氢氧化钠固体溶于水时会放出大量的热, 使溶液的温度升高, C正确; 烧碱是氢氧化钠的俗称, 纯碱是碳酸钠的俗称, 氢氧化钠与二氧化碳反应生成碳酸钠和水, 碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠, D正确。故选A。
10. B 【点拨】将甲中的浓氨水滴入乙中的氢氧化钠中, 由于浓氨水具有挥发性, 挥发出的氨分子会不断运动, 运动到浸有无色酚酞溶液的棉花上形成氨水, 氨水显碱性, 能使丙处浸有无色酚酞溶液的棉花变红, A不符合; 将甲中的石灰水滴入乙中的碳酸钠溶液中, 氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠, 这些物质都没有挥发性, 不能使丙处浸有无色酚酞溶液的棉花变红, B符合; 将甲中的稀盐酸滴入乙中的石灰石中, 稀盐酸与碳酸钙反应生成氯化钙、水和二氧化碳, 二氧化碳气体扩散到浸有紫色石蕊溶液的棉花上, 与水反应生成碳酸, 碳酸显酸性, 能使丙处浸有紫色石蕊溶液的棉花变红, C不符合; 将甲中的浓盐酸滴入乙中的锌粒上, 锌与盐酸反应放热, 加速浓盐酸的挥发, 挥发出的氯化氢分子不断运动, 运动到浸有紫色石蕊溶液的棉花上形成盐酸, 能使丙处浸有紫色石蕊溶液的棉花变红, D不符合。故选B。
11. B 【点拨】将二氧化碳通入紫色石蕊溶液中, 溶液变红是因为二氧化碳与水反应生成了碳酸, A错误; 碱溶液能使无色酚酞溶液变红, 则能使无色酚酞溶液变红的溶液一定显碱性, B正确; 氢氧化钠可与盐酸反应, 但氢氧化钠具有强烈的腐蚀性, 故不能用氢氧化钠治疗胃酸过多, C错误; 中和反应能生成盐和水, 但生成盐和水的反应不一定是中和反应, 如二氧化碳和氢氧化钠反应生成碳酸钠和水, D错误。故选B。
12. A 【点拨】沿漏斗内壁向烧杯中注入液体, 观察到实验2中湿润的紫色石蕊纸条比实验1中有更多红色斑点, 且实验2的温度上升幅度比实验1大, 说明实验2是将水注入浓硫酸中, 造成酸液飞溅, 则实验1是将浓硫酸注入水中。图中湿润的紫色石蕊纸条变为红色, 说明浓硫酸飞溅到湿润的紫色石蕊纸条上, 硫酸没有挥发性, A错误; 实验2是将水注入浓硫酸中, 因此更易造成酸液飞溅, B正确; 0~30 s内, 实验1比实验2温度上升幅度小, 因此实验1比实验2放热缓慢, C正确; 由以上分析可知, 实验1是将浓硫酸注入水中, D正确。故选A。
二、13. (1) 碱
(2) Al3+在人体内会阻止小肠壁对磷元素的吸收, 使血液和其他组织内磷元素的含量降低, 造成记忆力减退、免疫功能下降
(3) 增大接触面积, 使药物尽快起效, 药效完全发挥
(4) 胃溃疡患者不能服用碳酸氢钠片, 铝碳酸镁片发挥药效的时间更长
【点拨】(1) Mg(OH) 2由Mg2+和OH-构成, 属于碱。(2) 由短文可知, Al3+在人体内会阻止小肠壁对磷元素的吸收, 使血液和其他组织内磷元素的含量降低, 造成记忆力减退、免疫功能下降, 这是世界卫生组织把铝元素列为食品污染源之一的原因。(3) 服用铝碳酸镁片时, 嚼服可以增大接触面积, 药品中的有效成分与胃酸接触更充分, 使药物尽快起效, 药效完全发挥。(4) 由图可知, 碳酸氢钠与胃酸反应, 短时间内迅速产生大量二氧化碳气体, 对胃溃疡患者来说, 会造成胃穿孔而加重病情, 所以这类患者不能服用碳酸氢钠片; 铝碳酸镁片与胃酸反应, 反应相对缓慢一些, 因此发挥药效的时间更长。
14. (1) 铁架台
(2) AC; Zn+H2SO4=== ZnSO4+H2↑
(3) a; 烧杯中的水进入烧瓶, 形成红色喷泉
【点拨】(1) 图中仪器①是铁架台。(2) 用稀硫酸与锌粒制取氢气时, 为了便于控制反应速率, 需要控制稀硫酸的滴加速率, 故组装发生装置时应选择AC, 反应的化学方程式为Zn+H2SO4===ZnSO4+H2↑。(3) CO2的密度大于空气, F装置的瓶口朝下, 故收集CO2时气体应从a端通入; G装置中, 挤压胶头滴管使NaOH溶液进入烧瓶中, 振荡烧瓶, CO2与NaOH反应生成Na2CO3, 装置内压强减小, 打开止水夹, 烧杯中的水进入烧瓶, Na2CO3溶液显碱性, 能使酚酞溶液变红, 因而形成红色喷泉。
15. (1) 增大反应物的接触面积, 使反应更快、更充分
(2) 4FeS2+11O2 2Fe2O3+8SO2
(3) 5. 6 (4) 4; 炼铁
【点拨】(1) 将黄铁矿粉碎能增大黄铁矿与氧气的接触面积, 加快反应速率, 使反应更快、更充分。(2) 沸腾炉中, 反应物是FeS2和O2, 生成物是Fe2O3和SO2, 反应的化学方程式为4FeS2+11O2 2Fe2O3+8SO2。(3) 酸雨是指pH<5. 6的雨水。(4) 流程图中的氧化物有SO2、SO3、Fe2O3、H2O, 共4种; 炉渣(Fe2O3) 在工业上可用于炼铁。
16. (1) 步骤3中注射器B的活塞慢慢向左移动; 2NaOH+CO2=== Na2CO3+H2O
(2) B; 做对比实验(或排除二氧化碳溶于水的影响等, 合理均可)
(3) 稀盐酸(或稀硫酸等)
(4) 第一套装置中锥形瓶内的水沸腾, 第二套装置中无明显现象
(5) ①一段时间后大烧杯内的水面下降, 水槽内的水面上升。解释:黑藻在光照下能进行光合作用产生氧气, 使大烧杯内的压强增大, 当大烧杯内的压强大于外界大气压时, 大烧杯内的水被压入水槽内 ②大烧杯内水面上升, 水槽内水面下降
【点拨】(1) 氢氧化钠和二氧化碳反应:2NaOH+CO2=== Na2CO3+H2O, 导致注射器B中的二氧化碳减少, 压强减小, 故注射器B的活塞慢慢向左移动。(2) 二氧化碳能溶于水, 也能与氢氧化钠反应, 但与氢氧化钠反应导致压强减小的幅度较大, 故图3中的曲线B表示氢氧化钠溶液与二氧化碳的反应; 向二氧化碳中加入80 mL蒸馏水进行对比实验, 可以排除二氧化碳溶于水对实验产生的影响。(3) 氢氧化钠与二氧化碳反应生成碳酸钠和水, 碳酸钠能与酸反应生成二氧化碳, 故加入的试剂是稀盐酸或稀硫酸等。(4) 第一套装置中, 二氧化碳与氢氧化钠溶液反应生成碳酸钠和水, 试管内的二氧化碳被消耗, 装置内的压强减小, 锥形瓶内水的沸点降低, 所以96 ℃以上的水会沸腾; 第二套装置中, 试管内剩余大量二氧化碳, 压强变化不明显, 因此锥形瓶内的水无明显现象。(5) ①小烧杯内为CO2缓冲液时, 黑藻在光照下进行光合作用产生O2, 大烧杯内压强增大, 大于外界大气压, 大烧杯内的水被压入水槽内, 所以大烧杯内水面下降, 水槽内水面上升。②将小烧杯中的CO2缓冲液换成NaOH溶液时, 黑藻不能进行光合作用, 只能进行呼吸作用, 呼吸作用消耗氧气, 释放的CO2被NaOH溶液吸收, 大烧杯内压强减小, 小于外界大气压, 水槽内的水被压入大烧杯内, 所以大烧杯内水面上升, 水槽内水面下降。
17. (1) 解:设理论上消耗盐酸中氯化氢的质量为x。
NaOH + HCl=== NaCl+H2O
40 36. 5
20 g×10% x
= x=1. 825 g
答:理论上消耗盐酸中氯化氢的质量为1. 825 g。
(2) NaOH变质了, 生成的Na2CO3与盐酸反应生成了CO2气体
限时:45分钟 满分:40分
可能用到的相对原子质量: H—1 C—12 O—16 Na—23 Cl—35. 5
一、本大题包括12小题, 每小题1分, 共12分, 每小题的4个选项中只有1个符合题意。
1. 下列变化属于化学变化的是( )
A. 氢氧化钠潮解 B. 熟石灰变质
C. 浓硫酸吸水 D. 浓盐酸挥发
2. 在化学实验中或日常生活中都应强化安全意识, 提高安全素养。下列做法符合安全要求的是( )
A. 不慎将浓硫酸沾到皮肤上, 立即用氢氧化钠溶液冲洗
B. 在一氧化碳还原氧化铁的实验中, 将尾气直接排放
C. 稀释浓硫酸时, 将水慢慢注入浓硫酸中
D. 家中天然气泄漏时, 立即关闭阀门并打开门窗通风
3. 下列图示的实验操作中, 正确的是( )
4. 硼酸(化学式为H3BO3) 常用于治疗小儿湿疹。硼元素的相关信息如图所示, 下列说法正确的是( )
A. 硼属于金属元素
B. 硼酸中硼元素的化合价为+3
C. 硼元素的原子质量是10. 81
D. 氢氧化钠沾到皮肤上可立即涂上硼酸溶液
5. 连花清瘟胶囊源自传统中医名方, 可用于治疗流感, 现代仪器测得其成分之一是没食子酸(化学式为C7H6O5) 。下列有关没食子酸的说法正确的是( )
A. 属于氧化物
B. 碳、氢、氧元素的质量比为12:1:16
C. 1个没食子酸分子中含有3个原子
D. 完全燃烧生成CO2和H2O
6. 中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )
A. 氢氧化铝用于治疗胃酸过多
B. 生石灰用于加热即热食品
C. 熟石灰用于改良酸性土壤
D. 硼酸用于处理皮肤上沾有的碱
7. 蚊虫叮咬人的皮肤时会分泌蚁酸, 使皮肤肿痛。要减轻痛痒, 应在被叮咬处涂抹( )
物质 食醋 牛奶 食盐水 牙膏 肥皂水
pH 2~3 6~7 7 8~9 9~10
A. 食醋 B. 牛奶
C. 食盐水 D. 牙膏或肥皂水
8. 氢氧化钠溶液与稀盐酸恰好完全反应的微观示意图如下。下列说法不正确的是( )
A. 盐酸中存在的微粒有水分子和氯化氢分子
B. 该反应的微观实质是H+和OH-结合生成水分子
C. Na+和Cl-在该反应过程中没有被消耗
D. 恰好完全反应时, 溶液呈中性
9. 构建化学观念是学习化学的基础。下列说法错误的是( )
A. 分类观: 纯碱和火碱都属于碱
B. 微粒观: 稀盐酸、稀硫酸的化学性质相似, 是因为它们的溶液中都含有H+
C. 能量观: 氢氧化钠固体溶于水会放出大量的热
D. 转化观: 烧碱和纯碱在一定条件下可相互转化
10. 某实验小组用如图所示的装置进行微型实验。按下列表中选项加入试剂, 实验时滴入甲, 浸有丙的棉花不变红的是( )
选项 甲 乙 丙
A 浓氨水 氢氧化钠 无色酚酞溶液
B 石灰水 碳酸钠 无色酚酞溶液
C 稀盐酸 石灰石 紫色石蕊溶液
D 浓盐酸 锌粒 紫色石蕊溶液
11. 证据推理与模型认知是化学学科核心素养的重要组成部分。下列推理合理的是( )
A. 将二氧化碳通入紫色石蕊溶液中, 溶液变红, 说明二氧化碳是一种酸
B. 碱溶液能使无色酚酞溶液变红, 则能使无色酚酞溶液变红的溶液一定显
碱性
C. 氢氧化钠可与盐酸反应, 则能用氢氧化钠治疗胃酸过多
D. 中和反应生成盐和水, 则生成盐和水的反应都是中和反应
12. 探究浓硫酸稀释操作中浓硫酸和水的注入顺序对实验的影响, 实验装置如图1所示, 两个实验分别测得的温度变化如图2所示。沿漏斗内壁缓慢加入等体积液体后, 观察到实验2中湿润的紫色石蕊纸条比实验1中有更多红色斑点。下列有关分析错误的是( )
A. 湿润的紫色石蕊纸条变为红色, 说明硫酸易挥发
B. 实验2可能更易造成酸液飞溅
C. 0~30 s内, 实验1比实验2放热缓慢
D. 实验1的操作是将浓硫酸注入水中
二、非选择题(本大题包括5小题, 共28分)
13. (5分) 阅读下列短文, 回答问题。
治疗胃酸过多的药剂中主要含有Al(OH) 3、Mg(OH) 2、NaHCO3、铝碳酸镁片[Al2Mg6(OH) 16CO3·4H2O]等。
Al(OH) 3难溶于水, 但Al3+在人体内会阻止小肠壁对磷元素的吸收, 使血液和其他组织内磷元素的含量降低, 造成记忆力减退、免疫功能下降。世界卫生组织把铝元素列为食品污染源之一。
Mg(OH)2是一种常用的治疗胃酸过多的药剂, Mg(OH)2与胃酸反应生成Mg2+, 形成的凝胶样的Mg2+对胃酸起到一种隔离的作用, 使胃酸对胃黏膜下组织的刺激作用明显减弱。
NaHCO3是一种白色粉末, 加热至270 ℃完全分解, 遇酸则剧烈反应产生CO2。碳酸氢钠是厨房中常用的面食膨松剂, 医学中常用来治疗胃酸过多。
铝碳酸镁片[Al2Mg6(OH) 16CO3·4H2O]为白色片剂, 成人胃部不适时, 饭后1~2小时可嚼服1~2片。用铝碳酸镁片和碳酸氢钠片治疗胃酸过多时, 药品反应过程中产生CO2的量随时间变化的曲线如图所示。
(1) 从物质类别来看, Mg(OH) 2属于________(填“酸”“碱”或“盐”) 。
(2) 世界卫生组织把铝元素列为食品污染源之一, 原因是________________________________________________________________。
(3) 服用铝碳酸镁片时, 嚼服的目的是________________________________________________________________。
(4) 从安全性和药效时长的角度考虑, 写出由图可得知的信息: ________________________________________________________________。
14. (6分) 下图是实验室制取气体的有关仪器和装置, 据图回答下列问题。
(1) 仪器①的名称是________。
(2) 实验室用稀硫酸与锌粒制取氢气, 为了便于控制反应速率, 组装发生装置时应选择___________(填字母), 反应的化学方程式为______________________________。
(3) 用F装置收集二氧化碳时, 气体应从________(填“a”或“b”) 端通入。收集满二氧化碳后, 用F装置组装G装置, 挤压胶头滴管使NaOH溶液进入烧瓶中, 振荡烧瓶后打开止水夹, 观察到的现象是________________________________________________________________。
15. (6分) 工业上以黄铁矿(主要成分是FeS2) 为原料生产硫酸的流程如图所示:
(1) 将黄铁矿粉碎的目的是___________________________________________。
(2) 沸腾炉中发生反应的化学方程式为_________________________________。
(3) 若硫酸厂产生的废气未经处理就排放到空气中, 可能会形成酸雨, 我们把pH<________的降雨称为酸雨。
(4) 流程图中, 一共有________种氧化物。炉渣(Fe2O3) 在工业上可用于________。
16. (6分) 无明显反应现象的可视化是一项重要的研究课题。某化学兴趣小组以“探究二氧化碳与氢氧化钠是否反应”为主题展开化学反应可视化的项目式学习。
【任务一】证明反应物的减少或消失
实验一: 传统实验
该小组同学利用图1所示装置按照下列步骤展开探究。
步骤1: 关闭K1, 打开K2、K3, 将2 mL稀硫酸迅速全部注入注射器C中。
步骤2: 至不再产生气泡, 拉动注射器B的活塞, 将产生的气体全部抽出后, 关闭K3。
步骤3: 打开K1, 将2 mL氢氧化钠溶液注入注射器B中, 关闭K1后充分振荡, 观察现象。
(1) 上述实验中, 能证明氢氧化钠溶液与二氧化碳反应的现象是____________________________________, 该反应的化学方程式为________________________________________________________________。
实验二: 数字化实验
(2) 按照图2所示装置分别进行两次实验, 所得曲线如图3所示, 则图3中的曲线________(填“A”或“B”) 表示二氧化碳与氢氧化钠溶液的反应; 增加等体积二氧化碳与80 mL蒸馏水进行实验的目的是________________________________________________________________。
【任务二】证明有新物质生成
实验三: 产物转化法实验
(3) 小芳设计并进行实验: 向氢氧化钠溶液中通入二氧化碳, 然后向上述溶液中加入________, 一段时间后有气泡产生, 证明氢氧化钠溶液与二氧化碳发生了反应。
注意: 若答对以下小题奖励3分, 化学总得分不超过40分。
实验四: 创新实验
【查阅资料】气压减小时, 水的沸点会降低。
(4) 用两套图4所示装置进行实验, 在第一套装置中注入3 mL浓氢氧化钠溶液, 在第二套装置中注入3 mL水, 分别振荡试管, 观察到________________________________________________________________________________________的现象, 证明二氧化碳与氢氧化钠发生了反应。
(5) 小雨同学结合“探究藻类植物如何进行生命活动”, 设计了如图5所示的实验装置: 先在水槽内的支架上放两个盛有不同物质的小烧杯(CO2缓冲液能吸收、释放CO2, 使密闭装置内CO2的浓度保持不变) , 再往水槽内注入一定量的水, 最后用一个大烧杯罩住。在光照下实验持续一段时间后, 观察装置内液面变化情况。
①上述实验持续光照一段时间后, 请说出液面的变化情况并做出合理解释: _________________________________________________________________________________________________________________________________。
②若将CO2缓冲液换成NaOH溶液, 重新进行实验, 装置内液面的变化情况是______________________________________________________________。
17. (5分) 某同学做中和反应时, 取20 g 10%的NaOH溶液于烧杯中, 滴入2滴无色酚酞溶液, 然后边滴加稀盐酸边搅拌, 直到溶液恰好由红色变为无色(恰好完全反应) 。
(1) 计算恰好完全反应时, 理论上消耗盐酸中氯化氢的质量。(写出计算过程)
(2) 该同学发现实验过程中溶液里有少量气泡产生, 原因可能是________________________________________________________________。
答案
一、1. B 【点拨】氢氧化钠潮解时吸收水分, 没有新物质生成, 属于物理变化, A不符合; 熟石灰变质是氢氧化钙与二氧化碳发生反应生成了碳酸钙, 属于化学变化, B符合; 浓硫酸具有吸水性, 吸收水分的过程中没有新物质生成, 属于物理变化, C不符合; 浓盐酸具有挥发性, 挥发后溶质质量分数减小, 但没有新物质生成, 属于物理变化, D不符合。故选B。
2. D 【点拨】不慎将浓硫酸沾到皮肤上, 应立即用大量的水冲洗, 再涂上3%~5%的碳酸氢钠溶液, 氢氧化钠溶液具有强腐蚀性, 不能用于冲洗皮肤, A错误; 在一氧化碳还原氧化铁的实验中, 尾气中含有一氧化碳, 一氧化碳有毒, 直接排放会污染空气, B错误; 稀释浓硫酸时, 如果将水注入浓硫酸中, 会造成酸液飞溅, C错误; 家中天然气泄漏时, 为了防止天然气与空气混合后遇明火或电火花发生爆炸, 应立即关闭阀门并打开门窗通风, D正确。故选D。
3. D 【点拨】测定溶液的pH时, 不能将pH试纸直接伸入待测溶液中, 要用玻璃棒蘸取待测溶液滴在pH试纸上, 然后将pH试纸显示的颜色与标准比色卡对照, A错误; 稀释浓硫酸时, 要将浓硫酸沿烧杯内壁慢慢倒入水中, 不能将水倒入浓硫酸中, 防止酸液溅出, B错误; 配制氯化钠溶液时, 溶解操作应在烧杯中进行, 不能在量筒内进行, C错误; D图所示操作正确。故选D。
4. B 【点拨】硼属于非金属元素, A错误; H3BO3中, 氢元素的化合价为+1, 氧元素的化合价为-2, 根据化学式中各元素正、负化合价的代数和为零, 可知硼元素的化合价为+3, B正确; 硼元素的相对原子质量为10. 81, C错误; 氢氧化钠沾到皮肤上, 要立即用大量水冲洗, 然后涂上硼酸溶液, D错误。故选B。
5. D 【点拨】氧化物是由两种元素组成且其中一种为氧元素的化合物, 没食子酸(C7H6O5) 中含有三种元素, 不属于氧化物, A错误; C7H6O5中, 碳、氢、氧元素的质量比为(12×7) :(1×6) :(16×5) =42:3:40, B错误; 1个C7H6O5分子中含有18个原子, C错误; C7H6O5中含有C、H、O元素, 完全燃烧生成CO2和H2O, D正确。故选D。
6. B 【点拨】氢氧化铝用于治疗胃酸过多, 是因为氢氧化铝能与稀盐酸反应生成氯化铝和水, 属于中和反应, A不符合; 生石灰用于加热即热食品, 是因为氧化钙能与水反应生成氢氧化钙, 放出大量的热, 属于化合反应, B符合; 熟石灰用于改良酸性土壤, 是因为氢氧化钙能与土壤中的酸反应生成盐和水, 属于中和反应, C不符合; 硼酸用于处理皮肤上沾有的碱, 是因为硼酸能与碱反应生成盐和水, 属于中和反应, D不符合。故选B。
7. D 【点拨】食醋和牛奶的pH都小于7, 都显酸性, 都不能中和蚁酸, A、B错误; 食盐水的pH等于7, 显中性, 不能中和蚁酸, C错误; 牙膏和肥皂水的pH都大于7, 都显碱性, 都能中和蚁酸, D正确。故选D。
8. A 【点拨】盐酸中存在的微粒有氢离子、氯离子和水分子, A错误; 该反应的微观实质是氢离子和氢氧根离子结合生成水分子, 而钠离子、氯离子未发生变化, B、C正确; 氢氧化钠与稀盐酸恰好完全反应时, 溶液中只含有钠离子、氯离子和水分子, 故溶液显中性, D正确。故选A。
9. A 【点拨】火碱是氢氧化钠的俗称, 属于碱, 纯碱是碳酸钠的俗称, 属于盐, A错误; 稀盐酸、稀硫酸的化学性质相似, 是因为它们的溶液中都含有H+, 都具有酸的通性, B正确; 氢氧化钠固体溶于水时会放出大量的热, 使溶液的温度升高, C正确; 烧碱是氢氧化钠的俗称, 纯碱是碳酸钠的俗称, 氢氧化钠与二氧化碳反应生成碳酸钠和水, 碳酸钠能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠, D正确。故选A。
10. B 【点拨】将甲中的浓氨水滴入乙中的氢氧化钠中, 由于浓氨水具有挥发性, 挥发出的氨分子会不断运动, 运动到浸有无色酚酞溶液的棉花上形成氨水, 氨水显碱性, 能使丙处浸有无色酚酞溶液的棉花变红, A不符合; 将甲中的石灰水滴入乙中的碳酸钠溶液中, 氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠, 这些物质都没有挥发性, 不能使丙处浸有无色酚酞溶液的棉花变红, B符合; 将甲中的稀盐酸滴入乙中的石灰石中, 稀盐酸与碳酸钙反应生成氯化钙、水和二氧化碳, 二氧化碳气体扩散到浸有紫色石蕊溶液的棉花上, 与水反应生成碳酸, 碳酸显酸性, 能使丙处浸有紫色石蕊溶液的棉花变红, C不符合; 将甲中的浓盐酸滴入乙中的锌粒上, 锌与盐酸反应放热, 加速浓盐酸的挥发, 挥发出的氯化氢分子不断运动, 运动到浸有紫色石蕊溶液的棉花上形成盐酸, 能使丙处浸有紫色石蕊溶液的棉花变红, D不符合。故选B。
11. B 【点拨】将二氧化碳通入紫色石蕊溶液中, 溶液变红是因为二氧化碳与水反应生成了碳酸, A错误; 碱溶液能使无色酚酞溶液变红, 则能使无色酚酞溶液变红的溶液一定显碱性, B正确; 氢氧化钠可与盐酸反应, 但氢氧化钠具有强烈的腐蚀性, 故不能用氢氧化钠治疗胃酸过多, C错误; 中和反应能生成盐和水, 但生成盐和水的反应不一定是中和反应, 如二氧化碳和氢氧化钠反应生成碳酸钠和水, D错误。故选B。
12. A 【点拨】沿漏斗内壁向烧杯中注入液体, 观察到实验2中湿润的紫色石蕊纸条比实验1中有更多红色斑点, 且实验2的温度上升幅度比实验1大, 说明实验2是将水注入浓硫酸中, 造成酸液飞溅, 则实验1是将浓硫酸注入水中。图中湿润的紫色石蕊纸条变为红色, 说明浓硫酸飞溅到湿润的紫色石蕊纸条上, 硫酸没有挥发性, A错误; 实验2是将水注入浓硫酸中, 因此更易造成酸液飞溅, B正确; 0~30 s内, 实验1比实验2温度上升幅度小, 因此实验1比实验2放热缓慢, C正确; 由以上分析可知, 实验1是将浓硫酸注入水中, D正确。故选A。
二、13. (1) 碱
(2) Al3+在人体内会阻止小肠壁对磷元素的吸收, 使血液和其他组织内磷元素的含量降低, 造成记忆力减退、免疫功能下降
(3) 增大接触面积, 使药物尽快起效, 药效完全发挥
(4) 胃溃疡患者不能服用碳酸氢钠片, 铝碳酸镁片发挥药效的时间更长
【点拨】(1) Mg(OH) 2由Mg2+和OH-构成, 属于碱。(2) 由短文可知, Al3+在人体内会阻止小肠壁对磷元素的吸收, 使血液和其他组织内磷元素的含量降低, 造成记忆力减退、免疫功能下降, 这是世界卫生组织把铝元素列为食品污染源之一的原因。(3) 服用铝碳酸镁片时, 嚼服可以增大接触面积, 药品中的有效成分与胃酸接触更充分, 使药物尽快起效, 药效完全发挥。(4) 由图可知, 碳酸氢钠与胃酸反应, 短时间内迅速产生大量二氧化碳气体, 对胃溃疡患者来说, 会造成胃穿孔而加重病情, 所以这类患者不能服用碳酸氢钠片; 铝碳酸镁片与胃酸反应, 反应相对缓慢一些, 因此发挥药效的时间更长。
14. (1) 铁架台
(2) AC; Zn+H2SO4=== ZnSO4+H2↑
(3) a; 烧杯中的水进入烧瓶, 形成红色喷泉
【点拨】(1) 图中仪器①是铁架台。(2) 用稀硫酸与锌粒制取氢气时, 为了便于控制反应速率, 需要控制稀硫酸的滴加速率, 故组装发生装置时应选择AC, 反应的化学方程式为Zn+H2SO4===ZnSO4+H2↑。(3) CO2的密度大于空气, F装置的瓶口朝下, 故收集CO2时气体应从a端通入; G装置中, 挤压胶头滴管使NaOH溶液进入烧瓶中, 振荡烧瓶, CO2与NaOH反应生成Na2CO3, 装置内压强减小, 打开止水夹, 烧杯中的水进入烧瓶, Na2CO3溶液显碱性, 能使酚酞溶液变红, 因而形成红色喷泉。
15. (1) 增大反应物的接触面积, 使反应更快、更充分
(2) 4FeS2+11O2 2Fe2O3+8SO2
(3) 5. 6 (4) 4; 炼铁
【点拨】(1) 将黄铁矿粉碎能增大黄铁矿与氧气的接触面积, 加快反应速率, 使反应更快、更充分。(2) 沸腾炉中, 反应物是FeS2和O2, 生成物是Fe2O3和SO2, 反应的化学方程式为4FeS2+11O2 2Fe2O3+8SO2。(3) 酸雨是指pH<5. 6的雨水。(4) 流程图中的氧化物有SO2、SO3、Fe2O3、H2O, 共4种; 炉渣(Fe2O3) 在工业上可用于炼铁。
16. (1) 步骤3中注射器B的活塞慢慢向左移动; 2NaOH+CO2=== Na2CO3+H2O
(2) B; 做对比实验(或排除二氧化碳溶于水的影响等, 合理均可)
(3) 稀盐酸(或稀硫酸等)
(4) 第一套装置中锥形瓶内的水沸腾, 第二套装置中无明显现象
(5) ①一段时间后大烧杯内的水面下降, 水槽内的水面上升。解释:黑藻在光照下能进行光合作用产生氧气, 使大烧杯内的压强增大, 当大烧杯内的压强大于外界大气压时, 大烧杯内的水被压入水槽内 ②大烧杯内水面上升, 水槽内水面下降
【点拨】(1) 氢氧化钠和二氧化碳反应:2NaOH+CO2=== Na2CO3+H2O, 导致注射器B中的二氧化碳减少, 压强减小, 故注射器B的活塞慢慢向左移动。(2) 二氧化碳能溶于水, 也能与氢氧化钠反应, 但与氢氧化钠反应导致压强减小的幅度较大, 故图3中的曲线B表示氢氧化钠溶液与二氧化碳的反应; 向二氧化碳中加入80 mL蒸馏水进行对比实验, 可以排除二氧化碳溶于水对实验产生的影响。(3) 氢氧化钠与二氧化碳反应生成碳酸钠和水, 碳酸钠能与酸反应生成二氧化碳, 故加入的试剂是稀盐酸或稀硫酸等。(4) 第一套装置中, 二氧化碳与氢氧化钠溶液反应生成碳酸钠和水, 试管内的二氧化碳被消耗, 装置内的压强减小, 锥形瓶内水的沸点降低, 所以96 ℃以上的水会沸腾; 第二套装置中, 试管内剩余大量二氧化碳, 压强变化不明显, 因此锥形瓶内的水无明显现象。(5) ①小烧杯内为CO2缓冲液时, 黑藻在光照下进行光合作用产生O2, 大烧杯内压强增大, 大于外界大气压, 大烧杯内的水被压入水槽内, 所以大烧杯内水面下降, 水槽内水面上升。②将小烧杯中的CO2缓冲液换成NaOH溶液时, 黑藻不能进行光合作用, 只能进行呼吸作用, 呼吸作用消耗氧气, 释放的CO2被NaOH溶液吸收, 大烧杯内压强减小, 小于外界大气压, 水槽内的水被压入大烧杯内, 所以大烧杯内水面上升, 水槽内水面下降。
17. (1) 解:设理论上消耗盐酸中氯化氢的质量为x。
NaOH + HCl=== NaCl+H2O
40 36. 5
20 g×10% x
= x=1. 825 g
答:理论上消耗盐酸中氯化氢的质量为1. 825 g。
(2) NaOH变质了, 生成的Na2CO3与盐酸反应生成了CO2气体
同课章节目录
