2.2 金属的化学性质 第1课时(课件 17张ppt)
文档属性
| 名称 | 2.2 金属的化学性质 第1课时(课件 17张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-09-21 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
第2节
金属的化学性质
在下列金属单质中用红笔圈出你知道名称的金属,用蓝笔圈出你用过其制品的金属。刚才的礼花中又涉及到了哪些金属?
金属元素的中文名都带金字旁
你知道金属的哪些化学性质吗?
探究1
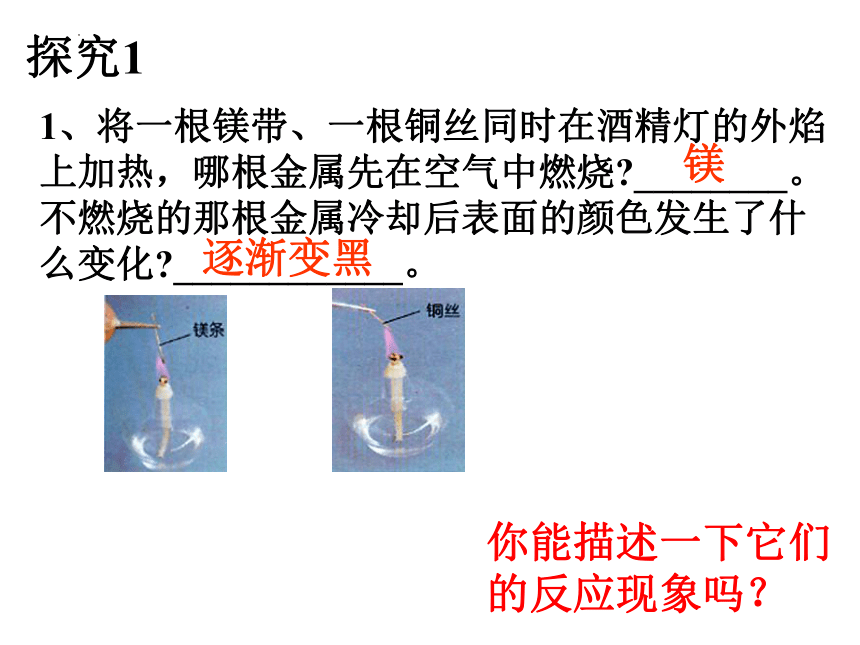
1、将一根镁带、一根铜丝同时在酒精灯的外焰上加热,哪根金属先在空气中燃烧 ________。不燃烧的那根金属冷却后表面的颜色发生了什么变化 ____________。
镁
逐渐变黑
你能描述一下它们的反应现象吗?
镁条在空气中剧烈燃烧,发出耀眼的白光,产生大量的热,生成一种白色的固体。
铜丝在空气中不能燃烧,发出红光,表面有一种黑色的固体生成。
CuO+2HCl==CuCl2+ H2O
黑色固体逐渐消失。
2、铁在潮湿的空气中会被空气中的氧气所氧化而生锈。
1、铝在常温下与氧气发生反应生成一层致密的氧化铝保护膜。
4Al+3O2=2Al2O3
生活常识:铝制品不能用钢刷擦洗,
还不能盛放酸性或碱性物质。
你知道其中的原因吗?
Al2O3+6HCl==2AlCl3+ 3H2O
Al2O3+ 2NaOH==2NaAlO2+ H2O
破坏了表面的保护膜,进而腐蚀铝。
我家新买的铝锅长时间没用虽没生锈但变黑了?
结论:
大多数金属能与氧气发生反应生成氧化物。
1、金属+O2==金属氧化物
金属的化学性质
将铝片放入盛有稀盐酸的试管中,观察并记录现象:
大量的气泡产生
2Al + 6HCl = 2AlCl3 + 3H2↑
是否所有的金属都能被酸腐蚀
不会的,如金、银、铂等很难被腐蚀。
探究2
思考:
二、金属与酸的反应
现象:
金属镁、锌逐渐减少甚至消失,有气泡产生,镁产生气泡速度比锌的快;铜片无变化。
继续探究:
镁条、锌粒、铜片分别
放入稀盐酸中
镁
锌
铜
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
用拇指按住盛有锌粒和稀盐酸的试管口,将燃着的火柴接近试管口,松开拇指。
检验产生的气体
实验:
现象:
有爆鸣声
结论:
产生的气体为氢气
金属和稀硫酸的反应
3、取少量镁条、锌粒、铜片分别放入盛有稀硫酸的3支试管中,观察现象:________。试验产生的气体。
同1
Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
4、跟稀盐酸、稀硫酸不发生反应的金属是____。
铜
(实验室制氢气)
推测:
为什么镁和锌能与酸反应放出氢气,而铜不能?
为什么镁与酸反应放出氢气的速度比锌的快?
与金属的活泼程度(金属活动性)有关
实验室制氢气,选什么金属好,说出你的理由?
结论:
大多数金属能与氧气发生反应生成氧化物。
1、金属+O2==金属氧化物
一些金属能与酸发生反应生成盐和氢气。
2、金属+酸==盐+ H2↑
金属的化学性质
上述反应与前面学过的化合、分解、复分解反应有什么不同?
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
单质
化合物
单质
化合物
由一种单质跟一种化合物起反应生成另一种单质和另一种化合物的反应叫做置换反应
+
=
+
A+BC=B+AC
比较:四种基本反应类型
反应类型 反应物 生成物
化合反应
分解反应
复分解反应
置换反应
两种或两种以上
两种或两种以上
两种化合物
一种单质和一种化合物
一种
一种
两种新化合物
一种新单质和一种新化合物
1.家用铝锅、铁锅为什么不能用来长时间盛放
酸性食品?
2.不法商贩常常用铝制的假银元坑害消费者,小明
在市场上买了一枚银元,请你用化学方法帮他鉴别
这枚银元的真假。
3.如何鉴别真假黄金?你能有几种方法?看谁想的
更多
小结:
今天大家有什么收获?
一、金属的化学性质
1、金属+O2==金属氧化物
2、金属+酸==盐+ H2↑
这些反应的难易程度及剧烈程度与金属的活泼性有关
二、置换反应
第2节
金属的化学性质
在下列金属单质中用红笔圈出你知道名称的金属,用蓝笔圈出你用过其制品的金属。刚才的礼花中又涉及到了哪些金属?
金属元素的中文名都带金字旁
你知道金属的哪些化学性质吗?
探究1
1、将一根镁带、一根铜丝同时在酒精灯的外焰上加热,哪根金属先在空气中燃烧 ________。不燃烧的那根金属冷却后表面的颜色发生了什么变化 ____________。
镁
逐渐变黑
你能描述一下它们的反应现象吗?
镁条在空气中剧烈燃烧,发出耀眼的白光,产生大量的热,生成一种白色的固体。
铜丝在空气中不能燃烧,发出红光,表面有一种黑色的固体生成。
CuO+2HCl==CuCl2+ H2O
黑色固体逐渐消失。
2、铁在潮湿的空气中会被空气中的氧气所氧化而生锈。
1、铝在常温下与氧气发生反应生成一层致密的氧化铝保护膜。
4Al+3O2=2Al2O3
生活常识:铝制品不能用钢刷擦洗,
还不能盛放酸性或碱性物质。
你知道其中的原因吗?
Al2O3+6HCl==2AlCl3+ 3H2O
Al2O3+ 2NaOH==2NaAlO2+ H2O
破坏了表面的保护膜,进而腐蚀铝。
我家新买的铝锅长时间没用虽没生锈但变黑了?
结论:
大多数金属能与氧气发生反应生成氧化物。
1、金属+O2==金属氧化物
金属的化学性质
将铝片放入盛有稀盐酸的试管中,观察并记录现象:
大量的气泡产生
2Al + 6HCl = 2AlCl3 + 3H2↑
是否所有的金属都能被酸腐蚀
不会的,如金、银、铂等很难被腐蚀。
探究2
思考:
二、金属与酸的反应
现象:
金属镁、锌逐渐减少甚至消失,有气泡产生,镁产生气泡速度比锌的快;铜片无变化。
继续探究:
镁条、锌粒、铜片分别
放入稀盐酸中
镁
锌
铜
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
用拇指按住盛有锌粒和稀盐酸的试管口,将燃着的火柴接近试管口,松开拇指。
检验产生的气体
实验:
现象:
有爆鸣声
结论:
产生的气体为氢气
金属和稀硫酸的反应
3、取少量镁条、锌粒、铜片分别放入盛有稀硫酸的3支试管中,观察现象:________。试验产生的气体。
同1
Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
4、跟稀盐酸、稀硫酸不发生反应的金属是____。
铜
(实验室制氢气)
推测:
为什么镁和锌能与酸反应放出氢气,而铜不能?
为什么镁与酸反应放出氢气的速度比锌的快?
与金属的活泼程度(金属活动性)有关
实验室制氢气,选什么金属好,说出你的理由?
结论:
大多数金属能与氧气发生反应生成氧化物。
1、金属+O2==金属氧化物
一些金属能与酸发生反应生成盐和氢气。
2、金属+酸==盐+ H2↑
金属的化学性质
上述反应与前面学过的化合、分解、复分解反应有什么不同?
Mg + 2HCl = MgCl2 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
单质
化合物
单质
化合物
由一种单质跟一种化合物起反应生成另一种单质和另一种化合物的反应叫做置换反应
+
=
+
A+BC=B+AC
比较:四种基本反应类型
反应类型 反应物 生成物
化合反应
分解反应
复分解反应
置换反应
两种或两种以上
两种或两种以上
两种化合物
一种单质和一种化合物
一种
一种
两种新化合物
一种新单质和一种新化合物
1.家用铝锅、铁锅为什么不能用来长时间盛放
酸性食品?
2.不法商贩常常用铝制的假银元坑害消费者,小明
在市场上买了一枚银元,请你用化学方法帮他鉴别
这枚银元的真假。
3.如何鉴别真假黄金?你能有几种方法?看谁想的
更多
小结:
今天大家有什么收获?
一、金属的化学性质
1、金属+O2==金属氧化物
2、金属+酸==盐+ H2↑
这些反应的难易程度及剧烈程度与金属的活泼性有关
二、置换反应
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
