2.2 金属的化学性质 第2课时(课件 12张ppt)
文档属性
| 名称 | 2.2 金属的化学性质 第2课时(课件 12张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-09-21 00:00:00 | ||
图片预览



文档简介
(共12张PPT)
第二节 金属的化学性质
(第二课时)
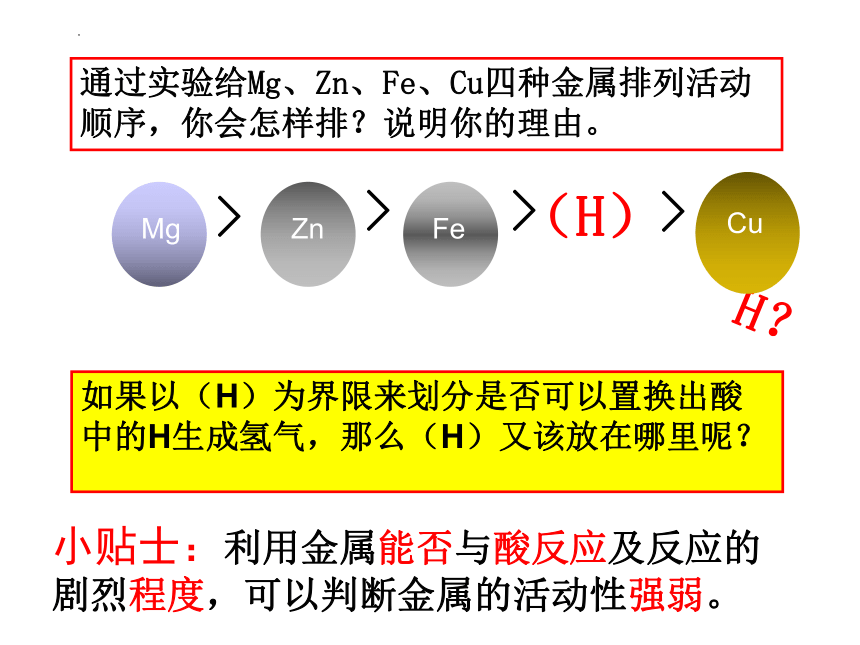
通过实验给Mg、Zn、Fe、Cu四种金属排列活动顺序,你会怎样排?说明你的理由。
Zn
Mg
Fe
>
>
Cu
>
如果以(H)为界限来划分是否可以置换出酸中的H生成氢气,那么(H)又该放在哪里呢?
H?
(H)
>
>
Cu
小贴士:利用金属能否与酸反应及反应的剧烈程度,可以判断金属的活动性强弱。
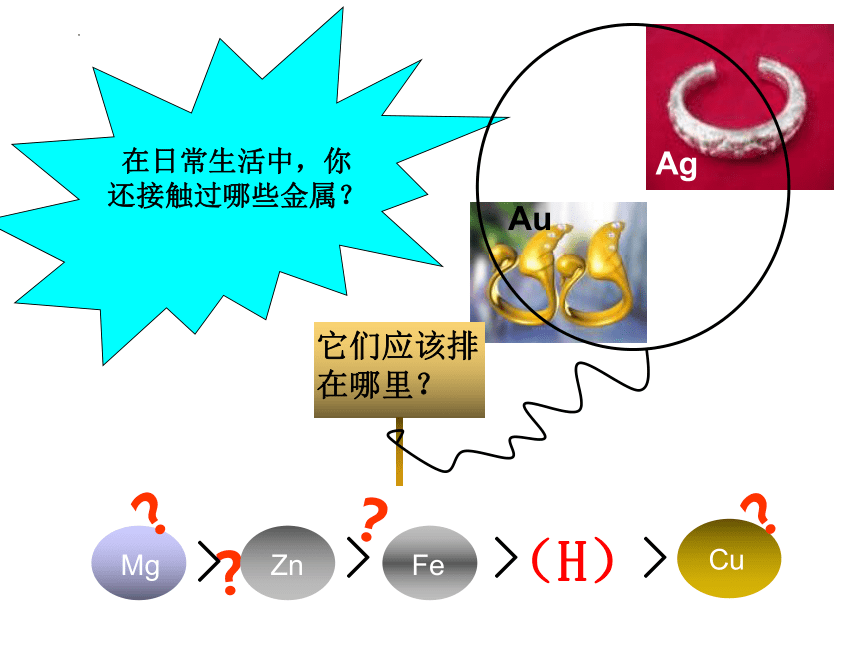
在日常生活中,你还接触过哪些金属?
?
Zn
Mg
>
>
Fe
(H)
>
>
Cu
?
?
?
Ag
Au
它们应该排在哪里?
Ag
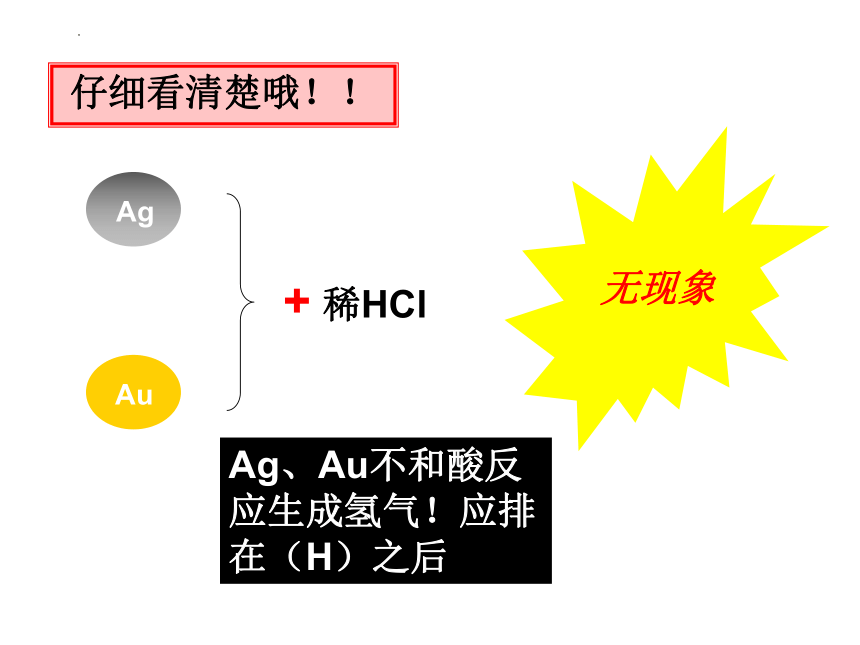
Au
+ 稀HCl
仔细看清楚哦!!
无现象
Ag、Au不和酸反应生成氢气!应排在(H)之后
Ag、Au和Cu都不和酸反应,究竟怎么判断它们的活动性强弱呢??
Fe > Cu
Fe + H2SO4 FeSO4 + H2
Cu + H2SO4
提示:
在盛有硫酸铜溶液的试管里浸入一段洁净的铁钉,过一会儿取出,观察现象:
铁钉表面有一层红色物质生成
Fe+CuSO4=FeSO4+Cu
1
2
3
设计的实验
观察到的现象
得到的结论
如果只利用 Fe、Cu、 CuSO4、AgNO3、Fe(NO3)2、稀H2SO4来检验 Fe、Cu、Ag三种金属的活动性顺序,你会怎样设计。(请填写实验报告中设计的实验一栏)
自己动手吧!!
按照你的设计,逐步进行检验铁、铜、银活动性顺序,看结果是否和你预期的一样。并填写实验报告。
小结:活泼的金属可以把较不活泼的金属从它的盐溶液中置换出来。
盐溶液
浸入硝酸银溶液中的铜棒表面有一层银白色物质生成,而浸入硝酸亚铁溶液中的铜棒却没有发生变化。
Cu+2AgNO3=Cu(NO3)2+2Ag
新发现
Fe+CuSO4=FeSO4+Cu
金属与盐溶液反应为置换反应 铁显+2价
这也是一种判断金属活动性强弱的方法!!
Fe
Cu
Ag
>
>
Zn
Mg
Fe
>
>
(H)
>
>
Cu
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
应用规律:
1.在金属活动性顺序里,位于氢前的金属能置换出盐酸、稀硫酸中的氢。
2.在金属活动性顺序里,位于前面的金属能把后面的金属从它们化合物的溶液里置换出来。
(K、Ca、Na三种金属除外)
口诀:强换弱盐可溶,氢前金属置换氢。
1、已知下列反应:
(1)Zn + FeSO4 == ZnSO4 + Fe
(2)Cu + AgNO3 == Ag +Cu(NO3)2
(3)Fe + CuSO4 == FeSO4 + Cu
你能判断出这三种金属的活动性顺序吗?
练一练
2、如果用最简单的方法,证明锌、银、(H)、铜的活动性顺序,至少需要选用下列物质的________.
(1)Zn (2)Ag (3)Cu
(4)CuSO4 (5)稀硫酸
(6)AgNO3 (7)FeSO4 溶液
辨一辨:
黄金饰品中的假货常常鱼目混珠,社会上有些不法分子时常以黄铜冒充黄金进行诈骗活动。因为黄铜(铜、锌合金)单纯从颜色、外形上看,与黄金极为相似,所以很难区分。
现在你能当一回鉴定师,鉴别真假黄金了吗?
第二节 金属的化学性质
(第二课时)
通过实验给Mg、Zn、Fe、Cu四种金属排列活动顺序,你会怎样排?说明你的理由。
Zn
Mg
Fe
>
>
Cu
>
如果以(H)为界限来划分是否可以置换出酸中的H生成氢气,那么(H)又该放在哪里呢?
H?
(H)
>
>
Cu
小贴士:利用金属能否与酸反应及反应的剧烈程度,可以判断金属的活动性强弱。
在日常生活中,你还接触过哪些金属?
?
Zn
Mg
>
>
Fe
(H)
>
>
Cu
?
?
?
Ag
Au
它们应该排在哪里?
Ag
Au
+ 稀HCl
仔细看清楚哦!!
无现象
Ag、Au不和酸反应生成氢气!应排在(H)之后
Ag、Au和Cu都不和酸反应,究竟怎么判断它们的活动性强弱呢??
Fe > Cu
Fe + H2SO4 FeSO4 + H2
Cu + H2SO4
提示:
在盛有硫酸铜溶液的试管里浸入一段洁净的铁钉,过一会儿取出,观察现象:
铁钉表面有一层红色物质生成
Fe+CuSO4=FeSO4+Cu
1
2
3
设计的实验
观察到的现象
得到的结论
如果只利用 Fe、Cu、 CuSO4、AgNO3、Fe(NO3)2、稀H2SO4来检验 Fe、Cu、Ag三种金属的活动性顺序,你会怎样设计。(请填写实验报告中设计的实验一栏)
自己动手吧!!
按照你的设计,逐步进行检验铁、铜、银活动性顺序,看结果是否和你预期的一样。并填写实验报告。
小结:活泼的金属可以把较不活泼的金属从它的盐溶液中置换出来。
盐溶液
浸入硝酸银溶液中的铜棒表面有一层银白色物质生成,而浸入硝酸亚铁溶液中的铜棒却没有发生变化。
Cu+2AgNO3=Cu(NO3)2+2Ag
新发现
Fe+CuSO4=FeSO4+Cu
金属与盐溶液反应为置换反应 铁显+2价
这也是一种判断金属活动性强弱的方法!!
Fe
Cu
Ag
>
>
Zn
Mg
Fe
>
>
(H)
>
>
Cu
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
应用规律:
1.在金属活动性顺序里,位于氢前的金属能置换出盐酸、稀硫酸中的氢。
2.在金属活动性顺序里,位于前面的金属能把后面的金属从它们化合物的溶液里置换出来。
(K、Ca、Na三种金属除外)
口诀:强换弱盐可溶,氢前金属置换氢。
1、已知下列反应:
(1)Zn + FeSO4 == ZnSO4 + Fe
(2)Cu + AgNO3 == Ag +Cu(NO3)2
(3)Fe + CuSO4 == FeSO4 + Cu
你能判断出这三种金属的活动性顺序吗?
练一练
2、如果用最简单的方法,证明锌、银、(H)、铜的活动性顺序,至少需要选用下列物质的________.
(1)Zn (2)Ag (3)Cu
(4)CuSO4 (5)稀硫酸
(6)AgNO3 (7)FeSO4 溶液
辨一辨:
黄金饰品中的假货常常鱼目混珠,社会上有些不法分子时常以黄铜冒充黄金进行诈骗活动。因为黄铜(铜、锌合金)单纯从颜色、外形上看,与黄金极为相似,所以很难区分。
现在你能当一回鉴定师,鉴别真假黄金了吗?
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
