2024鲁科版新教材高中化学必修第一册同步练习--第1课时 氮气与氮的固定 氮的氧化物(含解析)
文档属性
| 名称 | 2024鲁科版新教材高中化学必修第一册同步练习--第1课时 氮气与氮的固定 氮的氧化物(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 457.7KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-22 00:00:00 | ||
图片预览




文档简介
2024鲁科版新教材高中化学必修第一册
第3节 氮的循环
第1课时 氮气与氮的固定 氮的氧化物
基础过关练
题组一 氮的固定
1.(2022北京人大附中期末)下列化学反应中起固氮作用的是( )
A.由氨气制碳酸氢铵
B.一氧化氮与氧气反应生成二氧化氮
C.氨气经催化氧化生成一氧化氮
D.闪电使氮气和氧气反应生成一氧化氮气体
2.(2021吉林长春期末)下列过程不属于氮的固定的是( )
A.将空气中的N2转化为含氮化合物
B.工业上用氢气与氮气合成氨
C.植物的根从土壤中吸收铵根离子和硝酸盐
D.豆科植物的根瘤菌把空气中的氮气转化为硝酸盐
题组二 氮气的性质
3.(2020上海金山一模)氮气常用作白炽灯灯泡中钨丝的保护气,这是因为( )
A.氮气比空气轻
B.氮气难溶于水
C.氮气是无色无味的气体
D.氮气很不活泼
4.下列关于N2的说法错误的是( )
A.通常情况下N2性质很稳定,所以N2可在电焊时做保护气
B.反应N2+O2 2NO是汽车尾气造成污染的主要原因之一
C.N2的质量约占空气总质量的
D.在反应3Mg+N2 Mg3N2中,N2做氧化剂
5.(2021山东济宁期中)下列关于氮元素及氮气性质的说法中,错误的是( )
A.氮气分子是双原子分子,氮在自然界中既以游离态存在又以化合态存在
B.氮气分子中的化学键很难被破坏,因此氮气的化学性质很稳定
C.反应N2+3Mg Mg3N2不属于氮的固定,工业合成氨的过程是固氮的过程
D.大气、陆地和水体中的氮元素在不停地进行着氮的循环
题组三 氮的氧化物
6.下列关于NO的说法不正确的是( )
A.为无色气体
B.是汽车尾气的有害成分之一
C.能用排空气法收集
D.既有氧化性,又有还原性
7.(2022北京海淀期末)下列关于NO2的说法中,正确的是( )
A.常温常压下为无色气体
B.NO可与O2反应生成NO2
C.密度比空气小
D.能用排水法收集
8.(2021河北辛集中学月考)下列关于NO2的说法正确的是( )
A.NO2能与水反应生成硝酸,但NO2不是酸性氧化物
B.NO2可由N2与O2反应直接制备
C.NO2与溴蒸气的鉴别可用NaOH溶液,溶于NaOH溶液得无色溶液的是NO2,得橙色溶液的为溴蒸气
D.NO2不是大气污染物
9.(2020湖南娄底一中期末)四支容积相同的试管中分别充满NO、SO2、NO2、Cl2中的一种,把它们分别倒立于盛有水的水槽中,充分放置后的现象如下图所示。其中原试管充满NO2的是( )
10.如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管完全被水充满,原来试管中盛装的不可能是( )
A.氮气与二氧化氮的混合气体
B.氧气与二氧化氮的混合气体
C.一氧化氮与二氧化氮的混合气体
D.二氧化氮气体
11.(2020北京平谷期末)为了有效实现NO和NO2的相互转化,设计如下实验。按图组装好实验装置,并检验装置气密性,实验前用排水法收集半瓶NO气体。
(1)打开止水夹,推动针筒活塞,使O2进入烧瓶。关闭止水夹,首先观察到烧瓶中的现象是 ,产生此现象的化学方程式为 。
(2)轻轻摇动烧瓶,观察到烧瓶中的现象为 ,产生此现象的化学方程式为 。
(3)欲使烧瓶中尽可能全充满液体,操作的关键是 。
题组四 自然界中的氮循环
12.(2022山东青岛莱西一中月考)自然界中氮元素部分循环如图所示,下列说法错误的是( )
A.反应①~⑥均属于氧化还原反应
B.反应①②⑤均属于氮的固定
C.反应⑥的离子方程式为+ N2↑+2H2O
D.向水体中大量排放N及N,会造成水质恶化
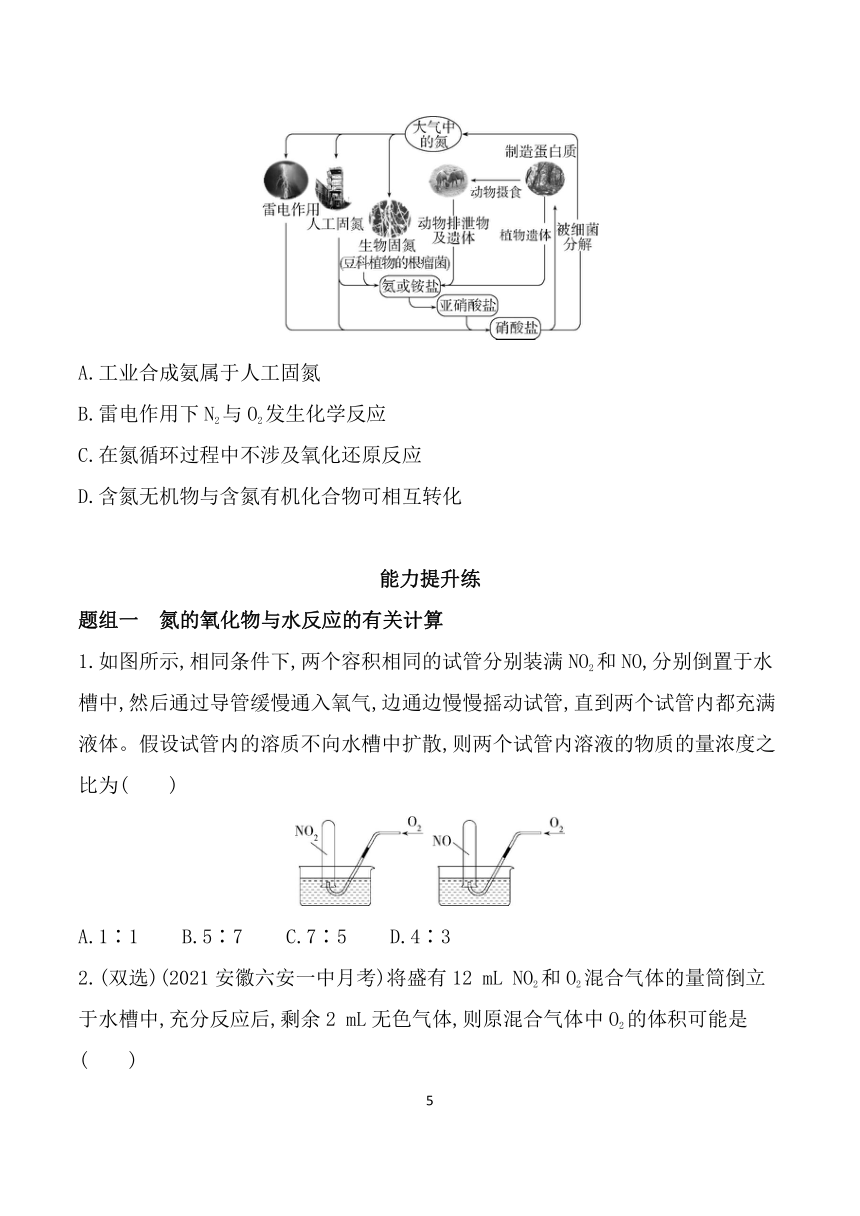
13.(2020北京房山期末)自然界中的氮循环如图所示。下列说法中,不正确的是( )
A.工业合成氨属于人工固氮
B.雷电作用下N2与O2发生化学反应
C.在氮循环过程中不涉及氧化还原反应
D.含氮无机物与含氮有机化合物可相互转化
能力提升练
题组一 氮的氧化物与水反应的有关计算
1.如图所示,相同条件下,两个容积相同的试管分别装满NO2和NO,分别倒置于水槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内都充满液体。假设试管内的溶质不向水槽中扩散,则两个试管内溶液的物质的量浓度之比为( )
A.1∶1 B.5∶7 C.7∶5 D.4∶3
2.(双选)(2021安徽六安一中月考)将盛有12 mL NO2和O2混合气体的量筒倒立于水槽中,充分反应后,剩余2 mL无色气体,则原混合气体中O2的体积可能是( )
A.1.2 mL B.2.4 mL
C.3.6 mL D.4 mL
题组二 氮氧化物的性质探究
3.(2022山东泰安期末)某无色混合气体可能含有NO、NO2、CO2、N2中的几种,将一定量的该气体依次经过如图实验的处理,结果得到酸性溶液,而无气体剩余。则该气体的组成为( )
A.NO、N2 B.NO、CO2
C.NO2、CO2 D.NO、CO2、N2
4.(2020河南驻马店期末)NO2是大气污染物之一,实验室拟将NO2与Cl2混合并用NaOH溶液吸收的方法消除其污染。回答下列问题:
(1)氯气的制备
①仪器M的名称是 。
②欲用MnO2和浓盐酸制备并收集一瓶纯净、干燥的氯气,选择上图中的装置,其连接顺序为 (按气流方向,用导管口处小写字母表示)。
③装置D的作用是 ;装置F的作用是 。
(2)用下图所示装置,探究Cl2和NO2在NaOH溶液中的反应。查阅有关资料可知:HNO2是一种弱酸,且不稳定,易分解生成H2O、NO和NO2。
①装置X和装置Z的作用是 。
②实验时观察到X试剂瓶中有黄绿色气体,Z试剂瓶中有红棕色气体,若通入适当比例的Cl2和NO2,Y中观察不到气体颜色,反应结束后在Y中加入稀硫酸无现象,则Y中发生反应的化学方程式是 。
③反应结束后,取适量Y中溶液置于试管中,加入稀硫酸,若有红棕色气体产生,解释产生该现象的原因: 。
答案全解全析
基础过关练
1.D 2.C 3.D 4.C 5.C 6.C 7.B 8.A
9.B 10.A 12.B 13.C
1.D 氮的固定是指将空气中游离态的氮(即N2)转化为含氮化合物的过程,故D符合题意。
2.C 植物的根从土壤中吸收铵根离子和硝酸盐,不是将游离态氮转化为化合态氮,不属于氮的固定,故C符合题意。
3.D 氮气常用作保护气,是由于氮气的化学性质不活泼,故选D。
4.C 通常情况下N2性质很稳定,所以N2可在电焊时做保护气,故A正确;N2+O2 2NO是汽车尾气造成污染的主要原因之一,故B正确;N2在空气中约占空气总体积的,故C错误;在反应3Mg+N2 Mg3N2中,N元素化合价降低,N2做氧化剂,故D正确。
5.C 氮的固定是游离态的氮变为化合态的氮,反应N2+3Mg Mg3N2属于氮的固定,C错误。
6.C NO的密度与空气相近,且能与空气中的氧气反应,不能用排空气法收集。
7.B 常温常压下NO2为红棕色气体,密度比空气大,易溶于水,不能用排水法收集,排除A、C、D;NO可与O2反应生成NO2,故B正确。
8.A NO2与H2O反应除生成HNO3外还生成NO,所以NO2不是酸性氧化物,故A正确;N2和O2在放电或高温条件下反应生成NO,不能直接生成NO2,故B错误;NO2、溴蒸气与NaOH溶液作用均得无色溶液,所以用NaOH溶液无法鉴别NO2与溴蒸气,故C错误;NO2会造成光化学烟雾或酸雨,NO2是大气污染物,故D错误。
9.B 根据3NO2+H2O 2HNO3+NO和NO难溶于水可知,将充满NO2的试管倒立于盛有水的水槽中,水上升到试管容积的三分之二处,符合条件的是B。
10.A 二氧化氮与水、氧气可发生反应:4NO2+O2+2H2O 4HNO3,一氧化氮与水、氧气可发生反应:4NO+3O2+2H2O 4HNO3,因此B、C、D项均不符合题意;氮气不溶于水,在溶液中不能与氧气反应,水不能完全充满试管,A项符合题意。
11.答案 (1)烧瓶上方气体变为红棕色 2NO+O2 2NO2
(2)红棕色气体变为无色,烧瓶中进入少量水 3NO2+H2O 2HNO3+NO
(3)慢慢通入氧气,并不断摇动烧瓶
解析 (1)无色的NO能与O2反应产生红棕色的NO2,故观察到烧瓶上方气体由无色变为红棕色。
(2)轻轻摇动烧瓶,使得NO2与水发生反应3NO2+H2O 2HNO3+NO,所以烧瓶中红棕色气体又变为无色,烧瓶中液面上升。
(3)欲使烧瓶中尽可能全充满液体,应通入氧气使NO与氧气反应转化为NO2,NO2再与水反应,最终全部转化为硝酸,操作的关键是慢慢通入氧气,并不断摇动烧瓶。
12.B 反应①~⑥中氮元素的化合价均发生了变化,均属于氧化还原反应,故A正确;反应①②不是游离态的氮转化为化合态的氮,不属于氮的固定,故B错误;根据图中的转化关系和得失电子守恒可知,反应⑥的离子方程式为+ N2↑+2H2O,故C正确;向水体中大量排放N及N,会引起水体富营养化,造成水质恶化,故D正确。
13.C 工业合成氨属于人工固氮,故A正确;在雷电作用下N2与O2发生化学反应生成NO,故B正确;在氮循环过程中人工固氮、氨或铵盐转化为亚硝酸盐、亚硝酸盐转化为硝酸盐、在雷电作用下氮的转化等都是氧化还原反应,故C不正确;硝酸盐可转化为蛋白质,动、植物遗体可转化为氨或铵盐,所以含氮无机物与含氮有机化合物可相互转化,故D正确。
能力提升练
1.A 2.AD 3.B
1.A 两试管中发生反应的化学方程式分别为4NO2+O2+2H2O 4HNO3、4NO+3O2+2H2O 4HNO3,O2足量,则生成HNO3的物质的量取决于NO2与NO的体积,由于NO2与NO体积相同,生成HNO3的物质的量相等,即两试管中HNO3的浓度相等,A项正确。
2.AD 剩余2 mL无色气体可能为氧气,也可能为一氧化氮。若剩余的2 mL无色气体为氧气,设参加反应的氧气的体积为x,则有:
4NO2+O2+2H2O 4HNO3
4x x
4x+x=12 mL-2 mL=10 mL,解得x=2 mL,所以氧气的体积为2 mL+2 mL=4 mL;
若剩余的2 mL无色气体为NO,根据反应3NO2+H2O 2HNO3+NO可知,参与此反应的NO2为6 mL,设混合气体中氧气的体积为y,则有:
4NO2+O2+2H2O 4HNO3
4y y
4y+y=12 mL-6 mL=6 mL,解得y=1.2 mL,故选AD。
3.B
无色混合气体通过盛有足量Na2O2的干燥管后,得到NO2和O2的混合气体,根据2Na2O2+2CO2 2Na2CO3+O2、2NO+O2 2NO2可知,原无色混合气体中含有NO、CO2,故选B。
4.答案 (1)①分液漏斗 ②b→e→f→g→h→c→d→i ③吸收Cl2中的HCl 除去多余的氯气,防止污染空气
(2)①观察气泡产生的快慢,便于控制Cl2和NO2的进入量的比例
②Cl2+2NO2+4NaOH 2NaNO3+2NaCl+2H2O ③NO2的量过多,NO2与NaOH溶液反应生成了NaNO2,加入稀硫酸后N发生歧化反应生成NO、H2O和NO2
解析 (1)①仪器M为分液漏斗。②实验室用二氧化锰和浓盐酸在加热条件下反应制取氯气,制得的氯气中含有氯化氢和水蒸气,依次通过盛有饱和食盐水、浓硫酸的洗气瓶除去杂质,氯气密度大于空气密度,用向上排空气法收集,尾气用氢氧化钠溶液吸收,所以正确的连接顺序为b→e→f→g→h→c→d→i。③浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢极易溶于水,氯气在饱和食盐水中溶解度很小,装置D中饱和食盐水可吸收氯气中的氯化氢;氯气有毒,多余的氯气需用氢氧化钠溶液进行吸收。(2)①氯气在饱和食盐水中溶解度很小,二氧化氮在四氯化碳中不溶,所以分别通入两种气体后,会看到产生气泡,通过观察产生气泡的快慢控制Cl2和NO2的进入量的比例。②通入适当比例的氯气和二氧化氮,Y中观察不到气体颜色,说明氯气和二氧化氮完全反应,反应结束后在Y中加入稀硫酸无现象,说明没有生成N,氯气、二氧化氮、NaOH发生氧化还原反应生成硝酸钠、氯化钠和水,化学方程式为Cl2+2NO2+4NaOH 2NaNO3+2NaCl+2H2O。③通入的二氧化氮量过多,则过量的二氧化氮与NaOH溶液反应生成了NaNO2,加入稀硫酸后N在酸性环境下发生歧化反应生成一氧化氮、水和二氧化氮,二氧化氮为红棕色气体,所以会看到出现红棕色气体。
11
第3节 氮的循环
第1课时 氮气与氮的固定 氮的氧化物
基础过关练
题组一 氮的固定
1.(2022北京人大附中期末)下列化学反应中起固氮作用的是( )
A.由氨气制碳酸氢铵
B.一氧化氮与氧气反应生成二氧化氮
C.氨气经催化氧化生成一氧化氮
D.闪电使氮气和氧气反应生成一氧化氮气体
2.(2021吉林长春期末)下列过程不属于氮的固定的是( )
A.将空气中的N2转化为含氮化合物
B.工业上用氢气与氮气合成氨
C.植物的根从土壤中吸收铵根离子和硝酸盐
D.豆科植物的根瘤菌把空气中的氮气转化为硝酸盐
题组二 氮气的性质
3.(2020上海金山一模)氮气常用作白炽灯灯泡中钨丝的保护气,这是因为( )
A.氮气比空气轻
B.氮气难溶于水
C.氮气是无色无味的气体
D.氮气很不活泼
4.下列关于N2的说法错误的是( )
A.通常情况下N2性质很稳定,所以N2可在电焊时做保护气
B.反应N2+O2 2NO是汽车尾气造成污染的主要原因之一
C.N2的质量约占空气总质量的
D.在反应3Mg+N2 Mg3N2中,N2做氧化剂
5.(2021山东济宁期中)下列关于氮元素及氮气性质的说法中,错误的是( )
A.氮气分子是双原子分子,氮在自然界中既以游离态存在又以化合态存在
B.氮气分子中的化学键很难被破坏,因此氮气的化学性质很稳定
C.反应N2+3Mg Mg3N2不属于氮的固定,工业合成氨的过程是固氮的过程
D.大气、陆地和水体中的氮元素在不停地进行着氮的循环
题组三 氮的氧化物
6.下列关于NO的说法不正确的是( )
A.为无色气体
B.是汽车尾气的有害成分之一
C.能用排空气法收集
D.既有氧化性,又有还原性
7.(2022北京海淀期末)下列关于NO2的说法中,正确的是( )
A.常温常压下为无色气体
B.NO可与O2反应生成NO2
C.密度比空气小
D.能用排水法收集
8.(2021河北辛集中学月考)下列关于NO2的说法正确的是( )
A.NO2能与水反应生成硝酸,但NO2不是酸性氧化物
B.NO2可由N2与O2反应直接制备
C.NO2与溴蒸气的鉴别可用NaOH溶液,溶于NaOH溶液得无色溶液的是NO2,得橙色溶液的为溴蒸气
D.NO2不是大气污染物
9.(2020湖南娄底一中期末)四支容积相同的试管中分别充满NO、SO2、NO2、Cl2中的一种,把它们分别倒立于盛有水的水槽中,充分放置后的现象如下图所示。其中原试管充满NO2的是( )
10.如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管完全被水充满,原来试管中盛装的不可能是( )
A.氮气与二氧化氮的混合气体
B.氧气与二氧化氮的混合气体
C.一氧化氮与二氧化氮的混合气体
D.二氧化氮气体
11.(2020北京平谷期末)为了有效实现NO和NO2的相互转化,设计如下实验。按图组装好实验装置,并检验装置气密性,实验前用排水法收集半瓶NO气体。
(1)打开止水夹,推动针筒活塞,使O2进入烧瓶。关闭止水夹,首先观察到烧瓶中的现象是 ,产生此现象的化学方程式为 。
(2)轻轻摇动烧瓶,观察到烧瓶中的现象为 ,产生此现象的化学方程式为 。
(3)欲使烧瓶中尽可能全充满液体,操作的关键是 。
题组四 自然界中的氮循环
12.(2022山东青岛莱西一中月考)自然界中氮元素部分循环如图所示,下列说法错误的是( )
A.反应①~⑥均属于氧化还原反应
B.反应①②⑤均属于氮的固定
C.反应⑥的离子方程式为+ N2↑+2H2O
D.向水体中大量排放N及N,会造成水质恶化
13.(2020北京房山期末)自然界中的氮循环如图所示。下列说法中,不正确的是( )
A.工业合成氨属于人工固氮
B.雷电作用下N2与O2发生化学反应
C.在氮循环过程中不涉及氧化还原反应
D.含氮无机物与含氮有机化合物可相互转化
能力提升练
题组一 氮的氧化物与水反应的有关计算
1.如图所示,相同条件下,两个容积相同的试管分别装满NO2和NO,分别倒置于水槽中,然后通过导管缓慢通入氧气,边通边慢慢摇动试管,直到两个试管内都充满液体。假设试管内的溶质不向水槽中扩散,则两个试管内溶液的物质的量浓度之比为( )
A.1∶1 B.5∶7 C.7∶5 D.4∶3
2.(双选)(2021安徽六安一中月考)将盛有12 mL NO2和O2混合气体的量筒倒立于水槽中,充分反应后,剩余2 mL无色气体,则原混合气体中O2的体积可能是( )
A.1.2 mL B.2.4 mL
C.3.6 mL D.4 mL
题组二 氮氧化物的性质探究
3.(2022山东泰安期末)某无色混合气体可能含有NO、NO2、CO2、N2中的几种,将一定量的该气体依次经过如图实验的处理,结果得到酸性溶液,而无气体剩余。则该气体的组成为( )
A.NO、N2 B.NO、CO2
C.NO2、CO2 D.NO、CO2、N2
4.(2020河南驻马店期末)NO2是大气污染物之一,实验室拟将NO2与Cl2混合并用NaOH溶液吸收的方法消除其污染。回答下列问题:
(1)氯气的制备
①仪器M的名称是 。
②欲用MnO2和浓盐酸制备并收集一瓶纯净、干燥的氯气,选择上图中的装置,其连接顺序为 (按气流方向,用导管口处小写字母表示)。
③装置D的作用是 ;装置F的作用是 。
(2)用下图所示装置,探究Cl2和NO2在NaOH溶液中的反应。查阅有关资料可知:HNO2是一种弱酸,且不稳定,易分解生成H2O、NO和NO2。
①装置X和装置Z的作用是 。
②实验时观察到X试剂瓶中有黄绿色气体,Z试剂瓶中有红棕色气体,若通入适当比例的Cl2和NO2,Y中观察不到气体颜色,反应结束后在Y中加入稀硫酸无现象,则Y中发生反应的化学方程式是 。
③反应结束后,取适量Y中溶液置于试管中,加入稀硫酸,若有红棕色气体产生,解释产生该现象的原因: 。
答案全解全析
基础过关练
1.D 2.C 3.D 4.C 5.C 6.C 7.B 8.A
9.B 10.A 12.B 13.C
1.D 氮的固定是指将空气中游离态的氮(即N2)转化为含氮化合物的过程,故D符合题意。
2.C 植物的根从土壤中吸收铵根离子和硝酸盐,不是将游离态氮转化为化合态氮,不属于氮的固定,故C符合题意。
3.D 氮气常用作保护气,是由于氮气的化学性质不活泼,故选D。
4.C 通常情况下N2性质很稳定,所以N2可在电焊时做保护气,故A正确;N2+O2 2NO是汽车尾气造成污染的主要原因之一,故B正确;N2在空气中约占空气总体积的,故C错误;在反应3Mg+N2 Mg3N2中,N元素化合价降低,N2做氧化剂,故D正确。
5.C 氮的固定是游离态的氮变为化合态的氮,反应N2+3Mg Mg3N2属于氮的固定,C错误。
6.C NO的密度与空气相近,且能与空气中的氧气反应,不能用排空气法收集。
7.B 常温常压下NO2为红棕色气体,密度比空气大,易溶于水,不能用排水法收集,排除A、C、D;NO可与O2反应生成NO2,故B正确。
8.A NO2与H2O反应除生成HNO3外还生成NO,所以NO2不是酸性氧化物,故A正确;N2和O2在放电或高温条件下反应生成NO,不能直接生成NO2,故B错误;NO2、溴蒸气与NaOH溶液作用均得无色溶液,所以用NaOH溶液无法鉴别NO2与溴蒸气,故C错误;NO2会造成光化学烟雾或酸雨,NO2是大气污染物,故D错误。
9.B 根据3NO2+H2O 2HNO3+NO和NO难溶于水可知,将充满NO2的试管倒立于盛有水的水槽中,水上升到试管容积的三分之二处,符合条件的是B。
10.A 二氧化氮与水、氧气可发生反应:4NO2+O2+2H2O 4HNO3,一氧化氮与水、氧气可发生反应:4NO+3O2+2H2O 4HNO3,因此B、C、D项均不符合题意;氮气不溶于水,在溶液中不能与氧气反应,水不能完全充满试管,A项符合题意。
11.答案 (1)烧瓶上方气体变为红棕色 2NO+O2 2NO2
(2)红棕色气体变为无色,烧瓶中进入少量水 3NO2+H2O 2HNO3+NO
(3)慢慢通入氧气,并不断摇动烧瓶
解析 (1)无色的NO能与O2反应产生红棕色的NO2,故观察到烧瓶上方气体由无色变为红棕色。
(2)轻轻摇动烧瓶,使得NO2与水发生反应3NO2+H2O 2HNO3+NO,所以烧瓶中红棕色气体又变为无色,烧瓶中液面上升。
(3)欲使烧瓶中尽可能全充满液体,应通入氧气使NO与氧气反应转化为NO2,NO2再与水反应,最终全部转化为硝酸,操作的关键是慢慢通入氧气,并不断摇动烧瓶。
12.B 反应①~⑥中氮元素的化合价均发生了变化,均属于氧化还原反应,故A正确;反应①②不是游离态的氮转化为化合态的氮,不属于氮的固定,故B错误;根据图中的转化关系和得失电子守恒可知,反应⑥的离子方程式为+ N2↑+2H2O,故C正确;向水体中大量排放N及N,会引起水体富营养化,造成水质恶化,故D正确。
13.C 工业合成氨属于人工固氮,故A正确;在雷电作用下N2与O2发生化学反应生成NO,故B正确;在氮循环过程中人工固氮、氨或铵盐转化为亚硝酸盐、亚硝酸盐转化为硝酸盐、在雷电作用下氮的转化等都是氧化还原反应,故C不正确;硝酸盐可转化为蛋白质,动、植物遗体可转化为氨或铵盐,所以含氮无机物与含氮有机化合物可相互转化,故D正确。
能力提升练
1.A 2.AD 3.B
1.A 两试管中发生反应的化学方程式分别为4NO2+O2+2H2O 4HNO3、4NO+3O2+2H2O 4HNO3,O2足量,则生成HNO3的物质的量取决于NO2与NO的体积,由于NO2与NO体积相同,生成HNO3的物质的量相等,即两试管中HNO3的浓度相等,A项正确。
2.AD 剩余2 mL无色气体可能为氧气,也可能为一氧化氮。若剩余的2 mL无色气体为氧气,设参加反应的氧气的体积为x,则有:
4NO2+O2+2H2O 4HNO3
4x x
4x+x=12 mL-2 mL=10 mL,解得x=2 mL,所以氧气的体积为2 mL+2 mL=4 mL;
若剩余的2 mL无色气体为NO,根据反应3NO2+H2O 2HNO3+NO可知,参与此反应的NO2为6 mL,设混合气体中氧气的体积为y,则有:
4NO2+O2+2H2O 4HNO3
4y y
4y+y=12 mL-6 mL=6 mL,解得y=1.2 mL,故选AD。
3.B
无色混合气体通过盛有足量Na2O2的干燥管后,得到NO2和O2的混合气体,根据2Na2O2+2CO2 2Na2CO3+O2、2NO+O2 2NO2可知,原无色混合气体中含有NO、CO2,故选B。
4.答案 (1)①分液漏斗 ②b→e→f→g→h→c→d→i ③吸收Cl2中的HCl 除去多余的氯气,防止污染空气
(2)①观察气泡产生的快慢,便于控制Cl2和NO2的进入量的比例
②Cl2+2NO2+4NaOH 2NaNO3+2NaCl+2H2O ③NO2的量过多,NO2与NaOH溶液反应生成了NaNO2,加入稀硫酸后N发生歧化反应生成NO、H2O和NO2
解析 (1)①仪器M为分液漏斗。②实验室用二氧化锰和浓盐酸在加热条件下反应制取氯气,制得的氯气中含有氯化氢和水蒸气,依次通过盛有饱和食盐水、浓硫酸的洗气瓶除去杂质,氯气密度大于空气密度,用向上排空气法收集,尾气用氢氧化钠溶液吸收,所以正确的连接顺序为b→e→f→g→h→c→d→i。③浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢极易溶于水,氯气在饱和食盐水中溶解度很小,装置D中饱和食盐水可吸收氯气中的氯化氢;氯气有毒,多余的氯气需用氢氧化钠溶液进行吸收。(2)①氯气在饱和食盐水中溶解度很小,二氧化氮在四氯化碳中不溶,所以分别通入两种气体后,会看到产生气泡,通过观察产生气泡的快慢控制Cl2和NO2的进入量的比例。②通入适当比例的氯气和二氧化氮,Y中观察不到气体颜色,说明氯气和二氧化氮完全反应,反应结束后在Y中加入稀硫酸无现象,说明没有生成N,氯气、二氧化氮、NaOH发生氧化还原反应生成硝酸钠、氯化钠和水,化学方程式为Cl2+2NO2+4NaOH 2NaNO3+2NaCl+2H2O。③通入的二氧化氮量过多,则过量的二氧化氮与NaOH溶液反应生成了NaNO2,加入稀硫酸后N在酸性环境下发生歧化反应生成一氧化氮、水和二氧化氮,二氧化氮为红棕色气体,所以会看到出现红棕色气体。
11
