2024鲁科版新教材高中化学必修第一册同步练习--第1课时 电解质的电离(含解析)
文档属性
| 名称 | 2024鲁科版新教材高中化学必修第一册同步练习--第1课时 电解质的电离(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 171.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-22 00:00:00 | ||
图片预览



文档简介
2024鲁科版新教材高中化学必修第一册
第2节 电解质的电离 离子反应
第1课时 电解质的电离
基础过关练
题组一 电解质的判断
1.下列物质都能导电,其中属于电解质的是( )
A.熔融的NaOH B.铁丝
C.稀硫酸 D.NaCl溶液
2.(2020江苏无锡、江阴四校期中)目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质。下列物质可用作该饮料中的电解质的是( )
A.Fe B.葡萄糖
C.MgSO4 D.CO2
题组二 电解质的电离
3.(2022湖北孝感期中)下列物质中,含有自由移动的Cl-的是( )
A.KClO3溶液 B.CaCl2固体
C.KCl溶液 D.液态HCl
4.(2022广东湛江期中)下列关于电解质的叙述正确的是( )
A.NaCl溶液在电流作用下电离出Na+和Cl-
B.凡是溶于水后能电离出H+的化合物就叫酸
C.HCl溶液能导电,而液态的HCl不导电
D.难溶物一定不属于电解质
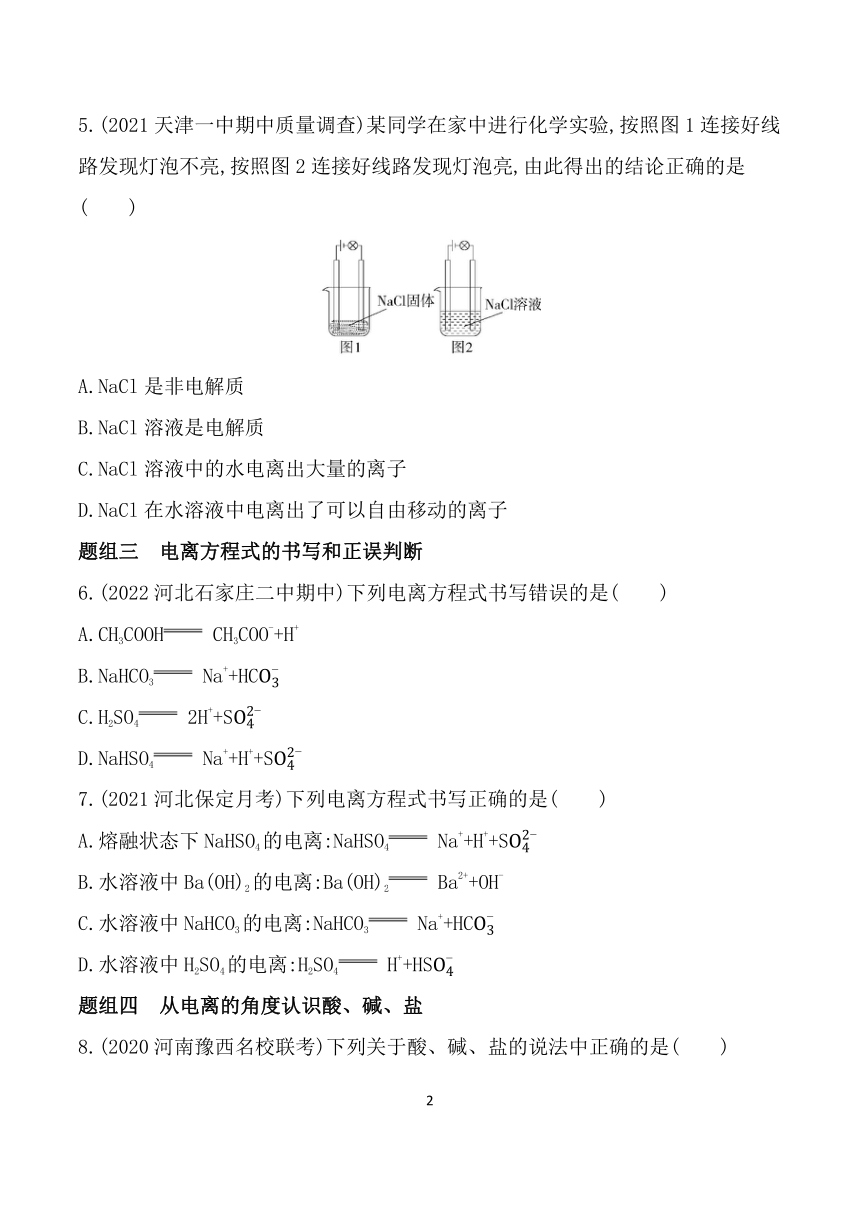
5.(2021天津一中期中质量调查)某同学在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl溶液中的水电离出大量的离子
D.NaCl在水溶液中电离出了可以自由移动的离子
题组三 电离方程式的书写和正误判断
6.(2022河北石家庄二中期中)下列电离方程式书写错误的是( )
A.CH3COOH CH3COO-+H+
B.NaHCO3 Na++HC
C.H2SO4 2H++S
D.NaHSO4 Na++H++S
7.(2021河北保定月考)下列电离方程式书写正确的是( )
A.熔融状态下NaHSO4的电离:NaHSO4 Na++H++S
B.水溶液中Ba(OH)2的电离:Ba(OH)2 Ba2++OH-
C.水溶液中NaHCO3的电离:NaHCO3 Na++HC
D.水溶液中H2SO4的电离:H2SO4 H++HS
题组四 从电离的角度认识酸、碱、盐
8.(2020河南豫西名校联考)下列关于酸、碱、盐的说法中正确的是( )
A.电离出的阳离子有H+的化合物叫酸,电离出OH-的化合物叫碱
B.氯化钠溶液在电流的作用下电离出Na+和Cl-
C.化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐
D.NaHSO4可以电离出H+,因此NaHSO4属于酸
能力提升练
题组一 电解质及其电离的分析与探究
1.(2022广东深圳实验学校月考)下列叙述中错误的是( )
A.氯化钠固体不导电的原因是氯化钠固体中不含阴、阳离子
B.熔融态能导电的不一定是电解质
C.硫酸不能导电而其水溶液能导电的原因是硫酸溶于水后在水分子的作用下产生自由移动的氢离子和硫酸根离子
D.硫酸钡的水溶液几乎不导电,但硫酸钡是强电解质
2.(2022广东佛山南海月考)在水溶液或熔融状态下能导电的化合物为电解质,如酸、碱、盐等。将固态氯化钠(b)分别加水(a)和加热熔融(c),并置于电场中。有关叙述正确的是( )
A.NaCl固体为纯净物而熔融NaCl为混合物
B.固态NaCl中存在NaCl分子
C.固态NaCl不能导电的原因是带电离子不能自由移动
D.在水溶液中,H2O包围着钠离子,且氢原子朝向Na+
题组二 探究电解质溶液的导电性
3.(2020湖南常德部分重点中学期中)某学生利用如图装置对电解质溶液的导电性进行实验探究。下列说法正确的是( )
A.闭合开关K,电流计指针发生偏转,证明HCl溶液是电解质
B.闭合开关K,向烧杯中加入NaCl固体,由于HCl与NaCl不反应,故电流计示数不发生变化
C.闭合开关K,向溶液中加入CaCO3固体,电流计示数变化不大
D.选取相同浓度的稀硫酸替换0.1 mol·L-1的HCl溶液,闭合开关K,电流计示数相同
4.(2021天津大港一中月考)导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质A可以是 (填序号)。
①干燥的氯化钠晶体;②干燥的氢氧化钠晶体;③蔗糖晶体;④酒精;⑤氯化钠溶液;⑥氢氧化钠溶液;⑦稀盐酸;⑧硫酸铜溶液。
(2)在电解质溶液的导电性实验装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液至过量时,灯泡由亮变暗,至熄灭后又逐渐变亮的是 (填字母)。
A.向盐酸中逐滴加入NaCl溶液
B.向稀硫酸中逐滴加入氢氧化钠溶液
C.向澄清石灰水中逐滴加入稀盐酸
D.向稀硫酸中逐滴加入氢氧化钡溶液
答案全解全析
基础过关练
1.A 2.C 3.C 4.C 5.D 6.A 7.C 8.C
1.A 电解质是指在水溶液里或熔融状态下能够导电的化合物,单质和混合物都不是电解质,故选A。
2.C Fe为单质,不属于电解质,故A错误;葡萄糖是化合物,但其在水溶液中和熔融状态下都不能导电,不属于电解质,故B错误;MgSO4为电解质,故C正确;二氧化碳不属于电解质,故D错误。
3.C A项,KClO3在水溶液中电离出K+、Cl,没有Cl-,不符合题意;B项,CaCl2固体中存在Ca2+和Cl-,但不能自由移动,不符合题意;C项,KCl在水溶液中电离出能自由移动的K+、Cl-,符合题意;D项,液态HCl中只存在氯化氢分子,不存在自由移动的Cl-,不符合题意。
4.C NaCl在水分子作用下,电离出Na+和Cl-,故A错误;溶于水后能电离出H+的化合物可能是酸,也可能是酸式盐,如NaHSO4,故B错误;HCl溶液中存在自由移动的H+和Cl-,能导电,而液态的HCl中只存在HCl分子,不导电,故C正确;难溶物如BaSO4溶于水的部分能电离,属于电解质,故D错误。
5.D NaCl是电解质,NaCl溶液属于混合物,不是电解质,故A、B错误;水为极弱的电解质,不能电离出大量的离子,故C错误;NaCl溶于水时,在水分子的作用下电离出了可以自由移动的离子,故D正确。
6.A 醋酸是弱酸,在水溶液中部分电离,其电离方程式为CH3COOH CH3COO-+H+,故A错误。
7.C 熔融状态下NaHSO4的电离方程式为NaHSO4 Na++HS,A错误;水溶液中Ba(OH)2的电离方程式为Ba(OH)2 Ba2++2OH-,B错误;水溶液中NaHCO3的电离方程式为NaHCO3 Na++HC,C正确;水溶液中H2SO4的电离方程式为H2SO4 2H++S,D错误。
8.C 电离出的阳离子全部是H+的化合物叫酸,电离出的阴离子全部是OH-的化合物叫碱,A项错误;氯化钠的电离不需要通电,B项错误;化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐,C项正确;NaHSO4可以电离出H+,但电离出的阳离子不全是H+,还有Na+,则NaHSO4不是酸,D项错误。
能力提升练
1.A 2.C 3.C
1.A 氯化钠固体中含有钠离子和氯离子,故A错误;熔融态的金属单质能导电,但金属单质不属于电解质,故B正确;硫酸是由分子构成的,纯净的硫酸不能导电,硫酸溶于水后在水分子的作用下产生自由移动的氢离子和硫酸根离子,其水溶液能导电,故C正确;硫酸钡的水溶液几乎不导电,但其溶解的部分能完全电离,因此硫酸钡是强电解质,故D正确。
2.C NaCl固体和熔融NaCl都只含一种物质,都是纯净物,故A错误;氯化钠是由钠离子和氯离子构成的,不存在分子,故B错误;固态NaCl中的阴离子、阳离子不能自由移动,所以不能导电,故C正确;钠离子带正电,水分子中的H带正电,根据电性关系可知,水分子中的氧原子朝向钠离子,故D错误。
3.C 开关K闭合后,电流计指针发生偏转,说明溶液中存在自由移动的离子,HCl发生了电离,HCl是电解质,但HCl溶液为混合物,不是电解质,A错误;向HCl溶液中加入NaCl固体,溶液中自由移动的离子浓度增大,故导电能力增强,电流计示数增大,B错误;向HCl溶液中加入CaCO3固体,发生反应2HCl+CaCO3 CaCl2+CO2↑+H2O,溶液中自由移动的离子浓度减小,但离子所带电荷数增大,故导电性变化不大,电流计示数变化不大,C正确;HCl溶液和稀硫酸浓度相同时溶液中离子浓度不同,离子所带电荷数也不同,故导电能力不同,电流计示数不同,D错误。
4.答案 (1)⑤⑥⑦⑧ (2)D
解析 (1)若灯泡亮,广口瓶内的物质A中含有能自由移动的离子。氯化钠晶体、氢氧化钠晶体虽由离子构成,但离子不能自由移动,所以不导电;蔗糖晶体和酒精均为非电解质,不能导电;氯化钠溶液、氢氧化钠溶液、稀盐酸、硫酸铜溶液中均含有大量自由移动的离子,可以导电;综上所述,物质A可以是⑤⑥⑦⑧。
(2)溶液能否导电,取决于溶液中是否有自由移动的离子;溶液导电性强弱与溶液中自由移动离子的浓度大小及离子所带电荷数多少有关。向盐酸中逐滴加入NaCl溶液,HCl和NaCl不发生反应,混合后仍为强电解质溶液,溶液中存在大量自由移动的离子,可导电,灯泡不会熄灭,故A不符合题意;向稀硫酸中逐滴加入氢氧化钠溶液,H2SO4与NaOH反应生成Na2SO4,仍为强电解质溶液,溶液中存在大量自由移动的离子,可导电,灯泡不会熄灭,故B不符合题意;向澄清石灰水中滴加稀盐酸,Ca(OH)2与HCl反应生成了可溶性的CaCl2,灯泡不会熄灭,故C不符合题意;向稀硫酸中逐滴加入Ba(OH)2溶液,发生反应H2SO4+Ba(OH)2 BaSO4↓+2H2O,溶液中离子浓度减小,恰好完全反应时,灯泡熄灭,继续滴加Ba(OH)2溶液,溶液中Ba2+、OH-数目增多,灯泡逐渐变亮,故D符合题意。
8
第2节 电解质的电离 离子反应
第1课时 电解质的电离
基础过关练
题组一 电解质的判断
1.下列物质都能导电,其中属于电解质的是( )
A.熔融的NaOH B.铁丝
C.稀硫酸 D.NaCl溶液
2.(2020江苏无锡、江阴四校期中)目前市场上有一种专门为婴幼儿设计的电解质饮料,适合在婴幼儿感冒、发烧时快速补充体内流失的电解质。下列物质可用作该饮料中的电解质的是( )
A.Fe B.葡萄糖
C.MgSO4 D.CO2
题组二 电解质的电离
3.(2022湖北孝感期中)下列物质中,含有自由移动的Cl-的是( )
A.KClO3溶液 B.CaCl2固体
C.KCl溶液 D.液态HCl
4.(2022广东湛江期中)下列关于电解质的叙述正确的是( )
A.NaCl溶液在电流作用下电离出Na+和Cl-
B.凡是溶于水后能电离出H+的化合物就叫酸
C.HCl溶液能导电,而液态的HCl不导电
D.难溶物一定不属于电解质
5.(2021天津一中期中质量调查)某同学在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是( )
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl溶液中的水电离出大量的离子
D.NaCl在水溶液中电离出了可以自由移动的离子
题组三 电离方程式的书写和正误判断
6.(2022河北石家庄二中期中)下列电离方程式书写错误的是( )
A.CH3COOH CH3COO-+H+
B.NaHCO3 Na++HC
C.H2SO4 2H++S
D.NaHSO4 Na++H++S
7.(2021河北保定月考)下列电离方程式书写正确的是( )
A.熔融状态下NaHSO4的电离:NaHSO4 Na++H++S
B.水溶液中Ba(OH)2的电离:Ba(OH)2 Ba2++OH-
C.水溶液中NaHCO3的电离:NaHCO3 Na++HC
D.水溶液中H2SO4的电离:H2SO4 H++HS
题组四 从电离的角度认识酸、碱、盐
8.(2020河南豫西名校联考)下列关于酸、碱、盐的说法中正确的是( )
A.电离出的阳离子有H+的化合物叫酸,电离出OH-的化合物叫碱
B.氯化钠溶液在电流的作用下电离出Na+和Cl-
C.化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐
D.NaHSO4可以电离出H+,因此NaHSO4属于酸
能力提升练
题组一 电解质及其电离的分析与探究
1.(2022广东深圳实验学校月考)下列叙述中错误的是( )
A.氯化钠固体不导电的原因是氯化钠固体中不含阴、阳离子
B.熔融态能导电的不一定是电解质
C.硫酸不能导电而其水溶液能导电的原因是硫酸溶于水后在水分子的作用下产生自由移动的氢离子和硫酸根离子
D.硫酸钡的水溶液几乎不导电,但硫酸钡是强电解质
2.(2022广东佛山南海月考)在水溶液或熔融状态下能导电的化合物为电解质,如酸、碱、盐等。将固态氯化钠(b)分别加水(a)和加热熔融(c),并置于电场中。有关叙述正确的是( )
A.NaCl固体为纯净物而熔融NaCl为混合物
B.固态NaCl中存在NaCl分子
C.固态NaCl不能导电的原因是带电离子不能自由移动
D.在水溶液中,H2O包围着钠离子,且氢原子朝向Na+
题组二 探究电解质溶液的导电性
3.(2020湖南常德部分重点中学期中)某学生利用如图装置对电解质溶液的导电性进行实验探究。下列说法正确的是( )
A.闭合开关K,电流计指针发生偏转,证明HCl溶液是电解质
B.闭合开关K,向烧杯中加入NaCl固体,由于HCl与NaCl不反应,故电流计示数不发生变化
C.闭合开关K,向溶液中加入CaCO3固体,电流计示数变化不大
D.选取相同浓度的稀硫酸替换0.1 mol·L-1的HCl溶液,闭合开关K,电流计示数相同
4.(2021天津大港一中月考)导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如图所示的装置里,若灯泡亮,广口瓶内的物质A可以是 (填序号)。
①干燥的氯化钠晶体;②干燥的氢氧化钠晶体;③蔗糖晶体;④酒精;⑤氯化钠溶液;⑥氢氧化钠溶液;⑦稀盐酸;⑧硫酸铜溶液。
(2)在电解质溶液的导电性实验装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液至过量时,灯泡由亮变暗,至熄灭后又逐渐变亮的是 (填字母)。
A.向盐酸中逐滴加入NaCl溶液
B.向稀硫酸中逐滴加入氢氧化钠溶液
C.向澄清石灰水中逐滴加入稀盐酸
D.向稀硫酸中逐滴加入氢氧化钡溶液
答案全解全析
基础过关练
1.A 2.C 3.C 4.C 5.D 6.A 7.C 8.C
1.A 电解质是指在水溶液里或熔融状态下能够导电的化合物,单质和混合物都不是电解质,故选A。
2.C Fe为单质,不属于电解质,故A错误;葡萄糖是化合物,但其在水溶液中和熔融状态下都不能导电,不属于电解质,故B错误;MgSO4为电解质,故C正确;二氧化碳不属于电解质,故D错误。
3.C A项,KClO3在水溶液中电离出K+、Cl,没有Cl-,不符合题意;B项,CaCl2固体中存在Ca2+和Cl-,但不能自由移动,不符合题意;C项,KCl在水溶液中电离出能自由移动的K+、Cl-,符合题意;D项,液态HCl中只存在氯化氢分子,不存在自由移动的Cl-,不符合题意。
4.C NaCl在水分子作用下,电离出Na+和Cl-,故A错误;溶于水后能电离出H+的化合物可能是酸,也可能是酸式盐,如NaHSO4,故B错误;HCl溶液中存在自由移动的H+和Cl-,能导电,而液态的HCl中只存在HCl分子,不导电,故C正确;难溶物如BaSO4溶于水的部分能电离,属于电解质,故D错误。
5.D NaCl是电解质,NaCl溶液属于混合物,不是电解质,故A、B错误;水为极弱的电解质,不能电离出大量的离子,故C错误;NaCl溶于水时,在水分子的作用下电离出了可以自由移动的离子,故D正确。
6.A 醋酸是弱酸,在水溶液中部分电离,其电离方程式为CH3COOH CH3COO-+H+,故A错误。
7.C 熔融状态下NaHSO4的电离方程式为NaHSO4 Na++HS,A错误;水溶液中Ba(OH)2的电离方程式为Ba(OH)2 Ba2++2OH-,B错误;水溶液中NaHCO3的电离方程式为NaHCO3 Na++HC,C正确;水溶液中H2SO4的电离方程式为H2SO4 2H++S,D错误。
8.C 电离出的阳离子全部是H+的化合物叫酸,电离出的阴离子全部是OH-的化合物叫碱,A项错误;氯化钠的电离不需要通电,B项错误;化合物电离时,生成金属阳离子(或铵根离子)和酸根离子的是盐,C项正确;NaHSO4可以电离出H+,但电离出的阳离子不全是H+,还有Na+,则NaHSO4不是酸,D项错误。
能力提升练
1.A 2.C 3.C
1.A 氯化钠固体中含有钠离子和氯离子,故A错误;熔融态的金属单质能导电,但金属单质不属于电解质,故B正确;硫酸是由分子构成的,纯净的硫酸不能导电,硫酸溶于水后在水分子的作用下产生自由移动的氢离子和硫酸根离子,其水溶液能导电,故C正确;硫酸钡的水溶液几乎不导电,但其溶解的部分能完全电离,因此硫酸钡是强电解质,故D正确。
2.C NaCl固体和熔融NaCl都只含一种物质,都是纯净物,故A错误;氯化钠是由钠离子和氯离子构成的,不存在分子,故B错误;固态NaCl中的阴离子、阳离子不能自由移动,所以不能导电,故C正确;钠离子带正电,水分子中的H带正电,根据电性关系可知,水分子中的氧原子朝向钠离子,故D错误。
3.C 开关K闭合后,电流计指针发生偏转,说明溶液中存在自由移动的离子,HCl发生了电离,HCl是电解质,但HCl溶液为混合物,不是电解质,A错误;向HCl溶液中加入NaCl固体,溶液中自由移动的离子浓度增大,故导电能力增强,电流计示数增大,B错误;向HCl溶液中加入CaCO3固体,发生反应2HCl+CaCO3 CaCl2+CO2↑+H2O,溶液中自由移动的离子浓度减小,但离子所带电荷数增大,故导电性变化不大,电流计示数变化不大,C正确;HCl溶液和稀硫酸浓度相同时溶液中离子浓度不同,离子所带电荷数也不同,故导电能力不同,电流计示数不同,D错误。
4.答案 (1)⑤⑥⑦⑧ (2)D
解析 (1)若灯泡亮,广口瓶内的物质A中含有能自由移动的离子。氯化钠晶体、氢氧化钠晶体虽由离子构成,但离子不能自由移动,所以不导电;蔗糖晶体和酒精均为非电解质,不能导电;氯化钠溶液、氢氧化钠溶液、稀盐酸、硫酸铜溶液中均含有大量自由移动的离子,可以导电;综上所述,物质A可以是⑤⑥⑦⑧。
(2)溶液能否导电,取决于溶液中是否有自由移动的离子;溶液导电性强弱与溶液中自由移动离子的浓度大小及离子所带电荷数多少有关。向盐酸中逐滴加入NaCl溶液,HCl和NaCl不发生反应,混合后仍为强电解质溶液,溶液中存在大量自由移动的离子,可导电,灯泡不会熄灭,故A不符合题意;向稀硫酸中逐滴加入氢氧化钠溶液,H2SO4与NaOH反应生成Na2SO4,仍为强电解质溶液,溶液中存在大量自由移动的离子,可导电,灯泡不会熄灭,故B不符合题意;向澄清石灰水中滴加稀盐酸,Ca(OH)2与HCl反应生成了可溶性的CaCl2,灯泡不会熄灭,故C不符合题意;向稀硫酸中逐滴加入Ba(OH)2溶液,发生反应H2SO4+Ba(OH)2 BaSO4↓+2H2O,溶液中离子浓度减小,恰好完全反应时,灯泡熄灭,继续滴加Ba(OH)2溶液,溶液中Ba2+、OH-数目增多,灯泡逐渐变亮,故D符合题意。
8
