2024鲁科版新教材高中化学选择性必修1同步练习--微项目 揭秘索尔维制碱法和侯氏制碱法(含解析)
文档属性
| 名称 | 2024鲁科版新教材高中化学选择性必修1同步练习--微项目 揭秘索尔维制碱法和侯氏制碱法(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 148.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-22 00:00:00 | ||
图片预览

文档简介
2024鲁科版新教材高中化学选择性必修1
微项目 揭秘索尔维制碱法和侯氏制碱法
基础过关练
1.“侯氏制碱法”的原理是NaCl+NH3+CO2+H2O NaHCO3↓+NH4Cl,模拟该制法的部分装置如图所示。下列操作正确的是( )
A.a通入CO2,然后b通入NH3,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放碱石灰
C.a通入NH3,然后b通入CO2,c中放蘸有稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3,c中放蘸有稀硫酸的脱脂棉
2.下表是几种物质在指定温度下的溶解度。工业上将相同物质的量的NaCl、CO2、NH3在30 ℃时配成溶液,此时溶液中无晶体析出。当降温至某温度时,开始析出晶体,此晶体是( )
盐温度/℃溶解度/g 0 10 20 30
NH4Cl 29.4 33.3 37.2 41.1
NH4HCO3 11.9 15.9 21.0 27.0
NaHCO3 6.9 8.15 9.6 11.1
NaCl 35.7 35.8 36.0 36.4
A.NH4Cl B.NH4HCO3 C.NaHCO3 D.NaCl
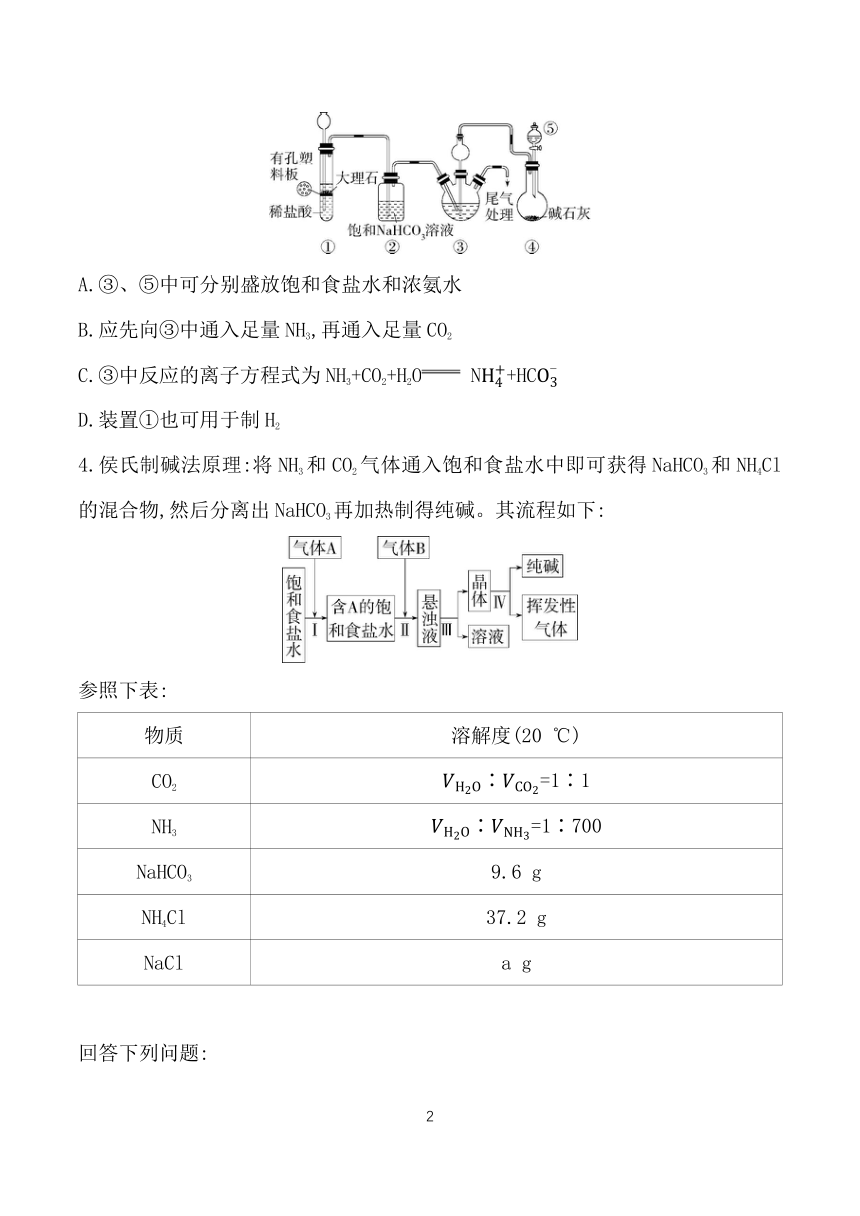
3.某小组设计如图所示装置(夹持装置略去),在实验室模拟侯氏制碱工艺中NaHCO3的制备,下列说法不正确的是( )
A.③、⑤中可分别盛放饱和食盐水和浓氨水
B.应先向③中通入足量NH3,再通入足量CO2
C.③中反应的离子方程式为NH3+CO2+H2O N+HC
D.装置①也可用于制H2
4.侯氏制碱法原理:将NH3和CO2气体通入饱和食盐水中即可获得NaHCO3和NH4Cl的混合物,然后分离出NaHCO3再加热制得纯碱。其流程如下:
参照下表:
物质 溶解度(20 ℃)
CO2 ∶=1∶1
NH3 ∶=1∶700
NaHCO3 9.6 g
NH4Cl 37.2 g
NaCl a g
回答下列问题:
(1)气体A、B依次是 。
A.CO2、NH3 B.NH3、CO2
C.任何顺序都可以
(2)写出Ⅰ和Ⅱ步骤总反应的化学方程式:
。由反应原理可知,a 9.6(填“<”“>”或“=”)。
(3)经步骤Ⅲ所得溶液中含有的盐为 (写化学式)。
(4)每当通入NH3 44.8 L(标准状况下)时可以得到纯碱100.0 g,则NH3的利用率为 。
答案全解全析
基础过关练
1.C 2.C 3.C
1.C 氨气在水中的溶解度比二氧化碳大,应先通入氨气,再通入二氧化碳,氨气不能直接通入水中,会发生倒吸,所以a通入氨气,然后b通入二氧化碳,氨气不能直接排放到空气中,应该用蘸有稀硫酸的脱脂棉吸收,故选C。
2.C 根据表中数据可知,相同温度下,NaHCO3的溶解度最小,故首先析出的物质应是NaHCO3。
3.C ③中盛放饱和食盐水,用来制备碳酸氢钠,⑤中盛放浓氨水,用来制取氨气,故A正确;由于NH3在水中的溶解度比CO2大,应先向③中通入足量氨气,再通入二氧化碳,故B正确;装置③中氨气、二氧化碳、氯化钠和水反应生成碳酸氢钠晶体和氯化铵,碳酸氢钠不能拆成离子的形式,故C不正确;可以利用装置①制氢气,故D正确。
4.答案 (1)B
(2)NH3+CO2+H2O+NaCl NaHCO3↓+NH4Cl >
(3)NaHCO3、NH4Cl
(4)94.35%
解析 (1)氨气在水溶液中溶解度大,故侯氏制碱法中先向饱和食盐水中通入NH3,后通入CO2。
(2)由侯氏制碱法原理可知,同温下NaCl的溶解度大于NaHCO3的溶解度,则a>9.6。
(4)由反应转化关系:NH3~NaCl~Na2CO3,当得到100.0 g纯碱时,消耗NH3的物质的量为×2≈1.887 mol,则NH3的利用率为×100%=94.35%。
4
微项目 揭秘索尔维制碱法和侯氏制碱法
基础过关练
1.“侯氏制碱法”的原理是NaCl+NH3+CO2+H2O NaHCO3↓+NH4Cl,模拟该制法的部分装置如图所示。下列操作正确的是( )
A.a通入CO2,然后b通入NH3,c中放碱石灰
B.b通入NH3,然后a通入CO2,c中放碱石灰
C.a通入NH3,然后b通入CO2,c中放蘸有稀硫酸的脱脂棉
D.b通入CO2,然后a通入NH3,c中放蘸有稀硫酸的脱脂棉
2.下表是几种物质在指定温度下的溶解度。工业上将相同物质的量的NaCl、CO2、NH3在30 ℃时配成溶液,此时溶液中无晶体析出。当降温至某温度时,开始析出晶体,此晶体是( )
盐温度/℃溶解度/g 0 10 20 30
NH4Cl 29.4 33.3 37.2 41.1
NH4HCO3 11.9 15.9 21.0 27.0
NaHCO3 6.9 8.15 9.6 11.1
NaCl 35.7 35.8 36.0 36.4
A.NH4Cl B.NH4HCO3 C.NaHCO3 D.NaCl
3.某小组设计如图所示装置(夹持装置略去),在实验室模拟侯氏制碱工艺中NaHCO3的制备,下列说法不正确的是( )
A.③、⑤中可分别盛放饱和食盐水和浓氨水
B.应先向③中通入足量NH3,再通入足量CO2
C.③中反应的离子方程式为NH3+CO2+H2O N+HC
D.装置①也可用于制H2
4.侯氏制碱法原理:将NH3和CO2气体通入饱和食盐水中即可获得NaHCO3和NH4Cl的混合物,然后分离出NaHCO3再加热制得纯碱。其流程如下:
参照下表:
物质 溶解度(20 ℃)
CO2 ∶=1∶1
NH3 ∶=1∶700
NaHCO3 9.6 g
NH4Cl 37.2 g
NaCl a g
回答下列问题:
(1)气体A、B依次是 。
A.CO2、NH3 B.NH3、CO2
C.任何顺序都可以
(2)写出Ⅰ和Ⅱ步骤总反应的化学方程式:
。由反应原理可知,a 9.6(填“<”“>”或“=”)。
(3)经步骤Ⅲ所得溶液中含有的盐为 (写化学式)。
(4)每当通入NH3 44.8 L(标准状况下)时可以得到纯碱100.0 g,则NH3的利用率为 。
答案全解全析
基础过关练
1.C 2.C 3.C
1.C 氨气在水中的溶解度比二氧化碳大,应先通入氨气,再通入二氧化碳,氨气不能直接通入水中,会发生倒吸,所以a通入氨气,然后b通入二氧化碳,氨气不能直接排放到空气中,应该用蘸有稀硫酸的脱脂棉吸收,故选C。
2.C 根据表中数据可知,相同温度下,NaHCO3的溶解度最小,故首先析出的物质应是NaHCO3。
3.C ③中盛放饱和食盐水,用来制备碳酸氢钠,⑤中盛放浓氨水,用来制取氨气,故A正确;由于NH3在水中的溶解度比CO2大,应先向③中通入足量氨气,再通入二氧化碳,故B正确;装置③中氨气、二氧化碳、氯化钠和水反应生成碳酸氢钠晶体和氯化铵,碳酸氢钠不能拆成离子的形式,故C不正确;可以利用装置①制氢气,故D正确。
4.答案 (1)B
(2)NH3+CO2+H2O+NaCl NaHCO3↓+NH4Cl >
(3)NaHCO3、NH4Cl
(4)94.35%
解析 (1)氨气在水溶液中溶解度大,故侯氏制碱法中先向饱和食盐水中通入NH3,后通入CO2。
(2)由侯氏制碱法原理可知,同温下NaCl的溶解度大于NaHCO3的溶解度,则a>9.6。
(4)由反应转化关系:NH3~NaCl~Na2CO3,当得到100.0 g纯碱时,消耗NH3的物质的量为×2≈1.887 mol,则NH3的利用率为×100%=94.35%。
4
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
