【高效备课】第3单元 课题3 元素 第2课时 元素周期表 课件+素材
文档属性
| 名称 | 【高效备课】第3单元 课题3 元素 第2课时 元素周期表 课件+素材 |

|
|
| 格式 | zip | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-22 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
第2课时
元素周期表
第三单元
物质构成的奥秘
课题3
元素
R·九年级化学上册
课前自学准备
课标要求
学习目标
初步认识元素周期表,知道它是学习和研究化学的工具,能根据原子序数,在元素周期表中找到指定元素和有关该元素的一些其他信息。
1.元素周期表共有 个横行, 个纵行,每一个横行叫做一个 ,每一个纵行叫做一个 。
2.元素周期表按元素原子 递增的顺序给元素编的序号,叫做原子序数。元素的原子序数与原子的 在数值上相同。
课前自学准备
预习检测
7
18
周期
族
核电荷数
核电荷数
课堂教学展示
新课导入
超市中的商品成千上万种,却分门别类、有序地摆放。
组成物质的一百多种元素,是按怎样的规律排列的呢?
课堂教学展示
课堂探究
知识点 元素周期表
许多化学家致力于元素周期表的排列,尤其是俄国化学家门捷列夫。他在前人工作的基础上,提出了独到的见解,为元素周期表的完成作出了巨大的贡献,因此被称为“一代科学勋臣”。
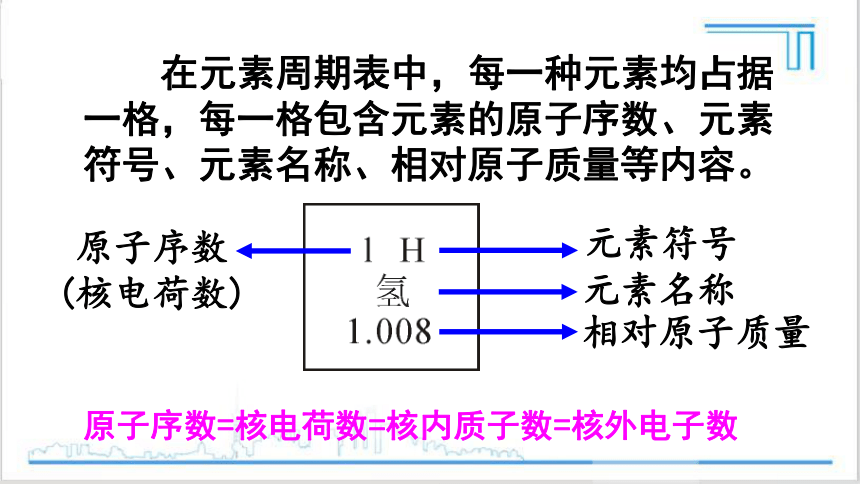
在元素周期表中,每一种元素均占据一格,每一格包含元素的原子序数、元素符号、元素名称、相对原子质量等内容。
原子序数
(核电荷数)
元素符号
元素名称
相对原子质量
原子序数=核电荷数=核内质子数=核外电子数
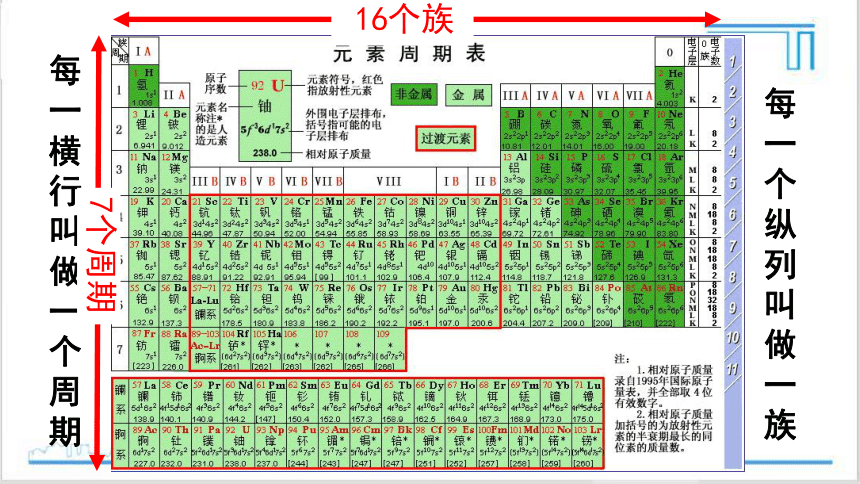
每一横行叫做一个周期
每一个纵列叫做一族
7个周期
16个族
元素周期表的意义:学习和研究化学的重要工具。
①为寻找新元素提供了理论依据。
②由于在元素周期表中位置越靠近的元素性质越相似,可以启发人们在元素周期表的一定的区域寻找新物质(如农药、催化剂、半导体材料等)。
【活动与探究】
(1)以邻座的同学为一小组,从元素周期表上查找原子序数为6、7、12、14、16、18、20、29、47的元素名称、符号、核外电子数和相对原子质量,并指出它们是金属、非金属还是稀有气体元素,每个同学查找几种元素,并互相订正答案。
【活动与探究】
(2)考查每周期开头的是什么类型的元素,靠近尾部的是什么类型的元素,结尾的是什么类型的元素。这说明元素之间存在着什么规律性的联系?“元素周期表”这个名称与这个规律有没有关系?
活动(1):
①6号元素为碳,符号C,核外电子数6,相对原子质量12,为非金属元素(以下顺序相同)。
②7号:氮,N,7,14,非金属。
③12号:镁,Mg,12,24,金属。
④14号:硅,Si,14,28,非金属。
⑤16号:硫,S,16,32,非金属。
⑥18号:氩,Ar,18,39.95,稀有气体。
⑦20号:钙,Ca,20,40,金属。
⑧29号:铜,Cu,29,63.5,金属。
⑨47号:银,Ag,47,108,金属。
活动(2):
除第一周期外,每周期开头为金属元素,靠近尾部是非金属元素,结尾是稀有气体元素。这说明元素之间随着原子序数的递增,元素的性质出现了周期性的变化。“元素周期表”的名称与这一规律有关。
例1 元素周期表,是学习和研究化学的工具。下图是钙元素的相关信息。
请回答:
钙元素属于 (填“金属”或“非金属”)元素,相对原子质量为 ,其元素的原子在化学变化中容易 (填“得到”或“失去”)电子形成离子,离子符号为 ,它与氯元素形成化合物的化学式为 。
课堂教学展示
典例剖析
40.08
CaCl2
金属
失去
Ca2+
例2 元素周期表是学习和研究化学的重要工具,试根据图示回答相应问题:
(1)图甲是铯元素在元素周期表中的信息,则铯元素属于
(填“金属”或“非金属”)元素,该元素原子的核外电子数为 。
(2)图乙为元素周期表的一部分,X、Y、Z代表三种不同元素,以下 判断正确。
A.原子序数Z>Y B.核外电子数:X=Y
C.Y和Z处于同一周期
金属
55
AC
课堂教学展示
课堂小结
元素周期表
简介
每一横行叫一个周期,共7个周期
每一纵列叫一个族,共16个族
元素之间随着原子序数的递增,元素的性质出现了周期性的变化
1.从课后习题中选取;
2.完成练习册本课时的习题。
课后反馈总结
课后作业
2.选择题
(5)稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
A.铈的原子序数是58
B.铈属于非金属元素
C.铈原子中的质子数为58
D.铈的相对原子质量是140.1
课后反馈总结
课本习题
练习与应用(P65)
B
6.查阅元素周期表,写出原子序数为20、26和53的元素名称和符号。举例说明生活中与它们有关的事例。
答:原子序数为20的元素为钙,元素符号为Ca;原子序数为26的元素为铁,元素符号为Fe;
原子序数为53的元素为碘,元素符号为I。
第2课时
元素周期表
第三单元
物质构成的奥秘
课题3
元素
R·九年级化学上册
课前自学准备
课标要求
学习目标
初步认识元素周期表,知道它是学习和研究化学的工具,能根据原子序数,在元素周期表中找到指定元素和有关该元素的一些其他信息。
1.元素周期表共有 个横行, 个纵行,每一个横行叫做一个 ,每一个纵行叫做一个 。
2.元素周期表按元素原子 递增的顺序给元素编的序号,叫做原子序数。元素的原子序数与原子的 在数值上相同。
课前自学准备
预习检测
7
18
周期
族
核电荷数
核电荷数
课堂教学展示
新课导入
超市中的商品成千上万种,却分门别类、有序地摆放。
组成物质的一百多种元素,是按怎样的规律排列的呢?
课堂教学展示
课堂探究
知识点 元素周期表
许多化学家致力于元素周期表的排列,尤其是俄国化学家门捷列夫。他在前人工作的基础上,提出了独到的见解,为元素周期表的完成作出了巨大的贡献,因此被称为“一代科学勋臣”。
在元素周期表中,每一种元素均占据一格,每一格包含元素的原子序数、元素符号、元素名称、相对原子质量等内容。
原子序数
(核电荷数)
元素符号
元素名称
相对原子质量
原子序数=核电荷数=核内质子数=核外电子数
每一横行叫做一个周期
每一个纵列叫做一族
7个周期
16个族
元素周期表的意义:学习和研究化学的重要工具。
①为寻找新元素提供了理论依据。
②由于在元素周期表中位置越靠近的元素性质越相似,可以启发人们在元素周期表的一定的区域寻找新物质(如农药、催化剂、半导体材料等)。
【活动与探究】
(1)以邻座的同学为一小组,从元素周期表上查找原子序数为6、7、12、14、16、18、20、29、47的元素名称、符号、核外电子数和相对原子质量,并指出它们是金属、非金属还是稀有气体元素,每个同学查找几种元素,并互相订正答案。
【活动与探究】
(2)考查每周期开头的是什么类型的元素,靠近尾部的是什么类型的元素,结尾的是什么类型的元素。这说明元素之间存在着什么规律性的联系?“元素周期表”这个名称与这个规律有没有关系?
活动(1):
①6号元素为碳,符号C,核外电子数6,相对原子质量12,为非金属元素(以下顺序相同)。
②7号:氮,N,7,14,非金属。
③12号:镁,Mg,12,24,金属。
④14号:硅,Si,14,28,非金属。
⑤16号:硫,S,16,32,非金属。
⑥18号:氩,Ar,18,39.95,稀有气体。
⑦20号:钙,Ca,20,40,金属。
⑧29号:铜,Cu,29,63.5,金属。
⑨47号:银,Ag,47,108,金属。
活动(2):
除第一周期外,每周期开头为金属元素,靠近尾部是非金属元素,结尾是稀有气体元素。这说明元素之间随着原子序数的递增,元素的性质出现了周期性的变化。“元素周期表”的名称与这一规律有关。
例1 元素周期表,是学习和研究化学的工具。下图是钙元素的相关信息。
请回答:
钙元素属于 (填“金属”或“非金属”)元素,相对原子质量为 ,其元素的原子在化学变化中容易 (填“得到”或“失去”)电子形成离子,离子符号为 ,它与氯元素形成化合物的化学式为 。
课堂教学展示
典例剖析
40.08
CaCl2
金属
失去
Ca2+
例2 元素周期表是学习和研究化学的重要工具,试根据图示回答相应问题:
(1)图甲是铯元素在元素周期表中的信息,则铯元素属于
(填“金属”或“非金属”)元素,该元素原子的核外电子数为 。
(2)图乙为元素周期表的一部分,X、Y、Z代表三种不同元素,以下 判断正确。
A.原子序数Z>Y B.核外电子数:X=Y
C.Y和Z处于同一周期
金属
55
AC
课堂教学展示
课堂小结
元素周期表
简介
每一横行叫一个周期,共7个周期
每一纵列叫一个族,共16个族
元素之间随着原子序数的递增,元素的性质出现了周期性的变化
1.从课后习题中选取;
2.完成练习册本课时的习题。
课后反馈总结
课后作业
2.选择题
(5)稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法中错误的是( )
A.铈的原子序数是58
B.铈属于非金属元素
C.铈原子中的质子数为58
D.铈的相对原子质量是140.1
课后反馈总结
课本习题
练习与应用(P65)
B
6.查阅元素周期表,写出原子序数为20、26和53的元素名称和符号。举例说明生活中与它们有关的事例。
答:原子序数为20的元素为钙,元素符号为Ca;原子序数为26的元素为铁,元素符号为Fe;
原子序数为53的元素为碘,元素符号为I。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
