2023-2024学年人教版九年级化学上册 3.2.1 原子的构成第1课时课件(共20张PPT)
文档属性
| 名称 | 2023-2024学年人教版九年级化学上册 3.2.1 原子的构成第1课时课件(共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-23 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
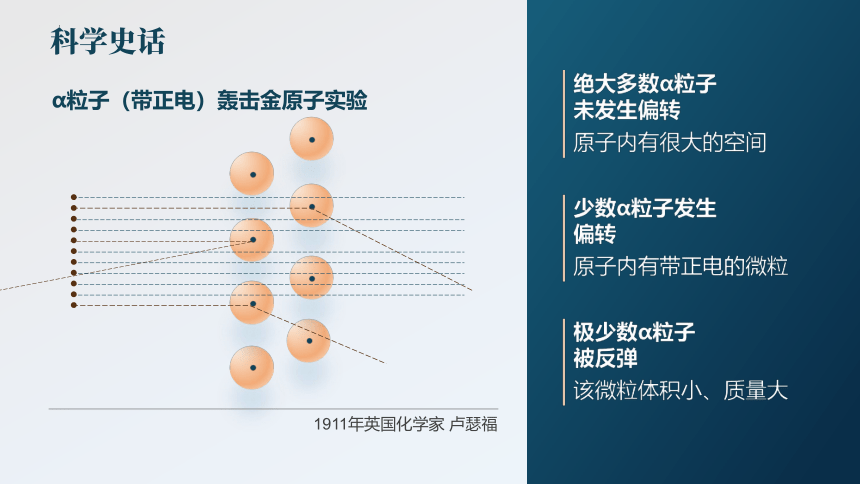
α粒子(带正电)轰击金原子实验
1911年英国化学家 卢瑟福
从三个角度看原子
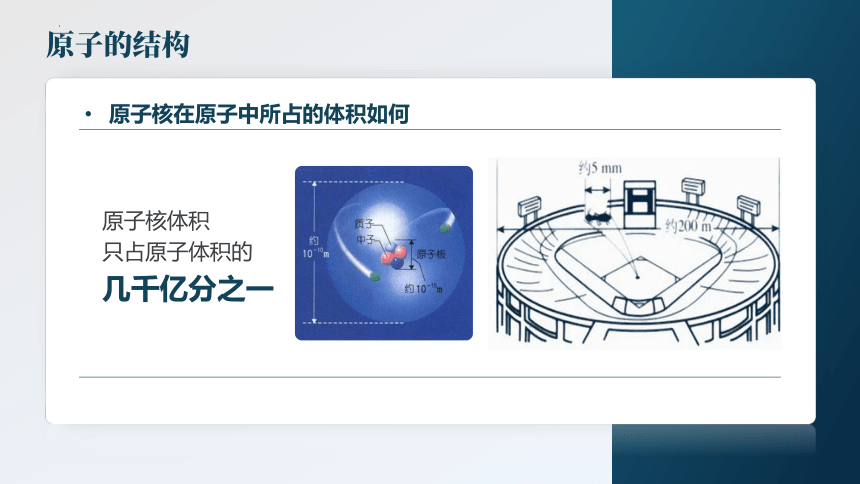
原子核在原子中所占的体积如何
原子核体积
只占原子体积的
几千亿分之一
-
-
-
-
-
-
+
+
+
+
+
+
原子的质量
主要集中在原子核上
+
1.6749×10-27 kg
质子
1.6726×10-27 kg
中子
-
质子质量的1/1836
电子
带正电
不带电
带负电
原子核
带正电
几种原子的构成
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
原子种类
核外电子数
质子数
中子数
几种原子的构成
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
原子种类
核外电子数
质子数
中子数
不是所有原子都有中子
原子中,质子数=核外电子数
不同种类原子,质子数不同
原子中,核电荷数=质子数
原子中,质子数不一定等于中子数
氢原子
原子呈电中性原因
1. 关于原子的叙述正确的是( )
2. 构成原子核的粒子一定有 ( )
A
质子
B
中 子
C
电 子
D
质子和中子
D
A
3. 原子的质量主要集中在 ( )
A
质子
B
中 子
C
电 子
D
原子核
D
A
原子是微粒中最小的
B
原子是不能再分的微粒
C
原子中不存在带电微粒
D
原子是化学变化中的最小微粒
4.下列关于原子核的说法错误的是( )
C
A
原子核在原子中所占的体积很小
B
原子核居于原子中心带正电荷
C
原子核居于原子中心带负电荷
D
原子的质量主要集中在原子核上
5. 铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和
82个中子,该原子的核外电子数是( )
A
24
B
58
C
82
D
140
B
6.在分子、原子、质子、中子、电子这些粒子中,选择合适的答案
随堂练习
(1)能直接构成物质的粒子有: .
(2)在化学变化中最小的粒子有: .
(3)不显电性的粒子有: .
(4)带正电的粒子有: .
(5)带负电的粒子有: .
(6)构成原子的微粒有: .
(7)构成原子核的微粒有: .
分子、原子
原子
分子、原子、中子
质子
电子
质子、中子、电子
质子、中子
最外层电子数
该层电子数
核电荷数
电子层
原子核
请你试试看画出下列原子的结构示意图
核外电子的排布规律
注:第1层为最外层时不超过2个
最外层不超过8个电子
第一层最多2个电子
第二层最多8个电子
由里向外逐层排满
镁原子 12
氖原子 10
氯原子 17
这些原子结构示意图告诉了我们哪些信息?
不同的元素或原子是因为 不同
质子数(核电荷数)决定元素或原子的种类
质子数(核电荷数)
下列结构中表示同种元素的是:
A
B
C
D
E
F
B和D
C和E
这些原子结构示意图告诉了我们哪些信息?
横看,同一行原子 相同
电子层数
纵看,同一列原子, 相同,化学性质相似
最外层电子数
这些原子结构示意图告诉了我们哪些信息?
稀有气体元素,最外层电子数 .
等于8,为稳定结构
稀
有
气
体
元
素
除He为2
下列微粒具有稳定结构的是:
A
B
C
D
E
F
D E F
这些原子结构示意图告诉了我们哪些信息?
金属元素,最外层电子数 ,通常容易 .
<4
稀
有
气
体
元
素
非金属元素,最外层电子数 ,通常容易 .
失电子
>4
得电子
金属元素
非金属元素
根据下列原子的结构示意图,回答下列问题:
A
B
C
D
(2)易失电子的原子的是 ;易得电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
(3)化学性质相似的是 .
B
C和D
C和D
A
α粒子(带正电)轰击金原子实验
1911年英国化学家 卢瑟福
从三个角度看原子
原子核在原子中所占的体积如何
原子核体积
只占原子体积的
几千亿分之一
-
-
-
-
-
-
+
+
+
+
+
+
原子的质量
主要集中在原子核上
+
1.6749×10-27 kg
质子
1.6726×10-27 kg
中子
-
质子质量的1/1836
电子
带正电
不带电
带负电
原子核
带正电
几种原子的构成
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
原子种类
核外电子数
质子数
中子数
几种原子的构成
氢 1 0 1
碳 6 6 6
氧 8 8 8
钠 11 12 11
氯 17 18 17
原子种类
核外电子数
质子数
中子数
不是所有原子都有中子
原子中,质子数=核外电子数
不同种类原子,质子数不同
原子中,核电荷数=质子数
原子中,质子数不一定等于中子数
氢原子
原子呈电中性原因
1. 关于原子的叙述正确的是( )
2. 构成原子核的粒子一定有 ( )
A
质子
B
中 子
C
电 子
D
质子和中子
D
A
3. 原子的质量主要集中在 ( )
A
质子
B
中 子
C
电 子
D
原子核
D
A
原子是微粒中最小的
B
原子是不能再分的微粒
C
原子中不存在带电微粒
D
原子是化学变化中的最小微粒
4.下列关于原子核的说法错误的是( )
C
A
原子核在原子中所占的体积很小
B
原子核居于原子中心带正电荷
C
原子核居于原子中心带负电荷
D
原子的质量主要集中在原子核上
5. 铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和
82个中子,该原子的核外电子数是( )
A
24
B
58
C
82
D
140
B
6.在分子、原子、质子、中子、电子这些粒子中,选择合适的答案
随堂练习
(1)能直接构成物质的粒子有: .
(2)在化学变化中最小的粒子有: .
(3)不显电性的粒子有: .
(4)带正电的粒子有: .
(5)带负电的粒子有: .
(6)构成原子的微粒有: .
(7)构成原子核的微粒有: .
分子、原子
原子
分子、原子、中子
质子
电子
质子、中子、电子
质子、中子
最外层电子数
该层电子数
核电荷数
电子层
原子核
请你试试看画出下列原子的结构示意图
核外电子的排布规律
注:第1层为最外层时不超过2个
最外层不超过8个电子
第一层最多2个电子
第二层最多8个电子
由里向外逐层排满
镁原子 12
氖原子 10
氯原子 17
这些原子结构示意图告诉了我们哪些信息?
不同的元素或原子是因为 不同
质子数(核电荷数)决定元素或原子的种类
质子数(核电荷数)
下列结构中表示同种元素的是:
A
B
C
D
E
F
B和D
C和E
这些原子结构示意图告诉了我们哪些信息?
横看,同一行原子 相同
电子层数
纵看,同一列原子, 相同,化学性质相似
最外层电子数
这些原子结构示意图告诉了我们哪些信息?
稀有气体元素,最外层电子数 .
等于8,为稳定结构
稀
有
气
体
元
素
除He为2
下列微粒具有稳定结构的是:
A
B
C
D
E
F
D E F
这些原子结构示意图告诉了我们哪些信息?
金属元素,最外层电子数 ,通常容易 .
<4
稀
有
气
体
元
素
非金属元素,最外层电子数 ,通常容易 .
失电子
>4
得电子
金属元素
非金属元素
根据下列原子的结构示意图,回答下列问题:
A
B
C
D
(2)易失电子的原子的是 ;易得电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
(3)化学性质相似的是 .
B
C和D
C和D
A
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
