化学人教版(2019)必修第一册 2.1.1活泼的金属单质-钠 课件(共19张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册 2.1.1活泼的金属单质-钠 课件(共19张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-23 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
第一节 钠及其化合物
第一课时 活泼的金属单质—钠
第二章 海水中的重要元素—钠和氯
1.从Na的原子结构认识钠的强还原性(易失去电子);
2.了解Na的物理性质
3.Na在不同条件与O2反应
4.Na与水反应的现象,会分析Na与酸、碱、盐溶液的反应
学习目标 1min
教师点拨 20min
易失去
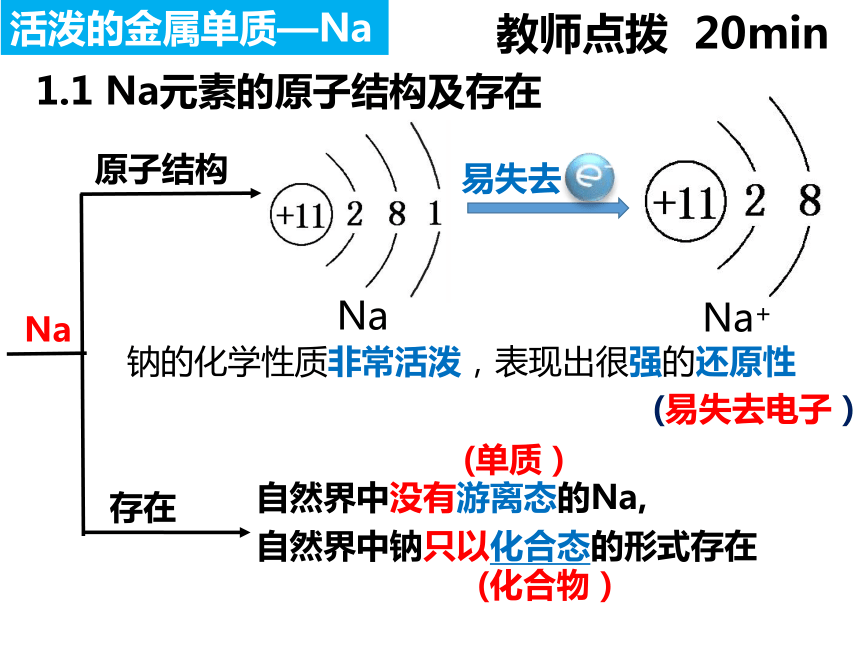
1.1 Na元素的原子结构及存在
Na
原子结构
存在
自然界中没有游离态的Na,
自然界中钠只以化合态的形式存在
Na
Na+
钠的化学性质非常活泼,表现出很强的还原性
(单质)
(化合物)
活泼的金属单质—Na
(易失去电子)
1.2 钠的单质
钠的物理性质 颜色
状态(常温下) 密度(与煤油比) 硬度(质地) 银白色金属光泽
固体
比煤油大
软
【实验2-1】切割金属钠
实验现象:取出的金属钠表面呈灰黄色 切开后的切口露出了银白色光泽 切口在空气中很快变暗
活泼的金属单质—Na
1.2 钠的单质
【实验2-1】切割金属钠
【思考】金属钠应该如何保存?
氧化钠
(白色固体)
保存在煤油或石蜡油中,以隔绝空气。切割后多余的金属钠要及时放回瓶中。
实验现象:取出的金属钠表面呈灰黄色 切开后的切口露出了银白色光泽 切口在空气中很快变暗
4Na+O2=2Na2O
活泼的金属单质—Na
1.2 钠的单质
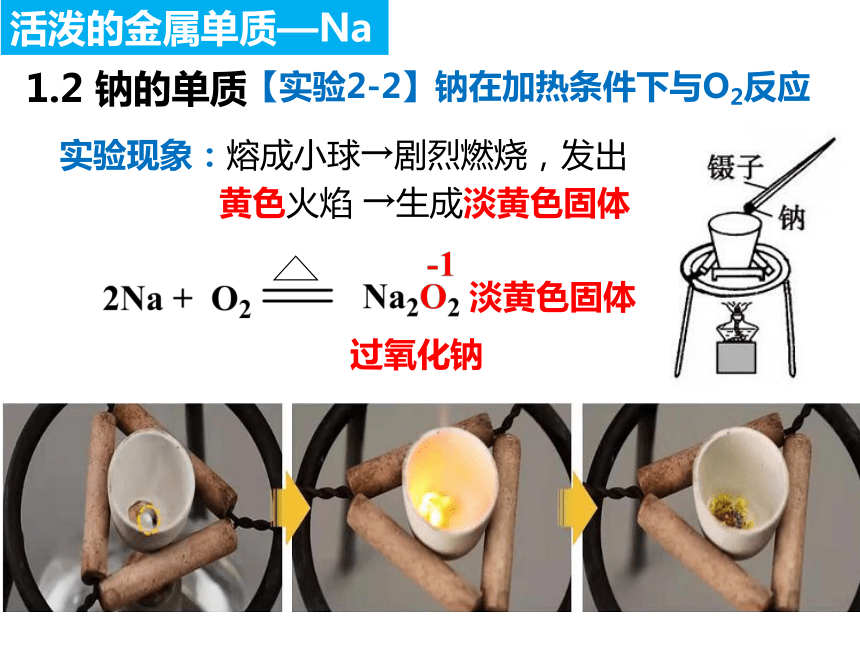
【实验2-2】钠在加热条件下与O2反应
实验现象:熔成小球→剧烈燃烧,发出
黄色火焰 →生成淡黄色固体
淡黄色固体
过氧化钠
活泼的金属单质—Na
碱性氧化物
物理变化
化学变化
活泼的金属单质—Na
【思考】钠露置在空气中会有什么变化呢?
1.2 钠的单质
【实验】钠与水的反应
实验现象 结论或解释
钠__在水面上 钠的密度比水___
钠___成小球 钠的熔点___,反应放热
小球在水面上____ 反应产生的 推动小球运动
与水反应发出“嘶嘶”的 声,逐渐变小,最后消失 钠与水___ 反应,产生气体
反应后溶液的颜色逐渐变___ 有___物质(______ )生成
浮
小
熔
低
游
气体
响
剧烈
红
碱性
NaOH
离子方程式:
化学方程式:
2Na+2H2O=2NaOH+H2↑
活泼的金属单质—Na
需用干燥的沙土灭火。钠与H2O反应生成可燃性气体H2,易燃烧和爆炸。
活泼的金属单质—Na
【思考】钠等活泼金属着火时如何灭火?为什么不用水灭火?
Na与盐酸反应时更剧烈
离子方程式:
(实质是Na置换酸电离出的H+)
化学方程式:
【易错提醒】:Na先与酸反应,后面与水反应
遇酸酸优先
活泼的金属单质—Na
【思考】将钠分别投入水和盐酸中,哪个反应更剧烈?写出Na与盐酸反应的离子方程式。
【思考】将钠投入CuSO4溶液中,思考会出现什么现象。
将一块钠投入CuSO4溶液中,实验现象为钠立即熔为小球,并浮在水面四处游动,伴有嘶嘶的声响,同时溶液中有蓝色沉淀生成。请解释上述现象并写出有关化学方程式。
活泼的金属单质—Na
总反应方程式:
第一步(与水反应):
第二步(与盐反应):
生成沉淀+气体
遇酸酸优先,遇盐水在前
钠一定不能从盐溶液中置换出金属单质
活泼的金属单质—Na
2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑
对点即练
(正确的打“√”,错误的打“×”)
(2)钠与O2反应只能生成淡黄色固体Na2O2。( )
×
×
钠与水会反应
√
熔、沸点较低
×
钠与O2在常温和加热条件下分别生成Na2O和Na2O2
1.将适量金属钠投入下列溶液中,有气体放出,但无沉淀生成的是( )
A.盐酸
B.饱和氢氧化钠溶液
C.FeCl3溶液
D.CuSO4溶液
A
消耗水,析出NaOH晶体
Fe(OH)3↓
Cu(OH)2↓
对点即练
2.取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是( )①金属钠先熔化
②在空气中燃烧,放出黄色火花
③燃烧后得到白色固体
④燃烧时火焰为黄色
⑤燃烧后生成淡黄色固体物质A.①② B.①②③
C.①④⑤ D.④⑤
C
√
√
√
3.如图所示。将一小块金属钠投入盛有液体的烧杯中。下列说法错误的是(夹持装置已略去)( )
A.一段时间后,烧杯底部有红色难溶物生成B.若观察到金属钠被煤油浸没,则金属钠的密度比煤油大C.该实验进行过程中可观察到有气泡产生D.反应进行一段时间(反应未结束),此时温度计的读数大于起始时的读数
A
2Na+2H2O=2NaOH+H2↑
Na先与溶液中的水反应,不会有Cu单质生成
反应放热
4.下列有关金属钠的说法错误的是( )A.钠应保存在煤油中B.钠是银白色金属,硬度很大C.钠在反应中易失电子,表现出还原性D.钠与氧气反应的产物与反应条件有关
B
小
5.某位教师设计了钠与硫酸铜溶液反应实验装置(如图,夹持装置省略)。
①注射器针头 ②止水夹 ③短导管 ④细铜丝 ⑤⑦直通管 ⑥ 直角导管 ⑧⑨⑩单孔橡皮塞 乳胶管实验前要将装置中的直角导管
的上端要和直通管⑤的上端高度相当;同时止水夹要夹在导气管的乳胶管上,避免逸出气体。
回答下列问题:(1)向直通管⑤中注满硫酸铜溶液(开始两直通管高度相当),然后小心且迅速地用带有金属钠(置于细铜丝上)和导气管的橡胶塞塞紧试管。可观察到:
a.钠与硫酸铜溶液剧烈反应有无色气体产生,该气体为________, 直通管⑤液面逐渐下降,直通管⑦液面逐渐上升(液面高度如图所示),产生该现象的原因是________________________________,
直通管⑤中有蓝色絮状沉淀生成,该沉淀为________。b.把燃着的火柴置于注射器针头口,打开止水夹。可观察到的现象:______________________________________________。
(2)写出钠与硫酸铜溶液总反应的离子方程式: ____________________________。
(3)实验过程中可观察到蓝色絮状沉淀中有黑色物质,分析发现该黑色物质是氧化铜,写出生成黑色物质的化学方程式__________________________________
H2
反应产生氢气,直通管⑤中压强增加,所以直通管中⑦的液面升高
氢氧化铜沉淀
火柴继续燃烧,产生淡蓝色火焰
2Na+2H2O+Cu2+=Cu(OH)2↓+H2↑+2Na+
Cu(OH)2 CuO+H2O
第一节 钠及其化合物
第一课时 活泼的金属单质—钠
第二章 海水中的重要元素—钠和氯
1.从Na的原子结构认识钠的强还原性(易失去电子);
2.了解Na的物理性质
3.Na在不同条件与O2反应
4.Na与水反应的现象,会分析Na与酸、碱、盐溶液的反应
学习目标 1min
教师点拨 20min
易失去
1.1 Na元素的原子结构及存在
Na
原子结构
存在
自然界中没有游离态的Na,
自然界中钠只以化合态的形式存在
Na
Na+
钠的化学性质非常活泼,表现出很强的还原性
(单质)
(化合物)
活泼的金属单质—Na
(易失去电子)
1.2 钠的单质
钠的物理性质 颜色
状态(常温下) 密度(与煤油比) 硬度(质地) 银白色金属光泽
固体
比煤油大
软
【实验2-1】切割金属钠
实验现象:取出的金属钠表面呈灰黄色 切开后的切口露出了银白色光泽 切口在空气中很快变暗
活泼的金属单质—Na
1.2 钠的单质
【实验2-1】切割金属钠
【思考】金属钠应该如何保存?
氧化钠
(白色固体)
保存在煤油或石蜡油中,以隔绝空气。切割后多余的金属钠要及时放回瓶中。
实验现象:取出的金属钠表面呈灰黄色 切开后的切口露出了银白色光泽 切口在空气中很快变暗
4Na+O2=2Na2O
活泼的金属单质—Na
1.2 钠的单质
【实验2-2】钠在加热条件下与O2反应
实验现象:熔成小球→剧烈燃烧,发出
黄色火焰 →生成淡黄色固体
淡黄色固体
过氧化钠
活泼的金属单质—Na
碱性氧化物
物理变化
化学变化
活泼的金属单质—Na
【思考】钠露置在空气中会有什么变化呢?
1.2 钠的单质
【实验】钠与水的反应
实验现象 结论或解释
钠__在水面上 钠的密度比水___
钠___成小球 钠的熔点___,反应放热
小球在水面上____ 反应产生的 推动小球运动
与水反应发出“嘶嘶”的 声,逐渐变小,最后消失 钠与水___ 反应,产生气体
反应后溶液的颜色逐渐变___ 有___物质(______ )生成
浮
小
熔
低
游
气体
响
剧烈
红
碱性
NaOH
离子方程式:
化学方程式:
2Na+2H2O=2NaOH+H2↑
活泼的金属单质—Na
需用干燥的沙土灭火。钠与H2O反应生成可燃性气体H2,易燃烧和爆炸。
活泼的金属单质—Na
【思考】钠等活泼金属着火时如何灭火?为什么不用水灭火?
Na与盐酸反应时更剧烈
离子方程式:
(实质是Na置换酸电离出的H+)
化学方程式:
【易错提醒】:Na先与酸反应,后面与水反应
遇酸酸优先
活泼的金属单质—Na
【思考】将钠分别投入水和盐酸中,哪个反应更剧烈?写出Na与盐酸反应的离子方程式。
【思考】将钠投入CuSO4溶液中,思考会出现什么现象。
将一块钠投入CuSO4溶液中,实验现象为钠立即熔为小球,并浮在水面四处游动,伴有嘶嘶的声响,同时溶液中有蓝色沉淀生成。请解释上述现象并写出有关化学方程式。
活泼的金属单质—Na
总反应方程式:
第一步(与水反应):
第二步(与盐反应):
生成沉淀+气体
遇酸酸优先,遇盐水在前
钠一定不能从盐溶液中置换出金属单质
活泼的金属单质—Na
2Na+2H2O+CuSO4═Na2SO4+Cu(OH)2↓+H2↑
对点即练
(正确的打“√”,错误的打“×”)
(2)钠与O2反应只能生成淡黄色固体Na2O2。( )
×
×
钠与水会反应
√
熔、沸点较低
×
钠与O2在常温和加热条件下分别生成Na2O和Na2O2
1.将适量金属钠投入下列溶液中,有气体放出,但无沉淀生成的是( )
A.盐酸
B.饱和氢氧化钠溶液
C.FeCl3溶液
D.CuSO4溶液
A
消耗水,析出NaOH晶体
Fe(OH)3↓
Cu(OH)2↓
对点即练
2.取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是( )①金属钠先熔化
②在空气中燃烧,放出黄色火花
③燃烧后得到白色固体
④燃烧时火焰为黄色
⑤燃烧后生成淡黄色固体物质A.①② B.①②③
C.①④⑤ D.④⑤
C
√
√
√
3.如图所示。将一小块金属钠投入盛有液体的烧杯中。下列说法错误的是(夹持装置已略去)( )
A.一段时间后,烧杯底部有红色难溶物生成B.若观察到金属钠被煤油浸没,则金属钠的密度比煤油大C.该实验进行过程中可观察到有气泡产生D.反应进行一段时间(反应未结束),此时温度计的读数大于起始时的读数
A
2Na+2H2O=2NaOH+H2↑
Na先与溶液中的水反应,不会有Cu单质生成
反应放热
4.下列有关金属钠的说法错误的是( )A.钠应保存在煤油中B.钠是银白色金属,硬度很大C.钠在反应中易失电子,表现出还原性D.钠与氧气反应的产物与反应条件有关
B
小
5.某位教师设计了钠与硫酸铜溶液反应实验装置(如图,夹持装置省略)。
①注射器针头 ②止水夹 ③短导管 ④细铜丝 ⑤⑦直通管 ⑥ 直角导管 ⑧⑨⑩单孔橡皮塞 乳胶管实验前要将装置中的直角导管
的上端要和直通管⑤的上端高度相当;同时止水夹要夹在导气管的乳胶管上,避免逸出气体。
回答下列问题:(1)向直通管⑤中注满硫酸铜溶液(开始两直通管高度相当),然后小心且迅速地用带有金属钠(置于细铜丝上)和导气管的橡胶塞塞紧试管。可观察到:
a.钠与硫酸铜溶液剧烈反应有无色气体产生,该气体为________, 直通管⑤液面逐渐下降,直通管⑦液面逐渐上升(液面高度如图所示),产生该现象的原因是________________________________,
直通管⑤中有蓝色絮状沉淀生成,该沉淀为________。b.把燃着的火柴置于注射器针头口,打开止水夹。可观察到的现象:______________________________________________。
(2)写出钠与硫酸铜溶液总反应的离子方程式: ____________________________。
(3)实验过程中可观察到蓝色絮状沉淀中有黑色物质,分析发现该黑色物质是氧化铜,写出生成黑色物质的化学方程式__________________________________
H2
反应产生氢气,直通管⑤中压强增加,所以直通管中⑦的液面升高
氢氧化铜沉淀
火柴继续燃烧,产生淡蓝色火焰
2Na+2H2O+Cu2+=Cu(OH)2↓+H2↑+2Na+
Cu(OH)2 CuO+H2O
