【同步作业】第5单元 化学方程式 单元复习提升(课件版)
文档属性
| 名称 | 【同步作业】第5单元 化学方程式 单元复习提升(课件版) |  | |
| 格式 | pptx | ||
| 文件大小 | 4.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-26 11:04:42 | ||
图片预览








文档简介
(共26张PPT)
参加化学反应的各物质的质量总和①等于反应后生成
适用于所有
内容的各物质的质量总和
化学变化
化学反应前后元素的②)种类、质量及各物质的③质量
宏观总和都不变
质量守
实质
恒定律
微观化学反应前后原子的种类、④数目、】
质量都不变
应用
实验验证。若有气体参加或生成,实验应在⑤密闭容器内进行
定义
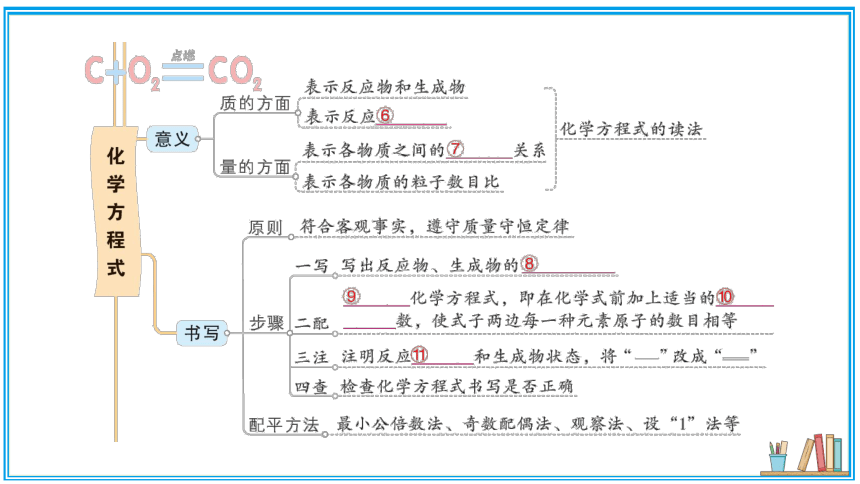
用化学式来表示化学反应的式子
点燃
co,
表示反应物和生成物
质的方面
表示反应⑥条件
意义。
化学方程式的读法
表示各物质之间的⑦质量关系
化学方程式
量的方面
表示各物质的粒子数目比
原则。符合客观事实,遵守质量守恒定律
写。写出反应物、生成物的⑧)化学式
⑨配平化学方程式,即在化学式前加上适当的⑩化净
书写o
步骤
二配计量数,使式子两边每一种元素原子的数目相等
三注注明反应①条件和生成物状态,将“
一”改成“
四查检查化学方程式书写是否正确
配平方法。最小公倍数法、奇数配偶法、观察法、设“1”法等
例1
黔东南州中考]“微观-宏观-符号”三重表征
是化学独特的表示物质及其变化的方法。如图是
液化石油气成分之一燃烧前后分子种类变化的微
观示意图,下列说法正确的是(
氢原子
点燃
O
氧原子
甲
乙
丙
丁
○
碳原子
○
氢原子
,点燃
○
氧原子
丙
丁
碳原子
A.生成丙与丁物质的质量比为11:6
B.反应前后各元素的化合价均不变
C.参加反应的甲与乙的分子个数比为1:1
D.甲中碳、氢元素质量比为3:8
解析:由微观反应示意图可知,该反应是C3H。和O,在点
燃的条件下反应生成C0,和H,O,化学方程式为C3Hs+
点燃
50,
3C0,+4H,0。由化学方程式可知,生成丙与丁物
质的质量比为(44×3):(18×4)=11:6;在该反应中,有单
质参与反应,且生成物全部是化合物,所以一定存在元素
化合价的改变;由化学方程式可知,参加反应的甲(CH、)
与乙(0,)的分子个数比为1:5;甲物质的化学式为C3H,
其中碳、氢元素质量比为(12×3):(1×8)=9:2。
冲刺训练1
[宜昌中考改编]
硅是重要的半导体材料,X+H,
一定条件
3HCl+Si(高纯)是工
业制硅流程中的化学反应之一
下列说法错误的是(
C
A.反应中元素种类不变
B.反应中各原子数目不变
C.X的化学式是SiHCI2
D.该反应遵守质量守恒定律
例2金属钨(W)可作灯泡的灯丝,钨合金材料坚硬、
耐磨、耐热。H,与W0,在1000℃条件下反应可得到
金属钨和水。工业上制WO,的流程如图所示:
黑钨矿
在空气中
Na,WO
H,O
碳酸钠
混合焙烧
H,WO.
加热
热的浓盐酸
WO
(1)4FeW0,+4Na,C0,+0,△4Na,Ww0,+2Fe,0,+
4
参加化学反应的各物质的质量总和①等于反应后生成
适用于所有
内容的各物质的质量总和
化学变化
化学反应前后元素的②)种类、质量及各物质的③质量
宏观总和都不变
质量守
实质
恒定律
微观化学反应前后原子的种类、④数目、】
质量都不变
应用
实验验证。若有气体参加或生成,实验应在⑤密闭容器内进行
定义
用化学式来表示化学反应的式子
点燃
co,
表示反应物和生成物
质的方面
表示反应⑥条件
意义。
化学方程式的读法
表示各物质之间的⑦质量关系
化学方程式
量的方面
表示各物质的粒子数目比
原则。符合客观事实,遵守质量守恒定律
写。写出反应物、生成物的⑧)化学式
⑨配平化学方程式,即在化学式前加上适当的⑩化净
书写o
步骤
二配计量数,使式子两边每一种元素原子的数目相等
三注注明反应①条件和生成物状态,将“
一”改成“
四查检查化学方程式书写是否正确
配平方法。最小公倍数法、奇数配偶法、观察法、设“1”法等
例1
黔东南州中考]“微观-宏观-符号”三重表征
是化学独特的表示物质及其变化的方法。如图是
液化石油气成分之一燃烧前后分子种类变化的微
观示意图,下列说法正确的是(
氢原子
点燃
O
氧原子
甲
乙
丙
丁
○
碳原子
○
氢原子
,点燃
○
氧原子
丙
丁
碳原子
A.生成丙与丁物质的质量比为11:6
B.反应前后各元素的化合价均不变
C.参加反应的甲与乙的分子个数比为1:1
D.甲中碳、氢元素质量比为3:8
解析:由微观反应示意图可知,该反应是C3H。和O,在点
燃的条件下反应生成C0,和H,O,化学方程式为C3Hs+
点燃
50,
3C0,+4H,0。由化学方程式可知,生成丙与丁物
质的质量比为(44×3):(18×4)=11:6;在该反应中,有单
质参与反应,且生成物全部是化合物,所以一定存在元素
化合价的改变;由化学方程式可知,参加反应的甲(CH、)
与乙(0,)的分子个数比为1:5;甲物质的化学式为C3H,
其中碳、氢元素质量比为(12×3):(1×8)=9:2。
冲刺训练1
[宜昌中考改编]
硅是重要的半导体材料,X+H,
一定条件
3HCl+Si(高纯)是工
业制硅流程中的化学反应之一
下列说法错误的是(
C
A.反应中元素种类不变
B.反应中各原子数目不变
C.X的化学式是SiHCI2
D.该反应遵守质量守恒定律
例2金属钨(W)可作灯泡的灯丝,钨合金材料坚硬、
耐磨、耐热。H,与W0,在1000℃条件下反应可得到
金属钨和水。工业上制WO,的流程如图所示:
黑钨矿
在空气中
Na,WO
H,O
碳酸钠
混合焙烧
H,WO.
加热
热的浓盐酸
WO
(1)4FeW0,+4Na,C0,+0,△4Na,Ww0,+2Fe,0,+
4
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
