广东省湛江师范学院附属中学、湛江附中东方实验学校2014-2015学年高二上学期期中联考化学(理)
文档属性
| 名称 | 广东省湛江师范学院附属中学、湛江附中东方实验学校2014-2015学年高二上学期期中联考化学(理) |  | |
| 格式 | zip | ||
| 文件大小 | 372.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-01-12 16:02:30 | ||
图片预览




文档简介
1.某化合物的结构(键线式)及球棍模型如下:
Et代表的基团为—CH2CH3
该有机分子的核磁共振波谱图如下(单位是ppm)。
下列关于该有机物的叙述正确的是( )
A.该有机物不同化学环境的氢原子有8种 B.该有机物属于芳香族化合物
C.该有机物分子式为C9H14 O4 D.1 mol该有机物完全燃烧可以产生7 mol水
2.下列表示方法正确的是( )
① H2S分子的比例模型: ② NH4Cl电子式:
③ 苯乙醛结构简式: ④ 丙烷分子的球棍模型:
A.①④ B.①②④ C.①②③④ D.②③
3.下列物质中,属于酚类的是( )
4.下列烷烃的命名正确的是( )
A.2,4-二乙基戊烷 B.4-甲基-3-乙基已烷
C.2-甲基-3-丙基戊烷 D. 2,3,3-三甲基戊烷
5.某气态烃0.5 mol能与1 mol HCl完全加成,加成后产物分子上的氢原子又可与4 mol Cl2发生取代反应,则此气态烃可能是( )
A.CH2===CH—CH3 B.CH2===CH2C. CH2===CH—CH===CH2 D.CH2===C(CH3)2
6.下列说法正确的是( )
A.用酸性KMnO4溶液鉴别乙烯和乙炔
B.将铁屑、溴水、苯混合可制得溴苯
C.调查发现有些装饰程度较高的居室中,由装饰材料缓慢释放出来的化学污染物浓度过高,影响健康,这些污染物主要是甲酸和SO2等气体
D.将铜丝在酒精灯火焰上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
7.在一定条件下,等物质的量的乙烯和苯分别和足量氢气发生加成反应,消耗氢气的物质的量之比为( )。
A.1∶1 B.1∶2 C.1∶3 D.1∶4
8.下列关于乙醇的说法正确的是( )
A.乙醇在水溶液中能电离出少量的H+,所以乙醇是电解质
B.乙醇结构中有—OH,所以乙醇显碱性
C.乙醇分子中只有烃基上的氢原子可被钠置换出来
D.乙醇是一种很好的溶剂,能溶解许多无机化合物和有机化合物,人们用白酒浸泡中药制成药酒就是利用了这一性质
9.巴豆酸的结构简式为CH3—CH=CH—COOH。现有①氯化氢、②溴水、③纯碱溶液、④2-丁醇、⑤酸性KMnO4溶液,试根据巴豆酸的结构特点,判断在一定条件下,能与巴豆酸反应的物质是( )
A.只有②④⑤ B.只有①③④ C.只有①②③④ D.①②③④⑤
10.下列反应中,属于取代反应的是( )
①CH3CH=CH2+Br2CH3CHBrCH2Br ②CH3CH2OH CH2=CH2↑ +H2O
③CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O ④C6H6+HNO3C6H5NO2+H2O
A. ①② B.③④ C.①③ D.②④
11.对下图所示有机物分子的叙述错误的是( )
A.能发生碱性水解,1 mol该有机物完全反应消耗8 mol NaOH
B.常温下,能与Na2CO3溶液反应放出CO2
C.与稀硫酸共热,能生成两种有机物
D.该有机物的分子式为C14H10O9
12.下列离子方程式正确的是( )
A.实验室用大理石与醋酸反应制取二氧化碳:CaCO3+2H+=Ca2++CO2↑+H2O
B.氯乙酸与氢氧化钠溶液共热: CH2ClCOOH+OH- →CH2ClCOO-+H2O
C.苯与浓硫酸、浓硝酸的混合液共热制硝基苯:( )
D.用银氨溶液检验乙醛中的醛基:
CH3CHO +2[Ag(NH3) 2]++2OH-CH3COO-+NH4+ +3NH3+2Ag↓+ H2O
13.下列卤代烃中,能发生消去反应且能生成两种单烯烃的是( )
14. NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.0.1 mol C3H6Cl2中化学键总数为
B.42 g乙烯中含碳原子数为3
C.标准状况下,1L苯完全燃烧生成的气态产物的分子数为(6/22. 4)
D.0.1 mol乙醇完全燃烧所消耗的氧分子数一定为0.3
15.如下表所示,为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是( )
不纯物质
除杂试剂
分离方法
A
苯(甲苯)
KMnO4(酸化),NaOH溶液
分液
B
NH4Cl溶液(FeCl3)
NaOH溶液
过滤
C
乙酸乙酯(乙酸)
KOH溶液,水
分液
D
CO3(SO2)
Na2CO3
洗气
二、双项选择题(本题包括5小题,每小题4分,共20分。每小题有两个选项符合题意)
16.丙烯醛的结构简式为CH2=CHCHO,下列有关其性质的叙述中不正确的是( )
A.能使溴水褪色 B.能与过量的氢气充分反应生成丙醛
C.不能发生银镜反应 D.能被新制的氢氧化铜氧化
17.现代家居装修材料中,普遍存在着甲醛、苯及苯的同系物等有毒物质,如果不注意处理就会对人体产生极大的危害。按照有机物官能团的分类,甲醛属于醛。下面各项对有机物的分类方法与此方法相同的是( )
18.鼠尾草酚可用于防治骨质疏松,结构如图所示,下列说法正确的是( )
A.鼠尾草酚属于芳香烃
B.鼠尾草酚能与FeCl3溶液发生显色反应
C.鼠尾草酚分子式C18H29 O4
D.1mol鼠尾草酚与NaOH溶液反应最多消耗3molNaOH
19.下列物质不能和溴水发生化学反应而能使酸性高锰酸钾退色的是( )
A.C2H5OH B.苯酚 C.甲苯 D.乙醛
20.莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物(见下图)的说法正确的是( )
A.两种酸都能与溴水发生反应
B.鞣酸分子与莽草酸分子相比多了两个碳碳双键
C.1mol莽草酸完全燃烧消耗7molO2
D等物质的量的两种酸与足量氢氧化钠反应,消耗氢氧化钠的量相同
第二卷 非选择题(共50分)
21.(12分)PNA是一种具有良好的热稳定性、耐腐蚀性和抗水性的高分子化合物,常用作塑化剂,其合成路线如下图所示:
已知: ①R1CH=CHR2R1COOH + R2COOH (R1、R2代表烃基)
②
请回答:
(1)E→F的反应类型是 。
(2)C含有的官能团名称是 。
(3)A分子中只有一个氯原子,A→B的化学方程式是 。(注明反应条件)
(4)D能发生银镜反应,且分子中有支链,D的结构简式是 。
(5)E的结构简式是 。
(6)C与F在一定条件下生成增塑剂PNA的反应的化学方程式是: 。(不
用注明反应条件)
22.(12分)对二甲苯(英文名称p-xylene,缩写为PX)是一种低毒化合物,也是聚酯工业的重要原料,主要用于生产对苯二甲酸(PTA),对苯二甲酸再和乙二醇(EG)反应生成聚对苯二甲酸乙二醇酯(PET)。国内对二甲苯产量增长步伐放缓,供应缺口加大,近一半的PX依靠进口。以PX为主要原料生产PET的一种路线如下:
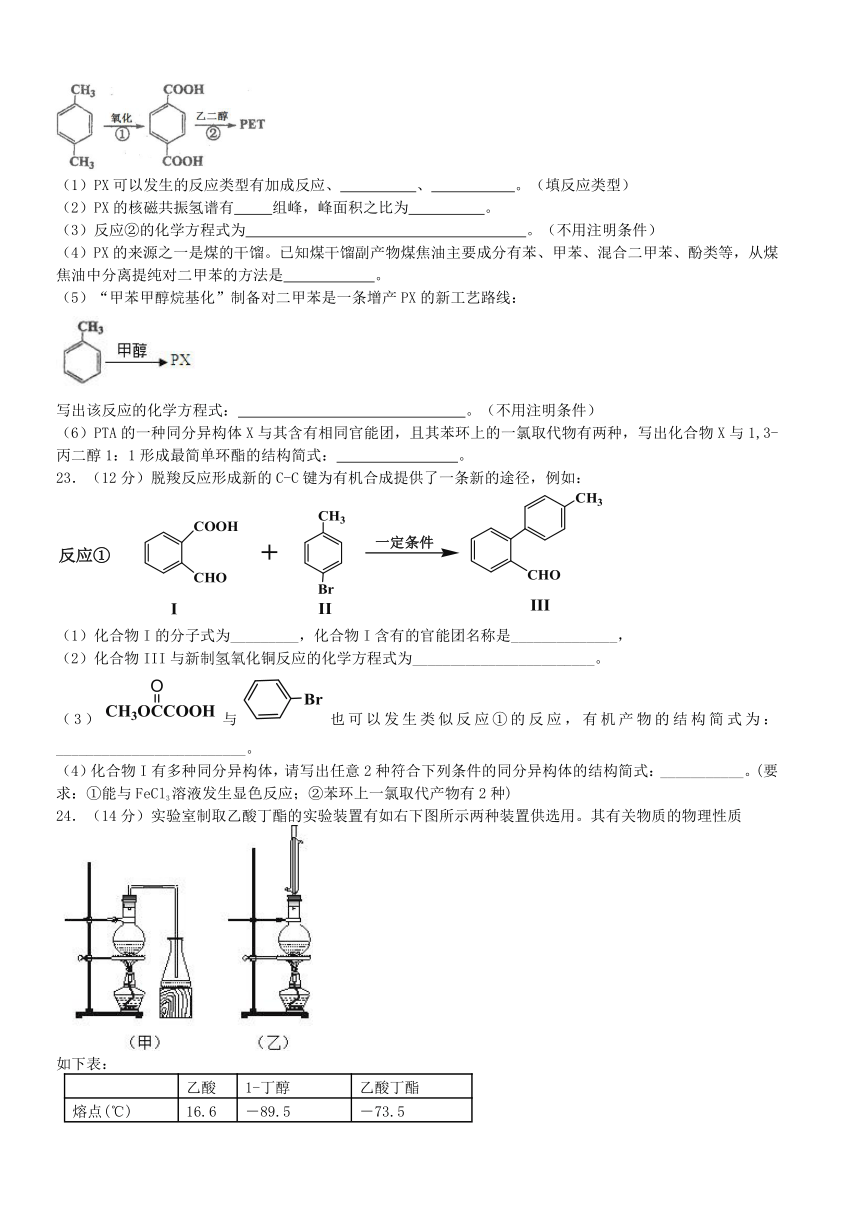
(1)PX可以发生的反应类型有加成反应、 、 。(填反应类型)
(2)PX的核磁共振氢谱有 组峰,峰面积之比为 。
(3)反应②的化学方程式为 。(不用注明条件)
(4)PX的来源之一是煤的干馏。已知煤干馏副产物煤焦油主要成分有苯、甲苯、混合二甲苯、酚类等,从煤焦油中分离提纯对二甲苯的方法是 。
(5)“甲苯甲醇烷基化”制备对二甲苯是一条增产PX的新工艺路线:
写出该反应的化学方程式: 。(不用注明条件)
(6)PTA的一种同分异构体X与其含有相同官能团,且其苯环上的一氯取代物有两种,写出化合物X与1,3-丙二醇1:1形成最简单环酯的结构简式: 。
23.(12分)脱羧反应形成新的C-C键为有机合成提供了一条新的途径,例如:
(1)化合物I的分子式为_________,化合物I含有的官能团名称是______________,
(2)化合物III与新制氢氧化铜反应的化学方程式为________________________。
(3)与也可以发生类似反应①的反应,有机产物的结构简式为:_________________________。
(4)化合物I有多种同分异构体,请写出任意2种符合下列条件的同分异构体的结构简式:___________。(要求:①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种)
24.(14分)实验室制取乙酸丁酯的实验装置有如右下图所示两种装置供选用。其有关物质的物理性质
如下表:
?
乙酸
1-丁醇
乙酸丁酯
熔点(℃)
16.6
-89.5
-73.5
沸点(℃)
117.9
117
126.3
密度(g/cm3)
1.05
0.81
0.88
水溶性
互溶
可溶(9g/100g水)
微溶
(1)制取乙酸丁酯的装置应选用_______(填“甲”或“乙”)。不选另一种装置的理由是????????????????????? 。
(2)该实验生成物中除了主产物乙酸丁酯外,还可能生成的有机副产物有(写出结构简式):??????????????????????? 、??????????????????? 。
(3)酯化反应是一个可逆反应,为提高1-丁醇的利用率,可采取的措施是????? 。
(4)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是___________(选填答案编号)。
?
(5)有机物的分离操作中,经常需要使用分液漏斗等仪器。使用分液漏斗前必须??? ;某同学在进行分液操作时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还可能? ?????????????????????。
参考答案
1.B【解析】从核磁共振波谱图中可以读出,一共有8个峰,即有8种不同环境的氢原子,A项正确;B项,从键线式中可以看出,其中不含有苯环,故不属于芳香族化合物,B项错误;C项,对比键线式,错误;D项该有机物共含有12个原子,故1 mol完全燃烧可得6 mol水,错误。
3.B【解析】苯环()与羟基(—OH)直接相连的有机化合物属于酚类。
4.D【解析】2,4-二乙基戊烷 应为3,5-二甲基庚烷,4-甲基-3-乙基已烷 应该为3-甲基-4-乙基已烷,2-甲基-3-丙基戊烷应该为2-甲基-3-乙基已烷,D正确。
5.C【解析】0.5 mol烃与1 mol HCl加成,则每个烃分子中多加了2个H和2个Cl,加成后0.5 mol产物可与4 mol Cl2发生取代反应,说明每个分子中有8个氢,那么与HCl加成前分子中应有6个氢原子,所以原来的烃是CH2===CH—CH===CH2。
7.C【解析】苯加成后生成环己烷(C6H12),1 mol苯消耗氢气3 mol;1 mol乙烯消耗氢气1 mol。
11.C【解析】A、该分子中含有酯基,可以在碱性条件下水解,该分子中还有5个酚羟基和1个羧基,且酯基水解后的产物中还有酚羟基,所以1 mol该有机物完全反应消耗8 mol NaOH,正确;B、分子中含有羧基,可以与碳酸钠溶液反应生成二氧化碳气体,正确;C、在酸性条件下水解生成的有机产物是一种,产物;D、根据其结构简式判断其分子式,正确,答案选C。
12.D【解析】 :A.醋酸是弱酸,不能写离子形式,错误;B.氯乙酸与氢氧化钠溶液共热时羧基和Cl原子都发生反应,错误;C.苯与浓硫酸、浓硝酸的混合液共热制硝基苯和水,错误;D.反应符合事实,离子拆写符合原则,正确。
15.A【解析】A.苯中甲苯容易被硫酸酸化KMnO4溶液氧化为苯甲酸,然后利用酸碱中和反应,用NaOH溶液中和,再利用苯不能溶于水,而苯甲酸钠溶于水的性质,通过分液的方法分离得到,正确;B .NH4Cl溶液混有FeCl3,若加入NaOH溶液,二者都会发生反应,所以不能达到分离的目的,错误; C.乙酸乙酯中混有乙酸,应该利用乙酸能够与碳酸钠发生反应产生容易溶于水的物质,而乙酸乙酯难溶于饱和碳酸钠溶液,密度比溶液小的性质,用饱和碳酸钠溶液,通过分液的方法分离得到;若用KOH溶液,则酯也会发生水解反应,错误;D.CO3气体中混有SO2气体,应该用饱和碳酸氢钠溶液来除去去,错误。
16.BC【解析】判断有机物的性质,关键是找出有机物中含有的官能团。根据有机物的结构简式可知,分子中含有的官能团有碳碳双键和醛基,所以选项BC是错误的,与过量的氢气充分反应生成1-丙醇,能发生银镜反应,AD正确,答案选BC。
20.AC【解析】A该物质含碳碳双键,因此能与溴水发生加成反应。B鞣酸不含碳碳双键,因此B选项是错误的。C莽草酸燃烧生成二氧化碳和水,列反应方程式出来即可知1mol莽草酸完全燃烧消耗7molO2。D选项醇羟基不能与氢氧化钠反应,因此1摩尔莽草酸消耗1摩尔氢氧化钠。1鞣酸消耗4摩尔的氢氧化钠。所以答案选AC
21.(12分)【答案】(1)加成反应(或还原反应)(2分,漏“反应”二字扣1分)
(2)羧基(2分)
(3) [2分,漏写条件扣1分,将H2O写作条件,生成HCl的(或产物中漏写H2O的)扣1分]
(4) (2分) (5) (2分)
(2分)
注:可逆号写成箭头不扣分,聚合物不写端基原子不扣分,但水的系数是2n;高聚物漏写n或链节写错,但反应物结构简式对的扣1分,反应物和生成物写对配平错(或漏写水)扣1分。
【解析】(1)对二甲苯属苯的同系物,具有苯的同系物的性质。
(2)对二甲苯苯环上的四个氢原子等效,而甲基上的六个氢原子等效,所以峰面重叠则为6:4。
(3)缩合聚合反应,注意参照课本书写方法。
(4)分离相溶的混合物,采用蒸馏或分馏的方法。
(5)可以先根据题意写出反应物和PX,最后用原子守恒的方法写出小分子。
(6)根据含有相同的官能团,且一氯代物有两种,可知是邻苯二甲酸。
23.(12分)(1)C8H6O3 (2分), 羧基,醛基(2分)
(2)(2分)
(3)(2分)(4), , (4分,任意两种)。
【解析】(1)根据化合物I的结构简式可得该化合物的分子式为C8H6O3,化合物I含有的官能团名称是醛基、羧基;化合物I燃烧的方程式是:C8H6O3+8O28CO2+3H2O;可见1mol的化合物I完全燃烧消耗8mol的氧气;(2)在化合物III中含有1个醛基,所以能够与新制氢氧化铜反应,反应类型乙醛与新制氢氧化铜的反应,反应的化学方程式为;(3)与也可以发生类似反应①的反应,有机产物的结构简式为:;(4)化合物I有多种同分异构体,其中符合条件①能与FeCl3溶液发生显色反应;②苯环上一氯取代产物有2种的同分异构体的结构简式:, , 。
24.(1)(1分)乙。(3分)由于反应物乙酸、1-丁醇的沸点低于产物乙酸丁酯的沸点,若采用甲装置,会造成反应物的大量挥发,降低了反应物的转化率,乙装置含有冷凝回流装置,可以冷凝回流反应物,提高反应物的转化率,所以选乙装置。
(2)(2分)CH3CH2CH2CH2OCH2CH2CH2CH3????CH3CH2CH=CH2。
(3)(2分)①增加乙酸浓度②减小生成物浓度(或移走生成物)。
(4)(2分)AB。
(5)(2分)检查是否漏水或堵塞;(2分)分液漏斗上口玻璃塞未打开(或漏斗内部未与大气相通,或玻璃塞上的凹槽未与漏斗口上的小孔对准)。
【解析】(1)由于反应物乙酸、1-丁醇的沸点低于产物乙酸丁酯的沸点,若采用甲装置,会造成反应物的大量挥发,降低了反应物的转化率,乙装置含有冷凝回流装置,可以冷凝回流反应物,提高反应物的转化率,所以选乙装置。
(2)因为1-丁醇的浓硫酸、加热条件下可以发生消去反应和分子间脱水反应,所以可能生成的副产物有,CH3CH2CH2CH2OCH2CH2CH2CH3????CH3CH2CH=CH2。
(3)①增加乙酸浓度②减小生成物浓度(或移走生成物)。
(4)反应后的混合物中,乙酸能和水互溶,1-丁醇能溶于水。所以可加入饱和碳酸钠溶液振荡,进一步减少乙酸丁酯在水中的溶解度,然后分液可得乙酸丁酯,故肯定需要化学操作是AB。
同课章节目录
