2024新高考化学高考专题复习--专题九化学反应的热效应(含答案) (2)
文档属性
| 名称 | 2024新高考化学高考专题复习--专题九化学反应的热效应(含答案) (2) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-28 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2024新高考化学高考专题复习
专题九 化学反应的热效应
五年高考
考点1 化学反应中的能量变化
1.(2023北京,13,3分)一种分解氯化铵实现产物分离的物质转化关系如下,其中b、d代表MgO或Mg(OH)Cl中的一种。下列说法正确的是( )
A.a、c分别是HCl、NH3
B.d既可以是MgO,也可以是Mg(OH)Cl
C.已知MgCl2为副产物,则通入水蒸气可减少MgCl2的产生
D.等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
答案 C
2.(2022浙江1月选考,18,2分)相关有机物分别与氢气发生加成反应生成1 mol环己烷()的能量变化如图所示:
下列推理不正确的是( )
A.2ΔH1≈ΔH2,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
B.ΔH2<ΔH3,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
C.3ΔH1<ΔH4,说明苯分子中不存在三个完全独立的碳碳双键
D.ΔH3-ΔH1<0,ΔH4-ΔH3>0,说明苯分子具有特殊稳定性
答案 A
3.(2021山东,14,4分)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH-+CH3O-
能量变化如图所示。已知为快速平衡,下列说法正确的是( )
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在COH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
答案 B
4.(2021浙江1月选考,24,2分)在298.15 K、100 kPa条件下,N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,N2(g)、H2(g)和NH3(g)的比热容分别为29.1、28.9和35.6 J·K-1·mol-1。一定压强下,1 mol反应中,反应物[N2(g)+3H2(g)]、生成物[2NH3(g)]的能量随温度T的变化示意图合理的是( )
答案 B
5.(2020浙江7月选考,22,2分)关于下列ΔH的判断正确的是( )
C(aq)+H+(aq) HC(aq) ΔH1
C(aq)+H2O(l) HC(aq)+OH-(aq) ΔH2
OH-(aq)+H+(aq) H2O(l) ΔH3
OH-(aq)+CH3COOH(aq) CH3COO-(aq)+H2O(l) ΔH4
A.ΔH1<0 ΔH2<0 B.ΔH1<ΔH2 C.ΔH3<0 ΔH4>0 D.ΔH3>ΔH4
答案 B
6.(2023全国甲,28,15分)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①3O2(g) 2O3(g) K1 ΔH1=285 kJ·mol-1
②2CH4(g)+O2(g) 2CH3OH(l) K2 ΔH2=-329 kJ·mol-1
反应③CH4(g)+O3(g) CH3OH(l)+O2(g)的ΔH3= kJ·mol-1,平衡常数K3= (用K1、K2表示)。
(2)电喷雾电离等方法得到的M+(Fe+、Co+、Ni+等)与O3反应可得MO+。MO+与CH4反应能高选择性地生成甲醇。分别在300 K和310 K下(其他反应条件相同)进行反应MO++CH4 M++CH3OH,结果如下图所示。图中300 K的曲线是 (填“a”或“b”)。300 K、60 s时MO+的转化率为 (列出算式)。
(3)MO+分别与CH4、CD4反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH4示例)。
(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是 (填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则MO+与CD4反应的能量变化应为图中曲线 (填“c”或“d”)。
(ⅲ)MO+与CH2D2反应,氘代甲醇的产量CH2DOD CHD2OH(填“>”“=”或“<”)。若MO+与CHD3反应,生成的氘代甲醇有 种。
答案 (1)-307 (2)b 1-10-0.1 (3)(ⅰ)Ⅰ (ⅱ)c (ⅲ)< 2
考点2 热化学方程式的书写 盖斯定律的应用
1.(2022重庆,13,3分)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH4)2SO4的离子键强弱,设计如图所示的循环过程,可得ΔH4/(kJ·mol-1)为( )
A.+533 B.+686 C.+838 D.+1 143
答案 C
2.(2022浙江6月选考,18,2分)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H2 O2 H2O2 H2O
能量/kJ·mol-1 249 218 39 10 0 0 -136 -242
可根据HO(g)+HO(g) H2O2(g)计算出H2O2中氧氧单键的键能为214 kJ·mol-1。下列说法不正确的是( )
A.H2的键能为436 kJ·mol-1
B.O2的键能大于H2O2中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:HOOD.H2O(g)+O(g) H2O2(g) ΔH=-143 kJ·mol-1
答案 C
3.(2021北京,14,3分)丙烷经催化脱氢可制丙烯:C3H8 C3H6+H2。600 ℃,将一定浓度的CO2与固定浓度的C3H8通过含催化剂的恒容反应器,经相同时间,流出的C3H6、CO和H2浓度随初始CO2浓度的变化关系如图。
已知:①C3H8(g)+5O2(g) 3CO2(g)+4H2O(l) ΔH=-2 220 kJ·mol-1
②C3H6(g)+O2(g) 3CO2(g)+3H2O(l) ΔH=-2 058 kJ·mol-1
③H2(g)+O2(g) H2O(l) ΔH=-286 kJ·mol-1
下列说法不正确的是( )
A.C3H8(g) C3H6(g)+H2(g)
ΔH=+124 kJ·mol-1
B.c(H2)和c(C3H6)变化差异的原因:CO2+H2 CO+H2O
C.其他条件不变,投料比c(C3H8)/c(CO2)越大,C3H8转化率越大
D.若体系只有C3H6、CO、H2 和H2O生成,则初始物质浓度c0与流出物质浓度c之间一定存在:3c0(C3H8)+c0(CO2)=c(CO)+c(CO2)+3c(C3H8)+3c(C3H6)
答案 C
4.(2021浙江1月选考,20,2分)已知共价键的键能与热化学方程式信息如下表:
共价键 H—H H—O
键能/(kJ·mol-1) 436 463
热化学方程式 2H2(g)+O2(g) 2H2O(g) ΔH=-482 kJ·mol-1
则2O(g) O2(g)的ΔH为( )
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
答案 D
三年模拟
A组 基础题组
考点1 化学反应中的能量变化
1.(2023吉林市二调,10)1868年狄青和洪特发现了用空气中的氧气来氧化氯化氢气体制取氯气的方法:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)。该反应的能量变化如图所示,下列说法正确的是( )
A.该反应为吸热反应
B.若H2O为液态,则生成物总能量将变大
C.该反应发生时向环境释放能量
D.断开旧化学键吸收的总能量大于形成新化学键所释放的总能量
答案 C
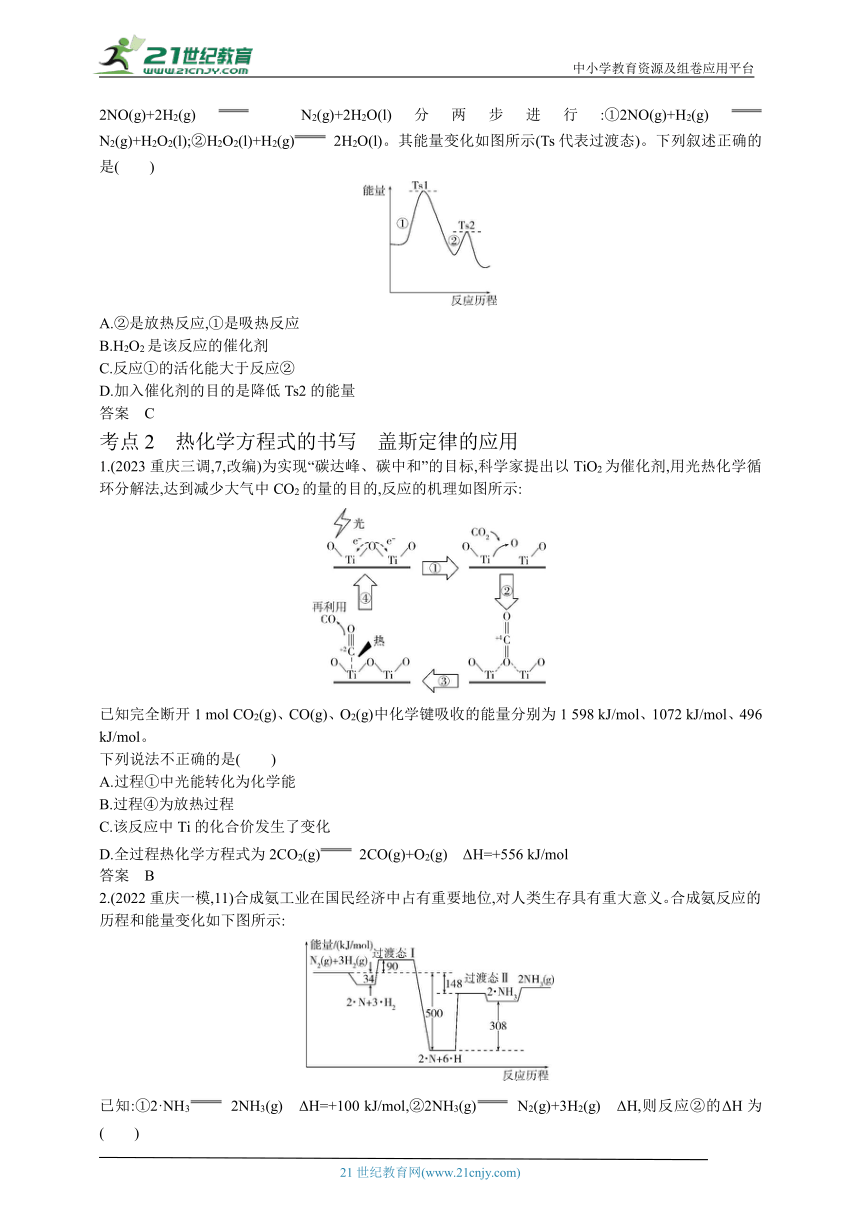
2.(2023河北衡水二中三调,8)氮的氧化物转化是环境化学热点问题之一。研究发现,H2还原NO的反应2NO(g)+2H2(g) N2(g)+2H2O(l)分两步进行:①2NO(g)+H2(g) N2(g)+H2O2(l);②H2O2(l)+H2(g) 2H2O(l)。其能量变化如图所示(Ts代表过渡态)。下列叙述正确的是( )
A.②是放热反应,①是吸热反应
B.H2O2是该反应的催化剂
C.反应①的活化能大于反应②
D.加入催化剂的目的是降低Ts2的能量
答案 C
考点2 热化学方程式的书写 盖斯定律的应用
1.(2023重庆三调,7,改编)为实现“碳达峰、碳中和”的目标,科学家提出以TiO2为催化剂,用光热化学循环分解法,达到减少大气中CO2的量的目的,反应的机理如图所示:
已知完全断开1 mol CO2(g)、CO(g)、O2(g)中化学键吸收的能量分别为1 598 kJ/mol、1072 kJ/mol、496 kJ/mol。
下列说法不正确的是( )
A.过程①中光能转化为化学能
B.过程④为放热过程
C.该反应中Ti的化合价发生了变化
D.全过程热化学方程式为2CO2(g) 2CO(g)+O2(g) ΔH=+556 kJ/mol
答案 B
2.(2022重庆一模,11)合成氨工业在国民经济中占有重要地位,对人类生存具有重大意义。合成氨反应的历程和能量变化如下图所示:
已知:①2·NH3 2NH3(g) ΔH=+100 kJ/mol,②2NH3(g) N2(g)+3H2(g) ΔH,则反应②的ΔH为( )
A.+92 kJ/mol B.-92 kJ/mol C.+192 kJ/mol D.+148 kJ/mol
答案 A
B组 综合题组
1.[2023河北学业水平选择性考试(一),6]反应的能量与反应历程的关系如下图所示。下列说法错误的是( )
A.第1步决定整个反应的快慢
B.第2步为放热过程
C.该反应的焓变大小取决于第1、2、3步正、逆反应的活化能大小
D.该反应适宜在碱性条件下进行
答案 C
2.(2023山西临汾一模,10)不同含金化合物催化乙烯加氢的反应历程如下图所示:
下列说法正确的是( )
A.从图中可得1 mol C2H4(g)具有的能量比1 mol C2H6(g)的能量高
B.过渡态1比过渡态2物质的稳定性弱
C.在催化剂AuP催化下,该反应的ΔH=-233.7 kJ·mol-1
D.相比催化剂AuP,AuF催化乙烯加氢的效果更好
答案 B
3.(2023安徽蚌埠二模,12)已知复杂反应的速率由反应历程中活化能最大的一步基元反应决定。卤代烃的取代反应有以下两种反应历程,其反应过程中的能量变化如图所示:
下列说法中错误的是( )
A.卤代烃的取代为放热反应
B.SN1反应速率与c(Nu-)和c(R3CX)相关
C.SN2反应速率与c(RX)和c(Nu-)相关
D.SN1机理为两步反应,SN2机理为一步反应
答案 B
4.(2022湖北襄阳二模,11)苯的亲电取代反应分两步进行,可表示为E++ +H+,生成中间体的一步是加成过程,中间体失去H+的一步是消除过程,其机理亦称加成—消除机理。苯的亲电取代反应进程和能量的关系如图,下列说法错误的是( )
A.第一步反应为苯亲电取代的决速步骤
B.E1与E2的差值为总反应的焓变
C.中间体的能量比苯的高,稳定性比苯的差
D.反应过程中,环上碳原子的杂化类型发生了变化
答案 B
5.(2022福建龙岩三检,9)在Fe+催化下乙烷氧化的反应机理如图所示(图中为副反应)。下列说法正确的是( )
A.FeO+、N2均为反应中间体
B.X既含极性共价键也含非极性共价键
C.该机理涉及的反应均为氧化还原反应
D.每生成1 mol CH3CHO,消耗的N2O大于2 mol
答案 D
6.(2022河北邯郸二模,8)据报道,我国科学家研制出以石墨烯为载体的催化剂,在25 ℃下用H2O2直接将CH4转化为含氧有机物,其主要原理如图所示。下列说法不正确的是( )
A.石墨烯为载体的催化剂的作用是破坏C—H键
B.步骤ⅴ、ⅵ的总反应方程式是H2O2+HCHO HCOOH+H2O
C.步骤ⅱ得到的产物所有原子可能共面
D.上述反应过程中,用虚线圆框住的部分表示不稳定的自由基状态
答案 C
7.(2022重庆育才中学二诊,8)甲醇水蒸气催化重整是获取H2的重要方法,反应CH3OH(g)+H2O(g) CO2(g)+3H2(g) ΔH>0,能量变化如图1所示。830 ℃时,相同时间内向反应体系中投入一定量CaO做对比实验,结果如图2所示,下列说法中正确的是( )
图1 图2
A.该反应的ΔH=(a-b-c) kJ·mol-1
B.CaO表面积越大,吸收CO2效果越好
C.该反应在低温下能自发进行
D.选择适当催化剂降低ΔH3可显著提高催化重整反应速率
答案 B
考法训练
考法 反应历程与能量图像分析
1.(2023浙江1月选考,14,3分)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知O2(g)和Cl2(g)的相对能量为0],下列说法不正确的是( )
A.E6-E3=E5-E2
B.可计算Cl—Cl键能为2(E2-E3) kJ·mol-1
C.相同条件下,O3的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:ClO(g)+O(g) O2(g)+Cl(g) ΔH=(E5-E4) kJ·mol-1
答案 C
2.(2022辽宁,10,3分)利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021年诺贝尔化学奖。某Diels-Alder反应催化机理如下。下列说法错误的是 ( )
A.总反应为加成反应 B.Ⅰ和Ⅴ互为同系物
C.Ⅵ是反应的催化剂 D.化合物X为H2O
答案 B
3.(2022浙江1月选考,24,2分)某课题组设计一种固定CO2的方法,原理如图。下列说法不正确的是( )
A.反应原料中的原子100%转化为产物
B.该过程在化合物X和I-催化下完成
C.该过程仅涉及加成反应
D.若原料用,则产物为
答案 C
4.(2021重庆,10,3分)“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物N2O和CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热ΔH=-283 kJ/mol,则2N2O(g) 2N2(g)+O2(g)的反应热ΔH(kJ/mol)为( )
A.-152 B.-76 C.+76 D.+152
答案 A
5.(2023辽宁沈阳联合模拟,11,改编)下图是用钌(Ru)基催化剂催化CO2(g)和H2(g)的反应示意图,当反应生成46 g液态HCOOH时放出31.2 kJ的热量。下列说法错误的是( )
A.反应历程中存在极性键、非极性键的断裂与形成
B.图示中物质Ⅰ为该反应的催化剂,物质Ⅱ、Ⅲ为中间产物
C.将反应Ⅰ、Ⅱ、Ⅲ相加可得总反应
D.由题意知:HCOOH(l) CO2(g)+H2(g) ΔH=+31.2 kJ·mol-1
答案 A
6.(2022辽宁选择性考试二模,10)丙烯(CH2CHCH3)在一定条件下与HX发生加成反应生成两种卤代烃的能量变化如图所示,下列说法错误的是( )
A.反应后生成物中2-卤丙烷含量较多
B.两个反应的正反应的活化能都比逆反应的高
C.平衡后降低温度,1-卤丙烷和2-卤丙烷的产量都增加
D.第Ⅰ阶段的速率决定着生成1-卤丙烷反应的速率快慢
答案 B
7.(2022河北秦皇岛三模,12)在催化剂表面CO2与H2反应的部分历程如图所示,吸附在催化剂表面的物种用“·”标注,Ts表示过渡态。下列说法错误的是( )
A.物质吸附在催化剂表面时通常比其形成的过渡状态稳定
B.②→③是图中①至⑥的历程中的决速步骤
C.③→④的过程中断裂了非极性共价键
D.反应·CO2(g)+H2(g) ·CO+H2O(g)的ΔH<0
答案 C
8.(2022福建三明质检,7)以Pd纳米粒子为核、空心多孔碳球为壳的封装型催化剂将H2和O2直接合成H2O2的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是( )
(a)直接合成法 (b)电催化还原法
A.直接合成法中,步骤②吸收能量,步骤④释放能量
B.电催化还原法制备H2O2的优点之一是避免了H2和O2共存的易爆环境
C.电催化还原时,2e-路径的步骤少,反应速率快
D.若催化剂表面对*OOH吸附过强,则易生成O*,导致H2O2的产率降低
答案 C
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024新高考化学高考专题复习
专题九 化学反应的热效应
五年高考
考点1 化学反应中的能量变化
1.(2023北京,13,3分)一种分解氯化铵实现产物分离的物质转化关系如下,其中b、d代表MgO或Mg(OH)Cl中的一种。下列说法正确的是( )
A.a、c分别是HCl、NH3
B.d既可以是MgO,也可以是Mg(OH)Cl
C.已知MgCl2为副产物,则通入水蒸气可减少MgCl2的产生
D.等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
答案 C
2.(2022浙江1月选考,18,2分)相关有机物分别与氢气发生加成反应生成1 mol环己烷()的能量变化如图所示:
下列推理不正确的是( )
A.2ΔH1≈ΔH2,说明碳碳双键加氢放出的热量与分子内碳碳双键数目成正比
B.ΔH2<ΔH3,说明单双键交替的两个碳碳双键间存在相互作用,有利于物质稳定
C.3ΔH1<ΔH4,说明苯分子中不存在三个完全独立的碳碳双键
D.ΔH3-ΔH1<0,ΔH4-ΔH3>0,说明苯分子具有特殊稳定性
答案 A
3.(2021山东,14,4分)18O标记的乙酸甲酯在足量NaOH溶液中发生水解,部分反应历程可表示为:
+OH-+CH3O-
能量变化如图所示。已知为快速平衡,下列说法正确的是( )
A.反应Ⅱ、Ⅲ为决速步
B.反应结束后,溶液中存在18OH-
C.反应结束后,溶液中存在COH
D.反应Ⅰ与反应Ⅳ活化能的差值等于图示总反应的焓变
答案 B
4.(2021浙江1月选考,24,2分)在298.15 K、100 kPa条件下,N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ·mol-1,N2(g)、H2(g)和NH3(g)的比热容分别为29.1、28.9和35.6 J·K-1·mol-1。一定压强下,1 mol反应中,反应物[N2(g)+3H2(g)]、生成物[2NH3(g)]的能量随温度T的变化示意图合理的是( )
答案 B
5.(2020浙江7月选考,22,2分)关于下列ΔH的判断正确的是( )
C(aq)+H+(aq) HC(aq) ΔH1
C(aq)+H2O(l) HC(aq)+OH-(aq) ΔH2
OH-(aq)+H+(aq) H2O(l) ΔH3
OH-(aq)+CH3COOH(aq) CH3COO-(aq)+H2O(l) ΔH4
A.ΔH1<0 ΔH2<0 B.ΔH1<ΔH2 C.ΔH3<0 ΔH4>0 D.ΔH3>ΔH4
答案 B
6.(2023全国甲,28,15分)甲烷选择性氧化制备甲醇是一种原子利用率高的方法。回答下列问题:
(1)已知下列反应的热化学方程式:
①3O2(g) 2O3(g) K1 ΔH1=285 kJ·mol-1
②2CH4(g)+O2(g) 2CH3OH(l) K2 ΔH2=-329 kJ·mol-1
反应③CH4(g)+O3(g) CH3OH(l)+O2(g)的ΔH3= kJ·mol-1,平衡常数K3= (用K1、K2表示)。
(2)电喷雾电离等方法得到的M+(Fe+、Co+、Ni+等)与O3反应可得MO+。MO+与CH4反应能高选择性地生成甲醇。分别在300 K和310 K下(其他反应条件相同)进行反应MO++CH4 M++CH3OH,结果如下图所示。图中300 K的曲线是 (填“a”或“b”)。300 K、60 s时MO+的转化率为 (列出算式)。
(3)MO+分别与CH4、CD4反应,体系的能量随反应进程的变化如下图所示(两者历程相似,图中以CH4示例)。
(ⅰ)步骤Ⅰ和Ⅱ中涉及氢原子成键变化的是 (填“Ⅰ”或“Ⅱ”)。
(ⅱ)直接参与化学键变化的元素被替换为更重的同位素时,反应速率会变慢,则MO+与CD4反应的能量变化应为图中曲线 (填“c”或“d”)。
(ⅲ)MO+与CH2D2反应,氘代甲醇的产量CH2DOD CHD2OH(填“>”“=”或“<”)。若MO+与CHD3反应,生成的氘代甲醇有 种。
答案 (1)-307 (2)b 1-10-0.1 (3)(ⅰ)Ⅰ (ⅱ)c (ⅲ)< 2
考点2 热化学方程式的书写 盖斯定律的应用
1.(2022重庆,13,3分)“千畦细浪舞晴空”,氮肥保障了现代农业的丰收。为探究(NH4)2SO4的离子键强弱,设计如图所示的循环过程,可得ΔH4/(kJ·mol-1)为( )
A.+533 B.+686 C.+838 D.+1 143
答案 C
2.(2022浙江6月选考,18,2分)标准状态下,下列物质气态时的相对能量如下表:
物质(g) O H HO HOO H2 O2 H2O2 H2O
能量/kJ·mol-1 249 218 39 10 0 0 -136 -242
可根据HO(g)+HO(g) H2O2(g)计算出H2O2中氧氧单键的键能为214 kJ·mol-1。下列说法不正确的是( )
A.H2的键能为436 kJ·mol-1
B.O2的键能大于H2O2中氧氧单键的键能的两倍
C.解离氧氧单键所需能量:HOO
答案 C
3.(2021北京,14,3分)丙烷经催化脱氢可制丙烯:C3H8 C3H6+H2。600 ℃,将一定浓度的CO2与固定浓度的C3H8通过含催化剂的恒容反应器,经相同时间,流出的C3H6、CO和H2浓度随初始CO2浓度的变化关系如图。
已知:①C3H8(g)+5O2(g) 3CO2(g)+4H2O(l) ΔH=-2 220 kJ·mol-1
②C3H6(g)+O2(g) 3CO2(g)+3H2O(l) ΔH=-2 058 kJ·mol-1
③H2(g)+O2(g) H2O(l) ΔH=-286 kJ·mol-1
下列说法不正确的是( )
A.C3H8(g) C3H6(g)+H2(g)
ΔH=+124 kJ·mol-1
B.c(H2)和c(C3H6)变化差异的原因:CO2+H2 CO+H2O
C.其他条件不变,投料比c(C3H8)/c(CO2)越大,C3H8转化率越大
D.若体系只有C3H6、CO、H2 和H2O生成,则初始物质浓度c0与流出物质浓度c之间一定存在:3c0(C3H8)+c0(CO2)=c(CO)+c(CO2)+3c(C3H8)+3c(C3H6)
答案 C
4.(2021浙江1月选考,20,2分)已知共价键的键能与热化学方程式信息如下表:
共价键 H—H H—O
键能/(kJ·mol-1) 436 463
热化学方程式 2H2(g)+O2(g) 2H2O(g) ΔH=-482 kJ·mol-1
则2O(g) O2(g)的ΔH为( )
A.428 kJ·mol-1 B.-428 kJ·mol-1 C.498 kJ·mol-1 D.-498 kJ·mol-1
答案 D
三年模拟
A组 基础题组
考点1 化学反应中的能量变化
1.(2023吉林市二调,10)1868年狄青和洪特发现了用空气中的氧气来氧化氯化氢气体制取氯气的方法:4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)。该反应的能量变化如图所示,下列说法正确的是( )
A.该反应为吸热反应
B.若H2O为液态,则生成物总能量将变大
C.该反应发生时向环境释放能量
D.断开旧化学键吸收的总能量大于形成新化学键所释放的总能量
答案 C
2.(2023河北衡水二中三调,8)氮的氧化物转化是环境化学热点问题之一。研究发现,H2还原NO的反应2NO(g)+2H2(g) N2(g)+2H2O(l)分两步进行:①2NO(g)+H2(g) N2(g)+H2O2(l);②H2O2(l)+H2(g) 2H2O(l)。其能量变化如图所示(Ts代表过渡态)。下列叙述正确的是( )
A.②是放热反应,①是吸热反应
B.H2O2是该反应的催化剂
C.反应①的活化能大于反应②
D.加入催化剂的目的是降低Ts2的能量
答案 C
考点2 热化学方程式的书写 盖斯定律的应用
1.(2023重庆三调,7,改编)为实现“碳达峰、碳中和”的目标,科学家提出以TiO2为催化剂,用光热化学循环分解法,达到减少大气中CO2的量的目的,反应的机理如图所示:
已知完全断开1 mol CO2(g)、CO(g)、O2(g)中化学键吸收的能量分别为1 598 kJ/mol、1072 kJ/mol、496 kJ/mol。
下列说法不正确的是( )
A.过程①中光能转化为化学能
B.过程④为放热过程
C.该反应中Ti的化合价发生了变化
D.全过程热化学方程式为2CO2(g) 2CO(g)+O2(g) ΔH=+556 kJ/mol
答案 B
2.(2022重庆一模,11)合成氨工业在国民经济中占有重要地位,对人类生存具有重大意义。合成氨反应的历程和能量变化如下图所示:
已知:①2·NH3 2NH3(g) ΔH=+100 kJ/mol,②2NH3(g) N2(g)+3H2(g) ΔH,则反应②的ΔH为( )
A.+92 kJ/mol B.-92 kJ/mol C.+192 kJ/mol D.+148 kJ/mol
答案 A
B组 综合题组
1.[2023河北学业水平选择性考试(一),6]反应的能量与反应历程的关系如下图所示。下列说法错误的是( )
A.第1步决定整个反应的快慢
B.第2步为放热过程
C.该反应的焓变大小取决于第1、2、3步正、逆反应的活化能大小
D.该反应适宜在碱性条件下进行
答案 C
2.(2023山西临汾一模,10)不同含金化合物催化乙烯加氢的反应历程如下图所示:
下列说法正确的是( )
A.从图中可得1 mol C2H4(g)具有的能量比1 mol C2H6(g)的能量高
B.过渡态1比过渡态2物质的稳定性弱
C.在催化剂AuP催化下,该反应的ΔH=-233.7 kJ·mol-1
D.相比催化剂AuP,AuF催化乙烯加氢的效果更好
答案 B
3.(2023安徽蚌埠二模,12)已知复杂反应的速率由反应历程中活化能最大的一步基元反应决定。卤代烃的取代反应有以下两种反应历程,其反应过程中的能量变化如图所示:
下列说法中错误的是( )
A.卤代烃的取代为放热反应
B.SN1反应速率与c(Nu-)和c(R3CX)相关
C.SN2反应速率与c(RX)和c(Nu-)相关
D.SN1机理为两步反应,SN2机理为一步反应
答案 B
4.(2022湖北襄阳二模,11)苯的亲电取代反应分两步进行,可表示为E++ +H+,生成中间体的一步是加成过程,中间体失去H+的一步是消除过程,其机理亦称加成—消除机理。苯的亲电取代反应进程和能量的关系如图,下列说法错误的是( )
A.第一步反应为苯亲电取代的决速步骤
B.E1与E2的差值为总反应的焓变
C.中间体的能量比苯的高,稳定性比苯的差
D.反应过程中,环上碳原子的杂化类型发生了变化
答案 B
5.(2022福建龙岩三检,9)在Fe+催化下乙烷氧化的反应机理如图所示(图中为副反应)。下列说法正确的是( )
A.FeO+、N2均为反应中间体
B.X既含极性共价键也含非极性共价键
C.该机理涉及的反应均为氧化还原反应
D.每生成1 mol CH3CHO,消耗的N2O大于2 mol
答案 D
6.(2022河北邯郸二模,8)据报道,我国科学家研制出以石墨烯为载体的催化剂,在25 ℃下用H2O2直接将CH4转化为含氧有机物,其主要原理如图所示。下列说法不正确的是( )
A.石墨烯为载体的催化剂的作用是破坏C—H键
B.步骤ⅴ、ⅵ的总反应方程式是H2O2+HCHO HCOOH+H2O
C.步骤ⅱ得到的产物所有原子可能共面
D.上述反应过程中,用虚线圆框住的部分表示不稳定的自由基状态
答案 C
7.(2022重庆育才中学二诊,8)甲醇水蒸气催化重整是获取H2的重要方法,反应CH3OH(g)+H2O(g) CO2(g)+3H2(g) ΔH>0,能量变化如图1所示。830 ℃时,相同时间内向反应体系中投入一定量CaO做对比实验,结果如图2所示,下列说法中正确的是( )
图1 图2
A.该反应的ΔH=(a-b-c) kJ·mol-1
B.CaO表面积越大,吸收CO2效果越好
C.该反应在低温下能自发进行
D.选择适当催化剂降低ΔH3可显著提高催化重整反应速率
答案 B
考法训练
考法 反应历程与能量图像分析
1.(2023浙江1月选考,14,3分)标准状态下,气态反应物和生成物的相对能量与反应历程示意图如下[已知O2(g)和Cl2(g)的相对能量为0],下列说法不正确的是( )
A.E6-E3=E5-E2
B.可计算Cl—Cl键能为2(E2-E3) kJ·mol-1
C.相同条件下,O3的平衡转化率:历程Ⅱ>历程Ⅰ
D.历程Ⅰ、历程Ⅱ中速率最快的一步反应的热化学方程式为:ClO(g)+O(g) O2(g)+Cl(g) ΔH=(E5-E4) kJ·mol-1
答案 C
2.(2022辽宁,10,3分)利用有机分子模拟生物体内“醛缩酶”催化Diels-Alder反应取得重要进展,荣获2021年诺贝尔化学奖。某Diels-Alder反应催化机理如下。下列说法错误的是 ( )
A.总反应为加成反应 B.Ⅰ和Ⅴ互为同系物
C.Ⅵ是反应的催化剂 D.化合物X为H2O
答案 B
3.(2022浙江1月选考,24,2分)某课题组设计一种固定CO2的方法,原理如图。下列说法不正确的是( )
A.反应原料中的原子100%转化为产物
B.该过程在化合物X和I-催化下完成
C.该过程仅涉及加成反应
D.若原料用,则产物为
答案 C
4.(2021重庆,10,3分)“天朗气清,惠风和畅。”研究表明,利用Ir+可催化消除大气污染物N2O和CO,简化中间反应进程后,相对能量变化如图所示。已知CO(g)的燃烧热ΔH=-283 kJ/mol,则2N2O(g) 2N2(g)+O2(g)的反应热ΔH(kJ/mol)为( )
A.-152 B.-76 C.+76 D.+152
答案 A
5.(2023辽宁沈阳联合模拟,11,改编)下图是用钌(Ru)基催化剂催化CO2(g)和H2(g)的反应示意图,当反应生成46 g液态HCOOH时放出31.2 kJ的热量。下列说法错误的是( )
A.反应历程中存在极性键、非极性键的断裂与形成
B.图示中物质Ⅰ为该反应的催化剂,物质Ⅱ、Ⅲ为中间产物
C.将反应Ⅰ、Ⅱ、Ⅲ相加可得总反应
D.由题意知:HCOOH(l) CO2(g)+H2(g) ΔH=+31.2 kJ·mol-1
答案 A
6.(2022辽宁选择性考试二模,10)丙烯(CH2CHCH3)在一定条件下与HX发生加成反应生成两种卤代烃的能量变化如图所示,下列说法错误的是( )
A.反应后生成物中2-卤丙烷含量较多
B.两个反应的正反应的活化能都比逆反应的高
C.平衡后降低温度,1-卤丙烷和2-卤丙烷的产量都增加
D.第Ⅰ阶段的速率决定着生成1-卤丙烷反应的速率快慢
答案 B
7.(2022河北秦皇岛三模,12)在催化剂表面CO2与H2反应的部分历程如图所示,吸附在催化剂表面的物种用“·”标注,Ts表示过渡态。下列说法错误的是( )
A.物质吸附在催化剂表面时通常比其形成的过渡状态稳定
B.②→③是图中①至⑥的历程中的决速步骤
C.③→④的过程中断裂了非极性共价键
D.反应·CO2(g)+H2(g) ·CO+H2O(g)的ΔH<0
答案 C
8.(2022福建三明质检,7)以Pd纳米粒子为核、空心多孔碳球为壳的封装型催化剂将H2和O2直接合成H2O2的机理如图(a)所示。电催化还原O2时的两种可能转化路径如图(b)所示(其中吸附在催化剂表面的物种用*标注)。下列说法错误的是( )
(a)直接合成法 (b)电催化还原法
A.直接合成法中,步骤②吸收能量,步骤④释放能量
B.电催化还原法制备H2O2的优点之一是避免了H2和O2共存的易爆环境
C.电催化还原时,2e-路径的步骤少,反应速率快
D.若催化剂表面对*OOH吸附过强,则易生成O*,导致H2O2的产率降低
答案 C
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
