2023-2024学年天津市杨村重点中学高三(上)开学化学试卷(含解析)
文档属性
| 名称 | 2023-2024学年天津市杨村重点中学高三(上)开学化学试卷(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 605.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-09-29 22:12:24 | ||
图片预览



文档简介
2023-2024学年天津市杨村重点中学高三(上)开学化学试卷
一、单选题(本大题共14小题,共42.0分)
1.下列我国古代优秀艺术作品中,所用材料不属于无机非金属材料的是( )
A.商代后母戊鼎 B.新石器时代人面鱼纹彩陶盆 C.明永乐青花竹石芭蕉纹梅瓶 D.三国青瓷羊形烛台
A. B. C. D.
2.下列叙述正确的是( )
A. 用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇 B. 甲醇既可发生取代反应也可发生加成反应
C. 烷烃的沸点高低仅取决于碳原子数的多少 D. 戊二烯与环戊烷互为同分异构体
3.鉴别、、可以选用的试剂是( )
碘水、淀粉溶液 氯水、溴水、苯 硝酸、溶液 氯水、苯溶液、
A. B. C. D.
4.下列离子方程式或化学方程式正确的是( )
A. 通入少量溶液中:
B. 焦炭还原二氧化硅生产硅:
C. 硫酸铝溶液中加入氨水,会生成白色沉淀:
D. 向小苏打溶液中加入过量石灰水:
5.已知为一种常见酸的浓溶液,能使蔗糖粉末变黑.与反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
A. 使蔗糖变黑的现象主要体现了的强氧化性
B. 若为铁,则足量与在室温下即可完全反应
C. 若为碳单质,则将通入少量的澄清石灰水中,最后有白色沉淀产生
D. 工业上,转化为的反应条件为加热、使用催化剂
6.高分子材料在疫情防控和治疗中起到了重要的作用。下列说法正确的是( )
A. 聚乙烯是生产隔离衣的主要材料,能使酸性高锰酸钾溶液褪色
B. 聚丙烯酸树脂是打印护目镜镜框材料的成分之一,可以与溶液反应
C. 天然橡胶是制作医用无菌橡胶手套的原料,它是异戊二烯发生缩聚反应的产物
D. 聚乙二醇可用于制备治疗新冠病毒的药物,聚乙二醇的结构简式为
7.某有机物的结构简式为
,下列说法正确的是( )
A. 的名称为,,三甲基乙基戊醇
B. 的消去反应产物有种
C. 能发生取代反应
D. 不能发生氧化反应
8.已知酸性:
,综合考虑反应物的转化率和原料成本等因素,将
转变为
的最佳方法是( )
A. 与足量的溶液共热后,再通入足量
B. 与稀共热后,加入足量的溶液
C. 与稀共热后,加入足量的溶液
D. 与足量的溶液共热后,再加入适量
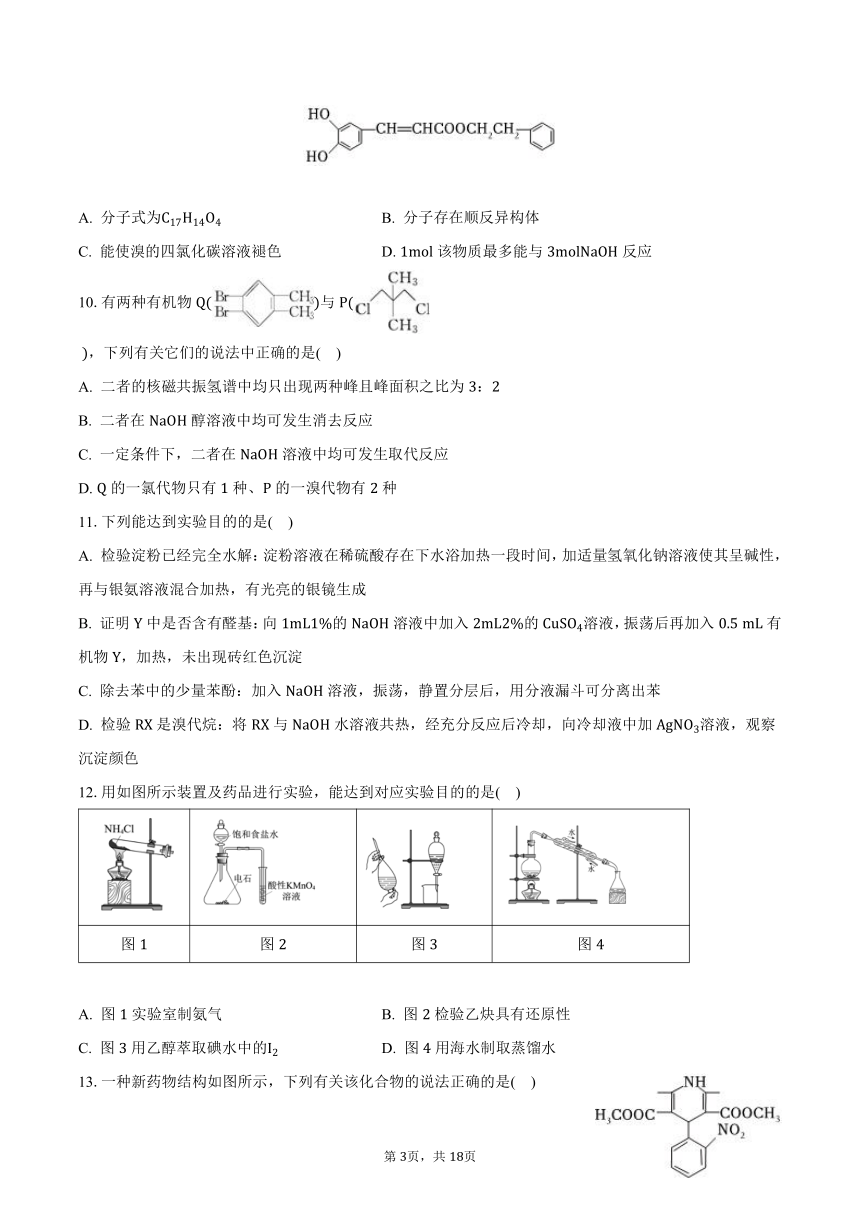
9.如图所示的是蜂胶里的活性成分,关于此物质说法不正确的是( )
A. 分子式为 B. 分子存在顺反异构体
C. 能使溴的四氯化碳溶液褪色 D. 该物质最多能与反应
10.有两种有机物与
,下列有关它们的说法中正确的是( )
A. 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为:
B. 二者在醇溶液中均可发生消去反应
C. 一定条件下,二者在溶液中均可发生取代反应
D. 的一氯代物只有种、的一溴代物有种
11.下列能达到实验目的的是( )
A. 检验淀粉已经完全水解:淀粉溶液在稀硫酸存在下水浴加热一段时间,加适量氢氧化钠溶液使其呈碱性,再与银氨溶液混合加热,有光亮的银镜生成
B. 证明中是否含有醛基:向的溶液中加入的溶液,振荡后再加入 有机物,加热,未出现砖红色沉淀
C. 除去苯中的少量苯酚:加入溶液,振荡,静置分层后,用分液漏斗可分离出苯
D. 检验是溴代烷:将与水溶液共热,经充分反应后冷却,向冷却液中加溶液,观察沉淀颜色
12.用如图所示装置及药品进行实验,能达到对应实验目的的是( )
图 图 图 图
A. 图实验室制氨气 B. 图检验乙炔具有还原性
C. 图用乙醇萃取碘水中的 D. 图用海水制取蒸馏水
13.一种新药物结构如图所示,下列有关该化合物的说法正确的是( )
A. 分子式为
B. 能发生水解反应、聚合反应、取代反应
C. 能与氢气发生加成反应,但不能与澳的四氯化碳溶液反应
D. 分子中含有三种官能团
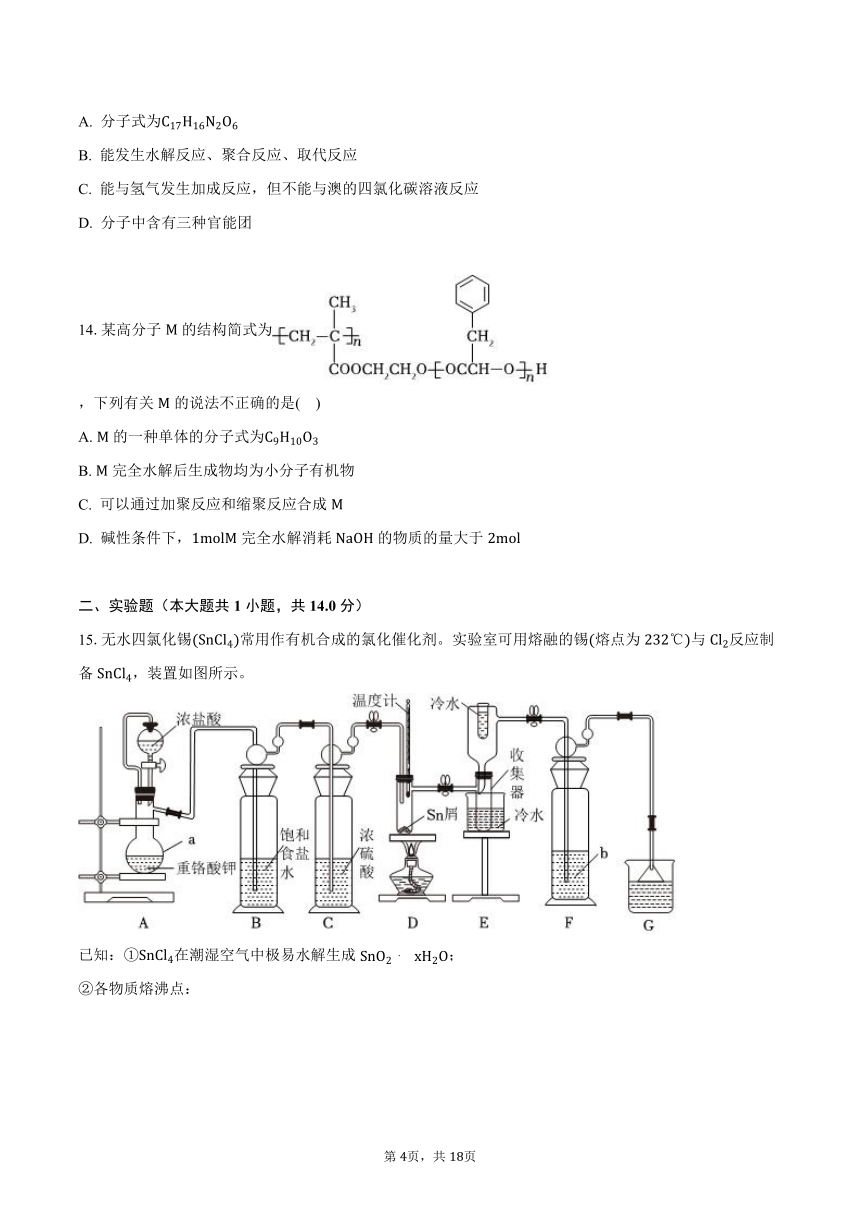
14.某高分子的结构简式为
,下列有关的说法不正确的是( )
A. 的一种单体的分子式为
B. 完全水解后生成物均为小分子有机物
C. 可以通过加聚反应和缩聚反应合成
D. 碱性条件下,完全水解消耗的物质的量大于
二、实验题(本大题共1小题,共14.0分)
15.无水四氯化锡常用作有机合成的氯化催化剂。实验室可用熔融的锡熔点为与反应制备,装置如图所示。
已知:在潮湿空气中极易水解生成;
各物质熔沸点:
物质 熔点 沸点
仪器的名称为 ______ ,重铬酸钾与浓盐酸反应时,还原产物是,装置中发生反应的离子方程式为 ______ 。
装置中试剂为 ______ ,其作用是 ______ 。
锡屑中含铜杂质导致中产生,但不影响中产品的纯度,原因是 ______ 。
所得产品中常溶有少量杂质,可用 ______ 方法提纯。
制得的产品中常含有,可用如下方法测定产品纯度:先准确称量产品于锥形瓶中,再加过量的溶液,发生反应:,再用标准溶液滴定生成的,此时还原产物为,消耗标准溶液,则产品的纯度为 ______ 。
三、简答题(本大题共3小题,共44.0分)
16.已知、、、、是化学中常见的物质,常温下,是一种无色无味的液体,它们之间有如下反应关系.
若是一种黑色单质,是一种常见的难挥发性酸,、都是气体,则为: ______ 为: ______ 填化学式
若是一种紫红色单质,是一种常见的挥发性酸,反应时生成的是无色气体,反应的离子方程式是 ______ ,在反应中表现出的性质是 ______ 、 ______ .
若实验室中利用和的反应制备气体,是一种无色、刺激性气味、密度比空气小的气体,则为: ______ 为: ______ 填化学式,实验室检验的常用方法是 ______ .
17.是一种重要的化工原料,它可由石油和煤焦油通过下列路线合成:
的名称是________;过程是_______变化填“物理”或“化学”,下同,过程是________变化。
反应的化学方程式为__________;反应的类型为__________。
鉴别与的方法是________。
中六元环上的氢原子被两个氯原子取代后的有机物有________种。
18.化合物是合成抗心律失常药物泰达隆的一种中间体,可通过以下方法合成:
已知:苯胺易被氧化甲基为邻对位定位基团,取代基优先取代在甲基的邻位或对位;羧基位间位定位基团,取代基优先取代在羧基的间位。
中的含氧官能团名称为 ______ 、 ______ 。任写两种
的反应类型为 ______ 。
写出同时满足下列条件的的两种同分异构体的结构简式 ______ 。
能发生银镜反应;
能发生水解反应,其水解产物之一能与溶液发生显色反应;
分子中只有种不同化学环境的氢。
经还原得到,的分子是为,写出的结构简式 ______ 。
写出的反应方程式 ______ 。
写出的作用为 ______ 。
请以甲苯和为原料用四步制备
,写出制备的合成路线流程图 ______ 。无机试剂任用,合成路线流程图示例见本题题干
答案和解析
1.【答案】
【解析】解:商代后母戊鼎是青铜器,所用材料青铜属于金属材料,不是无机非金属材料,故A选;
B.新石器时代人面鱼纹彩陶盆是瓷器,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料,故B不选;
C.明永乐青花竹石芭蕉纹梅瓶是瓷器,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料,故C不选;
D.三国青瓷羊形烛台是瓷器,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料,故D不选;
故选:。
商代后母戊鼎是青铜器,所用材料属于金属材料,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料.
本题考查了无机非金属材料,难度不大,无机非金属材是以某些元素的氧化物、碳化物、氮化物、卤素化合物、硼化物以及硅酸盐、铝酸盐、磷酸盐、硼酸盐等物质组成的材料,注意基础知识的积累.
2.【答案】
【解析】解:乙酸与碳酸钠反应生成气体,乙醇不能,现象不同可鉴别,故A正确;
B.甲醇中只有单键,可以发生取代反应,不能发生加成反应,故B错误;
C.烷烃中原子数越多、沸点越高,相同碳原子数时支链越多、沸点越低,则沸点与碳原子数及结构有关,故C错误;
D.戊二烯与环戊烷中原子数不同,二者不互为同分异构体,故D错误;
故选:。
A.乙酸与碳酸钠反应生成气体,乙醇不能;
B.甲醇中只有单键;
C.烷烃中原子数越多、沸点越高,相同碳原子数时支链越多、沸点越低;
D.戊二烯与环戊烷中原子数不同。
本题考查了有机物的结构与性质,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的易错点,题目难度不大。
3.【答案】
【解析】解:加入碘水、淀粉溶液,因三种物质都不反应,不能鉴别,故错误;
加入氯水,可生成和,在四氯化碳的颜色不同,可鉴别,故正确;
加入溴水,不能鉴别、,故错误;
加入硝酸、溶液分别与、、反应生成白色沉淀、浅黄色沉淀、黄色沉淀,可鉴别,故正确;
加入氯水,可生成和,与苯发生萃取后在苯的颜色不同,可鉴别,故正确;
加入溶液,不能检验、,故错误;
故选:。
鉴别、、,可根据阴离子的性质不同以及氧化性强弱判断反应的可能性,并结合萃取现象及卤化银沉淀的颜色进行检验。
本题考查物质的检验和鉴别,为高考常见题型,侧重于学生实验能力和综合运用化学知识的能力的考查,注意把握卤素单质的氧化性强弱及萃取现象,题目难度不大。
4.【答案】
【解析】解:具有还原性,具有氧化性,二者发生氧化还原反应生成硫酸钠、硫酸和氯化钠,离子方程式为,故A正确;
B.焦炭还原二氧化硅生产硅和一氧化碳,反应为,故B错误;
C.硫酸铝溶液中加入氨水,反应的离子方程式为,故C错误;
D.碳酸氢钠俗名小苏打,和过量石灰水反应生成碳酸钙、氢氧化钠和水,离子方程式为,故D错误;
故选:。
A.具有还原性,具有氧化性,二者发生氧化还原反应生成硫酸钠、硫酸和氯化钠;
B.焦炭还原二氧化硅生产硅和一氧化碳;
C.一水合氨是弱碱,不能拆分;
D.碳酸氢钠溶液中加入过量石灰水时生成碳酸钙、氢氧化钠和水。
本题考查离子方程式或化学方程式的正误判断,明确物质的性质、发生的反应、离子方程式的书写规则为解答关键,注意掌握与量有关离子方程式的书写,侧重考查学生的分析能力及规范答题能力,题目难度中等。
5.【答案】
【解析】解:浓硫酸具有脱水性,能够使蔗糖变黑,则是硫酸,和水反应生成硫酸,则是三氧化硫,和氧气反应生成三氧化硫,则是二氧化硫,
A.浓硫酸使蔗糖变黑体现浓硫酸的脱水性,故A错误;
B.浓硫酸具有强的氧化性,能够使铁发生钝化,阻止反应进行,故B错误;
C.若是碳,浓硫酸和碳反应生成二氧化碳、二氧化硫和水,二氧化碳和少量氢氧化钙反应生成可溶性的碳酸氢钙,故C错误;
D.工业上,二氧化硫转化为三氧化硫的反应条件为高温、常压、使用催化剂,故D正确;
故选:。
浓硫酸具有脱水性,能够使蔗糖变黑,则是硫酸,和水反应生成硫酸,则是三氧化硫,和氧气反应生成三氧化硫,则是二氧化硫,据此解答.
本题为框图推断题,熟悉浓硫酸脱水性、强的氧化性的性质是解题关键,突破口为“为一种常见酸的浓溶液,能使蔗糖粉末变黑”,题目难度不大.
6.【答案】
【解析】【分析】
本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的组成、结构和官能团的性质,把握有机物的应用,题目难度不大。
【解答】
A.聚乙烯不含碳碳双键,与酸性高锰酸钾不反应,故A错误;
B.聚丙烯酸树脂含有羧基,可与氢氧化钠溶液反应,故B正确;
C.异戊二烯含有碳碳双键,可发生加聚反应,天然橡胶是加聚产物,故C错误;
D.聚乙二醇结构简式为,题中缺少端基原子或原子团,故D错误。
故选:。
7.【答案】
【解析】解:编号错误,应为,,三甲基乙基戊醇,故A错误;
B.含有羟基,有个相邻碳原子上有氢原子,则的消去反应产物有种,故B错误;
C.含有羟基,能发生取代反应,故C正确;
D.有机物可燃烧,属于氧化反应,故D错误;
故选:。
有机物含有羟基,具有醇的性质,结合有机物的结构特点解答该题。
本题考查有机物的官能团及性质,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握结构与性质的关系是解答本题的关键,题目难度不大。
8.【答案】
【解析】解:.应先在碱性条件下水解生成,由于,则通入二氧化碳气体可生成,所以与足量的溶液共热后,再通入足量即可,故A正确;
B.与稀硫酸共热后生成邻羟基苯甲酸,邻羟基苯甲酸和碳酸钠反应生成,故B错误;
C.与稀共热后生成邻羟基苯甲酸,加入足量的溶液生成,故C错误;
D.与足量的溶液共热后生成,再加入适量生成,故D错误;
故选A.
酸性:,所以碳酸氢钠和反应生成苯甲酸钠、和不反应,将 转变为 ,应先在碱性条件下水解生成,由于,则通入二氧化碳气体可生成.
本题考查化学实验方案评价,为高频考点,侧重考查学生分析判断能力,根据物质结构结合酸性强弱确定反应先后顺序是解本题关键,注意酚羟基能和碳酸钠反应,易错选项是.
9.【答案】
【解析】解:根据结构简式知,其分子式为,故A错误;
B.该分子含有碳碳双键,双键碳上连接的两个基团不同,存在顺反异构,故B正确;
C.含有碳碳双键,可与溴发生加成反应,能使溴的四氯化碳溶液褪色,故C正确;
D.能与氢氧化钠反应的为酚羟基和酯基,则该物质最多能与反应,故D正确;
故选:。
由结构可知分子中含酚、碳碳双键、,结合酚、烯烃、酯的性质来解答。
本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意把握有机物的结构特点,为解答易错点,题目难度不大。
10.【答案】
【解析】解:二者的核磁共振氢谱中均只出现两种峰,且峰面积之比分别为:、:,故A错误;
B.二者在醇溶液中均不能发生消去反应,故B错误;
C.卤代烃、甲基等均可发生取代反应,则一定条件下,二者在溶液中均可发生取代反应,故C正确;
D.、中均含种,则一氯代物均有种,故D错误;
故选:。
A.由结构对称性可知,均含种,但原子数目不同;
B.中与苯环相连不能发生消去反应,中与相连的邻位上没有;
C.卤代烃、甲基等均可发生取代反应;
D.、中均含种.
本题考查有机物的结构与性质及推断,为高频考点,把握官能团与性质的关系为解答的关键,侧重结构对称性分析及卤代烃性质的考查,题目难度不大.
11.【答案】
【解析】解:由操作和现象可知,淀粉发生水解生成葡萄糖,确定水解程度,需检验淀粉是否剩余,该实验操作只能证明淀粉水解了,但是无法证明水解是否完全,故A错误;
B.新制得氢氧化铜悬浊液制备不对,应该向溶液中加入少量的溶液,保证溶液显示碱性,否则无法检验醛基,故B错误;
C.苯酚与反应后,与苯分层,然后分液可分离,故C正确;
D.水解后检验溴离子在酸性溶液中,则将与水溶液共热,经充分反应后冷却,向冷却液中加稀酸化后,再加溶液,观察沉淀颜色,若为淡黄色沉淀,可知为溴代烷,故D错误;
故选:。
A.由操作和现象可知,淀粉发生水解生成葡萄糖,确定水解程度需检验淀粉是否有剩余;
B.醛基的检验:加入新制得氢氧化铜悬浊液,加热,看是否出现砖红色沉淀;
C.苯酚与反应后,与苯分层;
D.卤代烃水解后,检验卤素离子在酸性溶液中进行检验。
本题考查化学实验方案的评价,为高频考点,把握物质的性质、物质的检验、物质的制备、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大。
12.【答案】
【解析】【分析】
本题考查化学实验方案的评价,为高频考点,把握物质的性质、混合物分离提纯、物质的制备及检验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大。
【解答】
A.氯化铵分解后,在试管口又化合生成氯化铵,则不能制备氨气,应选铵盐与碱加热制备,故A错误;
B.生成乙炔中混有硫化氢等,均可被高锰酸钾氧化,则溶液褪色,不能检验乙炔的还原性,故B错误;
C.乙醇与水互溶,不能萃取分离出碘,故C错误;
D.海水中水的沸点较低,则图中蒸馏装置可制取蒸馏水,故D正确。
故本题选D。
13.【答案】
【解析】解:分子中、、、原子个数依次是、、、,分子式为,故A错误;
B.具有硝基苯、酯、烯烃和氨的性质,酯基能发生水解反应,碳碳双键能发生加聚反应,酯基和亚氨基能发生取代反应,故B正确;
C.分子中苯环和碳碳双键能和氢气发生加成反应,碳碳双键能和溴发生加成反应,故C错误;
D.官能团有硝基、碳碳双键、酯基、亚氨基四种官能团,故D错误;
故选:。
A.分子中、、、原子个数依次是、、、;
B.具有硝基苯、酯、烯烃和氨的性质;
C.苯环和碳碳双键能和氢气发生加成反应,碳碳双键能和溴发生加成反应;
D.官能团有硝基、碳碳双键、酯基、亚氨基。
本题考查有机物的结构和性质,侧重考查分析、判断及知识综合运用能力,明确官能团及其性质的关系是解本题关键,题目难度不大。
14.【答案】
【解析】解:由结构可知,单体为、、,的单体之一的分子式为,故A正确;
B.完全水解生成乙二醇和两种高分子化合物,故B错误;
C.单体中存在、、,则通过加聚反应和缩聚反应可以生成,故C正确;
D. 中含,则碱性条件下,完全水解消耗的物质的量为,大于,故D正确;
故选:。
A.由结构可知,单体为、、;
B.完全水解生成乙二醇和两种高分子化合物;
C.单体中存在、、;
D. 中含。
本题考查有机物的结构与性质,为高频考点,明确高分子化合物的结构及官能团是解答本题的关键,注意加聚反应与缩聚反应的区别,题目难度中等.
15.【答案】蒸馏烧瓶 浓硫酸 防止水蒸气进入收集器 沸点较高,不会随着气体逸出 蒸馏法
【解析】解:分析可知,仪器为蒸馏烧瓶,在加热条件下可以氧化浓盐酸产生氯气,其还原产物为,中的化合价由价变为中的价,化合价变化,的化合价由价变为价,化合价变化,由于中的数目为,氯气中有个氯原子,故K的计量数为,的计量数为,反应的离子方程式为,
故答案为:蒸馏烧瓶;;
结合分析可知,装置中试剂为浓硫酸,其作用是防止水蒸气进入收集器,
故答案为:浓硫酸;防止水蒸气进入收集器;
锡屑中含铜杂质导致中产生,但不影响中产品的纯度,原因在于沸点较高,不会随着气体逸出,
故答案为:沸点较高,不会随着气体逸出;
结合图表数据分析可知,与沸点相差很大,故可用蒸馏法分离,
故答案为:蒸馏法;
滴定中,铁元素化合价升高一价,元素将价,则有关系式:,,故产品的纯度为,
故答案为:。
极易水解,反应应在无水环境下进行进行,装置:重铬酸钾和浓盐酸反应的方法制取,反应的方程式为:,制取的氯气中含有氯化氢,饱和食盐水可以降低氯气的溶解,还可洗去氯气中的氯化氢,在空气中极易水解,为防止其水解,用浓硫酸干燥氯气;和锡的反应制备,冷水冷却,可将气态的冷凝回流收集产物;装置中吸收未反应的氯气,防止污染空气,因极易水解,装置可防止溶液的水蒸气进入收集器中;金属锡易与氯气、氧气反应,反应时应先生成氯气,将氧气排出,据此分析回答问题。
本题考查物质的制备实验,为高频考点,把握物质的性质、制备原理、实验装置的作用、实验技能为解答关键,侧重分析与实验能力的考查,知道各个装置的作用及可能发生的反应,题目难度不大。
16.【答案】 氧化性 酸性 把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气
【解析】解:、、、、是化学中常见的物质,常温下,是一种无色无味的液体,考虑为,
是一种黑色单质,是一种常见的难挥发性酸,、都是气体,则为,为浓硫酸,、分别为二氧化碳、二氧化硫中的一种,该反应方程式为:浓,
故答案为:;;
是一种紫红色单质,是一种常见的挥发性酸,反应时生成的是无色气体,则为,为稀硝酸,为,为硝酸铜,反应的离子反应为,生成硝酸铜体现硝酸的酸性,生成体现硝酸的氧化性,
故答案为:;酸性;氧化性;
是一种无色、刺激性气味、密度比空气小的气体,则为,实验室利用铵盐与熟石灰反应制备氨气,该反应方程式为:,则为,
验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气,
故答案为:;;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气.
A、、、、是化学中常见的物质,常温下,是一种无色无味的液体,考虑为
是一种黑色单质,是一种常见的难挥发性酸,、都是气体,则为,为浓硫酸,、分别为二氧化碳、二氧化硫中的一种;
是一种紫红色单质,是一种常见的挥发性酸,反应时生成的是无色气体,则为,为稀硝酸,为,为硝酸铜;
是一种无色、刺激性气味、密度比空气小的气体,则为,实验室利用铵盐与熟石灰反应制备氨气,利用湿润的红色石蕊试纸检验氨气,或者利用氯化氢与氨气反应生成氯化铵检验.
本题考查无机物的推断,涉及浓硫酸、浓硝酸的性质及氨气的制备,需要学生熟练掌握元素化合物性质与转化,题目难度中等.
17.【答案】乙烯 化学 物理 取代反应或酯化反应 分别滴入酸性溶液,振荡,使溶液褪色的是,不褪色的是
【解析】解:的名称是乙烯;工业上通常对石油分馏产品进行裂解来获得乙烯,故过程为裂解,是化学变化;工业上通过对煤焦油进行分馏而获得苯,过程为分馏,是物理变化;
故答案为:乙烯;化学;物理;
反应为乙醇的催化氧化,化学方程式为;反应为乙酸与环己二醇反应生成酯,故为酯化反应或取代反应;
故答案为:;取代反应或酯化反应;
分子中没有碳碳双键,而分子中有碳碳双键,因此,鉴别与的方法是:分别滴入酸性溶液,振荡,使溶液褪色的是,不褪色的是;
故答案为:分别滴入酸性溶液,振荡,使溶液褪色的是,不褪色的是;
用定一议二法,分子有一定的对称性,六元环上的个碳原子均有原子可以被取代,如图所示,可以先把号或号的原子取代,然后分析另一个原子被取代的可能性,先取代,环上其他碳原子上的均可以被取代,但要注意左右对称,故有种;再先取代,则与相同的位置不能再取代,可以找到种,注意号碳上有个原子可以被取代。综上所述,可以确定中六元环上的氢原子被两个氯原子取代后的有机物有种;
故答案为:。
为,和发生酯化反应取代反应生成,为乙酸,氧化生成,所以为乙醛,催化氧化为,所以为乙醇,和加成生成,所以为乙烯,石油产品经裂解得到乙烯;工业上通过对煤焦油进行分馏而获得苯,发生部分加成生成,发生加成和取代反应生成,
用定一议二法,分子有一定的对称性,六元环上的个碳原子均有原子可以被取代,如图所示,可以先把号或号的原子取代,然后分析另一个原子被取代的可能性,先取代,环上其他碳原子上的均可以被取代,但要注意左右对称,故有种;再先取代,则与相同的位置不能再取代,可以找到种,注意号碳上有个原子可以被取代。
本题考查有机物的推断与合成,根据有机物的结构进行分析,需要学生熟练掌握官能团的性质与转化,试题培养了学生的知识迁移运用能力,难度中等。
18.【答案】羟基或羰基 酰胺键 消去反应 保护氨基
【解析】解:中的含氧官能团名称为羟基、羰基、酰胺键任写两种,
故答案为:羟基、羰基、酰胺键任写两种;
中醇羟基发生消去反应生成中碳碳双键,所以的反应类型为消去反应,
故答案为:消去反应;
的一种同分异构体:能发生银镜反应,说明含有醛基;能发生水解反应,其水解产物之一能与溶液发生显色反应,说明水解可生成酚羟基,应含有结构;分子中只有种不同化学环境的氢,应为对称结构,则同分异构体可为,
故答案为:;
通过以上分析知,的结构简式为,
故答案为:;
发生水解反应生成,的反应方程式为,
故答案为:;
的作用为保护氨基,
故答案为:保护氨基;
以甲苯和为原料用四步制备,苯环和硝酸发生取代反应生成硝基、硝基被还原生成氨基、氨基和乙酸酐发生取代反应生成,甲基被氧化生成,其合成路线为,
故答案为:。
中硝基被还原生成中氨基,中氨基上氢原子被取代生成,中苯环上的氢原子被取代生成,经还原得到,的分子是为,结合、结构简式差别知,中溴原子和酚羟基发生取代反应生成为,中醇羟基发生消去反应生成中碳碳双键,发生水解反应生成中氨基;
以甲苯和为原料用四步制备,苯环和硝酸发生取代反应生成硝基、硝基被还原生成氨基、氨基和乙酸酐发生取代反应生成,甲基被氧化生成。
本题考查有机物的合成与推断、有机反应类型、官能团结构与性质、限制条件同分异构体书写,是对有机会基础的综合考查,较好的考查学生信息获取与知识迁移运用,题目有利于培养学生的分析能力,难度中等。
第1页,共1页
一、单选题(本大题共14小题,共42.0分)
1.下列我国古代优秀艺术作品中,所用材料不属于无机非金属材料的是( )
A.商代后母戊鼎 B.新石器时代人面鱼纹彩陶盆 C.明永乐青花竹石芭蕉纹梅瓶 D.三国青瓷羊形烛台
A. B. C. D.
2.下列叙述正确的是( )
A. 用饱和碳酸氢钠溶液可以鉴别乙酸和乙醇 B. 甲醇既可发生取代反应也可发生加成反应
C. 烷烃的沸点高低仅取决于碳原子数的多少 D. 戊二烯与环戊烷互为同分异构体
3.鉴别、、可以选用的试剂是( )
碘水、淀粉溶液 氯水、溴水、苯 硝酸、溶液 氯水、苯溶液、
A. B. C. D.
4.下列离子方程式或化学方程式正确的是( )
A. 通入少量溶液中:
B. 焦炭还原二氧化硅生产硅:
C. 硫酸铝溶液中加入氨水,会生成白色沉淀:
D. 向小苏打溶液中加入过量石灰水:
5.已知为一种常见酸的浓溶液,能使蔗糖粉末变黑.与反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
A. 使蔗糖变黑的现象主要体现了的强氧化性
B. 若为铁,则足量与在室温下即可完全反应
C. 若为碳单质,则将通入少量的澄清石灰水中,最后有白色沉淀产生
D. 工业上,转化为的反应条件为加热、使用催化剂
6.高分子材料在疫情防控和治疗中起到了重要的作用。下列说法正确的是( )
A. 聚乙烯是生产隔离衣的主要材料,能使酸性高锰酸钾溶液褪色
B. 聚丙烯酸树脂是打印护目镜镜框材料的成分之一,可以与溶液反应
C. 天然橡胶是制作医用无菌橡胶手套的原料,它是异戊二烯发生缩聚反应的产物
D. 聚乙二醇可用于制备治疗新冠病毒的药物,聚乙二醇的结构简式为
7.某有机物的结构简式为
,下列说法正确的是( )
A. 的名称为,,三甲基乙基戊醇
B. 的消去反应产物有种
C. 能发生取代反应
D. 不能发生氧化反应
8.已知酸性:
,综合考虑反应物的转化率和原料成本等因素,将
转变为
的最佳方法是( )
A. 与足量的溶液共热后,再通入足量
B. 与稀共热后,加入足量的溶液
C. 与稀共热后,加入足量的溶液
D. 与足量的溶液共热后,再加入适量
9.如图所示的是蜂胶里的活性成分,关于此物质说法不正确的是( )
A. 分子式为 B. 分子存在顺反异构体
C. 能使溴的四氯化碳溶液褪色 D. 该物质最多能与反应
10.有两种有机物与
,下列有关它们的说法中正确的是( )
A. 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为:
B. 二者在醇溶液中均可发生消去反应
C. 一定条件下,二者在溶液中均可发生取代反应
D. 的一氯代物只有种、的一溴代物有种
11.下列能达到实验目的的是( )
A. 检验淀粉已经完全水解:淀粉溶液在稀硫酸存在下水浴加热一段时间,加适量氢氧化钠溶液使其呈碱性,再与银氨溶液混合加热,有光亮的银镜生成
B. 证明中是否含有醛基:向的溶液中加入的溶液,振荡后再加入 有机物,加热,未出现砖红色沉淀
C. 除去苯中的少量苯酚:加入溶液,振荡,静置分层后,用分液漏斗可分离出苯
D. 检验是溴代烷:将与水溶液共热,经充分反应后冷却,向冷却液中加溶液,观察沉淀颜色
12.用如图所示装置及药品进行实验,能达到对应实验目的的是( )
图 图 图 图
A. 图实验室制氨气 B. 图检验乙炔具有还原性
C. 图用乙醇萃取碘水中的 D. 图用海水制取蒸馏水
13.一种新药物结构如图所示,下列有关该化合物的说法正确的是( )
A. 分子式为
B. 能发生水解反应、聚合反应、取代反应
C. 能与氢气发生加成反应,但不能与澳的四氯化碳溶液反应
D. 分子中含有三种官能团
14.某高分子的结构简式为
,下列有关的说法不正确的是( )
A. 的一种单体的分子式为
B. 完全水解后生成物均为小分子有机物
C. 可以通过加聚反应和缩聚反应合成
D. 碱性条件下,完全水解消耗的物质的量大于
二、实验题(本大题共1小题,共14.0分)
15.无水四氯化锡常用作有机合成的氯化催化剂。实验室可用熔融的锡熔点为与反应制备,装置如图所示。
已知:在潮湿空气中极易水解生成;
各物质熔沸点:
物质 熔点 沸点
仪器的名称为 ______ ,重铬酸钾与浓盐酸反应时,还原产物是,装置中发生反应的离子方程式为 ______ 。
装置中试剂为 ______ ,其作用是 ______ 。
锡屑中含铜杂质导致中产生,但不影响中产品的纯度,原因是 ______ 。
所得产品中常溶有少量杂质,可用 ______ 方法提纯。
制得的产品中常含有,可用如下方法测定产品纯度:先准确称量产品于锥形瓶中,再加过量的溶液,发生反应:,再用标准溶液滴定生成的,此时还原产物为,消耗标准溶液,则产品的纯度为 ______ 。
三、简答题(本大题共3小题,共44.0分)
16.已知、、、、是化学中常见的物质,常温下,是一种无色无味的液体,它们之间有如下反应关系.
若是一种黑色单质,是一种常见的难挥发性酸,、都是气体,则为: ______ 为: ______ 填化学式
若是一种紫红色单质,是一种常见的挥发性酸,反应时生成的是无色气体,反应的离子方程式是 ______ ,在反应中表现出的性质是 ______ 、 ______ .
若实验室中利用和的反应制备气体,是一种无色、刺激性气味、密度比空气小的气体,则为: ______ 为: ______ 填化学式,实验室检验的常用方法是 ______ .
17.是一种重要的化工原料,它可由石油和煤焦油通过下列路线合成:
的名称是________;过程是_______变化填“物理”或“化学”,下同,过程是________变化。
反应的化学方程式为__________;反应的类型为__________。
鉴别与的方法是________。
中六元环上的氢原子被两个氯原子取代后的有机物有________种。
18.化合物是合成抗心律失常药物泰达隆的一种中间体,可通过以下方法合成:
已知:苯胺易被氧化甲基为邻对位定位基团,取代基优先取代在甲基的邻位或对位;羧基位间位定位基团,取代基优先取代在羧基的间位。
中的含氧官能团名称为 ______ 、 ______ 。任写两种
的反应类型为 ______ 。
写出同时满足下列条件的的两种同分异构体的结构简式 ______ 。
能发生银镜反应;
能发生水解反应,其水解产物之一能与溶液发生显色反应;
分子中只有种不同化学环境的氢。
经还原得到,的分子是为,写出的结构简式 ______ 。
写出的反应方程式 ______ 。
写出的作用为 ______ 。
请以甲苯和为原料用四步制备
,写出制备的合成路线流程图 ______ 。无机试剂任用,合成路线流程图示例见本题题干
答案和解析
1.【答案】
【解析】解:商代后母戊鼎是青铜器,所用材料青铜属于金属材料,不是无机非金属材料,故A选;
B.新石器时代人面鱼纹彩陶盆是瓷器,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料,故B不选;
C.明永乐青花竹石芭蕉纹梅瓶是瓷器,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料,故C不选;
D.三国青瓷羊形烛台是瓷器,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料,故D不选;
故选:。
商代后母戊鼎是青铜器,所用材料属于金属材料,陶瓷属于硅酸盐产品,所用原料属于无机非金属材料.
本题考查了无机非金属材料,难度不大,无机非金属材是以某些元素的氧化物、碳化物、氮化物、卤素化合物、硼化物以及硅酸盐、铝酸盐、磷酸盐、硼酸盐等物质组成的材料,注意基础知识的积累.
2.【答案】
【解析】解:乙酸与碳酸钠反应生成气体,乙醇不能,现象不同可鉴别,故A正确;
B.甲醇中只有单键,可以发生取代反应,不能发生加成反应,故B错误;
C.烷烃中原子数越多、沸点越高,相同碳原子数时支链越多、沸点越低,则沸点与碳原子数及结构有关,故C错误;
D.戊二烯与环戊烷中原子数不同,二者不互为同分异构体,故D错误;
故选:。
A.乙酸与碳酸钠反应生成气体,乙醇不能;
B.甲醇中只有单键;
C.烷烃中原子数越多、沸点越高,相同碳原子数时支链越多、沸点越低;
D.戊二烯与环戊烷中原子数不同。
本题考查了有机物的结构与性质,把握官能团与性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意选项C为解答的易错点,题目难度不大。
3.【答案】
【解析】解:加入碘水、淀粉溶液,因三种物质都不反应,不能鉴别,故错误;
加入氯水,可生成和,在四氯化碳的颜色不同,可鉴别,故正确;
加入溴水,不能鉴别、,故错误;
加入硝酸、溶液分别与、、反应生成白色沉淀、浅黄色沉淀、黄色沉淀,可鉴别,故正确;
加入氯水,可生成和,与苯发生萃取后在苯的颜色不同,可鉴别,故正确;
加入溶液,不能检验、,故错误;
故选:。
鉴别、、,可根据阴离子的性质不同以及氧化性强弱判断反应的可能性,并结合萃取现象及卤化银沉淀的颜色进行检验。
本题考查物质的检验和鉴别,为高考常见题型,侧重于学生实验能力和综合运用化学知识的能力的考查,注意把握卤素单质的氧化性强弱及萃取现象,题目难度不大。
4.【答案】
【解析】解:具有还原性,具有氧化性,二者发生氧化还原反应生成硫酸钠、硫酸和氯化钠,离子方程式为,故A正确;
B.焦炭还原二氧化硅生产硅和一氧化碳,反应为,故B错误;
C.硫酸铝溶液中加入氨水,反应的离子方程式为,故C错误;
D.碳酸氢钠俗名小苏打,和过量石灰水反应生成碳酸钙、氢氧化钠和水,离子方程式为,故D错误;
故选:。
A.具有还原性,具有氧化性,二者发生氧化还原反应生成硫酸钠、硫酸和氯化钠;
B.焦炭还原二氧化硅生产硅和一氧化碳;
C.一水合氨是弱碱,不能拆分;
D.碳酸氢钠溶液中加入过量石灰水时生成碳酸钙、氢氧化钠和水。
本题考查离子方程式或化学方程式的正误判断,明确物质的性质、发生的反应、离子方程式的书写规则为解答关键,注意掌握与量有关离子方程式的书写,侧重考查学生的分析能力及规范答题能力,题目难度中等。
5.【答案】
【解析】解:浓硫酸具有脱水性,能够使蔗糖变黑,则是硫酸,和水反应生成硫酸,则是三氧化硫,和氧气反应生成三氧化硫,则是二氧化硫,
A.浓硫酸使蔗糖变黑体现浓硫酸的脱水性,故A错误;
B.浓硫酸具有强的氧化性,能够使铁发生钝化,阻止反应进行,故B错误;
C.若是碳,浓硫酸和碳反应生成二氧化碳、二氧化硫和水,二氧化碳和少量氢氧化钙反应生成可溶性的碳酸氢钙,故C错误;
D.工业上,二氧化硫转化为三氧化硫的反应条件为高温、常压、使用催化剂,故D正确;
故选:。
浓硫酸具有脱水性,能够使蔗糖变黑,则是硫酸,和水反应生成硫酸,则是三氧化硫,和氧气反应生成三氧化硫,则是二氧化硫,据此解答.
本题为框图推断题,熟悉浓硫酸脱水性、强的氧化性的性质是解题关键,突破口为“为一种常见酸的浓溶液,能使蔗糖粉末变黑”,题目难度不大.
6.【答案】
【解析】【分析】
本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握有机物的组成、结构和官能团的性质,把握有机物的应用,题目难度不大。
【解答】
A.聚乙烯不含碳碳双键,与酸性高锰酸钾不反应,故A错误;
B.聚丙烯酸树脂含有羧基,可与氢氧化钠溶液反应,故B正确;
C.异戊二烯含有碳碳双键,可发生加聚反应,天然橡胶是加聚产物,故C错误;
D.聚乙二醇结构简式为,题中缺少端基原子或原子团,故D错误。
故选:。
7.【答案】
【解析】解:编号错误,应为,,三甲基乙基戊醇,故A错误;
B.含有羟基,有个相邻碳原子上有氢原子,则的消去反应产物有种,故B错误;
C.含有羟基,能发生取代反应,故C正确;
D.有机物可燃烧,属于氧化反应,故D错误;
故选:。
有机物含有羟基,具有醇的性质,结合有机物的结构特点解答该题。
本题考查有机物的官能团及性质,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握结构与性质的关系是解答本题的关键,题目难度不大。
8.【答案】
【解析】解:.应先在碱性条件下水解生成,由于,则通入二氧化碳气体可生成,所以与足量的溶液共热后,再通入足量即可,故A正确;
B.与稀硫酸共热后生成邻羟基苯甲酸,邻羟基苯甲酸和碳酸钠反应生成,故B错误;
C.与稀共热后生成邻羟基苯甲酸,加入足量的溶液生成,故C错误;
D.与足量的溶液共热后生成,再加入适量生成,故D错误;
故选A.
酸性:,所以碳酸氢钠和反应生成苯甲酸钠、和不反应,将 转变为 ,应先在碱性条件下水解生成,由于,则通入二氧化碳气体可生成.
本题考查化学实验方案评价,为高频考点,侧重考查学生分析判断能力,根据物质结构结合酸性强弱确定反应先后顺序是解本题关键,注意酚羟基能和碳酸钠反应,易错选项是.
9.【答案】
【解析】解:根据结构简式知,其分子式为,故A错误;
B.该分子含有碳碳双键,双键碳上连接的两个基团不同,存在顺反异构,故B正确;
C.含有碳碳双键,可与溴发生加成反应,能使溴的四氯化碳溶液褪色,故C正确;
D.能与氢氧化钠反应的为酚羟基和酯基,则该物质最多能与反应,故D正确;
故选:。
由结构可知分子中含酚、碳碳双键、,结合酚、烯烃、酯的性质来解答。
本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,注意把握有机物的结构特点,为解答易错点,题目难度不大。
10.【答案】
【解析】解:二者的核磁共振氢谱中均只出现两种峰,且峰面积之比分别为:、:,故A错误;
B.二者在醇溶液中均不能发生消去反应,故B错误;
C.卤代烃、甲基等均可发生取代反应,则一定条件下,二者在溶液中均可发生取代反应,故C正确;
D.、中均含种,则一氯代物均有种,故D错误;
故选:。
A.由结构对称性可知,均含种,但原子数目不同;
B.中与苯环相连不能发生消去反应,中与相连的邻位上没有;
C.卤代烃、甲基等均可发生取代反应;
D.、中均含种.
本题考查有机物的结构与性质及推断,为高频考点,把握官能团与性质的关系为解答的关键,侧重结构对称性分析及卤代烃性质的考查,题目难度不大.
11.【答案】
【解析】解:由操作和现象可知,淀粉发生水解生成葡萄糖,确定水解程度,需检验淀粉是否剩余,该实验操作只能证明淀粉水解了,但是无法证明水解是否完全,故A错误;
B.新制得氢氧化铜悬浊液制备不对,应该向溶液中加入少量的溶液,保证溶液显示碱性,否则无法检验醛基,故B错误;
C.苯酚与反应后,与苯分层,然后分液可分离,故C正确;
D.水解后检验溴离子在酸性溶液中,则将与水溶液共热,经充分反应后冷却,向冷却液中加稀酸化后,再加溶液,观察沉淀颜色,若为淡黄色沉淀,可知为溴代烷,故D错误;
故选:。
A.由操作和现象可知,淀粉发生水解生成葡萄糖,确定水解程度需检验淀粉是否有剩余;
B.醛基的检验:加入新制得氢氧化铜悬浊液,加热,看是否出现砖红色沉淀;
C.苯酚与反应后,与苯分层;
D.卤代烃水解后,检验卤素离子在酸性溶液中进行检验。
本题考查化学实验方案的评价,为高频考点,把握物质的性质、物质的检验、物质的制备、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大。
12.【答案】
【解析】【分析】
本题考查化学实验方案的评价,为高频考点,把握物质的性质、混合物分离提纯、物质的制备及检验、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大。
【解答】
A.氯化铵分解后,在试管口又化合生成氯化铵,则不能制备氨气,应选铵盐与碱加热制备,故A错误;
B.生成乙炔中混有硫化氢等,均可被高锰酸钾氧化,则溶液褪色,不能检验乙炔的还原性,故B错误;
C.乙醇与水互溶,不能萃取分离出碘,故C错误;
D.海水中水的沸点较低,则图中蒸馏装置可制取蒸馏水,故D正确。
故本题选D。
13.【答案】
【解析】解:分子中、、、原子个数依次是、、、,分子式为,故A错误;
B.具有硝基苯、酯、烯烃和氨的性质,酯基能发生水解反应,碳碳双键能发生加聚反应,酯基和亚氨基能发生取代反应,故B正确;
C.分子中苯环和碳碳双键能和氢气发生加成反应,碳碳双键能和溴发生加成反应,故C错误;
D.官能团有硝基、碳碳双键、酯基、亚氨基四种官能团,故D错误;
故选:。
A.分子中、、、原子个数依次是、、、;
B.具有硝基苯、酯、烯烃和氨的性质;
C.苯环和碳碳双键能和氢气发生加成反应,碳碳双键能和溴发生加成反应;
D.官能团有硝基、碳碳双键、酯基、亚氨基。
本题考查有机物的结构和性质,侧重考查分析、判断及知识综合运用能力,明确官能团及其性质的关系是解本题关键,题目难度不大。
14.【答案】
【解析】解:由结构可知,单体为、、,的单体之一的分子式为,故A正确;
B.完全水解生成乙二醇和两种高分子化合物,故B错误;
C.单体中存在、、,则通过加聚反应和缩聚反应可以生成,故C正确;
D. 中含,则碱性条件下,完全水解消耗的物质的量为,大于,故D正确;
故选:。
A.由结构可知,单体为、、;
B.完全水解生成乙二醇和两种高分子化合物;
C.单体中存在、、;
D. 中含。
本题考查有机物的结构与性质,为高频考点,明确高分子化合物的结构及官能团是解答本题的关键,注意加聚反应与缩聚反应的区别,题目难度中等.
15.【答案】蒸馏烧瓶 浓硫酸 防止水蒸气进入收集器 沸点较高,不会随着气体逸出 蒸馏法
【解析】解:分析可知,仪器为蒸馏烧瓶,在加热条件下可以氧化浓盐酸产生氯气,其还原产物为,中的化合价由价变为中的价,化合价变化,的化合价由价变为价,化合价变化,由于中的数目为,氯气中有个氯原子,故K的计量数为,的计量数为,反应的离子方程式为,
故答案为:蒸馏烧瓶;;
结合分析可知,装置中试剂为浓硫酸,其作用是防止水蒸气进入收集器,
故答案为:浓硫酸;防止水蒸气进入收集器;
锡屑中含铜杂质导致中产生,但不影响中产品的纯度,原因在于沸点较高,不会随着气体逸出,
故答案为:沸点较高,不会随着气体逸出;
结合图表数据分析可知,与沸点相差很大,故可用蒸馏法分离,
故答案为:蒸馏法;
滴定中,铁元素化合价升高一价,元素将价,则有关系式:,,故产品的纯度为,
故答案为:。
极易水解,反应应在无水环境下进行进行,装置:重铬酸钾和浓盐酸反应的方法制取,反应的方程式为:,制取的氯气中含有氯化氢,饱和食盐水可以降低氯气的溶解,还可洗去氯气中的氯化氢,在空气中极易水解,为防止其水解,用浓硫酸干燥氯气;和锡的反应制备,冷水冷却,可将气态的冷凝回流收集产物;装置中吸收未反应的氯气,防止污染空气,因极易水解,装置可防止溶液的水蒸气进入收集器中;金属锡易与氯气、氧气反应,反应时应先生成氯气,将氧气排出,据此分析回答问题。
本题考查物质的制备实验,为高频考点,把握物质的性质、制备原理、实验装置的作用、实验技能为解答关键,侧重分析与实验能力的考查,知道各个装置的作用及可能发生的反应,题目难度不大。
16.【答案】 氧化性 酸性 把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气
【解析】解:、、、、是化学中常见的物质,常温下,是一种无色无味的液体,考虑为,
是一种黑色单质,是一种常见的难挥发性酸,、都是气体,则为,为浓硫酸,、分别为二氧化碳、二氧化硫中的一种,该反应方程式为:浓,
故答案为:;;
是一种紫红色单质,是一种常见的挥发性酸,反应时生成的是无色气体,则为,为稀硝酸,为,为硝酸铜,反应的离子反应为,生成硝酸铜体现硝酸的酸性,生成体现硝酸的氧化性,
故答案为:;酸性;氧化性;
是一种无色、刺激性气味、密度比空气小的气体,则为,实验室利用铵盐与熟石灰反应制备氨气,该反应方程式为:,则为,
验方法为把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气,
故答案为:;;把湿润的红色石蕊试纸靠近气体,若试纸变蓝,则证明该气体为氨气或用蘸有浓盐酸的玻璃棒靠近该气体,若有白烟生成,则证明该气体为氨气.
A、、、、是化学中常见的物质,常温下,是一种无色无味的液体,考虑为
是一种黑色单质,是一种常见的难挥发性酸,、都是气体,则为,为浓硫酸,、分别为二氧化碳、二氧化硫中的一种;
是一种紫红色单质,是一种常见的挥发性酸,反应时生成的是无色气体,则为,为稀硝酸,为,为硝酸铜;
是一种无色、刺激性气味、密度比空气小的气体,则为,实验室利用铵盐与熟石灰反应制备氨气,利用湿润的红色石蕊试纸检验氨气,或者利用氯化氢与氨气反应生成氯化铵检验.
本题考查无机物的推断,涉及浓硫酸、浓硝酸的性质及氨气的制备,需要学生熟练掌握元素化合物性质与转化,题目难度中等.
17.【答案】乙烯 化学 物理 取代反应或酯化反应 分别滴入酸性溶液,振荡,使溶液褪色的是,不褪色的是
【解析】解:的名称是乙烯;工业上通常对石油分馏产品进行裂解来获得乙烯,故过程为裂解,是化学变化;工业上通过对煤焦油进行分馏而获得苯,过程为分馏,是物理变化;
故答案为:乙烯;化学;物理;
反应为乙醇的催化氧化,化学方程式为;反应为乙酸与环己二醇反应生成酯,故为酯化反应或取代反应;
故答案为:;取代反应或酯化反应;
分子中没有碳碳双键,而分子中有碳碳双键,因此,鉴别与的方法是:分别滴入酸性溶液,振荡,使溶液褪色的是,不褪色的是;
故答案为:分别滴入酸性溶液,振荡,使溶液褪色的是,不褪色的是;
用定一议二法,分子有一定的对称性,六元环上的个碳原子均有原子可以被取代,如图所示,可以先把号或号的原子取代,然后分析另一个原子被取代的可能性,先取代,环上其他碳原子上的均可以被取代,但要注意左右对称,故有种;再先取代,则与相同的位置不能再取代,可以找到种,注意号碳上有个原子可以被取代。综上所述,可以确定中六元环上的氢原子被两个氯原子取代后的有机物有种;
故答案为:。
为,和发生酯化反应取代反应生成,为乙酸,氧化生成,所以为乙醛,催化氧化为,所以为乙醇,和加成生成,所以为乙烯,石油产品经裂解得到乙烯;工业上通过对煤焦油进行分馏而获得苯,发生部分加成生成,发生加成和取代反应生成,
用定一议二法,分子有一定的对称性,六元环上的个碳原子均有原子可以被取代,如图所示,可以先把号或号的原子取代,然后分析另一个原子被取代的可能性,先取代,环上其他碳原子上的均可以被取代,但要注意左右对称,故有种;再先取代,则与相同的位置不能再取代,可以找到种,注意号碳上有个原子可以被取代。
本题考查有机物的推断与合成,根据有机物的结构进行分析,需要学生熟练掌握官能团的性质与转化,试题培养了学生的知识迁移运用能力,难度中等。
18.【答案】羟基或羰基 酰胺键 消去反应 保护氨基
【解析】解:中的含氧官能团名称为羟基、羰基、酰胺键任写两种,
故答案为:羟基、羰基、酰胺键任写两种;
中醇羟基发生消去反应生成中碳碳双键,所以的反应类型为消去反应,
故答案为:消去反应;
的一种同分异构体:能发生银镜反应,说明含有醛基;能发生水解反应,其水解产物之一能与溶液发生显色反应,说明水解可生成酚羟基,应含有结构;分子中只有种不同化学环境的氢,应为对称结构,则同分异构体可为,
故答案为:;
通过以上分析知,的结构简式为,
故答案为:;
发生水解反应生成,的反应方程式为,
故答案为:;
的作用为保护氨基,
故答案为:保护氨基;
以甲苯和为原料用四步制备,苯环和硝酸发生取代反应生成硝基、硝基被还原生成氨基、氨基和乙酸酐发生取代反应生成,甲基被氧化生成,其合成路线为,
故答案为:。
中硝基被还原生成中氨基,中氨基上氢原子被取代生成,中苯环上的氢原子被取代生成,经还原得到,的分子是为,结合、结构简式差别知,中溴原子和酚羟基发生取代反应生成为,中醇羟基发生消去反应生成中碳碳双键,发生水解反应生成中氨基;
以甲苯和为原料用四步制备,苯环和硝酸发生取代反应生成硝基、硝基被还原生成氨基、氨基和乙酸酐发生取代反应生成,甲基被氧化生成。
本题考查有机物的合成与推断、有机反应类型、官能团结构与性质、限制条件同分异构体书写,是对有机会基础的综合考查,较好的考查学生信息获取与知识迁移运用,题目有利于培养学生的分析能力,难度中等。
第1页,共1页
同课章节目录
