2023九(上)针对性训练(第二章)A(含答案)
文档属性
| 名称 | 2023九(上)针对性训练(第二章)A(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-10-07 09:03:38 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2023针对性训练 第二章A
一、选择题
1. 永嘉乌牛早茶是我国茶类中较早发芽的品种,3月上旬即可采制,味醇气香,为茶中珍品。根据信息回答。乌牛早茶中含有茶氨酸(C2H14N2O3),它属于物质类别中的( )
A、单质 B、氧化物 C、无机物 D、有机物
2. 使用氢能源汽车可有效减少二氧化碳的排放,实现“碳中和”。单质硼(B)可与水反应制取氢气,化学方程式为:2B+6H2O2B(OH)3+3H2↑,该反应属于( )
A、置换反应 B、化合反应 C、分解反应 D、复分解反应
3. 为验证Fe、Cu的金属活动性,下列方案中不可行的是( )
4. 材料与人类生活密切相关,下列物品的主要成分属于有机合成材料的是( )
A、铁艺笔筒 B、塑料垃圾桶 C、木质书桌 D、陶瓷餐具
5. 我国科学家研究出碳化钼(Mo2C)负载金原子组成的高效催化体系,使水煤气中的CO和H2O在120℃下发生反应,反应微观模型如图所示,下列说法正确的是( )
A、金原子对CO起吸附催化作用
B、反应中分子的数目发生了改变
C、该化学反应类型为化合反应
D、碳化钼在反应前后化学性质发生了改变
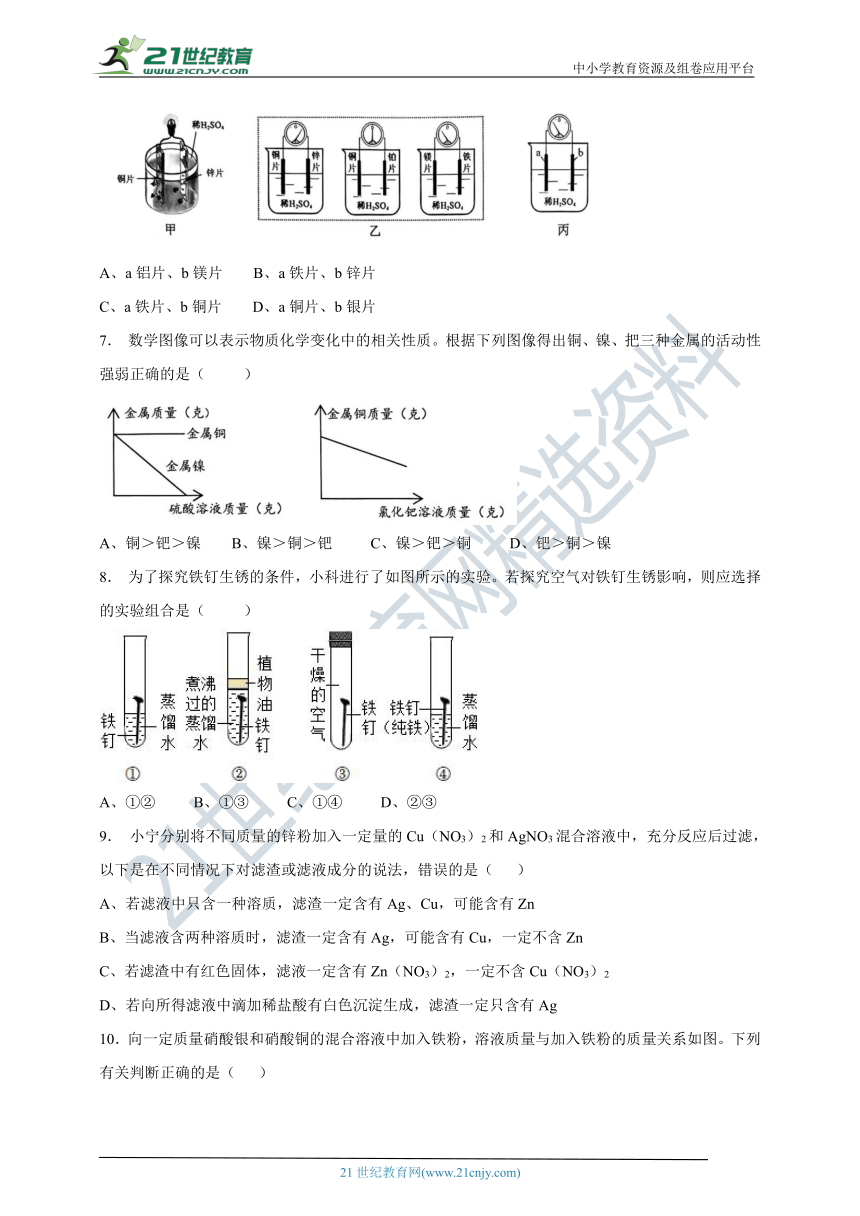
6. (2023·绍兴)小敏阅读教材得知:将铜片和锌片同时插入稀H2SO4,可以组成一个电池(图甲)。那么该电池的正负极与什么有关呢?对此,小敏做了三组实验,并借助灵敏电流表进行判断(图乙)。发现该电池的正负极与金属活动性强弱有关,且存在一定规律。据此判断,下列金属片组合可以使电流表指针向左偏转(图丙)的是( )
A、a铝片、b镁片 B、a铁片、b锌片
C、a铁片、b铜片 D、a铜片、b银片
7. 数学图像可以表示物质化学变化中的相关性质。根据下列图像得出铜、镍、把三种金属的活动性强弱正确的是( )
A、铜>钯>镍 B、镍>铜>钯 C、镍>钯>铜 D、钯>铜>镍
8. 为了探究铁钉生锈的条件,小科进行了如图所示的实验。若探究空气对铁钉生锈影响,则应选择的实验组合是( )
A、①② B、①③ C、①④ D、②③
9. 小宁分别将不同质量的锌粉加入一定量的Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤,以下是在不同情况下对滤渣或滤液成分的说法,错误的是( )
A、若滤液中只含一种溶质,滤渣一定含有Ag、Cu,可能含有Zn
B、当滤液含两种溶质时,滤渣一定含有Ag,可能含有Cu,一定不含Zn
C、若滤渣中有红色固体,滤液一定含有Zn(NO3)2,一定不含Cu(NO3)2
D、若向所得滤液中滴加稀盐酸有白色沉淀生成,滤渣一定只含有Ag
10.向一定质量硝酸银和硝酸铜的混合溶液中加入铁粉,溶液质量与加入铁粉的质量关系如图。下列有关判断正确的是( )
A、在a点时溶液中只含有的金属离子为Cu2+、Ag+
B、在b点时向溶液中滴加稀盐酸有白色沉淀生成
C、在c点时过滤后得到溶液的质量大于原混合溶液的质量
D、在d点时过滤得到的固体物质一定有Ag、Cu、Fe
11.模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸铜和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( )
A B C D
12.将镁粉(如图0b段)和稀盐酸(b点后)先后加入到一定量的氯化铜溶液中,搅拌使之充分反应,过滤得到沉淀物。整个过程中加入物质的质量与沉淀物的质量关系如图所示。下列说法错误的是( )
A、横坐标b的数值为4.8
B、图像中m点对应的沉淀物是Cu
C、实验过程中共产生MgCl2的质量为9.5g
D、取n点对应的滤液加铁粉,会产生气泡
13.比较归纳是化学学习中常用的一种方法。以下是C、CH4、CO三种物质转化为CO2的转化关系,①C→CO2;②CH4→CO2;③CO→CO2,对它们的比较归纳正确的是( )
A、三种转化发生的都是化合反应
B、三种转化的过程中都放出热量
C、三种物质都只能跟氧气反应才能转化为二氧化碳
D、三种物质都可以在点燃条件下发生反应转化为二氧化碳
14.小金为探究金属的化学性质进行了以下实验,下列说法错误的是( )
A、对照试管A与B,不能判定锌、铁两者的活动性顺序
B、对照试管C与D,不能判定铁、铜、银三者的活动性顺序
C、试管C反应结束后,试管内溶液质量增大
D、试管D反应结束后,铁丝下端表面变红色
15.某化学小组在一定量AgNO3和Al(NO3)3的混合溶液中加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,则①溶液甲中一定含有Al(NO3)3和Zn(NO3)2;②固体乙中一定含有Ag,可能含有Cu和Zn;③若溶液甲呈蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2;④向固体乙中滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2。上述四种说法正确的个数为( )
A、1个 B、2个 C、3个 D、4个
二、填空题
16.(2023·金华)2023世界氢能技术大会于5月22~26日在中国举行,大会聚焦双碳战略下全球氢能领域的最新研究成果。目前有科学家利用太阳能产生激光,再用激光使水分解得到氢气和氧气实现“制氢”;在“储氢”领域,可以将二氧化碳和氢气在一定条件下反应生成甲烷和水,实现二氧化碳的再利用和“储氢”。回答下列问题。
(1)上述“制氢”过程中用激光使水分解的反应,属于基本反应类型中的_______。
(2)上述“储氢“过程中发生反应的化学方程式为_________。
17.2023年杭州亚运会火种灯采用双层玻璃结构,在低温、严寒、大风等环境下不会熄灭。其创意源自于青铜器精品“中华第一灯”——西汉长信宫灯。
(1)火种燃料使用的清洁能源是丙烷(C3H8),丙烷属于化合物中的______ (选填“有机物”或“无机物”)。
(2)如果灯体上部封闭,不与导烟气腔连通,火焰容易熄灭,原因是_________。
(3)我国炼铜技术历史悠久。古人将赤铜(Cu2O)和炉甘石、木炭粉混合高温制得黄铜:X+Cu2O+C QUOTE Zn+2Cu+2CO2↑。则炉甘石主要成分X的化学式为_________。
18.如图是科学兴趣小组的同学利用“W”型管进行CO还原CuO的微型实验简略图,请回答问题:
(1)反应前应该先________。(填“点燃酒精灯”或“通一氧化碳”)
(2)小科在C处增加一个点燃的酒精灯,他这样做的目的是________。
19.(2023 包头)内蒙古矿产资源丰富,某炼铁厂利用当地的煤炭和赤铁矿石作为高炉炼铁的主要原料,其主要反应过程如图所示(部分反应物、生成物及反应条件已略去)。
据此回答问题:
(1)A的化学式为_________。
(2)用化学方程式表示一氧化碳炼铁的原理_______________,实际上高炉炼得的铁是生铁,生铁属于_________(填“纯净物”或“混合物”)。
(3)生铁等金属制品易锈蚀,请你列举一种防止铁制品锈蚀的方法_________。
20.(2023 成都)利用如图实验探究金属的化学性质。
(1)实验一:水的作用是_________。实验中,观察到发出白光后铁丝并未燃烧,原因是_________。
(2)实验二:两个反应均生成了______(填物质名称)。比较铁和铝的金属活动性强弱,从试剂角度需考虑:①加入同样大小的铁片和铝片;②____________。
(3)实验三:反应的化学方程式为____________。再补充一个实验可得出Cu、Fe、Ag的金属活动性顺序。设计并进行实验,补全下表。
实验步骤(可用图示) 实验现象 实验结论
21.生活中的常见物品往往由多种材料组成,如图是温州市街道垃圾桶的材料组成。
(1)按照物质的组成来分类,垃圾桶的三种材料中,___________属于有机合成材料。
(2)垃圾桶的铁质外筒很容易生锈,请你提一条防止生锈的建议:_____________________。
(3)金属材料的回收利用,有利于材料的综合利用。实验室里有一杯含 Al(NO3)3、Cu(NO3)2、 AgNO3的废液,小明向杯中加入一定质量的锌粉,充分反应后滤液从蓝色变成浅蓝色,过滤得到滤渣。则滤渣中回收到的金属一定含有_________。
22.(2023 广州)我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。
(1)日常生活中,适合制作电缆的金属是__________(填标号)。
A、金 B、铜 C、汞 D、钨
(2)明代《天工开物》描述了锡的冶炼方法,如图a。
①原料锡砂中的SnO2和木炭反应得到锡和二氧化碳,化学方程式为____________________。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是_____________。
(3)图b为古代炼锌工艺原理示意图。炉甘石成分是ZnCO3,高温易分解生成ZnO。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是_________。
②已知锌的沸点为907℃,泥罐下部温度可达1200℃,上部约为600℃,该工艺从反应混合物中收集液态锌的方法属于__________(填标号)。
A、结晶 B、蒸发 C、蒸馏 D、升华
③必须冷却后才能取锌,是为了防止发生反应:______________(写化学方程式)。
(4)湿法冶金利用置换反应。向Cu(NO3)2、AgNO3混合液中加入Fe粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是________。
23.(2023·金华)某混合气体由CO、CO2、H2、水蒸气中的两种组成。小金利用如图装置探究其成分(所用药品均足量,反应均完全)。
(1)检查装置气密性:在甲、丙装置中倒入适量的水,关闭丙丁之间止水夹,往甲装置中鼓入一定量空气后,停止鼓气。如果气密性良好,甲装置中广口瓶内观察到的现象是_________。
(2)实验过程中,先点燃丁处酒精灯,再通入混合气体,过一会点燃乙处酒精灯,先观察到丙装置中澄清石灰水变浑浊,过一会观察到乙装置中黑色粉末变红,甲装置电子天平读数恒定不变,则原混合气体组成可能是________。
三、探究题
24.食品脱氧剂的主要成分是铁粉,另还有少量的活性炭和氯化钠等物质,能通过化学反应除尽密 闭包装袋中的氧气,使食品处于无氧状态,有效控制微生物的生长,延长食品保质期。某兴趣小组在学校实验室用图甲的装置检验食品脱氧剂的除氧能力。
(1)图甲的实验前,需要检查装置气密性,具体的操作:____________________。
(2)在图甲的装置中装入 1 克食品脱氧剂,记录量筒内液面随时间变化的情况如下表:
实验时间(分钟) 0 5 10 30 35 45
量筒内液面的刻度(毫升) 50 35 27.5 20 20 20
根据实验数据,兴趣小组推理出30分钟时食品脱氧剂基本耗尽了广口瓶中的氧气,他们推理的依据是:_______________________________。
(3)兴趣小组进一步设计了图乙和图丙的对照实验,他们要探究的问题是:___________。
25.小龙利用“氢气还原氧化铜" 实验验证水的组成,实验装置及药品如图所示。回答问题:
(1)为了实验安全,在开始加热硬质玻璃管内氧化铜前,应先进行的实验操作是________。
(2)小港认为U型管的末端还应该接上一个相同的U型管(内装碱石灰),你觉得是否有必要,请说明理由________。
(3)为验证水的组成,实验中需要测出的数据是________。
四、简答题
26.黄铜(铜锌合金)长期使用会锈蚀,铜锈主要成分为 Cu2(OH)2CO3。查阅资料:铜锈可以与稀硫酸反应。其化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,杂质不与稀硫酸反应。从废黄铜中制备铜和硫酸锌的工艺流程如图。
(1)实验前需将废黄铜粉碎,其目的是:_______。
(2)溶液A中含有的溶质是___________________。
(3)小龙制备硫酸锌晶体前,先将锌和稀硫酸充分反应后过滤,发现滤液中含有硫酸,使制得的硫酸锌纯度下降。为了测定所得滤液中硫酸锌和硫酸的质量比,他取少量滤液倒入烧杯,将溶质质量分数为10%的氢氧化钠溶液逐渐加入。除要知道实验前氢氧化钠溶液质量外,实验中还要通过测量获取哪两个数据,才可计算硫酸锌与硫酸的质量比?______。(硫酸锌与氢氧化钠反应的化学方程式:ZnSO4+2NaOH=Zn(OH)2↓+Na2SO4)
27.中国“天宫”空间站设计有水处理系统,通过蒸馏将宇航员的汗液、尿液等进行回收处理,并用于电解制氧气。
(1)尿液加热蒸馏时会产生有毒物质,为安全起见,必须在较低温度下使尿液中的水蒸发。可采取的方法是_________。
(2)3名航天员每天约需1650升氧气,若每天净化回收5.4千克水并全部用于电解制氧气,能否满足航天员呼吸所需?(氧气的密度为1.3克/升,2H2O2H2↑+O2↑)
(3)除电解水之外,制取氧气的方法还有:①超氧化物制氧:4KO2+2CO2=2K2CO3+3O2;
②氯酸盐热分解制氧:2NaClO32NaCl+3O2↑。在航天器中,最终选择了电解水制氧气,相较方法①和②,其优势是____________。
参考答案
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 D A C B A C B A C D
题号 11 12 13 14 15
答案 C C D C D
二、填空题
16.(1)分解反应
(2)CO2+4H2CH4+2H2O
17.(1)有机物
(2)隔绝氧气(氧气或者空气不够)
(3)ZnCO3(碳酸锌)
18.(1)通一氧化碳 (2)尾气处理,防止污染空气
19.(1)CO2
(2)Fe2O3+3CO2Fe+3CO2;混合物
(3)刷漆
20.(1)防止生成的高温熔化物溅落下来使瓶底炸裂;火柴燃烧消耗了较多的氧气,使氧气不足;
(2)氢气;加入等体积等浓度的稀盐酸
(3)Cu+2AgNO3=Cu(NO3)2+2Ag
取少量硫酸亚铁溶液于试管中,放入铜丝
无明显变化
21.(1)塑料顶盖 (2)刷油漆等 (3)银、铜
22.(1)B
(2)①C+SnO2Sn+CO2↑
②形成合金熔点降低
(3)①作还原剂 ②C ③2Zn+O22ZnO
(4)银离子或Ag+
23.(1)长导管中液柱液面高于瓶内液面并保持稳定
(2)①CO2 H2 ②CO2 CO
三、探究题
24.(1)用手或热毛巾捂住广口瓶,观察量筒内是否有气泡冒出,若有气泡冒出,则气密性良好
(2)30分钟时量筒内液面为20毫升,随后保持不变,有30毫升水进入集气瓶中,即消耗了约30毫升氧气,约占集气瓶中空气体积的1/5。
(3)铁粉和脱氧剂的脱氧能力一样吗?(或脱氧剂中的活性炭和氯化钠能加快脱氧速度吗?)
25.(1)通一段时间的氢气(或检验氢气纯度)
(2)有必要,因为U型管中的碱石灰会吸收空气中的水和二氧化碳干扰实验
(3)硬质玻璃管内的药品反应前后的质量差和U型管内药品反应前后的质量差
四、简答题
26.(1)增大反应接触面积,使锌、铜锈与稀硫酸充分反应
(2) CuSO4、ZnSO4、H2SO4
(3)刚出现沉淀时剩余氢氧化钠溶液的质量;不再出现沉淀时剩余氢氧化钠溶液的质量
27.(1)在低压环境下蒸馏
(2)解:氧气的质量为1.3克/升×1650升=2145克=2.145千克
设5.4千克H2O电解生成氧气的质量为x。
2H2O2H2↑+O2↑
36 32
5.4千克 x
=
x=4.8千克>2.145千克
答:能满足航天员呼吸所需。
(3)原料易得;实现水循环利用;空间站电能充足,无需考虑耗能;
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
2023针对性训练 第二章A
一、选择题
1. 永嘉乌牛早茶是我国茶类中较早发芽的品种,3月上旬即可采制,味醇气香,为茶中珍品。根据信息回答。乌牛早茶中含有茶氨酸(C2H14N2O3),它属于物质类别中的( )
A、单质 B、氧化物 C、无机物 D、有机物
2. 使用氢能源汽车可有效减少二氧化碳的排放,实现“碳中和”。单质硼(B)可与水反应制取氢气,化学方程式为:2B+6H2O2B(OH)3+3H2↑,该反应属于( )
A、置换反应 B、化合反应 C、分解反应 D、复分解反应
3. 为验证Fe、Cu的金属活动性,下列方案中不可行的是( )
4. 材料与人类生活密切相关,下列物品的主要成分属于有机合成材料的是( )
A、铁艺笔筒 B、塑料垃圾桶 C、木质书桌 D、陶瓷餐具
5. 我国科学家研究出碳化钼(Mo2C)负载金原子组成的高效催化体系,使水煤气中的CO和H2O在120℃下发生反应,反应微观模型如图所示,下列说法正确的是( )
A、金原子对CO起吸附催化作用
B、反应中分子的数目发生了改变
C、该化学反应类型为化合反应
D、碳化钼在反应前后化学性质发生了改变
6. (2023·绍兴)小敏阅读教材得知:将铜片和锌片同时插入稀H2SO4,可以组成一个电池(图甲)。那么该电池的正负极与什么有关呢?对此,小敏做了三组实验,并借助灵敏电流表进行判断(图乙)。发现该电池的正负极与金属活动性强弱有关,且存在一定规律。据此判断,下列金属片组合可以使电流表指针向左偏转(图丙)的是( )
A、a铝片、b镁片 B、a铁片、b锌片
C、a铁片、b铜片 D、a铜片、b银片
7. 数学图像可以表示物质化学变化中的相关性质。根据下列图像得出铜、镍、把三种金属的活动性强弱正确的是( )
A、铜>钯>镍 B、镍>铜>钯 C、镍>钯>铜 D、钯>铜>镍
8. 为了探究铁钉生锈的条件,小科进行了如图所示的实验。若探究空气对铁钉生锈影响,则应选择的实验组合是( )
A、①② B、①③ C、①④ D、②③
9. 小宁分别将不同质量的锌粉加入一定量的Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤,以下是在不同情况下对滤渣或滤液成分的说法,错误的是( )
A、若滤液中只含一种溶质,滤渣一定含有Ag、Cu,可能含有Zn
B、当滤液含两种溶质时,滤渣一定含有Ag,可能含有Cu,一定不含Zn
C、若滤渣中有红色固体,滤液一定含有Zn(NO3)2,一定不含Cu(NO3)2
D、若向所得滤液中滴加稀盐酸有白色沉淀生成,滤渣一定只含有Ag
10.向一定质量硝酸银和硝酸铜的混合溶液中加入铁粉,溶液质量与加入铁粉的质量关系如图。下列有关判断正确的是( )
A、在a点时溶液中只含有的金属离子为Cu2+、Ag+
B、在b点时向溶液中滴加稀盐酸有白色沉淀生成
C、在c点时过滤后得到溶液的质量大于原混合溶液的质量
D、在d点时过滤得到的固体物质一定有Ag、Cu、Fe
11.模型能够直观反映化学变化的结果。将一定质量的镁条放入某一溶液(如图),其溶质硫酸铜和硫酸亚铁的质量相同,充分反应后烧杯内固体的组成和质量大小关系不可能的是( )
A B C D
12.将镁粉(如图0b段)和稀盐酸(b点后)先后加入到一定量的氯化铜溶液中,搅拌使之充分反应,过滤得到沉淀物。整个过程中加入物质的质量与沉淀物的质量关系如图所示。下列说法错误的是( )
A、横坐标b的数值为4.8
B、图像中m点对应的沉淀物是Cu
C、实验过程中共产生MgCl2的质量为9.5g
D、取n点对应的滤液加铁粉,会产生气泡
13.比较归纳是化学学习中常用的一种方法。以下是C、CH4、CO三种物质转化为CO2的转化关系,①C→CO2;②CH4→CO2;③CO→CO2,对它们的比较归纳正确的是( )
A、三种转化发生的都是化合反应
B、三种转化的过程中都放出热量
C、三种物质都只能跟氧气反应才能转化为二氧化碳
D、三种物质都可以在点燃条件下发生反应转化为二氧化碳
14.小金为探究金属的化学性质进行了以下实验,下列说法错误的是( )
A、对照试管A与B,不能判定锌、铁两者的活动性顺序
B、对照试管C与D,不能判定铁、铜、银三者的活动性顺序
C、试管C反应结束后,试管内溶液质量增大
D、试管D反应结束后,铁丝下端表面变红色
15.某化学小组在一定量AgNO3和Al(NO3)3的混合溶液中加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,则①溶液甲中一定含有Al(NO3)3和Zn(NO3)2;②固体乙中一定含有Ag,可能含有Cu和Zn;③若溶液甲呈蓝色,则溶液甲一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2;④向固体乙中滴加盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2。上述四种说法正确的个数为( )
A、1个 B、2个 C、3个 D、4个
二、填空题
16.(2023·金华)2023世界氢能技术大会于5月22~26日在中国举行,大会聚焦双碳战略下全球氢能领域的最新研究成果。目前有科学家利用太阳能产生激光,再用激光使水分解得到氢气和氧气实现“制氢”;在“储氢”领域,可以将二氧化碳和氢气在一定条件下反应生成甲烷和水,实现二氧化碳的再利用和“储氢”。回答下列问题。
(1)上述“制氢”过程中用激光使水分解的反应,属于基本反应类型中的_______。
(2)上述“储氢“过程中发生反应的化学方程式为_________。
17.2023年杭州亚运会火种灯采用双层玻璃结构,在低温、严寒、大风等环境下不会熄灭。其创意源自于青铜器精品“中华第一灯”——西汉长信宫灯。
(1)火种燃料使用的清洁能源是丙烷(C3H8),丙烷属于化合物中的______ (选填“有机物”或“无机物”)。
(2)如果灯体上部封闭,不与导烟气腔连通,火焰容易熄灭,原因是_________。
(3)我国炼铜技术历史悠久。古人将赤铜(Cu2O)和炉甘石、木炭粉混合高温制得黄铜:X+Cu2O+C QUOTE Zn+2Cu+2CO2↑。则炉甘石主要成分X的化学式为_________。
18.如图是科学兴趣小组的同学利用“W”型管进行CO还原CuO的微型实验简略图,请回答问题:
(1)反应前应该先________。(填“点燃酒精灯”或“通一氧化碳”)
(2)小科在C处增加一个点燃的酒精灯,他这样做的目的是________。
19.(2023 包头)内蒙古矿产资源丰富,某炼铁厂利用当地的煤炭和赤铁矿石作为高炉炼铁的主要原料,其主要反应过程如图所示(部分反应物、生成物及反应条件已略去)。
据此回答问题:
(1)A的化学式为_________。
(2)用化学方程式表示一氧化碳炼铁的原理_______________,实际上高炉炼得的铁是生铁,生铁属于_________(填“纯净物”或“混合物”)。
(3)生铁等金属制品易锈蚀,请你列举一种防止铁制品锈蚀的方法_________。
20.(2023 成都)利用如图实验探究金属的化学性质。
(1)实验一:水的作用是_________。实验中,观察到发出白光后铁丝并未燃烧,原因是_________。
(2)实验二:两个反应均生成了______(填物质名称)。比较铁和铝的金属活动性强弱,从试剂角度需考虑:①加入同样大小的铁片和铝片;②____________。
(3)实验三:反应的化学方程式为____________。再补充一个实验可得出Cu、Fe、Ag的金属活动性顺序。设计并进行实验,补全下表。
实验步骤(可用图示) 实验现象 实验结论
21.生活中的常见物品往往由多种材料组成,如图是温州市街道垃圾桶的材料组成。
(1)按照物质的组成来分类,垃圾桶的三种材料中,___________属于有机合成材料。
(2)垃圾桶的铁质外筒很容易生锈,请你提一条防止生锈的建议:_____________________。
(3)金属材料的回收利用,有利于材料的综合利用。实验室里有一杯含 Al(NO3)3、Cu(NO3)2、 AgNO3的废液,小明向杯中加入一定质量的锌粉,充分反应后滤液从蓝色变成浅蓝色,过滤得到滤渣。则滤渣中回收到的金属一定含有_________。
22.(2023 广州)我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。
(1)日常生活中,适合制作电缆的金属是__________(填标号)。
A、金 B、铜 C、汞 D、钨
(2)明代《天工开物》描述了锡的冶炼方法,如图a。
①原料锡砂中的SnO2和木炭反应得到锡和二氧化碳,化学方程式为____________________。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是_____________。
(3)图b为古代炼锌工艺原理示意图。炉甘石成分是ZnCO3,高温易分解生成ZnO。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是_________。
②已知锌的沸点为907℃,泥罐下部温度可达1200℃,上部约为600℃,该工艺从反应混合物中收集液态锌的方法属于__________(填标号)。
A、结晶 B、蒸发 C、蒸馏 D、升华
③必须冷却后才能取锌,是为了防止发生反应:______________(写化学方程式)。
(4)湿法冶金利用置换反应。向Cu(NO3)2、AgNO3混合液中加入Fe粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是________。
23.(2023·金华)某混合气体由CO、CO2、H2、水蒸气中的两种组成。小金利用如图装置探究其成分(所用药品均足量,反应均完全)。
(1)检查装置气密性:在甲、丙装置中倒入适量的水,关闭丙丁之间止水夹,往甲装置中鼓入一定量空气后,停止鼓气。如果气密性良好,甲装置中广口瓶内观察到的现象是_________。
(2)实验过程中,先点燃丁处酒精灯,再通入混合气体,过一会点燃乙处酒精灯,先观察到丙装置中澄清石灰水变浑浊,过一会观察到乙装置中黑色粉末变红,甲装置电子天平读数恒定不变,则原混合气体组成可能是________。
三、探究题
24.食品脱氧剂的主要成分是铁粉,另还有少量的活性炭和氯化钠等物质,能通过化学反应除尽密 闭包装袋中的氧气,使食品处于无氧状态,有效控制微生物的生长,延长食品保质期。某兴趣小组在学校实验室用图甲的装置检验食品脱氧剂的除氧能力。
(1)图甲的实验前,需要检查装置气密性,具体的操作:____________________。
(2)在图甲的装置中装入 1 克食品脱氧剂,记录量筒内液面随时间变化的情况如下表:
实验时间(分钟) 0 5 10 30 35 45
量筒内液面的刻度(毫升) 50 35 27.5 20 20 20
根据实验数据,兴趣小组推理出30分钟时食品脱氧剂基本耗尽了广口瓶中的氧气,他们推理的依据是:_______________________________。
(3)兴趣小组进一步设计了图乙和图丙的对照实验,他们要探究的问题是:___________。
25.小龙利用“氢气还原氧化铜" 实验验证水的组成,实验装置及药品如图所示。回答问题:
(1)为了实验安全,在开始加热硬质玻璃管内氧化铜前,应先进行的实验操作是________。
(2)小港认为U型管的末端还应该接上一个相同的U型管(内装碱石灰),你觉得是否有必要,请说明理由________。
(3)为验证水的组成,实验中需要测出的数据是________。
四、简答题
26.黄铜(铜锌合金)长期使用会锈蚀,铜锈主要成分为 Cu2(OH)2CO3。查阅资料:铜锈可以与稀硫酸反应。其化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑,杂质不与稀硫酸反应。从废黄铜中制备铜和硫酸锌的工艺流程如图。
(1)实验前需将废黄铜粉碎,其目的是:_______。
(2)溶液A中含有的溶质是___________________。
(3)小龙制备硫酸锌晶体前,先将锌和稀硫酸充分反应后过滤,发现滤液中含有硫酸,使制得的硫酸锌纯度下降。为了测定所得滤液中硫酸锌和硫酸的质量比,他取少量滤液倒入烧杯,将溶质质量分数为10%的氢氧化钠溶液逐渐加入。除要知道实验前氢氧化钠溶液质量外,实验中还要通过测量获取哪两个数据,才可计算硫酸锌与硫酸的质量比?______。(硫酸锌与氢氧化钠反应的化学方程式:ZnSO4+2NaOH=Zn(OH)2↓+Na2SO4)
27.中国“天宫”空间站设计有水处理系统,通过蒸馏将宇航员的汗液、尿液等进行回收处理,并用于电解制氧气。
(1)尿液加热蒸馏时会产生有毒物质,为安全起见,必须在较低温度下使尿液中的水蒸发。可采取的方法是_________。
(2)3名航天员每天约需1650升氧气,若每天净化回收5.4千克水并全部用于电解制氧气,能否满足航天员呼吸所需?(氧气的密度为1.3克/升,2H2O2H2↑+O2↑)
(3)除电解水之外,制取氧气的方法还有:①超氧化物制氧:4KO2+2CO2=2K2CO3+3O2;
②氯酸盐热分解制氧:2NaClO32NaCl+3O2↑。在航天器中,最终选择了电解水制氧气,相较方法①和②,其优势是____________。
参考答案
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 D A C B A C B A C D
题号 11 12 13 14 15
答案 C C D C D
二、填空题
16.(1)分解反应
(2)CO2+4H2CH4+2H2O
17.(1)有机物
(2)隔绝氧气(氧气或者空气不够)
(3)ZnCO3(碳酸锌)
18.(1)通一氧化碳 (2)尾气处理,防止污染空气
19.(1)CO2
(2)Fe2O3+3CO2Fe+3CO2;混合物
(3)刷漆
20.(1)防止生成的高温熔化物溅落下来使瓶底炸裂;火柴燃烧消耗了较多的氧气,使氧气不足;
(2)氢气;加入等体积等浓度的稀盐酸
(3)Cu+2AgNO3=Cu(NO3)2+2Ag
取少量硫酸亚铁溶液于试管中,放入铜丝
无明显变化
21.(1)塑料顶盖 (2)刷油漆等 (3)银、铜
22.(1)B
(2)①C+SnO2Sn+CO2↑
②形成合金熔点降低
(3)①作还原剂 ②C ③2Zn+O22ZnO
(4)银离子或Ag+
23.(1)长导管中液柱液面高于瓶内液面并保持稳定
(2)①CO2 H2 ②CO2 CO
三、探究题
24.(1)用手或热毛巾捂住广口瓶,观察量筒内是否有气泡冒出,若有气泡冒出,则气密性良好
(2)30分钟时量筒内液面为20毫升,随后保持不变,有30毫升水进入集气瓶中,即消耗了约30毫升氧气,约占集气瓶中空气体积的1/5。
(3)铁粉和脱氧剂的脱氧能力一样吗?(或脱氧剂中的活性炭和氯化钠能加快脱氧速度吗?)
25.(1)通一段时间的氢气(或检验氢气纯度)
(2)有必要,因为U型管中的碱石灰会吸收空气中的水和二氧化碳干扰实验
(3)硬质玻璃管内的药品反应前后的质量差和U型管内药品反应前后的质量差
四、简答题
26.(1)增大反应接触面积,使锌、铜锈与稀硫酸充分反应
(2) CuSO4、ZnSO4、H2SO4
(3)刚出现沉淀时剩余氢氧化钠溶液的质量;不再出现沉淀时剩余氢氧化钠溶液的质量
27.(1)在低压环境下蒸馏
(2)解:氧气的质量为1.3克/升×1650升=2145克=2.145千克
设5.4千克H2O电解生成氧气的质量为x。
2H2O2H2↑+O2↑
36 32
5.4千克 x
=
x=4.8千克>2.145千克
答:能满足航天员呼吸所需。
(3)原料易得;实现水循环利用;空间站电能充足,无需考虑耗能;
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
