2023九(上)针对性训练(第二章)B(含答案)
文档属性
| 名称 | 2023九(上)针对性训练(第二章)B(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-10-07 09:08:21 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2023针对性训练 第二章B
一、选择题
1. (2023 江西)大国工匠秦世俊展现数控技术所使用的0.01mm铝箔,是由铝块加工而成,这体现了铝具有( )
A、密度小 B、导电性 C、导热性 D、延展性
2. 某工厂排放的废水中含有较多的硫酸铜,从回收利用铜的角度考虑,切实可行的方案是在废水中加入( )
A、盐酸 B、硫酸 C、铁粉 D、碳酸钙
3. (2023 陕西)用下列各组物质进行实验,能验证Mg、Ag、Cu三种金属活动性强弱的是( )
A、Mg、Ag、Cu、稀硫酸 B、Mg、Ag、CuSO4溶液
C、Ag、Cu、MgCl2溶液 D、Ag、CuCl2溶液、MgSO4溶液
4. 锰(Mn)和镍(Ni)是两种不常见的金属,为了比较锰、镍和锌的金属活动性,小明同学在老师的指导下进行了实验,结果如下表:
则它们的金属活动性顺序为( )
A、Zn >Ni>Mn B、Zn>Mn>Ni C、Mn>Zn>Ni D、Ni>Mn>Zn
5. 将镁、锌、铜、银四种金属片加入盛有稀硫酸的试管中,观测结果如图,则其中发生的化学反应类型为( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应
6. 房屋装修过程中易产生有毒气体甲醛(化学式CH2O),如图表示甲醛在纳米膜催化下与氧气()反应转化为水和二氧化碳的过程。其中“”表示的分子是( )
A、CH2O B、O2 C、CO2 D、H2O
7. 秀秀通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A、Fe>Ag>R B、Fe>R>Ag
C、R>Fe>Ag D、Ag>R>Fe
8. (2023 广州)钴(Co)的金属活动性与铁相似,钴的化合物相关性质如表。下列预测合理的是( )
物质 CoO Co(OH)2 CoCl2 CoCO3
在水中的溶解性 难溶,灰绿色固体 难溶,粉红色固体 易溶,溶液呈粉红色 难溶,粉红色固体
A、Co能从MgCl2溶液中置换出Mg
B、CoO能与盐酸反应得到粉红色溶液
C、CoCO3能与盐酸反应生成H2
D、Co(OH)2可由Co与NaOH溶液反应制得
9. 我国自主研发的深海载人潜水器球壳,是世界上最大的载人舱球壳,已在马里亚纳海沟海域完成万米海试任务。在开发深海潜水舱时,科研团队要考虑深海压强大、海水腐蚀强、上浮困难等问题,如图是中科院研究团队研发的钛合金深海潜水器球舱,解决了以上问题。以下说法不正确的是( )
A、钛合金属于化合物
B、钛合金具有较好的抗压和抗腐蚀性能
C、钛合金的密度大小会影响上浮的难易程度
D、合金往往比纯金属具有更好的性能
10.(2023 郴州)为验证铁、铜、银三种金属的活动性顺序,小东设计了如下所示的两组实验。下列说法正确的是( )
A、通过实验①、②能够验证三种金属的活动性顺序
B、实验②中发生的反应是:2Ag+CuSO4=Ag2SO4+Cu
C、实验①中溶液质量逐渐增大
D、实验①中溶液颜色由蓝色变为黄色
11.(2023·绍兴)《天工开物》中记载烧制青砖时“火候足,止薪之候,泥固塞其孔,然后使水转釉”。该过程的主要化学反应为:Fe2O3+CO2FeO+CO2。下列说法正确的是( )
A、该反应属于置换反应
B、CO的相对分子质量为28克
C、FeO中铁元素的化合价为+2价
D、塞住砖窑的通气孔,窑内柴火会较快熄灭,是由于缺少可燃物
12.兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象,下列说法不正确的是( )
A、由实验可判断出铁、铜、锌的活动性顺序
B、两支试管混合后,固体总质量一定增加
C、滤渣中一定有Cu,一定没有Fe和Zn
D、滤液中的溶质一定有FeCl2、ZnCl2和CuCl2
13.芯片是计算机、智能家电的核心部件,它是以高纯度的单质硅(Si)为材料制成的。硅及其氧化物能发生如下反应:
①Si+O2 SiO2
②SiO2+Na2CO3Na2SiO3+CO2↑
③SiO2+2CSi+2CO↑
④Si+2NaOH+H2O Na2SiO3+2H2↑
下列说法错误的是( )
A、反应①中Si得到氧发生了氧化反应
B、反应③属于置换反应
C、上述反应中共生成三种还原性气体
D、Si和SiO2在一定条件下可以相互转化
14.将铁粉(on段)和稀硫酸(n点后)先后加入到一定量的硫酸铜溶液中,搅拌使之充分反应。过程中加入物质的质量与烧杯中剩余固体的质量关系如图所示。下列说法正确的是( )
A、a、b点对应的剩余固体只有一种
B、m<6.4
C、实验过程中共产生FeSO4的质量为15.2g
D、n点对应的横坐标数值为11.2
15.向m克AgNO3、Cu(NO3)2和Fe(NO3)2的混合溶液中加入一定量的锌粉,充分反应后,过滤所得滤液的质量仍为m克。下列分析合理的是( )
①该过程至少发生了三个化学反应
②滤渣中一定有Ag、Cu,可能有Fe
③向滤渣中加稀盐酸,一定有气泡产生
④滤液中一定含有Zn(NO3)2,可能含有Cu(NO3)2和Fe(NO3)2,一定没有AgNO3
A、①② B、①③ C、②④ D、③④
二、填空题
16.中国古代科学和科学工艺历史悠久、成就卓越,是劳动人民生产、生活智慧的结晶。
(1)东汉《神农本草经》曾记载石胆“能化铁为铜”。叙述的是用硫酸铜和铁反应制取铜,这是湿法炼铜的最早记载。用硫酸铜和铁反应制取铜的变化属于______变化。
(2)西晋《蜀都赋》中有“火井沈荧于幽谷,高焰飞煽于天垂。”描写的是天然气(主要成分是甲烷)燃烧时的现象,甲烷能燃烧的性质属于_______性质。
17.金属材料在生活中用途很广,铜丝通常用作导线是利用了其良好的 性;厨房中用的铝锅通常比较耐腐蚀,是因为铝的表面生成了一层致密的 (填化学式)保护膜 。
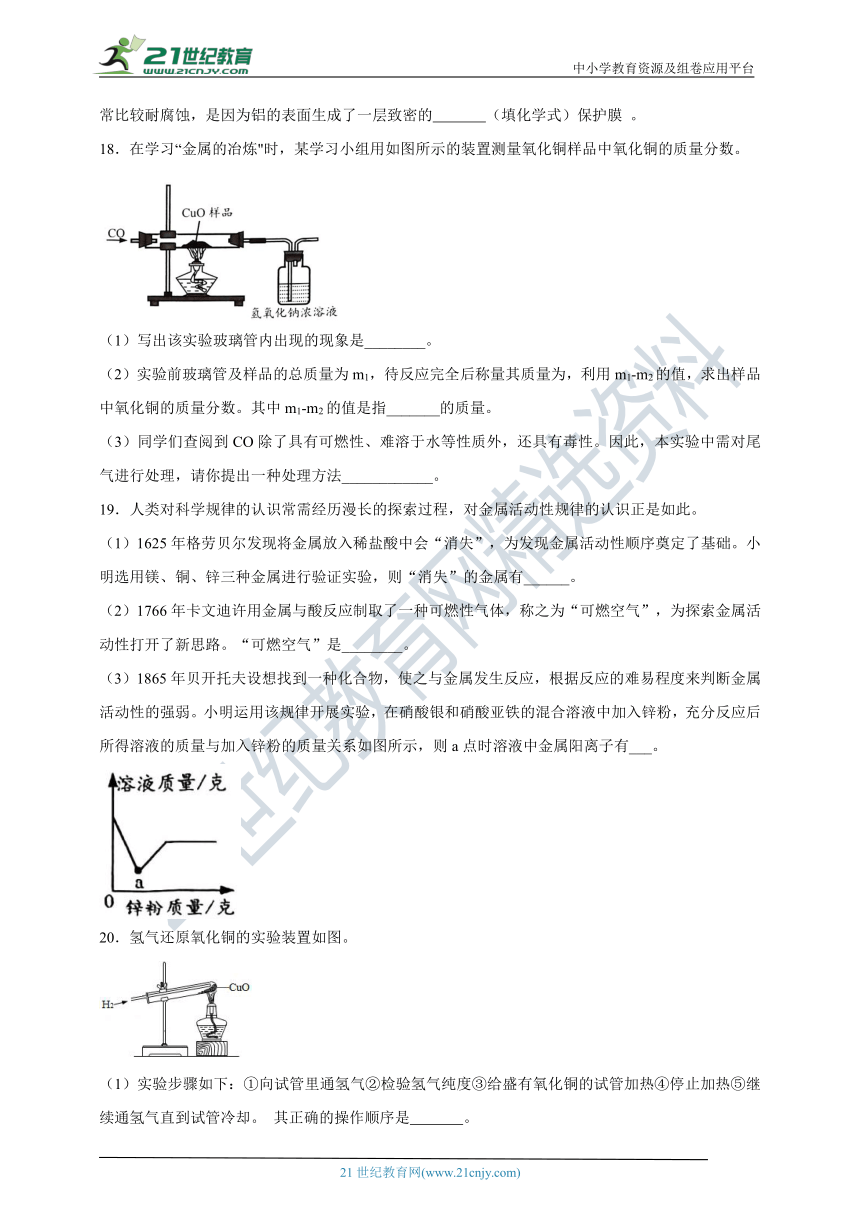
18.在学习“金属的冶炼"时,某学习小组用如图所示的装置测量氧化铜样品中氧化铜的质量分数。
(1)写出该实验玻璃管内出现的现象是________。
(2)实验前玻璃管及样品的总质量为m1,待反应完全后称量其质量为,利用m1-m2的值,求出样品中氧化铜的质量分数。其中m1-m2的值是指_______的质量。
(3)同学们查阅到CO除了具有可燃性、难溶于水等性质外,还具有毒性。因此,本实验中需对尾气进行处理,请你提出一种处理方法____________。
19.人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识正是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,为发现金属活动性顺序奠定了基础。小明选用镁、铜、锌三种金属进行验证实验,则“消失”的金属有______。
(2)1766年卡文迪许用金属与酸反应制取了一种可燃性气体,称之为“可燃空气”,为探索金属活动性打开了新思路。“可燃空气”是________。
(3)1865年贝开托夫设想找到一种化合物,使之与金属发生反应,根据反应的难易程度来判断金属活动性的强弱。小明运用该规律开展实验,在硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示,则a点时溶液中金属阳离子有___。
20.氢气还原氧化铜的实验装置如图。
(1)实验步骤如下:①向试管里通氢气②检验氢气纯度③给盛有氧化铜的试管加热④停止加热⑤继续通氢气直到试管冷却。 其正确的操作顺序是 。
(2)试管内的实验现象是 。
21.如图甲是市售“洗衣凝珠”,它是由一层薄膜包裹洗衣液制成的新型洗涤产品。该薄膜的主要化学成分是聚乙烯醇塑料(也称PVA) ,PVA的化学式是(C2H4O)n。请回答:
(1)从物质的分类来看,PVA属于_______(选填“有机物”或“无机物”)
(2)根据图乙使用说明,推测PVA的物理性质之一是________。
(3)醋酸(CH3COOH)是合成PVA的原料之一。醋酸分子中碳原子和氢原子的个数比为_______。
22.如图是探究铁锈蚀条件的装置。调节U形管L端与R端的液面高度一致,塞紧木塞,一周后观察a中铁钉生锈,b中铁钉没变化。
(1)还可以观察到L端与R端液面高度________( 填"L高R低”、 "L低R高”或“一样高”) 。
(2)比较a、b铁钉,说明铁锈蚀需要_________。
23.(2023·舟山)如图是“铁粉和硫黄反应”的改进实验,将铁粉和硫黄混合物置于两块石英玻璃片之间,并固定。在酒精灯上加热,产生红色火星,固体由棕灰色变为黑色。
(1)铁粉和硫黄在两块玻璃片之间,反应时几乎接触不到氧气,减少了______(填化学式)气体的生成,更加环保。
(2)向反应后的黑色固体滴入稀硫酸,有臭鸡蛋气味的硫化氢(H2S)气体产生,说明铁粉和硫黄发生反应。H2S中硫元素的化合价为_______。
(3)反应后的黑色固体加入CuSO4溶液中,生成红色物质,说明黑色固体中有____剩余。
三、探究题
24.沼气是指在缺氧条件下有机物经微生物发酵所产生的气体,主成分为甲烷(不溶于水)、二氧化碳气体(其他气体忽略)。小宁想探究不同温度对沼气产量的影响。
步骤一:从池塘中挖取含有微生物的污泥,并去除杂质。
步骤二:将适量的有机厨余、水、污泥均匀混合后,分成三等份,分别置于三个发酵瓶中,再将发酵瓶分别放入三个不同温度的恒温水浴锅中。每隔24小时测量集气瓶中的排开水量并记录。
步骤三:每次检测后,将集气瓶重新装满水再放回水槽中,继续收集气体,实验结果如表所示。
水浴温度/℃ 排开水量/g
第一天 第二天 第三天 第四天 第五天
24 30 110 160 182 172
28 55 175 278 212 181
34 107 501 431 170 153
(1)从收集沼气来看,下列装置合理的是________。
(2)分析表中数据,排开水量越大,则当天该条件下发酵的速率越_______,该反应过程中作为催化剂的是_______(选填“有机厨余”或“污泥”)。
(3)继续收集沼气直至每个温度下排开水量为零。不考虑沼气溢出,每个温度下的总排开水量相等是因为____________。
25.半水煤气是工业合成氨的原料气,其主要成分是 H2、CO、CO2、N2和水蒸气。科学兴趣小组为检验半水煤气的某些成分,设计的实验方案如图所示。
查阅资料可知碱石灰是 CaO和NaOH的混合物。回答下列问题:
(1)A瓶中产生白色沉淀,其反应的化学方程式是_______。
(2)B装置的作用是_______。
(3)若C中黑色粉末变红,D中集气瓶内壁起雾并出现液滴,则证明半水煤气中含有______。
(4)根据实验装置可知,只需观察到______的现象,即可证明半水煤气中有CO存在。
四、简答题
26.LPG是指经高压或低温液化的石油气,简称“液化石油气”,主要成分是丙烷、丁烷等物质,其燃烧产物主要是二氧化碳和水。
(1)LPG有轻微麻醉性,过量吸入会使人缺氧窒息甚至死亡。家庭瓶装LPG常添加适量的乙硫醇(乙硫醇化学式为C2H5S,具有强烈、持久且具刺激性的蒜臭味),从安全角度分析添加乙硫醇的目的______________。乙硫醇中碳元素与氢元素的质量比是___________。
(2)温州市各县区较多小区已完成燃气置换工作,用天然气替换液化石油气。完全燃烧1千克液化石油气和1千克天然气释放的热量和产生CO2的质量如图所示。请结合图表分析燃气置换工作的意义______________。
27.在空间站里,氧气和二氧化碳是怎么循环的呢?空间站中的水、气整合循环系统利用“萨巴蒂尔反应”,将CO2转化为H2O,H2O进入氧气生成系统实现O2 的再生,流程如图所示。
请根据图示回答下列问题:
(1)水、气整合循环系统中,发生的反应为CO2+H2H2O+X。已知物质X由两种元素组成,且其中氢元素质量分数为25%,则X的化学式为______。进入氧气生成系统发生电解的水的质量_____(填“大于”、“等于”或“小于”)水、气整合循环系统中生成水的质量。
(2)Na2O2可作空间站的氧气再生剂,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。已知每位成年人一天所需氧气约为0.8kg,若三位宇航员呼吸需要的氧气全部由Na2O2提供,为了满足183天的太空生活,三位宇航员至少需要携带多少千克的Na2O2?
参考答案
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 D C B C C C B B A A
题号 11 12 13 14 15
答案 C D C D C
二、填空题
16.(1)化学 (2)化学
17.导电 Al2O3
18.(1)黑色粉末变成红色 (2)氧元素 (3)将尾气点燃(或用气囊收集)
19.(1)镁、锌 (2)氢气 (3)Zn2+、Fe2+
20.(1)②①③④⑤
(2)黑色粉末逐渐变红色,试管口有水珠生成
21.(1) 有机物 (2)可溶于水 (3) 1:2
22.(1)L高R低 (2)水
23.(1)SO2 (2)-2 (3)铁
三、探究题
24.(1)A
(2)快;污泥
(3)三个发酵瓶中的有机厨余质量相等,根据质量守恒定律可知,它们产生的甲烷总量是一样的
25.(1)CO2+Ca(OH)2=CaCO3↓+H2O
(2)吸收二氧化碳和水蒸气
(3)H2
(4)E中的澄清石灰水变浑浊
四、简答题
26.(1)液化石油气泄漏时更易被察觉 24:5
(2)燃烧相同质量的液化石油气和天然气,天然气放出的热量较多,且产生的二氧化碳较小,有利于碳中和
27. (1)CH4 大于
(2)解:设每生成0.8kg氧气所需的Na2O2的质量为x。
2Na2O2+2CO2=2Na2CO3+O2
156 32
x 0.8kg
=
x=3.9kg
三位宇航员在太空生活183天需要携带O2的质量为:
3.9kg×3×183=2141.1kg
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
2023针对性训练 第二章B
一、选择题
1. (2023 江西)大国工匠秦世俊展现数控技术所使用的0.01mm铝箔,是由铝块加工而成,这体现了铝具有( )
A、密度小 B、导电性 C、导热性 D、延展性
2. 某工厂排放的废水中含有较多的硫酸铜,从回收利用铜的角度考虑,切实可行的方案是在废水中加入( )
A、盐酸 B、硫酸 C、铁粉 D、碳酸钙
3. (2023 陕西)用下列各组物质进行实验,能验证Mg、Ag、Cu三种金属活动性强弱的是( )
A、Mg、Ag、Cu、稀硫酸 B、Mg、Ag、CuSO4溶液
C、Ag、Cu、MgCl2溶液 D、Ag、CuCl2溶液、MgSO4溶液
4. 锰(Mn)和镍(Ni)是两种不常见的金属,为了比较锰、镍和锌的金属活动性,小明同学在老师的指导下进行了实验,结果如下表:
则它们的金属活动性顺序为( )
A、Zn >Ni>Mn B、Zn>Mn>Ni C、Mn>Zn>Ni D、Ni>Mn>Zn
5. 将镁、锌、铜、银四种金属片加入盛有稀硫酸的试管中,观测结果如图,则其中发生的化学反应类型为( )
A、化合反应 B、分解反应 C、置换反应 D、复分解反应
6. 房屋装修过程中易产生有毒气体甲醛(化学式CH2O),如图表示甲醛在纳米膜催化下与氧气()反应转化为水和二氧化碳的过程。其中“”表示的分子是( )
A、CH2O B、O2 C、CO2 D、H2O
7. 秀秀通过实验探究某种金属R的活动性强弱,并根据实验现象编制检索表如图,根据检索表可知,金属R的活动性强弱排序正确的是( )
A、Fe>Ag>R B、Fe>R>Ag
C、R>Fe>Ag D、Ag>R>Fe
8. (2023 广州)钴(Co)的金属活动性与铁相似,钴的化合物相关性质如表。下列预测合理的是( )
物质 CoO Co(OH)2 CoCl2 CoCO3
在水中的溶解性 难溶,灰绿色固体 难溶,粉红色固体 易溶,溶液呈粉红色 难溶,粉红色固体
A、Co能从MgCl2溶液中置换出Mg
B、CoO能与盐酸反应得到粉红色溶液
C、CoCO3能与盐酸反应生成H2
D、Co(OH)2可由Co与NaOH溶液反应制得
9. 我国自主研发的深海载人潜水器球壳,是世界上最大的载人舱球壳,已在马里亚纳海沟海域完成万米海试任务。在开发深海潜水舱时,科研团队要考虑深海压强大、海水腐蚀强、上浮困难等问题,如图是中科院研究团队研发的钛合金深海潜水器球舱,解决了以上问题。以下说法不正确的是( )
A、钛合金属于化合物
B、钛合金具有较好的抗压和抗腐蚀性能
C、钛合金的密度大小会影响上浮的难易程度
D、合金往往比纯金属具有更好的性能
10.(2023 郴州)为验证铁、铜、银三种金属的活动性顺序,小东设计了如下所示的两组实验。下列说法正确的是( )
A、通过实验①、②能够验证三种金属的活动性顺序
B、实验②中发生的反应是:2Ag+CuSO4=Ag2SO4+Cu
C、实验①中溶液质量逐渐增大
D、实验①中溶液颜色由蓝色变为黄色
11.(2023·绍兴)《天工开物》中记载烧制青砖时“火候足,止薪之候,泥固塞其孔,然后使水转釉”。该过程的主要化学反应为:Fe2O3+CO2FeO+CO2。下列说法正确的是( )
A、该反应属于置换反应
B、CO的相对分子质量为28克
C、FeO中铁元素的化合价为+2价
D、塞住砖窑的通气孔,窑内柴火会较快熄灭,是由于缺少可燃物
12.兴趣小组按如图流程进行实验(每步均充分反应),反应结束后,将烧杯内物质进行过滤,向滤渣中加入少量稀盐酸,无明显现象,下列说法不正确的是( )
A、由实验可判断出铁、铜、锌的活动性顺序
B、两支试管混合后,固体总质量一定增加
C、滤渣中一定有Cu,一定没有Fe和Zn
D、滤液中的溶质一定有FeCl2、ZnCl2和CuCl2
13.芯片是计算机、智能家电的核心部件,它是以高纯度的单质硅(Si)为材料制成的。硅及其氧化物能发生如下反应:
①Si+O2 SiO2
②SiO2+Na2CO3Na2SiO3+CO2↑
③SiO2+2CSi+2CO↑
④Si+2NaOH+H2O Na2SiO3+2H2↑
下列说法错误的是( )
A、反应①中Si得到氧发生了氧化反应
B、反应③属于置换反应
C、上述反应中共生成三种还原性气体
D、Si和SiO2在一定条件下可以相互转化
14.将铁粉(on段)和稀硫酸(n点后)先后加入到一定量的硫酸铜溶液中,搅拌使之充分反应。过程中加入物质的质量与烧杯中剩余固体的质量关系如图所示。下列说法正确的是( )
A、a、b点对应的剩余固体只有一种
B、m<6.4
C、实验过程中共产生FeSO4的质量为15.2g
D、n点对应的横坐标数值为11.2
15.向m克AgNO3、Cu(NO3)2和Fe(NO3)2的混合溶液中加入一定量的锌粉,充分反应后,过滤所得滤液的质量仍为m克。下列分析合理的是( )
①该过程至少发生了三个化学反应
②滤渣中一定有Ag、Cu,可能有Fe
③向滤渣中加稀盐酸,一定有气泡产生
④滤液中一定含有Zn(NO3)2,可能含有Cu(NO3)2和Fe(NO3)2,一定没有AgNO3
A、①② B、①③ C、②④ D、③④
二、填空题
16.中国古代科学和科学工艺历史悠久、成就卓越,是劳动人民生产、生活智慧的结晶。
(1)东汉《神农本草经》曾记载石胆“能化铁为铜”。叙述的是用硫酸铜和铁反应制取铜,这是湿法炼铜的最早记载。用硫酸铜和铁反应制取铜的变化属于______变化。
(2)西晋《蜀都赋》中有“火井沈荧于幽谷,高焰飞煽于天垂。”描写的是天然气(主要成分是甲烷)燃烧时的现象,甲烷能燃烧的性质属于_______性质。
17.金属材料在生活中用途很广,铜丝通常用作导线是利用了其良好的 性;厨房中用的铝锅通常比较耐腐蚀,是因为铝的表面生成了一层致密的 (填化学式)保护膜 。
18.在学习“金属的冶炼"时,某学习小组用如图所示的装置测量氧化铜样品中氧化铜的质量分数。
(1)写出该实验玻璃管内出现的现象是________。
(2)实验前玻璃管及样品的总质量为m1,待反应完全后称量其质量为,利用m1-m2的值,求出样品中氧化铜的质量分数。其中m1-m2的值是指_______的质量。
(3)同学们查阅到CO除了具有可燃性、难溶于水等性质外,还具有毒性。因此,本实验中需对尾气进行处理,请你提出一种处理方法____________。
19.人类对科学规律的认识常需经历漫长的探索过程,对金属活动性规律的认识正是如此。
(1)1625年格劳贝尔发现将金属放入稀盐酸中会“消失”,为发现金属活动性顺序奠定了基础。小明选用镁、铜、锌三种金属进行验证实验,则“消失”的金属有______。
(2)1766年卡文迪许用金属与酸反应制取了一种可燃性气体,称之为“可燃空气”,为探索金属活动性打开了新思路。“可燃空气”是________。
(3)1865年贝开托夫设想找到一种化合物,使之与金属发生反应,根据反应的难易程度来判断金属活动性的强弱。小明运用该规律开展实验,在硝酸银和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图所示,则a点时溶液中金属阳离子有___。
20.氢气还原氧化铜的实验装置如图。
(1)实验步骤如下:①向试管里通氢气②检验氢气纯度③给盛有氧化铜的试管加热④停止加热⑤继续通氢气直到试管冷却。 其正确的操作顺序是 。
(2)试管内的实验现象是 。
21.如图甲是市售“洗衣凝珠”,它是由一层薄膜包裹洗衣液制成的新型洗涤产品。该薄膜的主要化学成分是聚乙烯醇塑料(也称PVA) ,PVA的化学式是(C2H4O)n。请回答:
(1)从物质的分类来看,PVA属于_______(选填“有机物”或“无机物”)
(2)根据图乙使用说明,推测PVA的物理性质之一是________。
(3)醋酸(CH3COOH)是合成PVA的原料之一。醋酸分子中碳原子和氢原子的个数比为_______。
22.如图是探究铁锈蚀条件的装置。调节U形管L端与R端的液面高度一致,塞紧木塞,一周后观察a中铁钉生锈,b中铁钉没变化。
(1)还可以观察到L端与R端液面高度________( 填"L高R低”、 "L低R高”或“一样高”) 。
(2)比较a、b铁钉,说明铁锈蚀需要_________。
23.(2023·舟山)如图是“铁粉和硫黄反应”的改进实验,将铁粉和硫黄混合物置于两块石英玻璃片之间,并固定。在酒精灯上加热,产生红色火星,固体由棕灰色变为黑色。
(1)铁粉和硫黄在两块玻璃片之间,反应时几乎接触不到氧气,减少了______(填化学式)气体的生成,更加环保。
(2)向反应后的黑色固体滴入稀硫酸,有臭鸡蛋气味的硫化氢(H2S)气体产生,说明铁粉和硫黄发生反应。H2S中硫元素的化合价为_______。
(3)反应后的黑色固体加入CuSO4溶液中,生成红色物质,说明黑色固体中有____剩余。
三、探究题
24.沼气是指在缺氧条件下有机物经微生物发酵所产生的气体,主成分为甲烷(不溶于水)、二氧化碳气体(其他气体忽略)。小宁想探究不同温度对沼气产量的影响。
步骤一:从池塘中挖取含有微生物的污泥,并去除杂质。
步骤二:将适量的有机厨余、水、污泥均匀混合后,分成三等份,分别置于三个发酵瓶中,再将发酵瓶分别放入三个不同温度的恒温水浴锅中。每隔24小时测量集气瓶中的排开水量并记录。
步骤三:每次检测后,将集气瓶重新装满水再放回水槽中,继续收集气体,实验结果如表所示。
水浴温度/℃ 排开水量/g
第一天 第二天 第三天 第四天 第五天
24 30 110 160 182 172
28 55 175 278 212 181
34 107 501 431 170 153
(1)从收集沼气来看,下列装置合理的是________。
(2)分析表中数据,排开水量越大,则当天该条件下发酵的速率越_______,该反应过程中作为催化剂的是_______(选填“有机厨余”或“污泥”)。
(3)继续收集沼气直至每个温度下排开水量为零。不考虑沼气溢出,每个温度下的总排开水量相等是因为____________。
25.半水煤气是工业合成氨的原料气,其主要成分是 H2、CO、CO2、N2和水蒸气。科学兴趣小组为检验半水煤气的某些成分,设计的实验方案如图所示。
查阅资料可知碱石灰是 CaO和NaOH的混合物。回答下列问题:
(1)A瓶中产生白色沉淀,其反应的化学方程式是_______。
(2)B装置的作用是_______。
(3)若C中黑色粉末变红,D中集气瓶内壁起雾并出现液滴,则证明半水煤气中含有______。
(4)根据实验装置可知,只需观察到______的现象,即可证明半水煤气中有CO存在。
四、简答题
26.LPG是指经高压或低温液化的石油气,简称“液化石油气”,主要成分是丙烷、丁烷等物质,其燃烧产物主要是二氧化碳和水。
(1)LPG有轻微麻醉性,过量吸入会使人缺氧窒息甚至死亡。家庭瓶装LPG常添加适量的乙硫醇(乙硫醇化学式为C2H5S,具有强烈、持久且具刺激性的蒜臭味),从安全角度分析添加乙硫醇的目的______________。乙硫醇中碳元素与氢元素的质量比是___________。
(2)温州市各县区较多小区已完成燃气置换工作,用天然气替换液化石油气。完全燃烧1千克液化石油气和1千克天然气释放的热量和产生CO2的质量如图所示。请结合图表分析燃气置换工作的意义______________。
27.在空间站里,氧气和二氧化碳是怎么循环的呢?空间站中的水、气整合循环系统利用“萨巴蒂尔反应”,将CO2转化为H2O,H2O进入氧气生成系统实现O2 的再生,流程如图所示。
请根据图示回答下列问题:
(1)水、气整合循环系统中,发生的反应为CO2+H2H2O+X。已知物质X由两种元素组成,且其中氢元素质量分数为25%,则X的化学式为______。进入氧气生成系统发生电解的水的质量_____(填“大于”、“等于”或“小于”)水、气整合循环系统中生成水的质量。
(2)Na2O2可作空间站的氧气再生剂,化学方程式为:2Na2O2+2CO2=2Na2CO3+O2。已知每位成年人一天所需氧气约为0.8kg,若三位宇航员呼吸需要的氧气全部由Na2O2提供,为了满足183天的太空生活,三位宇航员至少需要携带多少千克的Na2O2?
参考答案
一、选择题
题号 1 2 3 4 5 6 7 8 9 10
答案 D C B C C C B B A A
题号 11 12 13 14 15
答案 C D C D C
二、填空题
16.(1)化学 (2)化学
17.导电 Al2O3
18.(1)黑色粉末变成红色 (2)氧元素 (3)将尾气点燃(或用气囊收集)
19.(1)镁、锌 (2)氢气 (3)Zn2+、Fe2+
20.(1)②①③④⑤
(2)黑色粉末逐渐变红色,试管口有水珠生成
21.(1) 有机物 (2)可溶于水 (3) 1:2
22.(1)L高R低 (2)水
23.(1)SO2 (2)-2 (3)铁
三、探究题
24.(1)A
(2)快;污泥
(3)三个发酵瓶中的有机厨余质量相等,根据质量守恒定律可知,它们产生的甲烷总量是一样的
25.(1)CO2+Ca(OH)2=CaCO3↓+H2O
(2)吸收二氧化碳和水蒸气
(3)H2
(4)E中的澄清石灰水变浑浊
四、简答题
26.(1)液化石油气泄漏时更易被察觉 24:5
(2)燃烧相同质量的液化石油气和天然气,天然气放出的热量较多,且产生的二氧化碳较小,有利于碳中和
27. (1)CH4 大于
(2)解:设每生成0.8kg氧气所需的Na2O2的质量为x。
2Na2O2+2CO2=2Na2CO3+O2
156 32
x 0.8kg
=
x=3.9kg
三位宇航员在太空生活183天需要携带O2的质量为:
3.9kg×3×183=2141.1kg
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
