第二单元 第二节 碱及其性质 课件(共29张PPT) 2023--2024学年九年级化学鲁教版(五四学制)全一册
文档属性
| 名称 | 第二单元 第二节 碱及其性质 课件(共29张PPT) 2023--2024学年九年级化学鲁教版(五四学制)全一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 384.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-01 00:00:00 | ||
图片预览




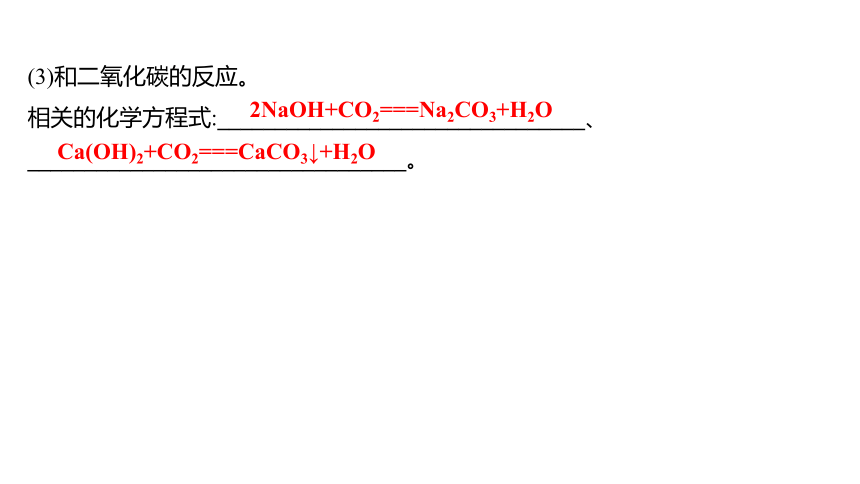




文档简介
(共29张PPT)
第二节 碱及其性质
基础·主干落实
一、常见的碱
1.碱的定义:溶于水后产生共同的阴离子——____________________的化合物。
2.初步认识NaOH和Ca(OH)2
物质 氢氧化钠 氢氧化钙
俗名 烧碱、_________或 ____________ 熟石灰或____________
色、态 ______________ ____________________
在水中的 溶解情况 _______溶于水, 溶解时_________热量 _______溶于水
吸湿性 易吸收___________, 可作____________ —
腐蚀性 ______________ ______________
氢氧根离子(OH-)
火碱
苛性钠
消石灰
白色固体
白色粉末状物质
易
放出
微
水蒸气
干燥剂
强腐蚀性
有腐蚀性
3.烧碱的使用注意事项
(1)暴露在空气中易吸收水蒸气而逐渐溶解,因此应_____________。
(2)若不慎沾到皮肤上,应立即_________________,然后再涂上_________溶液。
4.氢氧化钙的制取:化学方程式为___________________________、 _____________________(反应放出大量的热)。
密封保存
用大量水冲洗
硼酸
CaCO3 CaO+CO2↑
CaO+H2O===Ca(OH)2
二、碱的化学性质
1.NaOH、Ca(OH)2的化学性质
(1)和石蕊试液、酚酞试液的作用。
滴入石蕊试液后,溶液_________,滴入酚酞试液后,溶液_________。
(2)和CuCl2溶液、Na2CO3溶液的作用。
①氢氧化钠、氢氧化钙分别与氯化铜溶液反应的化学方程式为 ___________________________________、 ___________________________________。
②氢氧化钙溶液与碳酸钠溶液反应的化学方程式为
_______________________________________。
变蓝
变红
2NaOH+CuCl2===Cu(OH)2↓+2NaCl
Ca(OH)2+CuCl2===Cu(OH)2↓+CaCl2
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
(3)和二氧化碳的反应。
相关的化学方程式:________________________________、
_________________________________。
2NaOH+CO2===Na2CO3+H2O
Ca(OH)2+CO2===CaCO3↓+H2O
导·思
1.为什么检验二氧化碳气体要用澄清石灰水,而吸收二氧化碳一般用氢氧化钠溶液
提示:氢氧化钠溶液和澄清石灰水都可以和二氧化碳反应,由于二氧化碳和澄清石灰水反应时,溶液有明显的变浑浊现象,因此,检验二氧化碳气体时,常用澄清石灰水。而氢氧化钙微溶于水,氢氧化钠易溶于水,通常氢氧化钠溶液的浓度大,相同质量的石灰水和氢氧化钠溶液中,石灰水中含有的氢氧化钙较少,吸收的二氧化碳就少,而氢氧化钠溶液能吸收较多的二氧化碳。
2.CO2与NaOH溶液反应生成物的验证。如何设计实验证明CO2与NaOH溶液反应
提示:CO2与NaOH反应生成Na2CO3和水,只需验证Na2CO3的存在即可。可通过加盐酸、硫酸或Ca(OH)2溶液等试剂检验。具体方案为取少量溶液加入稀盐酸或稀硫酸,有气泡产生,或取少量溶液加入Ca(OH)2溶液,有白色沉淀产生,说明生成了Na2CO3,即证明CO2与NaOH溶液发生了反应。答案合理即可。
2.碱的通性
(1)碱具有相似化学性质即碱的通性的原因是碱溶液中都含有_______________。
(2)碱的通性。
①能使紫色石蕊试液_________,使无色酚酞试液_________。
②能与某些非金属氧化物反应,生成___________。
③能与某些盐反应生成_____________和_____________。
3. 碱的特性
不同的碱溶于水时解离出的阳离子不同,其性质也存在差异。例如:氢氧化钙溶
液能与碳酸钠溶液反应生成白色的碳酸钙沉淀,而氢氧化钠不能。
氢氧根离子
变蓝
变红
盐和水
另一种盐
另一种碱
易错辨析 判断下列说法是否正确。
(1)熟石灰和生石灰均属于碱。 ( )
(2)固体烧碱在空气中易吸收水蒸气而溶解。 ( )
(3)氢氧化钠溶液和氢氧化钙溶液均能使紫色石蕊试液和无色酚酞试液变红色。
( )
(4)氢氧化钠溶液与氯化铜溶液发生反应生成蓝色沉淀。 ( )
(5)浓硫酸、氢氧化钠、生石灰都可以作干燥剂,都是利用了其物理性质。( )
×
√
×
√
×
考点碱的化学性质
【典例1】(2023·淄博周村区期中)下列四种物质中,其中有一种能和其他三种物
质发生反应,该物质是 ( )
A.CO2
B.MgSO4溶液
C.CuCl2溶液
D.氢氧化钠溶液
重点·案例探析
D
变式训练 (2022·乐山中考)向某无色溶液中加入NaOH后能产生沉淀,则该溶液可
能是 ( )
A.MgCl2溶液
B.Ba(NO3)2溶液
C.K2CO3溶液
D.CuSO4溶液
A
【典例2】(2022·淄博周村期中)经过“碱的化学性质”的学习,小明同学用如图所示
的示意图归纳总结了NaOH四条化学性质。
(1)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞
试液变为红色,使无色酚酞试液变为红色的微粒是_________(填微粒符号)。
OH-
(2)为了验证反应③能够发生,可以选用的试剂是________。
A.CuCl2 B.NaCl
C.CuSO4 D.Na2CO3
(3)NaOH溶液露置于空气中易变质,所以必须密封保存。请你写出NaOH溶液变
质的化学方程式:________________________________。
AC
2NaOH+CO2===Na2CO3+H2O
借题发挥
(4)第(3)问中的化学反应是体现了图中NaOH的性质_______(填“①”“②”“③”
或“④”)。
(5)根据第(2)问提供的试剂写出反应③时可观察到的现象是_________________,
反应方程式为_____________________________________________________
___________________。
④
产生蓝色沉淀
CuCl2+2NaOH===Cu(OH)2↓+2NaCl、CuSO4+2NaOH===
Cu(OH)2↓+Na2SO4
【A层 基础练】
1.(2022·梧州中考)下列物质属于碱的是( )
A.H2SO4 B.SO2
C.KNO3 D.NaOH
2.(2022·柳州中考)化学课中老师给同学们变“魔术”:往浸过酚酞溶液的白色纸花
上喷了某种无色溶液后,白花瞬间变成了红花,老师喷的溶液可能是 ( )
A.水 B.稀盐酸
C.氨水 D.氯化钠溶液
素养·分层评价
D
C
3.下列物质的名称、俗名与化学式一致的是 ( )
选项 名称 俗名 化学式
A 氢氧化钠 烧碱 NaOH
B 氧化钙 生石灰 Ca(OH)2
C 氢氧化钙 熟石灰 CaO
D 乙醇 酒精 CH3COOH
A
4.(2022·淄博高青期中)下列关于氢氧化钙的描述不正确的是( )
A.是熟石灰的主要成分
B.对皮肤、衣服等有腐蚀作用
C.水溶液俗称石灰水
D.白色粉末状固体,易潮解
5.氢氧化钠、氢氧化钙的溶液都具有相似化学性质,其原因是 ( )
A.都能解离出金属离子
B.都含有氢元素和氧元素
C.都能使无色酚酞试液变成红色
D.溶液中都含有OH-
D
D
6.下列溶液在空气中敞口久置,因发生化学变化导致溶液质量减小的是 ( )
A.浓盐酸 B.浓硫酸
C.石灰水 D.烧碱溶液
7.(2023·淄博沂源期中)下列关于氢氧化钙的认识,不正确的是 ( )
A.组成:氢氧化钙溶液中Ca2+和OH-的数目相同
B.性质:能与CO2等非金属氧化物反应
C.用途:可用于土壤改良
D.制备:可由生石灰和水反应制得
C
A
8.(2022·淄博沂源期中)欲证明“CO2与NaOH发生了化学反应”,某化学兴趣小组进
行以下探究实验(实验装置中夹持仪器已略去),下列说法不正确的是 ( )
A.实验前,U形管两端的液面必须保持相平
B.实验后,恢复到室温时U形管中的液面左高右低
C.观察到B选项中的现象可得出结论:CO2与NaOH发生了化学反应
D.若用KOH溶液代替NaOH溶液,可观察到相同的实验现象
C
9.学校运动场跑道线常用材料是称作石灰的物质,其化学名为_____________。
它的水溶液俗称___________,可由生石灰与水反应制得,化学方程式为
_________________________。实验室也常用它来检验CO2的存在,化学方程式为
_________________________________。盛该溶液的试剂瓶时间长了,试剂瓶内壁
会生成一层白膜,这“白膜”的化学式是____________________,因“白膜”不溶于水,
所以不能用水冲洗,应先用___________清洗,再用水清洗。
氢氧化钙
石灰水
CaO+H2O===Ca(OH)2
Ca(OH)2+CO2===CaCO3↓+H2O
CaCO3(或碳酸钙)
稀盐酸
【B层 能力练】
10.(2022·淄博高青期中)现有两瓶失去标签的无色溶液,分别是稀盐酸和石灰水,
下列试剂不能鉴别开来的是 ( )
A.氯化钠溶液
B.氯化铜溶液
C.紫色石蕊试液
D.无色酚酞试液
A
11.(2022·淄博高青期中)将碳酸钠溶液分别滴加到澄清石灰水和氢氧化钠溶液中,
下列说法正确的是 ( )
A.两支试管都没有明显现象
B.右边试管中发生的反应方程式是2NaOH+Na2CO3===2NaOH+Na2CO3
C.左边试管中发生的反应方程式是Ca(OH)2+Na2CO3===CaCO3+2NaOH
D.该实验证明,不同的碱化学性质具有差异性
D
12.实验探究是获取证据的重要途径。“扬帆”学习小组阅读资料获知氢氧化钡[Ba(OH)2]与氢氧
化钙的化学性质相似,为了验证氢氧化钡的某些化学性质,他们设计如图所示实验。其中不能
达到实验目的的是 ( )
A.实验①验证氢氧化钡溶液显碱性
B.实验②验证氢氧化钡能与酸反应
C.实验③验证氢氧化钡能与某些盐反应
D.实验④验证氢氧化钡能与某些非金属氧化物反应
B
13.(2023·淄博张店区期中)忘记盖瓶塞的氢氧化钠溶液可能变质。如表中分析与
设计错误的是 ( )
选项 问题 分析与设计
A 为何变质 2NaOH+CO2===Na2CO3+H2O
B 是否变质 取样,滴加氯化钙溶液,观察是否生成沉淀
C 是否全部变质 取样,加入足量稀盐酸,观察是否产生气泡
D 如何除去杂质 取样,加入适量氢氧化钙溶液,过滤
C
14.完成下列问题:
(1)图1中,观察到的现象是_______________。
(2)图2中,观察到的现象是_________________。
(3)图3中,将针筒中的氢氧化钠溶液注入充满二氧化碳气体的锥形瓶中,观察到的
现象是_____________。
有同学认为:图3中的现象,不足以证明二氧化碳和氢氧化钠溶液发生了化学反应,
原因是___________________________________。
液体变红色
生成蓝色沉淀
气球膨胀
二氧化碳溶于水也会产生类似现象
15.生石灰和水反应得到熟石灰。现有露天堆置的熟石灰,某兴趣小组的同学要对
它进行成分分析,进而确定其变质情况。取样品少许,进行如下实验,请你帮助完
成有关问题:
【提出问题】熟石灰是否变质
【猜想与假设】猜想①:没有变质;
猜想②:全部变质;猜想③:_____________。
部分变质
【实验探究】
实验方案 实验现象 实验结论
方案1:取少量粉末于试管中,加少许水振荡 有白色不溶物出现 猜想②正确
方案2: Ⅰ.取方案1中的上层清液于试管中,滴加酚酞 溶液变红色 ______________
Ⅱ.向方案1中的不溶物中滴加稀盐酸 产生气泡 猜想③ 正确
【交流思考】(1)方案1的实验结论是否正确 你的回答是_________(填“正确”或
“错误”),理由是______________________________________________。
(2)写出方案2中产生气体反应的化学方程式________________________________。
【反思拓展】若较长时间场外堆置存放熟石灰,为防止熟石灰变质应注意的问题
是_______________________________。
错误
氢氧化钙微溶于水,白色不溶物可能是氢氧化钙
CaCO3+2HCl===CaCl2+H2O+CO2↑
尽量减少熟石灰与空气的接触
本课结束
第二节 碱及其性质
基础·主干落实
一、常见的碱
1.碱的定义:溶于水后产生共同的阴离子——____________________的化合物。
2.初步认识NaOH和Ca(OH)2
物质 氢氧化钠 氢氧化钙
俗名 烧碱、_________或 ____________ 熟石灰或____________
色、态 ______________ ____________________
在水中的 溶解情况 _______溶于水, 溶解时_________热量 _______溶于水
吸湿性 易吸收___________, 可作____________ —
腐蚀性 ______________ ______________
氢氧根离子(OH-)
火碱
苛性钠
消石灰
白色固体
白色粉末状物质
易
放出
微
水蒸气
干燥剂
强腐蚀性
有腐蚀性
3.烧碱的使用注意事项
(1)暴露在空气中易吸收水蒸气而逐渐溶解,因此应_____________。
(2)若不慎沾到皮肤上,应立即_________________,然后再涂上_________溶液。
4.氢氧化钙的制取:化学方程式为___________________________、 _____________________(反应放出大量的热)。
密封保存
用大量水冲洗
硼酸
CaCO3 CaO+CO2↑
CaO+H2O===Ca(OH)2
二、碱的化学性质
1.NaOH、Ca(OH)2的化学性质
(1)和石蕊试液、酚酞试液的作用。
滴入石蕊试液后,溶液_________,滴入酚酞试液后,溶液_________。
(2)和CuCl2溶液、Na2CO3溶液的作用。
①氢氧化钠、氢氧化钙分别与氯化铜溶液反应的化学方程式为 ___________________________________、 ___________________________________。
②氢氧化钙溶液与碳酸钠溶液反应的化学方程式为
_______________________________________。
变蓝
变红
2NaOH+CuCl2===Cu(OH)2↓+2NaCl
Ca(OH)2+CuCl2===Cu(OH)2↓+CaCl2
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
(3)和二氧化碳的反应。
相关的化学方程式:________________________________、
_________________________________。
2NaOH+CO2===Na2CO3+H2O
Ca(OH)2+CO2===CaCO3↓+H2O
导·思
1.为什么检验二氧化碳气体要用澄清石灰水,而吸收二氧化碳一般用氢氧化钠溶液
提示:氢氧化钠溶液和澄清石灰水都可以和二氧化碳反应,由于二氧化碳和澄清石灰水反应时,溶液有明显的变浑浊现象,因此,检验二氧化碳气体时,常用澄清石灰水。而氢氧化钙微溶于水,氢氧化钠易溶于水,通常氢氧化钠溶液的浓度大,相同质量的石灰水和氢氧化钠溶液中,石灰水中含有的氢氧化钙较少,吸收的二氧化碳就少,而氢氧化钠溶液能吸收较多的二氧化碳。
2.CO2与NaOH溶液反应生成物的验证。如何设计实验证明CO2与NaOH溶液反应
提示:CO2与NaOH反应生成Na2CO3和水,只需验证Na2CO3的存在即可。可通过加盐酸、硫酸或Ca(OH)2溶液等试剂检验。具体方案为取少量溶液加入稀盐酸或稀硫酸,有气泡产生,或取少量溶液加入Ca(OH)2溶液,有白色沉淀产生,说明生成了Na2CO3,即证明CO2与NaOH溶液发生了反应。答案合理即可。
2.碱的通性
(1)碱具有相似化学性质即碱的通性的原因是碱溶液中都含有_______________。
(2)碱的通性。
①能使紫色石蕊试液_________,使无色酚酞试液_________。
②能与某些非金属氧化物反应,生成___________。
③能与某些盐反应生成_____________和_____________。
3. 碱的特性
不同的碱溶于水时解离出的阳离子不同,其性质也存在差异。例如:氢氧化钙溶
液能与碳酸钠溶液反应生成白色的碳酸钙沉淀,而氢氧化钠不能。
氢氧根离子
变蓝
变红
盐和水
另一种盐
另一种碱
易错辨析 判断下列说法是否正确。
(1)熟石灰和生石灰均属于碱。 ( )
(2)固体烧碱在空气中易吸收水蒸气而溶解。 ( )
(3)氢氧化钠溶液和氢氧化钙溶液均能使紫色石蕊试液和无色酚酞试液变红色。
( )
(4)氢氧化钠溶液与氯化铜溶液发生反应生成蓝色沉淀。 ( )
(5)浓硫酸、氢氧化钠、生石灰都可以作干燥剂,都是利用了其物理性质。( )
×
√
×
√
×
考点碱的化学性质
【典例1】(2023·淄博周村区期中)下列四种物质中,其中有一种能和其他三种物
质发生反应,该物质是 ( )
A.CO2
B.MgSO4溶液
C.CuCl2溶液
D.氢氧化钠溶液
重点·案例探析
D
变式训练 (2022·乐山中考)向某无色溶液中加入NaOH后能产生沉淀,则该溶液可
能是 ( )
A.MgCl2溶液
B.Ba(NO3)2溶液
C.K2CO3溶液
D.CuSO4溶液
A
【典例2】(2022·淄博周村期中)经过“碱的化学性质”的学习,小明同学用如图所示
的示意图归纳总结了NaOH四条化学性质。
(1)为了验证反应②,小明同学向NaOH溶液中滴入无色酚酞试液,观察到无色酚酞
试液变为红色,使无色酚酞试液变为红色的微粒是_________(填微粒符号)。
OH-
(2)为了验证反应③能够发生,可以选用的试剂是________。
A.CuCl2 B.NaCl
C.CuSO4 D.Na2CO3
(3)NaOH溶液露置于空气中易变质,所以必须密封保存。请你写出NaOH溶液变
质的化学方程式:________________________________。
AC
2NaOH+CO2===Na2CO3+H2O
借题发挥
(4)第(3)问中的化学反应是体现了图中NaOH的性质_______(填“①”“②”“③”
或“④”)。
(5)根据第(2)问提供的试剂写出反应③时可观察到的现象是_________________,
反应方程式为_____________________________________________________
___________________。
④
产生蓝色沉淀
CuCl2+2NaOH===Cu(OH)2↓+2NaCl、CuSO4+2NaOH===
Cu(OH)2↓+Na2SO4
【A层 基础练】
1.(2022·梧州中考)下列物质属于碱的是( )
A.H2SO4 B.SO2
C.KNO3 D.NaOH
2.(2022·柳州中考)化学课中老师给同学们变“魔术”:往浸过酚酞溶液的白色纸花
上喷了某种无色溶液后,白花瞬间变成了红花,老师喷的溶液可能是 ( )
A.水 B.稀盐酸
C.氨水 D.氯化钠溶液
素养·分层评价
D
C
3.下列物质的名称、俗名与化学式一致的是 ( )
选项 名称 俗名 化学式
A 氢氧化钠 烧碱 NaOH
B 氧化钙 生石灰 Ca(OH)2
C 氢氧化钙 熟石灰 CaO
D 乙醇 酒精 CH3COOH
A
4.(2022·淄博高青期中)下列关于氢氧化钙的描述不正确的是( )
A.是熟石灰的主要成分
B.对皮肤、衣服等有腐蚀作用
C.水溶液俗称石灰水
D.白色粉末状固体,易潮解
5.氢氧化钠、氢氧化钙的溶液都具有相似化学性质,其原因是 ( )
A.都能解离出金属离子
B.都含有氢元素和氧元素
C.都能使无色酚酞试液变成红色
D.溶液中都含有OH-
D
D
6.下列溶液在空气中敞口久置,因发生化学变化导致溶液质量减小的是 ( )
A.浓盐酸 B.浓硫酸
C.石灰水 D.烧碱溶液
7.(2023·淄博沂源期中)下列关于氢氧化钙的认识,不正确的是 ( )
A.组成:氢氧化钙溶液中Ca2+和OH-的数目相同
B.性质:能与CO2等非金属氧化物反应
C.用途:可用于土壤改良
D.制备:可由生石灰和水反应制得
C
A
8.(2022·淄博沂源期中)欲证明“CO2与NaOH发生了化学反应”,某化学兴趣小组进
行以下探究实验(实验装置中夹持仪器已略去),下列说法不正确的是 ( )
A.实验前,U形管两端的液面必须保持相平
B.实验后,恢复到室温时U形管中的液面左高右低
C.观察到B选项中的现象可得出结论:CO2与NaOH发生了化学反应
D.若用KOH溶液代替NaOH溶液,可观察到相同的实验现象
C
9.学校运动场跑道线常用材料是称作石灰的物质,其化学名为_____________。
它的水溶液俗称___________,可由生石灰与水反应制得,化学方程式为
_________________________。实验室也常用它来检验CO2的存在,化学方程式为
_________________________________。盛该溶液的试剂瓶时间长了,试剂瓶内壁
会生成一层白膜,这“白膜”的化学式是____________________,因“白膜”不溶于水,
所以不能用水冲洗,应先用___________清洗,再用水清洗。
氢氧化钙
石灰水
CaO+H2O===Ca(OH)2
Ca(OH)2+CO2===CaCO3↓+H2O
CaCO3(或碳酸钙)
稀盐酸
【B层 能力练】
10.(2022·淄博高青期中)现有两瓶失去标签的无色溶液,分别是稀盐酸和石灰水,
下列试剂不能鉴别开来的是 ( )
A.氯化钠溶液
B.氯化铜溶液
C.紫色石蕊试液
D.无色酚酞试液
A
11.(2022·淄博高青期中)将碳酸钠溶液分别滴加到澄清石灰水和氢氧化钠溶液中,
下列说法正确的是 ( )
A.两支试管都没有明显现象
B.右边试管中发生的反应方程式是2NaOH+Na2CO3===2NaOH+Na2CO3
C.左边试管中发生的反应方程式是Ca(OH)2+Na2CO3===CaCO3+2NaOH
D.该实验证明,不同的碱化学性质具有差异性
D
12.实验探究是获取证据的重要途径。“扬帆”学习小组阅读资料获知氢氧化钡[Ba(OH)2]与氢氧
化钙的化学性质相似,为了验证氢氧化钡的某些化学性质,他们设计如图所示实验。其中不能
达到实验目的的是 ( )
A.实验①验证氢氧化钡溶液显碱性
B.实验②验证氢氧化钡能与酸反应
C.实验③验证氢氧化钡能与某些盐反应
D.实验④验证氢氧化钡能与某些非金属氧化物反应
B
13.(2023·淄博张店区期中)忘记盖瓶塞的氢氧化钠溶液可能变质。如表中分析与
设计错误的是 ( )
选项 问题 分析与设计
A 为何变质 2NaOH+CO2===Na2CO3+H2O
B 是否变质 取样,滴加氯化钙溶液,观察是否生成沉淀
C 是否全部变质 取样,加入足量稀盐酸,观察是否产生气泡
D 如何除去杂质 取样,加入适量氢氧化钙溶液,过滤
C
14.完成下列问题:
(1)图1中,观察到的现象是_______________。
(2)图2中,观察到的现象是_________________。
(3)图3中,将针筒中的氢氧化钠溶液注入充满二氧化碳气体的锥形瓶中,观察到的
现象是_____________。
有同学认为:图3中的现象,不足以证明二氧化碳和氢氧化钠溶液发生了化学反应,
原因是___________________________________。
液体变红色
生成蓝色沉淀
气球膨胀
二氧化碳溶于水也会产生类似现象
15.生石灰和水反应得到熟石灰。现有露天堆置的熟石灰,某兴趣小组的同学要对
它进行成分分析,进而确定其变质情况。取样品少许,进行如下实验,请你帮助完
成有关问题:
【提出问题】熟石灰是否变质
【猜想与假设】猜想①:没有变质;
猜想②:全部变质;猜想③:_____________。
部分变质
【实验探究】
实验方案 实验现象 实验结论
方案1:取少量粉末于试管中,加少许水振荡 有白色不溶物出现 猜想②正确
方案2: Ⅰ.取方案1中的上层清液于试管中,滴加酚酞 溶液变红色 ______________
Ⅱ.向方案1中的不溶物中滴加稀盐酸 产生气泡 猜想③ 正确
【交流思考】(1)方案1的实验结论是否正确 你的回答是_________(填“正确”或
“错误”),理由是______________________________________________。
(2)写出方案2中产生气体反应的化学方程式________________________________。
【反思拓展】若较长时间场外堆置存放熟石灰,为防止熟石灰变质应注意的问题
是_______________________________。
错误
氢氧化钙微溶于水,白色不溶物可能是氢氧化钙
CaCO3+2HCl===CaCl2+H2O+CO2↑
尽量减少熟石灰与空气的接触
本课结束
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
