河南省漯河市重点中学2023-2024学年高二上学期月考备考化学练习三(含解析)
文档属性
| 名称 | 河南省漯河市重点中学2023-2024学年高二上学期月考备考化学练习三(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-01 00:00:00 | ||
图片预览




文档简介
漯河市重点中学2023-2024学年高二上学期月考备考
化学练习三
考试范围:选择性必修二加选择性必修一第一章;考试时间:75分钟;
第I卷(选择题)
一、单选题
1.2022年北京冬奥会充分体现了“绿色冬奥”和“科技冬奥”的理念,向世界展现了中国的“科技力量”。下列有关说法中错误的是
A.制作冰墩墩的PVC(聚氯乙烯)和PC(聚碳酸酯)均是有机合成高分子化合物
B.冬奥会火炬采用碳纤维和复合材质打造,碳纤维和C60、C70等互为同位素
C.国家速滑馆“冰丝带”采用二氧化碳跨临界直接制冰,该过程主要是物理变化
D.奥运比赛期间全部使用绿色电能,其中风能、水能和太阳能均属于一次能源
2.硼(B)元素位于第二周期第ⅢA族,与硅处于对角线位置,有对角相似的性质。下列说法错误的是
A.基态硼原子的价电子排布式为,易形成离子键
B.类比晶体硅,晶体硼为共价晶体,硬度极高
C.类比为分子晶体,推测为分子晶体
D.硼酸电离方程式为
3.一种锌的配合物结构如图所示,下列有关说法正确的是
A.中心离子提供空轨道的能级是3d和4s
B.该配合物中H N H的键角比中H N H的键角小
C.溴原子不同形状的轨道上的电子数之比是8∶17∶10
D.该化合物中C、N的杂化类型相同
4.高纯度的是一种半导体材料,如图是锗在元素周期表中的信息,下列说法正确的是
A.价电子数为2
B.原子的相对原子质量为72.61
C.原子序数与同主族相邻元素相差18
D.位于ⅥA族。处于金属元素与非金属元素分界处
5.甲胺铅碘[]是新型太阳能电池的敏化剂,已知[]的摩尔质量为,其晶胞结构如图所示。下列有关说法不正确的是
A.若B代表,则C代表
B.该晶胞沿体对角线方向的投影图为
C.距离A最近且等距离的C有8个
D.为阿伏加德罗常数的值,则该晶体的密度为
6.下列说法不正确的是
A.同一原子中,1s、2s、3s电子的能量逐渐增大
B.在电子云图中,用小黑点表示绕核做高速圆周运动的电子
C.、、轨道相互垂直,且能量相等
D.通过原子光谱上的特征谱线能鉴定某些元素
7.燃烧热指时,纯物质完全燃烧生成指定产物时所放出的热量,如C转化为、转化为。已知丙烷的燃烧热,下列有关丙烷的说法正确的是
A.丙烷的燃烧反应中,反应物的焓小于生成物的焓
B.
C.
D.甲烷的燃烧热,等质量的甲烷、丙烷完全燃烧甲烷放出的热量多
8.下列说法中正确的是
A.常温下能发生的反应一定是放热反应
B.、,△H1>△H2
C.CH4(g)的燃烧热△H=-890.3kJ·mol-1,则101kPa时,8gCH4(g)完全燃烧生成CO2(g)和H2O(l)时所放出的热量为445.15kJ
D.同温同压下,在光照和点燃条件下的焓变不同
9.CO2与CH4的催化重整有利于减少空气中的CO2,实现碳中和。
已知:① △H1=akJ·mol-1
② △H2=bkJ·mol-1
③ △H3=ckJ·mol-1
则的△H4为
A.(-a-b+c)kJ·mol-1 B.(a+b-c)kJ·mol-1
C.(-a+b-c)kJ·mol-1 D.(a-b-c)kJ·mol-1
10.图1为某晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。为所取晶胞的下底面,为锐角等于的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
A.befc B.kecb C.jkba D.dchg
11.某种离子液体的结构如图所示,其中X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,Z与Q同主族。下列说法错误的是
A.简单离子半径: B.简单氢化物键角:
C.最高价氧化物对应水化物的酸性: D.阴离子立体构型为正八面体形
12.下表是同周期三种主族元素X、Y、Z的电离能数据(单位:kJ·mol )。下列判断错误的是
元素代号
X 496 4562 6912 9543
Y 578 1817 2745 11575
Z 738 1451 7733 10540
A.,故金属性:Y>Z B.元素Z位于元素周期表s区
C.元素Y价电子排布式为 D.元素X是第IA族元素
13.对下列事实的解释不正确的是
选项 事实 解释
A 金属银具有良好的导电性 金属银中有“自由电子”
B ICl中I表现为正价 电负性:Cl>I
C 碘易溶于四氯化碳 碘分子和四氯化碳分子都是非极性分子
D Cl2、Br2、I2的熔沸点依次升高 Cl2、Br2、I2中共价键强度依次减小
A.A B.B C.C D.D
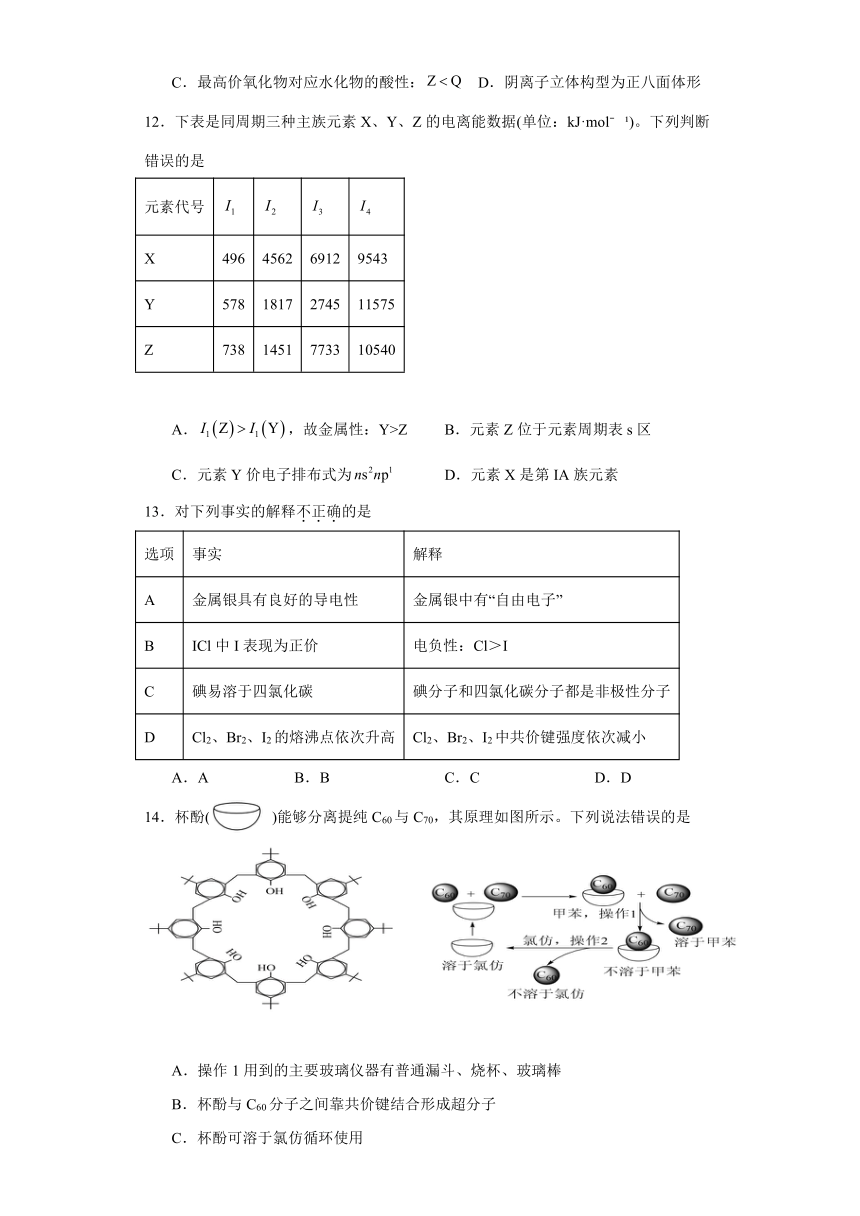
14.杯酚( )能够分离提纯C60与C70,其原理如图所示。下列说法错误的是
A.操作1用到的主要玻璃仪器有普通漏斗、烧杯、玻璃棒
B.杯酚与C60分子之间靠共价键结合形成超分子
C.杯酚可溶于氯仿循环使用
D.杯酚晶体属于分子晶体
15.下列热化学方程式正确的是
A.甲烷的燃烧热=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) =-890.3kJ/mol
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)2NH3(g) =-38.6kJ/mol
C.HCl和NaOH反应的中和热=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为2×(-57.3)kJ/mol
D.已知C(s)+O2(g)=CO2(g) =a,C(s)+O2(g)=CO(g) =b,则a<b
16.碱金属氯化物是典型的离子化合物,NaCl和CsCl的晶胞结构如图所示,其中的碱金属离子能够与冠醚形成超分子,下列说法正确的是
A.NaCl晶体中a离子的配位数为12
B.每个CsCl晶胞中含有个1个CsCl分子
C.碱金属离子与冠醚通过离子键形成超分子
D.不同空穴尺寸的冠醚可识别不同的碱金属离子
17.胆矾()是一种重要的盐,在电镀、印染、颜料、农药等领域都有着广泛的应用,可写作,其结构如图1,胆矾溶于水可得溶液,如图2所示,向溶液中逐滴加入浓氨水至过量,得到透明的深蓝色溶液,其溶质为,再向其中加入乙醇,可析出深蓝色的晶体,其组成为,下列有关说法不正确的是
A.由图1知胆矾中的水在不同温度下会分步失去
B.胆矾晶体中存在离子键、共价键、氢键及范德华力
C.该实验证明配离子比稳定
D.加入乙醇能使在水中的溶解度减小
18.自然界的氟化钙矿物为萤石或氟石,的晶体结构呈立方体形,其晶胞侧视图及晶胞结构如图,下列说法错误的是
A.基态F原子的电子排布式为
B.与最邻近的数为4
C.两个最近的之间的距离为
D.晶体密度为
19.下列有关物质结构与性质的说法中错误的是
A.根据VSEPR理论可知分子内键角依次减小
B.的电负性比的大,可推断的酸性强于
C.第四周期元素中,的第一电离能低于
D.因为水分子间存在氢键,故的稳定性大于
20.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 溶解度(20℃):大于 阴离子电荷
C 熔点:远高于(178℃升华) 晶体类型
D 酸性:远强于 羟基极性
A.A B.B C.C D.D
第II卷(非选择题)
21.原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E元素原子序数为29,请用元素符号或化学式回答问题:
(1)E原子价层电子的轨道表达式为 ;基态E原子电子占据的最高能层的符号为 。
(2)X、Y、Z 的第一电离能由小到大的顺序为 。
(3)已知YZ与XQ2互为等电子体,则 1 mol YZ中含有π键数目为 。
(4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 。
(5)E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图所示,该晶体的化学式为 。Z的配位数为 。设晶胞边长为 a cm,该晶体的密度为 g/cm3(阿伏加德罗常数用NA表示,列出计算式即可)。
22.Mn能改善钢材热加工性能,并改善钢材的冷脆倾向,同时不显著降低钢材的塑性、冲击韧性。根据要求回答下列问题:
(1)的核外电子排布式为 ,
基态Mn原子能级最高的电子的电子云轮廓图形状为 。
(2)Fe、Mn元素的部分电离能数据如下表:
元素 Fe Mn
电离能/() 759 717
1561 1509
2957 3248
从上表两元素部分电离能数据的比较可知,气态再失去一个电子比气态再失去一个电子难,原因是 。
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与形成黄色的配合物,其结构为。
①锰试剂分子中,电负性最大的原子是 ,采取杂化的原子是 ;
②锰试剂分子中能与形成配位键的原子是 。
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。
①图乙中a点和c点的原子坐标参数分别为(0,0,0)和,则b点的原子坐标参数为 ;
②设图甲晶体的密度为,设表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为 pm(用含、的关系式表示最简化的计算式即可)。
23.近日,《自然—通讯》发表了我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,可直接在二氧化硅表面生长高质量六方氮化硼薄膜。
(1)下列原子的电子排布式的状态中,能量最高的是_____(用字母表示)。
A. B.
C. D.
(2)第二周期主族元素中,按第一电离能大小排序,第一电离能在和之间的元素有 种。
(3)与形成的可用于制造汽车的安全气囊,其中阴离子的空间构型为 ,在空气中燃烧则发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为 光谱(填“发射”或“吸收”)。
(4)是一种有效、安全的固体储氢材料,可由与反应生成,分子中与之间形成 键,提供空轨道的原子为 (填元素符号),
(5)在催化剂作用可转化为,的结构如图所示:
在该反应中,B原子的杂化轨道类型由 变为 。分子中,与原子相连的呈正电性,与原子相连的呈负电性,分子中三种元素电负性由大到小的顺序是
(6)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿轴的投影图如右所示,该物质化学式为 。
24.(1)下列各组物质性质的比较,结论正确的是 (填字母序号)。
A.分子的极性:B.比中的配位键稳定
C.在中的溶解度:D.基态原子中未成对电子数:
(2)有四种不同堆积方式的金属晶体的晶胞如图所示(假设图中金属的摩尔质量为,金属原子半径为,用表示阿伏加 德罗常数的值),有关说法正确的是 (填字母序号)。
①②③④
A.①和②中原子的配位数均为8 B.③和④中原子的配位数均为12
C.②中金属的密度为:D.④中空间利用率为:%
(3)“摩尔盐”是分析化学中的重要试剂,化学式为。“摩尔盐”在一定条件下分解的方程式为:。
回答下列问题:
①铁元素在元素周期表中位于 区,其价层电子排布图(轨道式)为 。
②组成“摩尔盐”的非金属元素中电负性最大的元素为 (填元素符号),“摩尔盐”的分解产物中属于非极性分子的化合物是 (填化学式)。
③常用于检验,与互为等电子体的单质的分子式为 。分子中键和键的个数之比为 。
④可与噻吩()和吡咯()形成配位化合物。噻吩中原子和原子的杂化分式分别为: 。噻吩难溶于水,吡咯能溶于水,原因为: 。
参考答案:
1.B
2.A【详解】A.硼是5号元素,其基态硼原子的价电子排布式为,由于与硅处于对角线位置,有对角相似的性质,硅形成共价键,则B形成共价键,故A错误;
B.与硅处于对角线位置,有对角相似的性质,类比晶体硅,晶体硼为共价晶体,硬度大,熔点高,故B正确;
C.为分子晶体,类比推测为分子晶体,故C正确;
D.硼酸是一元弱酸,其电离方程式为,故D正确。
3.C【详解】A.配合物中心离子为,核外电子排布式为,提供空轨道的能级是4s和4p,故A错误;
B.配合物中氮原子的孤电子对与形成配位键,对成键电子对的排斥力减小,键角变大,所以该配合物中H N H的键角比中H N H的键角大,故B错误;
C.溴原子的核外电子排布式为,不同形状的轨道上的电子数之比是8∶17∶10,故C正确;
D.该化合物中C原子为杂化,N原子为杂化,故D错误。
4.C【详解】A.根据价电子排布式4s24p2可知价电子数为4,A错误;
B.根据锗在元素周期表中的信息,锗元素的相对原子质量为72.61,即元素的相对原子质量,而不是原子的相对原子质量,B错误;
C锗原子序数为32,位于第四周期IVA族,同主族相邻元素为硅、锡,原子序数均相差18,D.根据价电子排布式4s24p2,可得Ge位于IVA族,位于金属元素与非金属元素分界处,5.C【详解】A. 根据图中信息B得个数为1,C位于面心,共3个,因此若B代表,则C代表,故A正确;
B. 该晶胞沿体对角线方向投影,体对角线方向的2个顶点和体心投到1个点,另外6个原子在六边形内部形成1个小六边形,因此该晶胞沿体对角线方向的投影图为,
C. 距离A最近且等距离的C有12个,等距离的每个面有4个,有3个面,故C错误;
D. 为阿伏加德罗常数的值,则该晶体的密度为,
6.B【详解】A相同能级,能层越大,能量越大,1s、2s、3s电子的能量逐渐增大,A正确;
B.在电子云示意图中,通常用小黑点来表示电子在该点的出现几率而不是表示电子绕核作高速圆周运动的轨迹,B错误;
C.2px、2py、2pz轨道相互垂直,同一能级的不同轨道的能量相同,所以2px、2py、2pz轨道的能量相同,C正确;
D.不同元素的原子发生跃迁时会吸收或释放不同的光,在历史上,许多元素是通过原子光谱发现的,如铯和铷,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析,D正确;
7.D【分析】燃烧热为1mol纯物质完全燃烧生成稳定的化合物时所放出的热量,室温条件下,液态水稳定。
【详解】A.燃烧为放热反应,焓变为负值,则丙烷的燃烧反应中,反应物的焓大于生成物的焓,A错误;
B烷烃的标准燃烧热所指的稳定氧化物是指CO2气体和液态水,反应中为CO气体,B错误;
C.烷烃的标准燃烧热所指的稳定氧化物是指CO2气体和液态水,反应中为气态水,C错误;
D.在101kPa下,甲烷的热值是890.0kJ/mol÷16g/mol=55.625kJ/g,在101kPa下,丙烷的热值是2219.9kJ/mol÷44g/mol=50.452kJ/g,则等质量的甲烷、丙烷完全燃烧甲烷放出的热量多,、
8.C【详解】A.反应是否放热与反应是否需要加热无关,A项错误;
B.△H1<0、△H2>0,故△H1<△H2,B项错误;
C.CH4(g)的燃烧热△H=-890.3kJ·mol-1,表示1mol甲烷在常压下完全燃烧生成液态水时放热890.3kJ,8gCH4(g)的物质的量为0.5mol,完全燃烧生成CO2(g)和H2O(l)时所放出的热量为=445.15kJ,故C正确。
D.焓变与反应条件无关,D项错误。
9.A
10.A【分析】1个Zn原子位于晶胞体内,棱上的3个Zn原子和体内的Zn原子、O原子形成四面体结构,由于棱上的Zn原子需要共用,所以相邻的晶胞与该晶胞共用bc和cd
【详解】A.结合晶胞平移原则可知,befc与所取晶胞相邻的晶胞的底面相符,故A正确;
B.kecb违背晶胞平移原则,故B错误;C.jkba违背晶胞平移原则,故C错误;
D.dchg违背晶胞平移原则,故D错误;
11.C【分析】由题干离子液态的结构示意图可知,X周围形成1个共价键,Y周围形成4个共价键,其中一个Z周围形成3个共价键,另一个Z形成4个共价键,且整个离子带一个单位正电荷,即该Z原子失去一个电子,即Z的最外层上有5的电子,Z和Q为同主族,则Z为N,Q为P,W周围也只形成了1个共价键,故X为H,Y为C、W为F,据此分析解题。
【详解】A.由分析可知,Z、W、Q分别为N、F、P,根据电子层数越多半径越大,电子层数相同,核电荷数越大,半径越小,故简单离子半径P3->N3->F-即Q>Z>W,A正确;
B.由分析可知,Y、Z、Q分别为C、N、P,其简单氢化物即CH4、NH3和PH3,已知CH4为正四面体形,键角为109°28′,而NH3、PH3为三角锥形结构,键角小于109°28′,且P的电负性小于N,P的半径大于N,故NH3中共用电子对更加靠近,排斥力更大,键角NH3更大,故键角CH4>NH3>PH3即Y>Z>Q,B正确;
C.Z为N,Q为P,非金属性:N>P,则最高价氧化物水化物的酸性:HNO3>H3PO4,即Z>Q,C错误;
D.由题干离子液态的结构示意图可知,阴离子中心原子Q周围的价层电子对数为6,故其立体构型为正八面体形,D正确;
12.A【分析】根据表格中电离能的数据可知,X的较小,突增,故X的价电子数应为1,为第ⅠA族元素;Z的、较小,突增,说明Z的价电子数为2,为第ⅡA族元素;Y的、、均较小,突增,则Y的价电子数为3,为第ⅢA族元素。
【详解】A.三种元素处于同一周期,而同一周期中元素金属性从左向右依次减弱,故金属性:Z>Y,A项错误;B.元素Z为第ⅡA族元素,处于s区,B项正确;
C.元素Y处于第ⅢA族,价电子排布式为,C项正确;
D.根据分析可知元素X是第IA族元素,D项正确;
13.D【详解】A.金属银形成金属晶体,其由金属离子和自由电子构成,具有良好的导电性,A正确;B.由于电负性Cl>I ,所以ICl中I表现为正价,Cl表现为负价,B正确;
C碘分子和四氯化碳分子都是非极性分子,依据相似相溶原理,碘易溶于四氯化碳,C正确;
D虽然Cl2、Br2、I2中共价键强度依次减小,但分子晶体的熔沸点与共价键能无关,只取决于分子间的作用力,所以Cl2、Br2、I2的熔沸点随相对分子质量的增大而依次升高
14.B【详解】A.由题干图示信息可知,操作1分离固体和液体,故该操作为过滤,则用到的主要玻璃仪器有普通漏斗、烧杯、玻璃棒,A正确;
B.杯酚与C60分子两分子之间的作用力为分子间作用力,而不是共价键,B错误;
C.由题干图示信息可知,杯酚可溶于氯仿循环使用,C正确;
D.杯酚晶体是通过分子通过分子间作用力形成的分子晶体,D正确;
15.D【详解】A.由甲烷的燃烧热H= 890.3 kJ mol 1,燃烧热表示可燃物完全燃烧生成稳定的氧化物,产物水为液体水,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l) H= 890.3 kJ mol 1,A项错误;
B将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,合成氨为可逆反应,0.5 mol N2不能完全反应生成,则1molN2(g)充分反应生成NH3(g)放热大于38.6kJ,放热反应的焓变为负值,则N2(g)+3H2(g) 2NH3(g) △H< 38.6 kJ mol 1,B项错误;
C.中和热是一个定值,指常温下1molH+和1molOH-反应生成1molH2O放出的热量,不同的酸和碱反应会有不同的反应热,其值与中和热未必一致,C项错误;
D.完全燃烧比不完全燃烧放出热量多,燃烧反应的焓变为负值,由2C(s)+2O2(g)=2CO2(g) △H=a, 2C(s)+O2(g)=2CO(g) △H=b,可知a16.D【详解】A.钠离子的离子半径小于氯离子,因此氯化钠晶胞中a为离子半径较小的钠离子,每个钠离子同时吸引6个氯离子,钠离子的配位数为6,A项错误;
B.每个CsCl晶胞中含有8个和8个,因此每个CsCl晶胞中含有8个CsCl分子,
C.碱金属离子与冠醚通过配位键形成超分子,C项错误;
D冠醚与金属阳离子通过配位作用相结合,不同大小的冠醚可以识别不同大小的碱金属离子
17.C【详解】A.由图1可知,内界中水分子与铜离子形成配位键,结晶水与配合物形成氢键,氢键弱于配位键,所以胆矾中的水在不同温度下会分步失去,故A正确;
B.由图1可知,胆矾晶体中存在离子键、共价键、氢键及范德华力,故B正确;
C.由向硫酸铜溶液中逐滴加入浓氨水至过量,得到透明的深蓝色溶液可知,四氨合铜离子的稳定性强于四水合铜离子,故C错误;
D.由向深蓝色溶液中加入乙醇,可析出深蓝色的晶体可知,加入乙醇能使硫酸四氨合铜在水中的溶解度减小,故D正确;
18.B【详解】A.F是原子序数为9的元素,基态F原子的电子排布式为,A正确;
B.晶胞中与最邻近的数为8,B错误;
C.根据侧面图可看出,面对角线的长度为,边长为,两个最近的之间的距离为立方体边长的一半,所以两个最近的之间的距离为,C项正确;
D.根据图示可知晶胞中含4个和8个,边长为,利用得出,D项正确。
19.D【详解】A.为杂化,键角为,均为杂化,的键角为中含有孤电子对,键角约为,故键角依次减小,A正确;
B.的电负性比的大,的极性大于的极性,使—的极性大于的极性、导致中的羧基的极性更大,更易电离出,故的酸性强于,B正确;
C.的核外电子排布为,电子所在的轨道均处于全充满状态,较稳定,故第一电离能大于,C正确;
D.非金属简单氢化物的稳定性与分子内的化学键的键能有关,的稳定性大于的稳定性是因为中的键能大于中的键能,与分子间氢键无关,D错误;
20.B【详解】A.正戊烷和新戊烷都属于分子晶体,分子的极性越小,分子间作用力越小,熔沸点越低,A正确;
B.碳酸氢钠溶解度较小的原因是碳酸氢根间由于氢键出现聚合现象,与阴离子电荷无关,C.AlF3为离子晶体,微粒间作用为离子键,AlCl3为分子晶体,熔点受分子间作用力影响,一般离子键作用强于分子间作用力,C正确;
D.由于电负性F>C>H,-CF3为吸电子基,使得羧基上的羟基极性增强,氢原子更易电离,酸性增强,D正确;
21.(1) N (2)C22.(1) 1s22s22p63s23p63d5 花瓣形
(2)由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态变为不稳定的3d4状态,需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态变为较稳定的3d5半充满状态,需要的能量相对较少
(3) O C、N N、O (4) (1,1,0)
【详解】(1)Fe是26号元素,基态Fe原子的核外电子排布式为1s22s22p63s23p63d64s2,失去2个4s和1个3d电子变为,则的核外电子排布式为1s22s22p63s23p63d5。Mn是25号元素,基态Mn原子的核外电子排布式为1s22s22p63s23p63d54s2,由于能量4s<3d,则电子占据最高能级是3d,其电子云轮廓图形状为花瓣形,故答案为:1s22s22p63s23p63d5;花瓣形;
(2)从表中Fe、Mn两元素部分电离能数据的比较可知,气态再失去一个电子比气态再失去一个电子难,这是因为由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态变为不稳定的3d4状态,需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态变为较稳定的3d5半充满状态,需要的能量相对较少;
(3)①锰试剂分子中的元素有O、H、C、N,电负性最大的元素是O,采取杂化的原子是C、N,故答案为:O;C、N;
②N、O原子上存在孤电子对,可以作为配位原子,故答案为:N、O;
(4)①a点和c点的原子坐标参数分别为(0,0,0)和,而b点所在的位置为xoy所在坐标平面上,则b点的原子坐标参数为(1,1,0);
②设该晶胞的边长为apm,则距离最近的两个砷原子之间的距离为apm,该晶胞中的Ga位于顶点和面心,个数为8+6=4,As位于体内,个数为4,以该晶胞为研究对象,则晶胞的质量为g=,解得a=,故距离最近的两个砷原子之间的距离为pm,故答案为:。
23.(1)D (2)3 (3) 直线形 发射 (4) 配位键 (5) sp3 sp2 (6)
【详解】(1)A.基态原子的电子排布式,当一个电子吸收能量从跃迁到成为;
B.当一个电子吸收能量从跃迁到成为;
C.当一个电子吸收能量从跃迁到成为;
D.当一个电子吸收能量从跃迁到同时另一个电子吸收能量从跃迁到成为; 根据能量 ,所以吸收能量的大小为:。
(2)同周期主族元素随原子序数增大第一电离能呈增大趋势,IIA族、VA族为全充满或半充满稳定状态,第一电离能高于同周期相邻元素,因而在B与N之间还有Be、C、O三种元素,答案为3;
(3)N3-离子中心N原子价层电子对数=2+ =2,价层电子对数为2,孤电子对为0,N原子杂化方式为sp杂化,离子空间构型为直线形,电子从激发态跃迁到低能级,以光的形式释放能量,Na 元素发生焰色反应是因为产生了光子,发射光谱;答案为:直线形,发射;
(4)B原子形成3个B-H键,B原子有空轨道,氨分子中N原子有1对孤电子对,B与N之间形成配位键,氮原子提供孤电子对,答案为:配位键,;
(5)在BH3·NH3中B原子形成3个B-H键,B还形成1个配位键,B原子杂化轨道数目为4,B原子杂化方式为sp3杂化,中B原子杂化方式为sp2杂化,分子中,与原子相连的呈正电性,与原子相连的呈负电性,分子中三种元素电负性由大到小的顺序是 ,答案为:sp3,sp2,;
(6)由硼镁化合物的晶体结构可知位于正六棱柱的顶点和面心,由均摊法可以求出正六棱柱中含有个,由晶胞沿c轴的投影图可知本题所给晶体结构包含三个晶胞,则晶胞中Mg的个数为1;晶体结构中在正六棱柱体内共6个,则该物质的化学式为,答案为:。
24.AD BD d 、 吡咯能与水形成分子间氢键
【详解】(1)A.BCl3中B是采用sp2杂化,为平面三角形,是非极性分子;NCl3分子中N采用sp3杂化,为三角锥形,是极性分子,所以分子的极性:,A正确;
B.配位体给出电子能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定,O的给电子能力小于N,所以的配位键没有中的配位键稳定,B错误;
C.四氯化碳为非极性分子,易溶于非极性的二硫化碳中,水为极性分子,难溶于非极性的二硫化碳中,所以四氯化碳在中的溶解度大于水在中的溶解度,C错误;
D. Mn的价层电子排布式为3d54s2,有5个未成对电子,Si的价层电子排布式为3s23p2,有2个未成对电子,Cl价层电子排布式为3s23p5,有1个未成对电子,所以基态原子中未成对电子数:,D正确;
(2)A.①为简单堆积,配位数为6,②为体心立方堆积,配位数为8,A错误;
B.③为六方最密堆积,④为面心立方堆积,配位数均为12,B正确;
C.②中原子个数为,晶胞质量为2M,所以金属的密度为:,D.④为面心立方堆积,空间利用率为:=%,D正确;
(3)①铁的原子序数是26,位于第四周期第Ⅷ族,位于元素周期表中d区,根据核外电子排布规律可知铁的价层电子排布式为3d64s2,其电子排布图为,故本题答案为:d;;
②组成“摩尔盐”的非金属元素有H、N、O、S,其中电负性最大的元素为O,分解产物中三氧化硫是平面三角形结构,属于非极性分子,故本题答案为:O;SO3;
③等电子体是原子数相等,价电子数也相等的离子或分子,与CN-互为等电子体的单质的分子式为N2,分子的结构为H-C≡N,键和键的个数之比为1:1,故本题答案为:N2,;1:1;
④根据噻吩()的结构可知,噻吩中原子的杂化方式为,原子的杂化方式为。吡咯能与水形成分子间氢键,所以吡咯能溶于水,噻吩不能与水形成分子间氢键,所以噻吩难溶于水,故本题答案为:吡咯能与水形成分子间氢键;
化学练习三
考试范围:选择性必修二加选择性必修一第一章;考试时间:75分钟;
第I卷(选择题)
一、单选题
1.2022年北京冬奥会充分体现了“绿色冬奥”和“科技冬奥”的理念,向世界展现了中国的“科技力量”。下列有关说法中错误的是
A.制作冰墩墩的PVC(聚氯乙烯)和PC(聚碳酸酯)均是有机合成高分子化合物
B.冬奥会火炬采用碳纤维和复合材质打造,碳纤维和C60、C70等互为同位素
C.国家速滑馆“冰丝带”采用二氧化碳跨临界直接制冰,该过程主要是物理变化
D.奥运比赛期间全部使用绿色电能,其中风能、水能和太阳能均属于一次能源
2.硼(B)元素位于第二周期第ⅢA族,与硅处于对角线位置,有对角相似的性质。下列说法错误的是
A.基态硼原子的价电子排布式为,易形成离子键
B.类比晶体硅,晶体硼为共价晶体,硬度极高
C.类比为分子晶体,推测为分子晶体
D.硼酸电离方程式为
3.一种锌的配合物结构如图所示,下列有关说法正确的是
A.中心离子提供空轨道的能级是3d和4s
B.该配合物中H N H的键角比中H N H的键角小
C.溴原子不同形状的轨道上的电子数之比是8∶17∶10
D.该化合物中C、N的杂化类型相同
4.高纯度的是一种半导体材料,如图是锗在元素周期表中的信息,下列说法正确的是
A.价电子数为2
B.原子的相对原子质量为72.61
C.原子序数与同主族相邻元素相差18
D.位于ⅥA族。处于金属元素与非金属元素分界处
5.甲胺铅碘[]是新型太阳能电池的敏化剂,已知[]的摩尔质量为,其晶胞结构如图所示。下列有关说法不正确的是
A.若B代表,则C代表
B.该晶胞沿体对角线方向的投影图为
C.距离A最近且等距离的C有8个
D.为阿伏加德罗常数的值,则该晶体的密度为
6.下列说法不正确的是
A.同一原子中,1s、2s、3s电子的能量逐渐增大
B.在电子云图中,用小黑点表示绕核做高速圆周运动的电子
C.、、轨道相互垂直,且能量相等
D.通过原子光谱上的特征谱线能鉴定某些元素
7.燃烧热指时,纯物质完全燃烧生成指定产物时所放出的热量,如C转化为、转化为。已知丙烷的燃烧热,下列有关丙烷的说法正确的是
A.丙烷的燃烧反应中,反应物的焓小于生成物的焓
B.
C.
D.甲烷的燃烧热,等质量的甲烷、丙烷完全燃烧甲烷放出的热量多
8.下列说法中正确的是
A.常温下能发生的反应一定是放热反应
B.、,△H1>△H2
C.CH4(g)的燃烧热△H=-890.3kJ·mol-1,则101kPa时,8gCH4(g)完全燃烧生成CO2(g)和H2O(l)时所放出的热量为445.15kJ
D.同温同压下,在光照和点燃条件下的焓变不同
9.CO2与CH4的催化重整有利于减少空气中的CO2,实现碳中和。
已知:① △H1=akJ·mol-1
② △H2=bkJ·mol-1
③ △H3=ckJ·mol-1
则的△H4为
A.(-a-b+c)kJ·mol-1 B.(a+b-c)kJ·mol-1
C.(-a+b-c)kJ·mol-1 D.(a-b-c)kJ·mol-1
10.图1为某晶胞示意图,图2为若干晶胞无隙并置而成的底面O原子排列局部平面图。为所取晶胞的下底面,为锐角等于的菱形。以此为参考,图2中与所取晶胞相邻的晶胞的底面是
A.befc B.kecb C.jkba D.dchg
11.某种离子液体的结构如图所示,其中X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,Z与Q同主族。下列说法错误的是
A.简单离子半径: B.简单氢化物键角:
C.最高价氧化物对应水化物的酸性: D.阴离子立体构型为正八面体形
12.下表是同周期三种主族元素X、Y、Z的电离能数据(单位:kJ·mol )。下列判断错误的是
元素代号
X 496 4562 6912 9543
Y 578 1817 2745 11575
Z 738 1451 7733 10540
A.,故金属性:Y>Z B.元素Z位于元素周期表s区
C.元素Y价电子排布式为 D.元素X是第IA族元素
13.对下列事实的解释不正确的是
选项 事实 解释
A 金属银具有良好的导电性 金属银中有“自由电子”
B ICl中I表现为正价 电负性:Cl>I
C 碘易溶于四氯化碳 碘分子和四氯化碳分子都是非极性分子
D Cl2、Br2、I2的熔沸点依次升高 Cl2、Br2、I2中共价键强度依次减小
A.A B.B C.C D.D
14.杯酚( )能够分离提纯C60与C70,其原理如图所示。下列说法错误的是
A.操作1用到的主要玻璃仪器有普通漏斗、烧杯、玻璃棒
B.杯酚与C60分子之间靠共价键结合形成超分子
C.杯酚可溶于氯仿循环使用
D.杯酚晶体属于分子晶体
15.下列热化学方程式正确的是
A.甲烷的燃烧热=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) =-890.3kJ/mol
B.500℃、30MPa下,将0.5molN2(g)和1.5molH2(g)置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)2NH3(g) =-38.6kJ/mol
C.HCl和NaOH反应的中和热=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为2×(-57.3)kJ/mol
D.已知C(s)+O2(g)=CO2(g) =a,C(s)+O2(g)=CO(g) =b,则a<b
16.碱金属氯化物是典型的离子化合物,NaCl和CsCl的晶胞结构如图所示,其中的碱金属离子能够与冠醚形成超分子,下列说法正确的是
A.NaCl晶体中a离子的配位数为12
B.每个CsCl晶胞中含有个1个CsCl分子
C.碱金属离子与冠醚通过离子键形成超分子
D.不同空穴尺寸的冠醚可识别不同的碱金属离子
17.胆矾()是一种重要的盐,在电镀、印染、颜料、农药等领域都有着广泛的应用,可写作,其结构如图1,胆矾溶于水可得溶液,如图2所示,向溶液中逐滴加入浓氨水至过量,得到透明的深蓝色溶液,其溶质为,再向其中加入乙醇,可析出深蓝色的晶体,其组成为,下列有关说法不正确的是
A.由图1知胆矾中的水在不同温度下会分步失去
B.胆矾晶体中存在离子键、共价键、氢键及范德华力
C.该实验证明配离子比稳定
D.加入乙醇能使在水中的溶解度减小
18.自然界的氟化钙矿物为萤石或氟石,的晶体结构呈立方体形,其晶胞侧视图及晶胞结构如图,下列说法错误的是
A.基态F原子的电子排布式为
B.与最邻近的数为4
C.两个最近的之间的距离为
D.晶体密度为
19.下列有关物质结构与性质的说法中错误的是
A.根据VSEPR理论可知分子内键角依次减小
B.的电负性比的大,可推断的酸性强于
C.第四周期元素中,的第一电离能低于
D.因为水分子间存在氢键,故的稳定性大于
20.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
选项 性质差异 结构因素
A 沸点:正戊烷(36.1℃)高于新戊烷(9.5℃) 分子间作用力
B 溶解度(20℃):大于 阴离子电荷
C 熔点:远高于(178℃升华) 晶体类型
D 酸性:远强于 羟基极性
A.A B.B C.C D.D
第II卷(非选择题)
21.原子序数依次增大的X、Y、Z、Q、E五种元素中,X元素原子核外有三种不同的能级且各个能级所填充的电子数相同,Z是地壳内含量(质量分数)最高的元素,Q原子核外的M层中只有两对成对电子,E元素原子序数为29,请用元素符号或化学式回答问题:
(1)E原子价层电子的轨道表达式为 ;基态E原子电子占据的最高能层的符号为 。
(2)X、Y、Z 的第一电离能由小到大的顺序为 。
(3)已知YZ与XQ2互为等电子体,则 1 mol YZ中含有π键数目为 。
(4)X、Z与氢元素可形成化合物H2X2Z4,常用作工业除锈剂。H2X2Z4分子中X的杂化方式为 。
(5)E有可变价态,它的某价态的离子与Z的阴离子形成晶体的晶胞如图所示,该晶体的化学式为 。Z的配位数为 。设晶胞边长为 a cm,该晶体的密度为 g/cm3(阿伏加德罗常数用NA表示,列出计算式即可)。
22.Mn能改善钢材热加工性能,并改善钢材的冷脆倾向,同时不显著降低钢材的塑性、冲击韧性。根据要求回答下列问题:
(1)的核外电子排布式为 ,
基态Mn原子能级最高的电子的电子云轮廓图形状为 。
(2)Fe、Mn元素的部分电离能数据如下表:
元素 Fe Mn
电离能/() 759 717
1561 1509
2957 3248
从上表两元素部分电离能数据的比较可知,气态再失去一个电子比气态再失去一个电子难,原因是 。
(3)水杨醛缩邻氨基苯酚又被称为“锰试剂”,可与形成黄色的配合物,其结构为。
①锰试剂分子中,电负性最大的原子是 ,采取杂化的原子是 ;
②锰试剂分子中能与形成配位键的原子是 。
(4)将Mn掺入GaAs晶体(图甲)可得到稀磁性半导体材料(图乙),晶体结构不变。
①图乙中a点和c点的原子坐标参数分别为(0,0,0)和,则b点的原子坐标参数为 ;
②设图甲晶体的密度为,设表示阿伏加德罗常数的值,则该晶胞中距离最近的两个砷原子之间的距离为 pm(用含、的关系式表示最简化的计算式即可)。
23.近日,《自然—通讯》发表了我国复旦大学魏大程团队开发的一种共形六方氮化硼修饰技术,可直接在二氧化硅表面生长高质量六方氮化硼薄膜。
(1)下列原子的电子排布式的状态中,能量最高的是_____(用字母表示)。
A. B.
C. D.
(2)第二周期主族元素中,按第一电离能大小排序,第一电离能在和之间的元素有 种。
(3)与形成的可用于制造汽车的安全气囊,其中阴离子的空间构型为 ,在空气中燃烧则发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为 光谱(填“发射”或“吸收”)。
(4)是一种有效、安全的固体储氢材料,可由与反应生成,分子中与之间形成 键,提供空轨道的原子为 (填元素符号),
(5)在催化剂作用可转化为,的结构如图所示:
在该反应中,B原子的杂化轨道类型由 变为 。分子中,与原子相连的呈正电性,与原子相连的呈负电性,分子中三种元素电负性由大到小的顺序是
(6)一种硼镁化合物具有超导性能,晶体结构属于立方晶系,其晶体结构、晶胞沿轴的投影图如右所示,该物质化学式为 。
24.(1)下列各组物质性质的比较,结论正确的是 (填字母序号)。
A.分子的极性:B.比中的配位键稳定
C.在中的溶解度:D.基态原子中未成对电子数:
(2)有四种不同堆积方式的金属晶体的晶胞如图所示(假设图中金属的摩尔质量为,金属原子半径为,用表示阿伏加 德罗常数的值),有关说法正确的是 (填字母序号)。
①②③④
A.①和②中原子的配位数均为8 B.③和④中原子的配位数均为12
C.②中金属的密度为:D.④中空间利用率为:%
(3)“摩尔盐”是分析化学中的重要试剂,化学式为。“摩尔盐”在一定条件下分解的方程式为:。
回答下列问题:
①铁元素在元素周期表中位于 区,其价层电子排布图(轨道式)为 。
②组成“摩尔盐”的非金属元素中电负性最大的元素为 (填元素符号),“摩尔盐”的分解产物中属于非极性分子的化合物是 (填化学式)。
③常用于检验,与互为等电子体的单质的分子式为 。分子中键和键的个数之比为 。
④可与噻吩()和吡咯()形成配位化合物。噻吩中原子和原子的杂化分式分别为: 。噻吩难溶于水,吡咯能溶于水,原因为: 。
参考答案:
1.B
2.A【详解】A.硼是5号元素,其基态硼原子的价电子排布式为,由于与硅处于对角线位置,有对角相似的性质,硅形成共价键,则B形成共价键,故A错误;
B.与硅处于对角线位置,有对角相似的性质,类比晶体硅,晶体硼为共价晶体,硬度大,熔点高,故B正确;
C.为分子晶体,类比推测为分子晶体,故C正确;
D.硼酸是一元弱酸,其电离方程式为,故D正确。
3.C【详解】A.配合物中心离子为,核外电子排布式为,提供空轨道的能级是4s和4p,故A错误;
B.配合物中氮原子的孤电子对与形成配位键,对成键电子对的排斥力减小,键角变大,所以该配合物中H N H的键角比中H N H的键角大,故B错误;
C.溴原子的核外电子排布式为,不同形状的轨道上的电子数之比是8∶17∶10,故C正确;
D.该化合物中C原子为杂化,N原子为杂化,故D错误。
4.C【详解】A.根据价电子排布式4s24p2可知价电子数为4,A错误;
B.根据锗在元素周期表中的信息,锗元素的相对原子质量为72.61,即元素的相对原子质量,而不是原子的相对原子质量,B错误;
C锗原子序数为32,位于第四周期IVA族,同主族相邻元素为硅、锡,原子序数均相差18,D.根据价电子排布式4s24p2,可得Ge位于IVA族,位于金属元素与非金属元素分界处,5.C【详解】A. 根据图中信息B得个数为1,C位于面心,共3个,因此若B代表,则C代表,故A正确;
B. 该晶胞沿体对角线方向投影,体对角线方向的2个顶点和体心投到1个点,另外6个原子在六边形内部形成1个小六边形,因此该晶胞沿体对角线方向的投影图为,
C. 距离A最近且等距离的C有12个,等距离的每个面有4个,有3个面,故C错误;
D. 为阿伏加德罗常数的值,则该晶体的密度为,
6.B【详解】A相同能级,能层越大,能量越大,1s、2s、3s电子的能量逐渐增大,A正确;
B.在电子云示意图中,通常用小黑点来表示电子在该点的出现几率而不是表示电子绕核作高速圆周运动的轨迹,B错误;
C.2px、2py、2pz轨道相互垂直,同一能级的不同轨道的能量相同,所以2px、2py、2pz轨道的能量相同,C正确;
D.不同元素的原子发生跃迁时会吸收或释放不同的光,在历史上,许多元素是通过原子光谱发现的,如铯和铷,在现代化学中,常利用原子光谱上的特征谱线来鉴定元素,称为光谱分析,D正确;
7.D【分析】燃烧热为1mol纯物质完全燃烧生成稳定的化合物时所放出的热量,室温条件下,液态水稳定。
【详解】A.燃烧为放热反应,焓变为负值,则丙烷的燃烧反应中,反应物的焓大于生成物的焓,A错误;
B烷烃的标准燃烧热所指的稳定氧化物是指CO2气体和液态水,反应中为CO气体,B错误;
C.烷烃的标准燃烧热所指的稳定氧化物是指CO2气体和液态水,反应中为气态水,C错误;
D.在101kPa下,甲烷的热值是890.0kJ/mol÷16g/mol=55.625kJ/g,在101kPa下,丙烷的热值是2219.9kJ/mol÷44g/mol=50.452kJ/g,则等质量的甲烷、丙烷完全燃烧甲烷放出的热量多,、
8.C【详解】A.反应是否放热与反应是否需要加热无关,A项错误;
B.△H1<0、△H2>0,故△H1<△H2,B项错误;
C.CH4(g)的燃烧热△H=-890.3kJ·mol-1,表示1mol甲烷在常压下完全燃烧生成液态水时放热890.3kJ,8gCH4(g)的物质的量为0.5mol,完全燃烧生成CO2(g)和H2O(l)时所放出的热量为=445.15kJ,故C正确。
D.焓变与反应条件无关,D项错误。
9.A
10.A【分析】1个Zn原子位于晶胞体内,棱上的3个Zn原子和体内的Zn原子、O原子形成四面体结构,由于棱上的Zn原子需要共用,所以相邻的晶胞与该晶胞共用bc和cd
【详解】A.结合晶胞平移原则可知,befc与所取晶胞相邻的晶胞的底面相符,故A正确;
B.kecb违背晶胞平移原则,故B错误;C.jkba违背晶胞平移原则,故C错误;
D.dchg违背晶胞平移原则,故D错误;
11.C【分析】由题干离子液态的结构示意图可知,X周围形成1个共价键,Y周围形成4个共价键,其中一个Z周围形成3个共价键,另一个Z形成4个共价键,且整个离子带一个单位正电荷,即该Z原子失去一个电子,即Z的最外层上有5的电子,Z和Q为同主族,则Z为N,Q为P,W周围也只形成了1个共价键,故X为H,Y为C、W为F,据此分析解题。
【详解】A.由分析可知,Z、W、Q分别为N、F、P,根据电子层数越多半径越大,电子层数相同,核电荷数越大,半径越小,故简单离子半径P3->N3->F-即Q>Z>W,A正确;
B.由分析可知,Y、Z、Q分别为C、N、P,其简单氢化物即CH4、NH3和PH3,已知CH4为正四面体形,键角为109°28′,而NH3、PH3为三角锥形结构,键角小于109°28′,且P的电负性小于N,P的半径大于N,故NH3中共用电子对更加靠近,排斥力更大,键角NH3更大,故键角CH4>NH3>PH3即Y>Z>Q,B正确;
C.Z为N,Q为P,非金属性:N>P,则最高价氧化物水化物的酸性:HNO3>H3PO4,即Z>Q,C错误;
D.由题干离子液态的结构示意图可知,阴离子中心原子Q周围的价层电子对数为6,故其立体构型为正八面体形,D正确;
12.A【分析】根据表格中电离能的数据可知,X的较小,突增,故X的价电子数应为1,为第ⅠA族元素;Z的、较小,突增,说明Z的价电子数为2,为第ⅡA族元素;Y的、、均较小,突增,则Y的价电子数为3,为第ⅢA族元素。
【详解】A.三种元素处于同一周期,而同一周期中元素金属性从左向右依次减弱,故金属性:Z>Y,A项错误;B.元素Z为第ⅡA族元素,处于s区,B项正确;
C.元素Y处于第ⅢA族,价电子排布式为,C项正确;
D.根据分析可知元素X是第IA族元素,D项正确;
13.D【详解】A.金属银形成金属晶体,其由金属离子和自由电子构成,具有良好的导电性,A正确;B.由于电负性Cl>I ,所以ICl中I表现为正价,Cl表现为负价,B正确;
C碘分子和四氯化碳分子都是非极性分子,依据相似相溶原理,碘易溶于四氯化碳,C正确;
D虽然Cl2、Br2、I2中共价键强度依次减小,但分子晶体的熔沸点与共价键能无关,只取决于分子间的作用力,所以Cl2、Br2、I2的熔沸点随相对分子质量的增大而依次升高
14.B【详解】A.由题干图示信息可知,操作1分离固体和液体,故该操作为过滤,则用到的主要玻璃仪器有普通漏斗、烧杯、玻璃棒,A正确;
B.杯酚与C60分子两分子之间的作用力为分子间作用力,而不是共价键,B错误;
C.由题干图示信息可知,杯酚可溶于氯仿循环使用,C正确;
D.杯酚晶体是通过分子通过分子间作用力形成的分子晶体,D正确;
15.D【详解】A.由甲烷的燃烧热H= 890.3 kJ mol 1,燃烧热表示可燃物完全燃烧生成稳定的氧化物,产物水为液体水,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l) H= 890.3 kJ mol 1,A项错误;
B将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,合成氨为可逆反应,0.5 mol N2不能完全反应生成,则1molN2(g)充分反应生成NH3(g)放热大于38.6kJ,放热反应的焓变为负值,则N2(g)+3H2(g) 2NH3(g) △H< 38.6 kJ mol 1,B项错误;
C.中和热是一个定值,指常温下1molH+和1molOH-反应生成1molH2O放出的热量,不同的酸和碱反应会有不同的反应热,其值与中和热未必一致,C项错误;
D.完全燃烧比不完全燃烧放出热量多,燃烧反应的焓变为负值,由2C(s)+2O2(g)=2CO2(g) △H=a, 2C(s)+O2(g)=2CO(g) △H=b,可知a
B.每个CsCl晶胞中含有8个和8个,因此每个CsCl晶胞中含有8个CsCl分子,
C.碱金属离子与冠醚通过配位键形成超分子,C项错误;
D冠醚与金属阳离子通过配位作用相结合,不同大小的冠醚可以识别不同大小的碱金属离子
17.C【详解】A.由图1可知,内界中水分子与铜离子形成配位键,结晶水与配合物形成氢键,氢键弱于配位键,所以胆矾中的水在不同温度下会分步失去,故A正确;
B.由图1可知,胆矾晶体中存在离子键、共价键、氢键及范德华力,故B正确;
C.由向硫酸铜溶液中逐滴加入浓氨水至过量,得到透明的深蓝色溶液可知,四氨合铜离子的稳定性强于四水合铜离子,故C错误;
D.由向深蓝色溶液中加入乙醇,可析出深蓝色的晶体可知,加入乙醇能使硫酸四氨合铜在水中的溶解度减小,故D正确;
18.B【详解】A.F是原子序数为9的元素,基态F原子的电子排布式为,A正确;
B.晶胞中与最邻近的数为8,B错误;
C.根据侧面图可看出,面对角线的长度为,边长为,两个最近的之间的距离为立方体边长的一半,所以两个最近的之间的距离为,C项正确;
D.根据图示可知晶胞中含4个和8个,边长为,利用得出,D项正确。
19.D【详解】A.为杂化,键角为,均为杂化,的键角为中含有孤电子对,键角约为,故键角依次减小,A正确;
B.的电负性比的大,的极性大于的极性,使—的极性大于的极性、导致中的羧基的极性更大,更易电离出,故的酸性强于,B正确;
C.的核外电子排布为,电子所在的轨道均处于全充满状态,较稳定,故第一电离能大于,C正确;
D.非金属简单氢化物的稳定性与分子内的化学键的键能有关,的稳定性大于的稳定性是因为中的键能大于中的键能,与分子间氢键无关,D错误;
20.B【详解】A.正戊烷和新戊烷都属于分子晶体,分子的极性越小,分子间作用力越小,熔沸点越低,A正确;
B.碳酸氢钠溶解度较小的原因是碳酸氢根间由于氢键出现聚合现象,与阴离子电荷无关,C.AlF3为离子晶体,微粒间作用为离子键,AlCl3为分子晶体,熔点受分子间作用力影响,一般离子键作用强于分子间作用力,C正确;
D.由于电负性F>C>H,-CF3为吸电子基,使得羧基上的羟基极性增强,氢原子更易电离,酸性增强,D正确;
21.(1) N (2)C
(2)由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态变为不稳定的3d4状态,需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态变为较稳定的3d5半充满状态,需要的能量相对较少
(3) O C、N N、O (4) (1,1,0)
【详解】(1)Fe是26号元素,基态Fe原子的核外电子排布式为1s22s22p63s23p63d64s2,失去2个4s和1个3d电子变为,则的核外电子排布式为1s22s22p63s23p63d5。Mn是25号元素,基态Mn原子的核外电子排布式为1s22s22p63s23p63d54s2,由于能量4s<3d,则电子占据最高能级是3d,其电子云轮廓图形状为花瓣形,故答案为:1s22s22p63s23p63d5;花瓣形;
(2)从表中Fe、Mn两元素部分电离能数据的比较可知,气态再失去一个电子比气态再失去一个电子难,这是因为由Mn2+转化为Mn3+时,3d能级由较稳定的3d5半充满状态变为不稳定的3d4状态,需要的能量较多;而Fe2+转化为Fe3+时,3d能级由不稳定的3d6状态变为较稳定的3d5半充满状态,需要的能量相对较少;
(3)①锰试剂分子中的元素有O、H、C、N,电负性最大的元素是O,采取杂化的原子是C、N,故答案为:O;C、N;
②N、O原子上存在孤电子对,可以作为配位原子,故答案为:N、O;
(4)①a点和c点的原子坐标参数分别为(0,0,0)和,而b点所在的位置为xoy所在坐标平面上,则b点的原子坐标参数为(1,1,0);
②设该晶胞的边长为apm,则距离最近的两个砷原子之间的距离为apm,该晶胞中的Ga位于顶点和面心,个数为8+6=4,As位于体内,个数为4,以该晶胞为研究对象,则晶胞的质量为g=,解得a=,故距离最近的两个砷原子之间的距离为pm,故答案为:。
23.(1)D (2)3 (3) 直线形 发射 (4) 配位键 (5) sp3 sp2 (6)
【详解】(1)A.基态原子的电子排布式,当一个电子吸收能量从跃迁到成为;
B.当一个电子吸收能量从跃迁到成为;
C.当一个电子吸收能量从跃迁到成为;
D.当一个电子吸收能量从跃迁到同时另一个电子吸收能量从跃迁到成为; 根据能量 ,所以吸收能量的大小为:。
(2)同周期主族元素随原子序数增大第一电离能呈增大趋势,IIA族、VA族为全充满或半充满稳定状态,第一电离能高于同周期相邻元素,因而在B与N之间还有Be、C、O三种元素,答案为3;
(3)N3-离子中心N原子价层电子对数=2+ =2,价层电子对数为2,孤电子对为0,N原子杂化方式为sp杂化,离子空间构型为直线形,电子从激发态跃迁到低能级,以光的形式释放能量,Na 元素发生焰色反应是因为产生了光子,发射光谱;答案为:直线形,发射;
(4)B原子形成3个B-H键,B原子有空轨道,氨分子中N原子有1对孤电子对,B与N之间形成配位键,氮原子提供孤电子对,答案为:配位键,;
(5)在BH3·NH3中B原子形成3个B-H键,B还形成1个配位键,B原子杂化轨道数目为4,B原子杂化方式为sp3杂化,中B原子杂化方式为sp2杂化,分子中,与原子相连的呈正电性,与原子相连的呈负电性,分子中三种元素电负性由大到小的顺序是 ,答案为:sp3,sp2,;
(6)由硼镁化合物的晶体结构可知位于正六棱柱的顶点和面心,由均摊法可以求出正六棱柱中含有个,由晶胞沿c轴的投影图可知本题所给晶体结构包含三个晶胞,则晶胞中Mg的个数为1;晶体结构中在正六棱柱体内共6个,则该物质的化学式为,答案为:。
24.AD BD d 、 吡咯能与水形成分子间氢键
【详解】(1)A.BCl3中B是采用sp2杂化,为平面三角形,是非极性分子;NCl3分子中N采用sp3杂化,为三角锥形,是极性分子,所以分子的极性:,A正确;
B.配位体给出电子能力越强,则配位体与中心离子形成的配位键就越强,配合物也就越稳定,O的给电子能力小于N,所以的配位键没有中的配位键稳定,B错误;
C.四氯化碳为非极性分子,易溶于非极性的二硫化碳中,水为极性分子,难溶于非极性的二硫化碳中,所以四氯化碳在中的溶解度大于水在中的溶解度,C错误;
D. Mn的价层电子排布式为3d54s2,有5个未成对电子,Si的价层电子排布式为3s23p2,有2个未成对电子,Cl价层电子排布式为3s23p5,有1个未成对电子,所以基态原子中未成对电子数:,D正确;
(2)A.①为简单堆积,配位数为6,②为体心立方堆积,配位数为8,A错误;
B.③为六方最密堆积,④为面心立方堆积,配位数均为12,B正确;
C.②中原子个数为,晶胞质量为2M,所以金属的密度为:,D.④为面心立方堆积,空间利用率为:=%,D正确;
(3)①铁的原子序数是26,位于第四周期第Ⅷ族,位于元素周期表中d区,根据核外电子排布规律可知铁的价层电子排布式为3d64s2,其电子排布图为,故本题答案为:d;;
②组成“摩尔盐”的非金属元素有H、N、O、S,其中电负性最大的元素为O,分解产物中三氧化硫是平面三角形结构,属于非极性分子,故本题答案为:O;SO3;
③等电子体是原子数相等,价电子数也相等的离子或分子,与CN-互为等电子体的单质的分子式为N2,分子的结构为H-C≡N,键和键的个数之比为1:1,故本题答案为:N2,;1:1;
④根据噻吩()的结构可知,噻吩中原子的杂化方式为,原子的杂化方式为。吡咯能与水形成分子间氢键,所以吡咯能溶于水,噻吩不能与水形成分子间氢键,所以噻吩难溶于水,故本题答案为:吡咯能与水形成分子间氢键;
同课章节目录
