2023-2024学年人教版高中化学必修一 2.3.1 物质的量 课件(共27张PPT)
文档属性
| 名称 | 2023-2024学年人教版高中化学必修一 2.3.1 物质的量 课件(共27张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-01 00:00:00 | ||
图片预览






文档简介
(共27张PPT)
第二章 第三节 物质的量
第一课时
古时候,有一位王子想娶美丽的公主,国王出题刁难,问了一个问题,10Kg大米是多少粒?
王子不慌不忙,先数出一两大米有多少粒,然后再换算出10Kg中有多少粒。国王很高兴,将公主嫁给了王子。
180g水中有多少个水分子?
水分子数: 16.7万亿亿个
一滴水含有多少个水分子呢?
怎样计量一定量的水中含有多少水分子呢?
10亿人去数,100个/分钟/人,
3万年才能数完。
估一估
体积: 大约 0.05ml
学习目标:
1.掌握物质的量、阿伏加德罗常数、摩尔质量的基本含义和应用。
2.能从宏观和微观相结合的视角认识物质的质量与物质的量之间的关系。
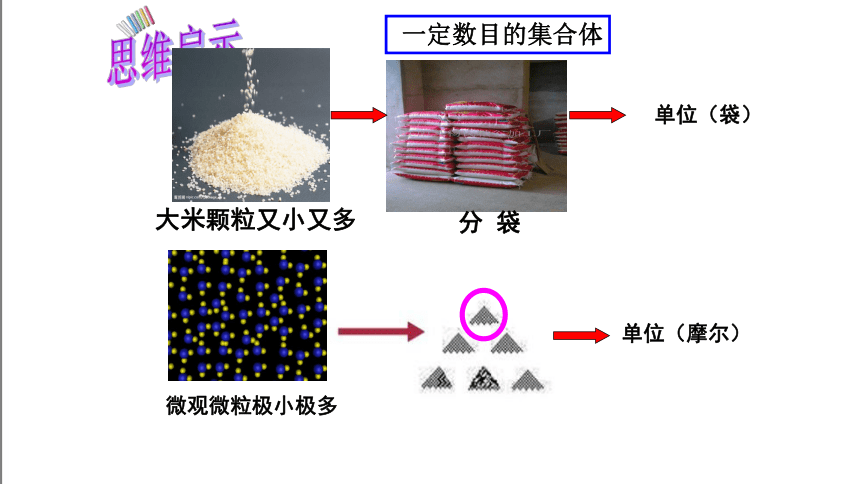
大米颗粒又小又多
分 袋
微观微粒极小极多
单位(袋)
单位(摩尔)
一定数目的集合体
思维启示
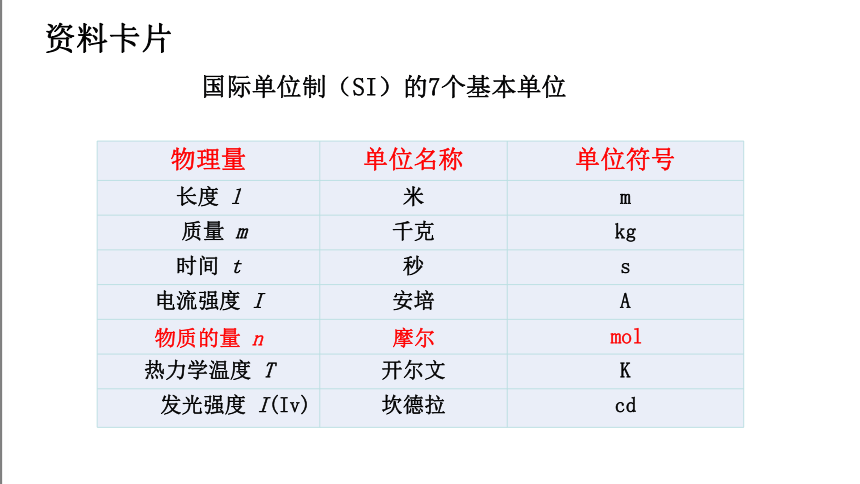
物理量 单位名称 单位符号
长度 l 米 m
质量 m 千克 kg
时间 t 秒 s
电流强度 I 安培 A
热力学温度 T 开尔文 K
发光强度 I(Iv) 坎德拉 cd
国际单位制(SI)的7个基本单位
物质的量 n
摩尔
mol
资料卡片
物质的量表示方式:1 mol H2SO4
数值 +
单位 +
符号
例如:
2 mol H2O、3 mol CO2、66 mol S、88 mol N2、
H2O的物质的量是2mol、CO2的物质的量是3mol。
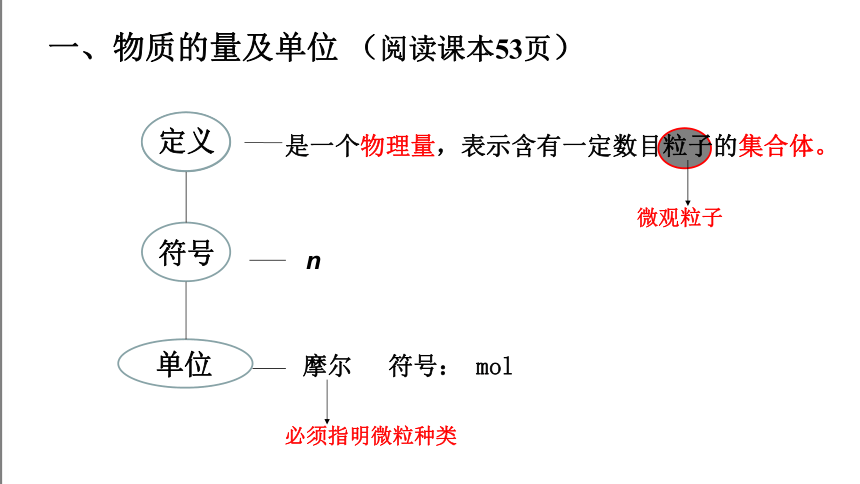
一、物质的量及单位 (阅读课本53页)
定义
是一个物理量,表示含有一定数目粒子的集合体。
符号
单位
摩尔 符号: mol
n
微观粒子
定义
必须指明微粒种类
学以致用
(1)物质的量就是物质的质量( )(2)摩尔是7个基本物理量之一( )
(3)1mol沙子( ) (4)1molH( )
(5)1mol氢( )
练习1.判断下列说法是否正确:
练习2.下列说法中不正确的是( )
A.物质的量就是物质的数量
B.摩尔是物质的量的单位
C.物质的量是以摩尔为单位计量微粒数目的物理量
D.物质的量是含有一定数目粒子的集体
×
×
×
×
√
A
1双筷子是2支,1 打鸡蛋是12个,1 箱啤酒是24听,那么,1 mol微观粒子是多少个呢?
1mol 粒子集合体所含粒子数约为6.02×1023
二、阿伏加德罗常数
1mol 任何粒子的粒子数
符号
定义
NA
约为6.02×1023 (近似值)
国际上规定:
单位
数值
mol-1
如果有 6.02×1023 粒大米让60亿人吃,每人每天吃1斤,可吃多少时间?
感受一下
14万年
巨大的数据
所以不能用mol作单位计量宏观物质。
粒子数 =
探究交流
粒子(H2O)(个) 物质的量(mol)
1 mol 水分子
2 mol 水分子
3 X 6.02×1023 水分子
1 X 6.02×1023
2 X 6.02×1023
3 mol
物质的量 X 6.02×1023
n
NA
·
N=
结论:
解:O2的分子数为
N(O2) = n × NA
【例1】在0.5 mol O2中含有的氧分子数目是多少?氧原子数目是多少?
N(O2) = 0.5 mol × 6.02×1023mol-1
N(O2) = 3.01 × 1023
氧原子数为
N(O) = 2 × N(O2)
N(O) = 2 × 3.01 × 1023
N(O) = 6.02×1023
物质的量
粒子数
NA
质 量
上图为课本第55页 图2-21 物质的量为1 mol的几种物质
思考:你发现了什么规律?
1mol任何粒子或物质的质量以克为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等。
三、摩尔质量(阅读课本55页)
1.定义:
4.数值:
2.符号:
3.常用单位:
单位物质的量的物质所具有的质量叫做摩尔质量。
g/mol(或 g·mol-1 )
M
摩尔质量以g·mol-1为单位时,数值等于其相对原子质量
或相对分子质量。
试试看:
2、Na2CO3的摩尔质量是 ,
1mol Na2CO3的质量是 。
106g/mol
106g
1、1mol H2的质量是 ;
1mol H2O的质量是 ;
1mol Cl2的质量是 ;
2g
18g
71g
问题探究
(1)1molO2的质量是多少?
(2)2molO2的质量是多少?
(3)n molO2的质量是多少?
1 mol× 32g/mol
2 mol× 32g/mol
nmol × 32g/mol
由以上可以得出物质的质量
与摩尔质量有什么关系?
【找规律】
m =n ×M
质量
物质的量
摩尔质量
m(Na2CO3)
n(Na2CO3)=
解: Na2CO3的相对分子质量为106,摩尔质量为 106g/mol。
M(Na2CO3)
26.5g
106g/mol
= 0.25mol
【典例示范】
例1.26.5gNa2CO3的物质的量是多少?
答:26.5gNa2CO3的物质的量是0.25mol。
=
我们学习了以下两个公式:
是否可以解决开始的那个问题,一杯水(180g)中有多少个水分子?
问题回归
180g水中有多少个水分子?
m(H2O)
n(H2O)=
解:M(H2O)=18g/mol
M(H2O)
180g
=
18g/mol
=10mol
N(H2O)=
=10mol×6.02×1023/mol
n(H2O)×NA
=6.02×1024
【学以致用】
180gH2O所含H2O分子的个数是多少?
答:180gH2O所含H2O分子的个数是6.02×1024 。
物质的量
宏观物质
微观粒子
课堂小结:
质量(m)
÷ NA
×NA
×M
÷ M
粒子数(N)
1.学案上的达标测试。
2.预习气体摩尔体积的相关内容。
作业:
第二章 第三节 物质的量
第一课时
古时候,有一位王子想娶美丽的公主,国王出题刁难,问了一个问题,10Kg大米是多少粒?
王子不慌不忙,先数出一两大米有多少粒,然后再换算出10Kg中有多少粒。国王很高兴,将公主嫁给了王子。
180g水中有多少个水分子?
水分子数: 16.7万亿亿个
一滴水含有多少个水分子呢?
怎样计量一定量的水中含有多少水分子呢?
10亿人去数,100个/分钟/人,
3万年才能数完。
估一估
体积: 大约 0.05ml
学习目标:
1.掌握物质的量、阿伏加德罗常数、摩尔质量的基本含义和应用。
2.能从宏观和微观相结合的视角认识物质的质量与物质的量之间的关系。
大米颗粒又小又多
分 袋
微观微粒极小极多
单位(袋)
单位(摩尔)
一定数目的集合体
思维启示
物理量 单位名称 单位符号
长度 l 米 m
质量 m 千克 kg
时间 t 秒 s
电流强度 I 安培 A
热力学温度 T 开尔文 K
发光强度 I(Iv) 坎德拉 cd
国际单位制(SI)的7个基本单位
物质的量 n
摩尔
mol
资料卡片
物质的量表示方式:1 mol H2SO4
数值 +
单位 +
符号
例如:
2 mol H2O、3 mol CO2、66 mol S、88 mol N2、
H2O的物质的量是2mol、CO2的物质的量是3mol。
一、物质的量及单位 (阅读课本53页)
定义
是一个物理量,表示含有一定数目粒子的集合体。
符号
单位
摩尔 符号: mol
n
微观粒子
定义
必须指明微粒种类
学以致用
(1)物质的量就是物质的质量( )(2)摩尔是7个基本物理量之一( )
(3)1mol沙子( ) (4)1molH( )
(5)1mol氢( )
练习1.判断下列说法是否正确:
练习2.下列说法中不正确的是( )
A.物质的量就是物质的数量
B.摩尔是物质的量的单位
C.物质的量是以摩尔为单位计量微粒数目的物理量
D.物质的量是含有一定数目粒子的集体
×
×
×
×
√
A
1双筷子是2支,1 打鸡蛋是12个,1 箱啤酒是24听,那么,1 mol微观粒子是多少个呢?
1mol 粒子集合体所含粒子数约为6.02×1023
二、阿伏加德罗常数
1mol 任何粒子的粒子数
符号
定义
NA
约为6.02×1023 (近似值)
国际上规定:
单位
数值
mol-1
如果有 6.02×1023 粒大米让60亿人吃,每人每天吃1斤,可吃多少时间?
感受一下
14万年
巨大的数据
所以不能用mol作单位计量宏观物质。
粒子数 =
探究交流
粒子(H2O)(个) 物质的量(mol)
1 mol 水分子
2 mol 水分子
3 X 6.02×1023 水分子
1 X 6.02×1023
2 X 6.02×1023
3 mol
物质的量 X 6.02×1023
n
NA
·
N=
结论:
解:O2的分子数为
N(O2) = n × NA
【例1】在0.5 mol O2中含有的氧分子数目是多少?氧原子数目是多少?
N(O2) = 0.5 mol × 6.02×1023mol-1
N(O2) = 3.01 × 1023
氧原子数为
N(O) = 2 × N(O2)
N(O) = 2 × 3.01 × 1023
N(O) = 6.02×1023
物质的量
粒子数
NA
质 量
上图为课本第55页 图2-21 物质的量为1 mol的几种物质
思考:你发现了什么规律?
1mol任何粒子或物质的质量以克为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等。
三、摩尔质量(阅读课本55页)
1.定义:
4.数值:
2.符号:
3.常用单位:
单位物质的量的物质所具有的质量叫做摩尔质量。
g/mol(或 g·mol-1 )
M
摩尔质量以g·mol-1为单位时,数值等于其相对原子质量
或相对分子质量。
试试看:
2、Na2CO3的摩尔质量是 ,
1mol Na2CO3的质量是 。
106g/mol
106g
1、1mol H2的质量是 ;
1mol H2O的质量是 ;
1mol Cl2的质量是 ;
2g
18g
71g
问题探究
(1)1molO2的质量是多少?
(2)2molO2的质量是多少?
(3)n molO2的质量是多少?
1 mol× 32g/mol
2 mol× 32g/mol
nmol × 32g/mol
由以上可以得出物质的质量
与摩尔质量有什么关系?
【找规律】
m =n ×M
质量
物质的量
摩尔质量
m(Na2CO3)
n(Na2CO3)=
解: Na2CO3的相对分子质量为106,摩尔质量为 106g/mol。
M(Na2CO3)
26.5g
106g/mol
= 0.25mol
【典例示范】
例1.26.5gNa2CO3的物质的量是多少?
答:26.5gNa2CO3的物质的量是0.25mol。
=
我们学习了以下两个公式:
是否可以解决开始的那个问题,一杯水(180g)中有多少个水分子?
问题回归
180g水中有多少个水分子?
m(H2O)
n(H2O)=
解:M(H2O)=18g/mol
M(H2O)
180g
=
18g/mol
=10mol
N(H2O)=
=10mol×6.02×1023/mol
n(H2O)×NA
=6.02×1024
【学以致用】
180gH2O所含H2O分子的个数是多少?
答:180gH2O所含H2O分子的个数是6.02×1024 。
物质的量
宏观物质
微观粒子
课堂小结:
质量(m)
÷ NA
×NA
×M
÷ M
粒子数(N)
1.学案上的达标测试。
2.预习气体摩尔体积的相关内容。
作业:
