3.3 第3课时 物质组成的定量表示 课件(共20张PPT) 2023-2024学年 鲁教版(五四制)八年级全册
文档属性
| 名称 | 3.3 第3课时 物质组成的定量表示 课件(共20张PPT) 2023-2024学年 鲁教版(五四制)八年级全册 |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-02 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
第三节 物质组成的表示
第3课时 物质组成的定量表示
*
水由什么构成的?
水有质量吗?
水分子有质量吗?
思考:
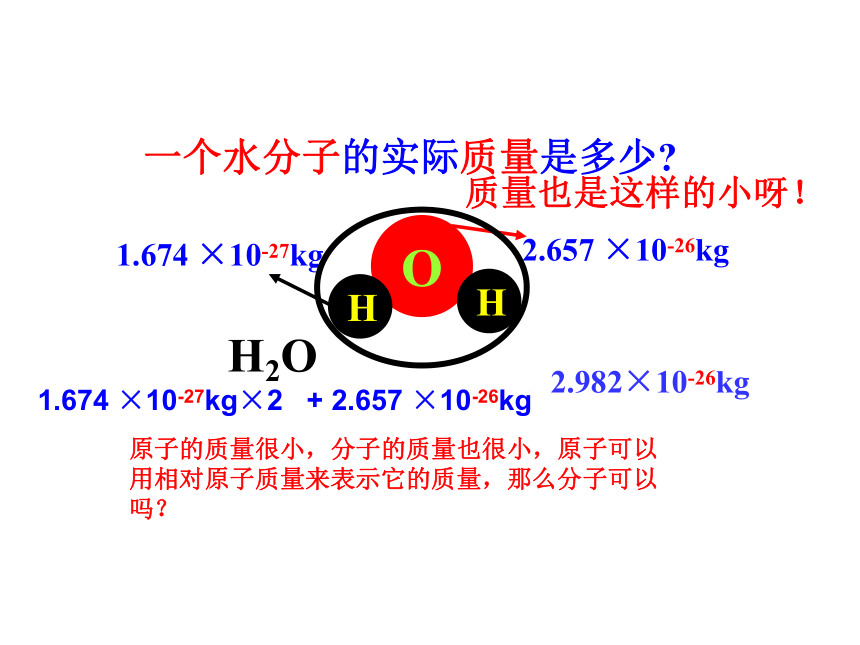
1.674 ×10-27kg
2.657 ×10-26kg
2.982×10-26kg
一个水分子的实际质量是多少
O
H
H
1.674 ×10-27kg×2 + 2.657 ×10-26kg
H2O
质量也是这样的小呀!
原子的质量很小,分子的质量也很小,原子可以用相对原子质量来表示它的质量,那么分子可以吗?
=
1、认识相对分子质量的含义。
2、理解元素质量比及元素质量分数。
3、掌握化学式的计算。
一、相对分子质量
课堂探讨1
1、概念:
化学式中各原子的相对原子质量的总和
2、注意事项:
( 1)相对分子质量的单位与相对原子质量的单位一样为1,一般不写出 (2)计算时所需的相对原子质量试卷中会提供,平时练习可以在课本查阅
3、计算方法与书写格式
讨论: 2N2 的相对分子质量如何计算?
(1)O2的化学式量= 16×2=32
(2)H2O的化学式量=1×2 + 16=18
注意:
①计算化学式量时元素符号右下角数字之间用“x”,元素符号之间用“+”。如:H2O的化学式量为1x2+16=18
②化学式中原子团右下角的数字表示其个数,计算时可先求出一个原子团的式量,再乘以其个数。如:Al(OH)3的化学式量为27+(16+1)x3=78
③结晶水合物中的“·”表示结合的含义,在计算结晶水合物的化学式量时应将“·”前后两部分的化学式量相加,而不能当作数学中的“乘”。
如:CuSO4·5H20的化学式量=64+32+16x4+5x(1x2+16)=250
*
练习:已知化合物R2O3 的相对分子质量(化学式量)是160,求 R的相对原子质量。
设R的相对原子质量为X
X×2+16×3=160
X=56
解:
答: R的相对原子质量为56
课堂探讨2
二、计算物质中组成元素的质量之比
1、公式:
元素的质量比=
“元素的相对原子质量×原子个数”的比
16
1
1
2、示例:计算下列物质中各元素的质量比:
CO2
CO(NH2)2
NH4NO3
C元素与O元素的质量比
H元素与N元素质量比
N元素与O元素质量比
=(1×12) ∶(16×2)
= 3 ∶8
=(1×4)∶(14×2)
= 1 ∶7
= (14 × 2)∶(16 × 3)
= 7 ∶12
1、同种元素的原子要合并计算2、要注意顺序:是谁比谁
*
物质的化学式量
该元素的相对原子质量
×
该元素的原子个数
1、公式 元素的质量分数
三、计算物质中某一元素的质量分数
=
×
100%
注意事项:
①质量分数——用百分数来表示
②意义
每100克物质中含有某元素的质量
课堂探讨3
2、示例:求硝酸铵(NH4NO3)中氮元素的质量分数3
X100%
X100%
=35%
四、化合物中元素的质量
1、公式:元素的质量=化合物的质量×元素的质量分数
2、示例:
80g硝酸铵(NH4NO3)氮元素的质量
硝酸铵(NH4NO3)中氮元素的质量分数
氮元素的质量= 80g × 35% = 28g
解:
14×2+1×4+16×3
× 100%
14×2
=35%
*
150千克的硝酸铵中有多少氮元素?
解 : 在NH4NO3中
=
14×2
14×2 + 1×4 + 16×3
×100%
=
28
80
×100%
= 35%
∴150千克的硝酸铵中含有的N元素的质量为
150千克×35% = 52.5 千克
答:150千克的硝酸铵中有52.5千克氮元素。
学以致用:
N的质量分数
氢元素和氧元素的质量比
水的化学式量(相对分子质量)
水中氢元素的质量分数
水中氧元素的质量分数
一个水分子中由两个氢原子和一个氧原子构成
一个水分子
水由氢元素和氧元素组成
水这种
物质
氢原子和氧原子的个数比
+1 -2
H O
定量
定性
知识点一:求相对分子质量
【典例1】下列相对分子质量计算正确的是( )
A.NO2的相对分子质量=14×16×2=448
B.2NH3的相对分子质量=2×14+1×3=31
C.O2的相对分子质量=16×2=32
D.Ca(OH)2的相对分子质量=40+(16+1)×2=74
√
知识点二:计算物质中组成元素的质量之比
【典例2】中成药莲花清瘟胶囊在防治新冠肺炎中作用显著,其主要成分之一的绿原酸的分子式为C16H18O9。下列有关说法不正确的是( )
A. 绿原酸由碳、氢、氧三种元素组成
B. 一个绿原酸分子中含有43个原子
C. 绿原酸分子中碳、氢原子个数之比为8:9
D. 绿原酸中碳、氧元素的质量之比为16:9
√
知识点三:计算物质中某一元素的质量分数
【典例3】生活中常使用消毒剂来杀菌、消毒。下列几种消毒液的有效成分(括号内物质)中,氧元素的质量分数最大的是( )
A.双氧水消毒液(H2O2)
B.“84"消毒液(NaClO)
C.酒精消毒液(C2H5OH)
D.过氧乙酸消毒液(C2H4O3)
√
1.甘油( )具有保湿作用。下列关于甘油的说法不正确的是( )
A. 由3种元素组成
B. 相对分子质量为( )
C. 碳、氢、氧3种原子的个数比为3:8:3
D. 碳元素的质量分数为
2.我国《新型冠状病毒感染的肺炎方案(试行第三版)》中提到可试用利托那韦进行抗病毒治疗,利托那韦的化学式为C37H48N6O5S2,下列关于利托那韦分子说法中正确的是( )
A.由5种元素组成的混合物
B.每个分子中含2个硫元素
C.氮、氧原子个数比为6:5
D.氢元素的质量分数最高
√
√
3.之前网上报道某公司非法使用草甘膦转基因大豆。草甘膦(化学式为C3H8NO5P)是一种有机磷除草剂,白色结晶,易溶于水、乙醇等,不可燃,常温下稳定。计算:
(1)草甘膦中碳元素与氧元素的质量比为_ 。
(2)草甘膦中磷元素的质量分数为 。(精确到0.1%)
(3)33.8克草甘膦中含有多少克磷元素?(写出计算步骤,精确到小数点后一位)
9:20
18.3%
解析:(1)分子中含3个碳原子和5个氧原子,草甘膦分子中碳元素与氧元素的质量比为
(2)所以磷元素的质量分数为
(3)33.8克草甘膦中含有磷元素的质量为
4.硅胶是常用的一种干燥剂。利用氯化钴含有不同数目的结晶水呈现不同颜色的性质,在制备硅胶时加入一些氯化钴得到变色硅胶。用CoCl2 xH2O表示含结晶水的氯化钴。试计算:
(1)若其中一种含结晶水的氯化钴的相对分子质量为238,则x= ,该结晶水合物中的氯、氧原子个数比为 ;
(2)若x=2,则氧元素的质量分数为 (计算结果精确到0.1%)。
6
1:3
19.3%
第三节 物质组成的表示
第3课时 物质组成的定量表示
*
水由什么构成的?
水有质量吗?
水分子有质量吗?
思考:
1.674 ×10-27kg
2.657 ×10-26kg
2.982×10-26kg
一个水分子的实际质量是多少
O
H
H
1.674 ×10-27kg×2 + 2.657 ×10-26kg
H2O
质量也是这样的小呀!
原子的质量很小,分子的质量也很小,原子可以用相对原子质量来表示它的质量,那么分子可以吗?
=
1、认识相对分子质量的含义。
2、理解元素质量比及元素质量分数。
3、掌握化学式的计算。
一、相对分子质量
课堂探讨1
1、概念:
化学式中各原子的相对原子质量的总和
2、注意事项:
( 1)相对分子质量的单位与相对原子质量的单位一样为1,一般不写出 (2)计算时所需的相对原子质量试卷中会提供,平时练习可以在课本查阅
3、计算方法与书写格式
讨论: 2N2 的相对分子质量如何计算?
(1)O2的化学式量= 16×2=32
(2)H2O的化学式量=1×2 + 16=18
注意:
①计算化学式量时元素符号右下角数字之间用“x”,元素符号之间用“+”。如:H2O的化学式量为1x2+16=18
②化学式中原子团右下角的数字表示其个数,计算时可先求出一个原子团的式量,再乘以其个数。如:Al(OH)3的化学式量为27+(16+1)x3=78
③结晶水合物中的“·”表示结合的含义,在计算结晶水合物的化学式量时应将“·”前后两部分的化学式量相加,而不能当作数学中的“乘”。
如:CuSO4·5H20的化学式量=64+32+16x4+5x(1x2+16)=250
*
练习:已知化合物R2O3 的相对分子质量(化学式量)是160,求 R的相对原子质量。
设R的相对原子质量为X
X×2+16×3=160
X=56
解:
答: R的相对原子质量为56
课堂探讨2
二、计算物质中组成元素的质量之比
1、公式:
元素的质量比=
“元素的相对原子质量×原子个数”的比
16
1
1
2、示例:计算下列物质中各元素的质量比:
CO2
CO(NH2)2
NH4NO3
C元素与O元素的质量比
H元素与N元素质量比
N元素与O元素质量比
=(1×12) ∶(16×2)
= 3 ∶8
=(1×4)∶(14×2)
= 1 ∶7
= (14 × 2)∶(16 × 3)
= 7 ∶12
1、同种元素的原子要合并计算2、要注意顺序:是谁比谁
*
物质的化学式量
该元素的相对原子质量
×
该元素的原子个数
1、公式 元素的质量分数
三、计算物质中某一元素的质量分数
=
×
100%
注意事项:
①质量分数——用百分数来表示
②意义
每100克物质中含有某元素的质量
课堂探讨3
2、示例:求硝酸铵(NH4NO3)中氮元素的质量分数3
X100%
X100%
=35%
四、化合物中元素的质量
1、公式:元素的质量=化合物的质量×元素的质量分数
2、示例:
80g硝酸铵(NH4NO3)氮元素的质量
硝酸铵(NH4NO3)中氮元素的质量分数
氮元素的质量= 80g × 35% = 28g
解:
14×2+1×4+16×3
× 100%
14×2
=35%
*
150千克的硝酸铵中有多少氮元素?
解 : 在NH4NO3中
=
14×2
14×2 + 1×4 + 16×3
×100%
=
28
80
×100%
= 35%
∴150千克的硝酸铵中含有的N元素的质量为
150千克×35% = 52.5 千克
答:150千克的硝酸铵中有52.5千克氮元素。
学以致用:
N的质量分数
氢元素和氧元素的质量比
水的化学式量(相对分子质量)
水中氢元素的质量分数
水中氧元素的质量分数
一个水分子中由两个氢原子和一个氧原子构成
一个水分子
水由氢元素和氧元素组成
水这种
物质
氢原子和氧原子的个数比
+1 -2
H O
定量
定性
知识点一:求相对分子质量
【典例1】下列相对分子质量计算正确的是( )
A.NO2的相对分子质量=14×16×2=448
B.2NH3的相对分子质量=2×14+1×3=31
C.O2的相对分子质量=16×2=32
D.Ca(OH)2的相对分子质量=40+(16+1)×2=74
√
知识点二:计算物质中组成元素的质量之比
【典例2】中成药莲花清瘟胶囊在防治新冠肺炎中作用显著,其主要成分之一的绿原酸的分子式为C16H18O9。下列有关说法不正确的是( )
A. 绿原酸由碳、氢、氧三种元素组成
B. 一个绿原酸分子中含有43个原子
C. 绿原酸分子中碳、氢原子个数之比为8:9
D. 绿原酸中碳、氧元素的质量之比为16:9
√
知识点三:计算物质中某一元素的质量分数
【典例3】生活中常使用消毒剂来杀菌、消毒。下列几种消毒液的有效成分(括号内物质)中,氧元素的质量分数最大的是( )
A.双氧水消毒液(H2O2)
B.“84"消毒液(NaClO)
C.酒精消毒液(C2H5OH)
D.过氧乙酸消毒液(C2H4O3)
√
1.甘油( )具有保湿作用。下列关于甘油的说法不正确的是( )
A. 由3种元素组成
B. 相对分子质量为( )
C. 碳、氢、氧3种原子的个数比为3:8:3
D. 碳元素的质量分数为
2.我国《新型冠状病毒感染的肺炎方案(试行第三版)》中提到可试用利托那韦进行抗病毒治疗,利托那韦的化学式为C37H48N6O5S2,下列关于利托那韦分子说法中正确的是( )
A.由5种元素组成的混合物
B.每个分子中含2个硫元素
C.氮、氧原子个数比为6:5
D.氢元素的质量分数最高
√
√
3.之前网上报道某公司非法使用草甘膦转基因大豆。草甘膦(化学式为C3H8NO5P)是一种有机磷除草剂,白色结晶,易溶于水、乙醇等,不可燃,常温下稳定。计算:
(1)草甘膦中碳元素与氧元素的质量比为_ 。
(2)草甘膦中磷元素的质量分数为 。(精确到0.1%)
(3)33.8克草甘膦中含有多少克磷元素?(写出计算步骤,精确到小数点后一位)
9:20
18.3%
解析:(1)分子中含3个碳原子和5个氧原子,草甘膦分子中碳元素与氧元素的质量比为
(2)所以磷元素的质量分数为
(3)33.8克草甘膦中含有磷元素的质量为
4.硅胶是常用的一种干燥剂。利用氯化钴含有不同数目的结晶水呈现不同颜色的性质,在制备硅胶时加入一些氯化钴得到变色硅胶。用CoCl2 xH2O表示含结晶水的氯化钴。试计算:
(1)若其中一种含结晶水的氯化钴的相对分子质量为238,则x= ,该结晶水合物中的氯、氧原子个数比为 ;
(2)若x=2,则氧元素的质量分数为 (计算结果精确到0.1%)。
6
1:3
19.3%
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
