2.1.1 活泼的金属单质——钠 课件(共21张PPT)
文档属性
| 名称 | 2.1.1 活泼的金属单质——钠 课件(共21张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-01 00:00:00 | ||
图片预览





文档简介
(共21张PPT)
第1节 钠及其化合物
第二章 海水中的重要元素
——钠和氯
第1课时
活泼的金属单质--钠
导入
海洋是一个巨大的化学资源宝库,含有80多种元素。
钠是其中含量较高的元素,也是典型的金属元素。
钠元素在自然界中都以化合物的形式存在,
钠的单质可以通过化学反应制得。
1.了解钠的主要性质,书写有关的化学方程式
2.以金属钠的学习为例逐步形成金属的研究思路和证据推理意识,培养求实、创新的良好品质
3.通过学习钠在生活中的应用,感受化学的魅力,发展社会参与意识
学习目标:
重点:钠与水的反应
难点:钠与水反应的探究实验
性质预测
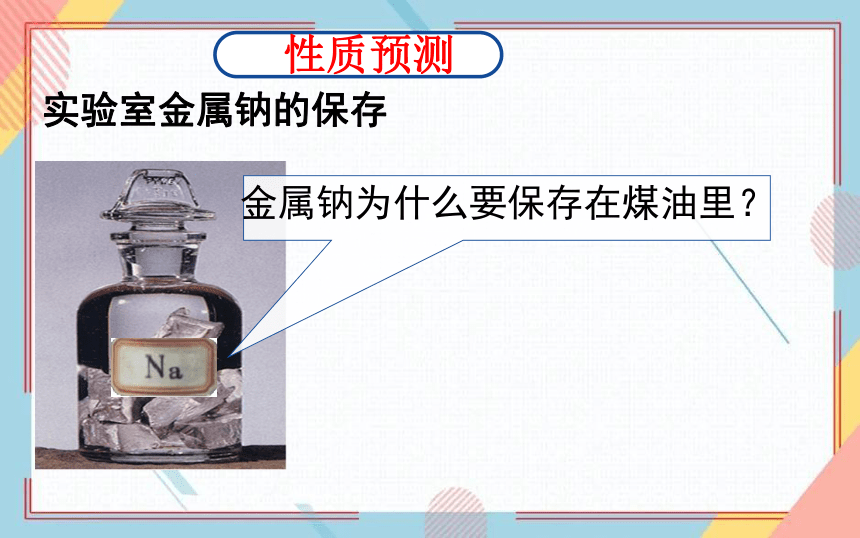
金属钠为什么要保存在煤油里?
实验室金属钠的保存
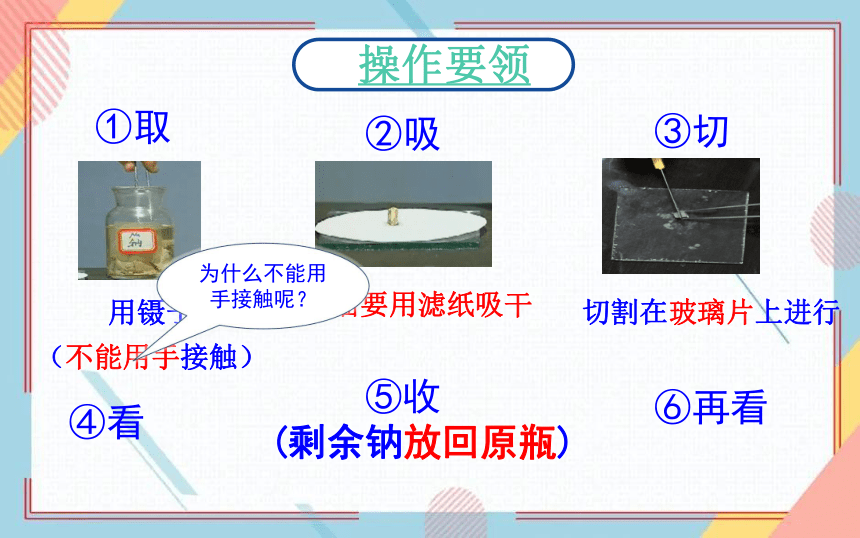
①取
②吸
③切
④看
⑤收 (剩余钠放回原瓶)
⑥再看
操作要领
煤油要用滤纸吸干
用镊子
(不能用手接触)
切割在玻璃片上进行
为什么不能用手接触呢?
新切开的钠的光亮的表面很快变暗了,因为:
4Na + O2 —— 2Na2O
0
0
+1
-2
1、钠和氧气反应(常温)
钠的化学性质
上面反应说明钠的化学性质十分活泼,所以保存时要隔绝空气,用煤油封存。
为什么保存
在石蜡油?
如果将钠加热,又会发生什么变化呢?
2、钠和氧气反应(加热)
钠的化学性质
[实验2-2]将一个干燥的坩埚加热,同时切取一块绿豆大的钠,迅速投到热坩埚中。继续加热坩埚片刻,待钠熔化后立即撤掉酒精灯,观察现象。
钠受热后先熔化与氧气剧烈反应,发出黄色火焰,生成一种淡黄色固体:
0
0
+1
-1
2Na + O2 —— Na2O2 (淡黄色)
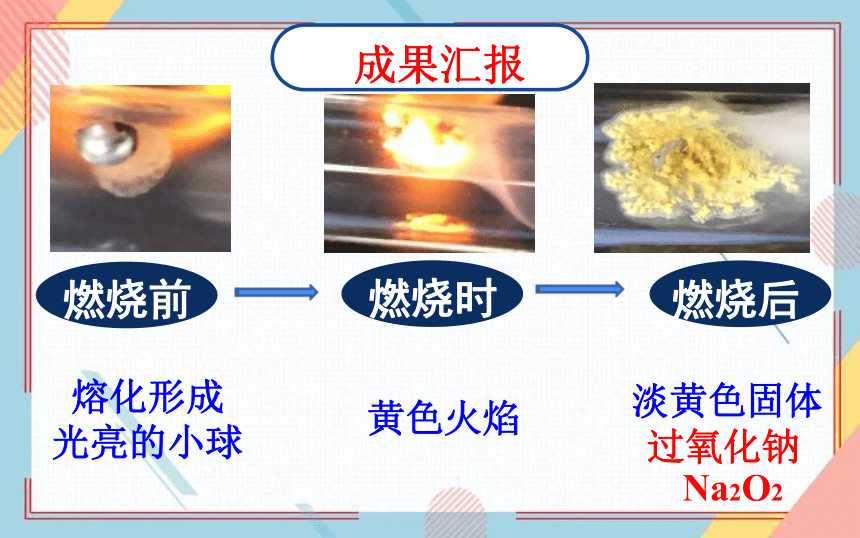
现象:
淡黄色固体
过氧化钠
Na2O2
燃烧前
熔化形成
光亮的小球
燃烧时
黄色火焰
燃烧后
成果汇报
(1)在氯气中燃烧:
现象:燃烧、产生白色的烟
(2)与硫反应:
现象:火星四射、发生爆炸
点燃
钠的化学性质
3、钠和其他非金属的反应
2Na + S —— Na2S
点燃
2Na + Cl2 —— 2NaCl
观察要点
1.钠是浮在水面上,还是沉于水底?
2.钠变成什么形状?
3.钠在水中是运动还是静止?
4.有无声响?
5.溶液颜色的变化?
①加半杯水
②加2滴酚酞
③加钠(绿豆大小)
实验探究二 金属钠与水反应
浮在水面上
熔化成小球
四处游动
发出“嘶嘶”响声
溶液变红色
1
2
3
浮
熔
游
响
红
成果汇报
小组交流
浮
熔
游
响
红
钠与水
有气体产生,反应剧烈
钠密度比水小
有碱性物质生成
反应放热、熔点低
思考1:生成的碱性物质是什么?
NaOH
实验现象 分析结论
金属钠浮在水面
密度比水小
熔成光亮的小球
反应放热,钠熔点小
四处游动
反应产生了气体
发出“嘶嘶”响声
反应产生了气体
溶液变红
生成碱性物质
你能推测金属钠与水反应产生的气体是哪种气体吗?
推理验证
Na + H2O NaOH +
0
+1
元素化合价升高
+1
-2
元素化合价降低
H2↑
→
===
2
2
2
可能是H2,
也可能是O2
1.钠为什么要保存在煤油中?
2.为什么取用钠时要用镊子而不能用手呢?
防止钠与手上汗液接触发生化学反应,使手受到灼伤或腐蚀。
钠不与煤油反应,且密度大于煤油,可沉在试剂瓶底部,可以隔绝空气。
理论联系实际
3.火灾现场有大量金属钠存在时,是否能用水灭火?
金属钠与水反应剧烈,且为放热反应,放出可燃性气体氢气。故不能用水灭火,应用干燥的沙土盖灭。
结论:钠与酸的反应比和水反应更剧烈。钠和水反应,实质上是跟水电离的H+反应。而酸中的H+浓度更大。
2Na + 2H+ —— H2↑+ 2Na+
5、钠和酸溶液反应
钠的化学性质
6、钠和盐溶液反应
结论:钠投入硫酸铜溶液时,金属钠会在水面上下浮动,极速游动变小,最终会有蓝色絮状物产生。
步骤1:2Na+2H2O=2NaOH+H2↑(先与水反应)
步骤2:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4(NaOH再与CuSO4反应)
不是置换
实验现象
决定
决定
很剧烈
钠的性质
强还原性,很活泼
反映
钠的结构
Na
Na+
失去最外层电子,化合价升高
反映
为什么钠具有强还原性?
溯本求源
预测性质
设计方案
实验探究
得出结论
宏微结合
绿色环保
证据推理
创新意识
研究物质性质的一般程序
金属钠的性质
质软可切割,硬度比较小,银白色,具有金属光泽固体
电和热的良导体,密度比水小0.97g/cm3
熔点低97.81℃,沸点882.9℃纳保存在煤油中
课堂小结
物理性质
与非金属的反应
化学性质
与氧气反应 4Na + O2 —— 2Na2O
2Na + O2 —— Na2O2
与氯气反应 2Na + Cl2 —— 2NaCl
与硫反应 2Na + S —— Na2S
点燃
与水的反应
2Na + 2H2O —— 2NaOH + H2↑
与酸、盐反应
1、以下说法错误的是( )
A、钠在常温下就容易被氧化 B、钠受热后能够着火燃烧
C、钠在空气中缓慢氧化能自燃 D、钠在氧气中燃烧更为剧烈
2、将一小块金属钠放在硬质玻璃管里加热:
①钠在燃烧前先熔化 ②燃烧后得到白色固体
③燃烧时火焰呈黄色 ④燃烧后生成淡黄色固体。
以上有关实验现象的描述正确的是:( )
A、③④ B、只有① C、①③④ D、①④
C
C
课堂练习
课堂练习
3.下列关于钠与水反应现象的描述,正确的组合是:( )
①钠浮在水面上 ②钠沉在水底下 ③立即熔化成银色的闪亮小球 ④ 小球迅速游动,逐渐减小,最后完全消失
⑤小球固定在水面某处不动,慢慢减小,直至消失
⑥发出嘶嘶的响声 ⑦反应后滴入酚酞试液显红色
⑧反应后滴入石蕊试液显红色
A、①②③④⑤⑥⑦⑧ B、①③④⑥⑦
C、②③④⑥⑦ D、③④⑤⑥⑦⑧
B
第1节 钠及其化合物
第二章 海水中的重要元素
——钠和氯
第1课时
活泼的金属单质--钠
导入
海洋是一个巨大的化学资源宝库,含有80多种元素。
钠是其中含量较高的元素,也是典型的金属元素。
钠元素在自然界中都以化合物的形式存在,
钠的单质可以通过化学反应制得。
1.了解钠的主要性质,书写有关的化学方程式
2.以金属钠的学习为例逐步形成金属的研究思路和证据推理意识,培养求实、创新的良好品质
3.通过学习钠在生活中的应用,感受化学的魅力,发展社会参与意识
学习目标:
重点:钠与水的反应
难点:钠与水反应的探究实验
性质预测
金属钠为什么要保存在煤油里?
实验室金属钠的保存
①取
②吸
③切
④看
⑤收 (剩余钠放回原瓶)
⑥再看
操作要领
煤油要用滤纸吸干
用镊子
(不能用手接触)
切割在玻璃片上进行
为什么不能用手接触呢?
新切开的钠的光亮的表面很快变暗了,因为:
4Na + O2 —— 2Na2O
0
0
+1
-2
1、钠和氧气反应(常温)
钠的化学性质
上面反应说明钠的化学性质十分活泼,所以保存时要隔绝空气,用煤油封存。
为什么保存
在石蜡油?
如果将钠加热,又会发生什么变化呢?
2、钠和氧气反应(加热)
钠的化学性质
[实验2-2]将一个干燥的坩埚加热,同时切取一块绿豆大的钠,迅速投到热坩埚中。继续加热坩埚片刻,待钠熔化后立即撤掉酒精灯,观察现象。
钠受热后先熔化与氧气剧烈反应,发出黄色火焰,生成一种淡黄色固体:
0
0
+1
-1
2Na + O2 —— Na2O2 (淡黄色)
现象:
淡黄色固体
过氧化钠
Na2O2
燃烧前
熔化形成
光亮的小球
燃烧时
黄色火焰
燃烧后
成果汇报
(1)在氯气中燃烧:
现象:燃烧、产生白色的烟
(2)与硫反应:
现象:火星四射、发生爆炸
点燃
钠的化学性质
3、钠和其他非金属的反应
2Na + S —— Na2S
点燃
2Na + Cl2 —— 2NaCl
观察要点
1.钠是浮在水面上,还是沉于水底?
2.钠变成什么形状?
3.钠在水中是运动还是静止?
4.有无声响?
5.溶液颜色的变化?
①加半杯水
②加2滴酚酞
③加钠(绿豆大小)
实验探究二 金属钠与水反应
浮在水面上
熔化成小球
四处游动
发出“嘶嘶”响声
溶液变红色
1
2
3
浮
熔
游
响
红
成果汇报
小组交流
浮
熔
游
响
红
钠与水
有气体产生,反应剧烈
钠密度比水小
有碱性物质生成
反应放热、熔点低
思考1:生成的碱性物质是什么?
NaOH
实验现象 分析结论
金属钠浮在水面
密度比水小
熔成光亮的小球
反应放热,钠熔点小
四处游动
反应产生了气体
发出“嘶嘶”响声
反应产生了气体
溶液变红
生成碱性物质
你能推测金属钠与水反应产生的气体是哪种气体吗?
推理验证
Na + H2O NaOH +
0
+1
元素化合价升高
+1
-2
元素化合价降低
H2↑
→
===
2
2
2
可能是H2,
也可能是O2
1.钠为什么要保存在煤油中?
2.为什么取用钠时要用镊子而不能用手呢?
防止钠与手上汗液接触发生化学反应,使手受到灼伤或腐蚀。
钠不与煤油反应,且密度大于煤油,可沉在试剂瓶底部,可以隔绝空气。
理论联系实际
3.火灾现场有大量金属钠存在时,是否能用水灭火?
金属钠与水反应剧烈,且为放热反应,放出可燃性气体氢气。故不能用水灭火,应用干燥的沙土盖灭。
结论:钠与酸的反应比和水反应更剧烈。钠和水反应,实质上是跟水电离的H+反应。而酸中的H+浓度更大。
2Na + 2H+ —— H2↑+ 2Na+
5、钠和酸溶液反应
钠的化学性质
6、钠和盐溶液反应
结论:钠投入硫酸铜溶液时,金属钠会在水面上下浮动,极速游动变小,最终会有蓝色絮状物产生。
步骤1:2Na+2H2O=2NaOH+H2↑(先与水反应)
步骤2:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4(NaOH再与CuSO4反应)
不是置换
实验现象
决定
决定
很剧烈
钠的性质
强还原性,很活泼
反映
钠的结构
Na
Na+
失去最外层电子,化合价升高
反映
为什么钠具有强还原性?
溯本求源
预测性质
设计方案
实验探究
得出结论
宏微结合
绿色环保
证据推理
创新意识
研究物质性质的一般程序
金属钠的性质
质软可切割,硬度比较小,银白色,具有金属光泽固体
电和热的良导体,密度比水小0.97g/cm3
熔点低97.81℃,沸点882.9℃纳保存在煤油中
课堂小结
物理性质
与非金属的反应
化学性质
与氧气反应 4Na + O2 —— 2Na2O
2Na + O2 —— Na2O2
与氯气反应 2Na + Cl2 —— 2NaCl
与硫反应 2Na + S —— Na2S
点燃
与水的反应
2Na + 2H2O —— 2NaOH + H2↑
与酸、盐反应
1、以下说法错误的是( )
A、钠在常温下就容易被氧化 B、钠受热后能够着火燃烧
C、钠在空气中缓慢氧化能自燃 D、钠在氧气中燃烧更为剧烈
2、将一小块金属钠放在硬质玻璃管里加热:
①钠在燃烧前先熔化 ②燃烧后得到白色固体
③燃烧时火焰呈黄色 ④燃烧后生成淡黄色固体。
以上有关实验现象的描述正确的是:( )
A、③④ B、只有① C、①③④ D、①④
C
C
课堂练习
课堂练习
3.下列关于钠与水反应现象的描述,正确的组合是:( )
①钠浮在水面上 ②钠沉在水底下 ③立即熔化成银色的闪亮小球 ④ 小球迅速游动,逐渐减小,最后完全消失
⑤小球固定在水面某处不动,慢慢减小,直至消失
⑥发出嘶嘶的响声 ⑦反应后滴入酚酞试液显红色
⑧反应后滴入石蕊试液显红色
A、①②③④⑤⑥⑦⑧ B、①③④⑥⑦
C、②③④⑥⑦ D、③④⑤⑥⑦⑧
B
