2.2.1 氯气的性质 课件(共17张PPT)
文档属性
| 名称 | 2.2.1 氯气的性质 课件(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 54.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-01 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
1915年4月20日,第一次世界大战的伊普雷战役中,德国5分钟释放了180吨氯气,使15000人中毒,致使其中5000多人死亡。
必修第一册
第二章 海水中的重要元素——钠和氯
第二节 氯及其化合物
第1课时 氯气的性质
PART
01
PART
02
PART
03
能从原子结构的角度认识氯元素是一种很活泼的非金属元素,其单质具有强氧化性
核心素养发展目标
通过实验探究氯气与金属单质、非金属单质反应,
促进“科学探究”化学核心素养的发展。
掌握氯气的物理性质和化学性质
18世纪70年代,瑞典化学家舍勒(C.W.Scheele,1742----1786) 将软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。受当时流行学说的影响,舍勒未能确认这种气体。
氯气的发现和确认
舍勒 (1742~1786)
瑞典化学家
直到1810年,英国化学家戴维( S.H.Davy,1778----1829)才确认这种气体是一种新元素组成的单质----氯气。
戴维(1778~1829)美国化学家
新华网报道:2005年3月29日,京沪高速公路淮安段一辆满载液氯的液罐车和对面来车相撞 ,大量液氯外泄。据目击者描述 : ”一股黄绿色的气体就像探照灯,光一样,‘唰’地射向高空,足有5米高,并有刺鼻的味道,眼睛也熏得有些睁不开 。”
事发后消防队员不断地用水枪喷射,但时值西南风,氯气迅速向西南方扩散 ,造成350 人中毒进医院救治, 另有28人中毒死亡的特大事故,附近居民采取应急措施,疏散到一高坡上。
导入新课
氯气的有哪些物理性质呢?
二、氯气的物理性质
通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。
实验操作
实验室闻气体的方法
氯气既然有毒,那我们如何闻氯气的气味?
在瓶口轻轻扇动,
方法:一扇
三闻
二飘
使极少量气体飘入鼻孔,
仔细辨别气味。
小结:实验室无论闻什么物质的气味都是采用这个方法。
结构决定性质
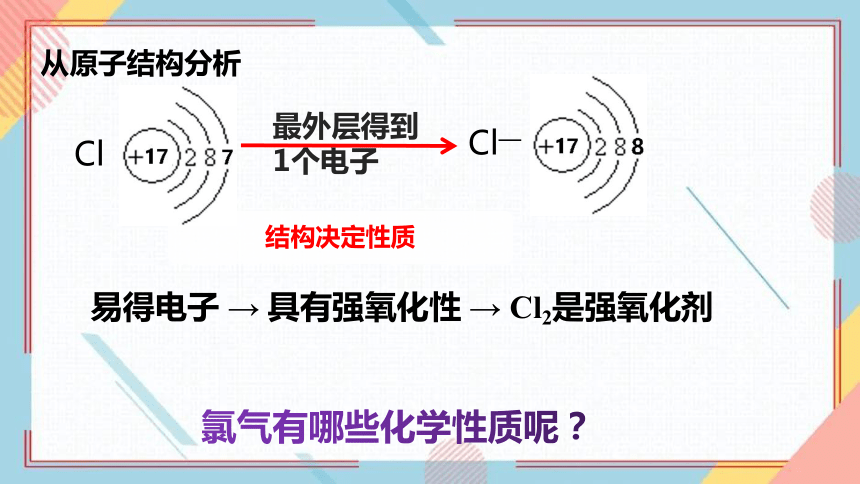
从原子结构分析
易得电子 → 具有强氧化性 → Cl2是强氧化剂
Cl
最外层得到
1个电子
Cl—
氯气有哪些化学性质呢?
二、氯气的化学性质
[实验] 钠、铁、铜在氯气中燃烧,观察实验现象
实验现象 反应方程式
钠
铁
铜
剧烈燃烧,产生大量白烟
结论:氯气的氧化性很强,与变价金属反应时,通常将其氧化为高价态。
剧烈燃烧,产生大量棕褐色烟,溶于水后形成黄色溶液
剧烈燃烧,产生大量棕黄色烟,溶于水后形成蓝绿色溶液
二、氯气的化学性质
1. 与金属单质反应:
Cu + Cl2 CuCl2
Δ
2Na + Cl2 2NaCl
Δ
2Fe+ 3Cl2 2FeCl3
Δ
[实验2-7]
在空气中点燃氢气,然后把导管缓慢伸入盛满氯气的集气瓶中,观察实验现象。
氢气在氯气中点燃
现象
方程式
用途
工业上制盐酸
H2 + Cl2 2HCl
安静地燃烧,发出苍白色火焰,集气瓶口有白雾
2.与非金属单质反应
解析:产物HCl在空气中与水蒸气结合,呈现雾状,所以瓶口有白雾。
思考:白雾是怎么形成的?
Cl2与H2混合,光照射发生爆炸
注意:
【思考与讨论】
我们以前学过的燃烧反应,都是物质在氧气中的燃烧。通过H2在Cl2中的燃烧,你对燃烧的条件及其本质有什么新的认识
燃烧不一定要有氧气参加,物质并不是只有在氧气中才可以燃烧。燃烧的本质是氧化还原反应。
燃烧的定义:任何发光发热的剧烈的化学反应。
燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。
燃烧的本质是氧化还原反应,所有发光发热的剧烈的化学反应都称为燃烧。
定义:任何发光发热的剧烈的化学反应叫燃烧。
通过H2在Cl2中的燃烧的实验,你对燃烧的条件及其本质有什么新的认识?
1、不能用金属跟氯气直接反应制得的氯化物的是( )
A.NaCl B.MgCl2
C.CuCl2 D.FeCl2
D
小试牛刀
2.下列对Cl2的性质叙述不正确的是( )
A.黄绿色 B.不溶于水
C.有毒 D.不支持燃烧
3.下列关于对燃烧现象的认识中,不正确的是( )
A.燃烧一定是氧化还原反应 B.燃烧一定发光放热
C.燃烧一定是化学反应 D.燃烧一定有氧气参与
小试牛刀
BD
D
燃烧:任何发光发热的剧烈的化学反应
课堂小结
一、氯气的物理性质
黄绿色有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水
二、氯气的化学性质
1. 与金属单质反应:
氯气的氧化性很强,与变价金属反应时,通常将其氧化为高价态。
2.与非金属单质反应
1915年4月20日,第一次世界大战的伊普雷战役中,德国5分钟释放了180吨氯气,使15000人中毒,致使其中5000多人死亡。
必修第一册
第二章 海水中的重要元素——钠和氯
第二节 氯及其化合物
第1课时 氯气的性质
PART
01
PART
02
PART
03
能从原子结构的角度认识氯元素是一种很活泼的非金属元素,其单质具有强氧化性
核心素养发展目标
通过实验探究氯气与金属单质、非金属单质反应,
促进“科学探究”化学核心素养的发展。
掌握氯气的物理性质和化学性质
18世纪70年代,瑞典化学家舍勒(C.W.Scheele,1742----1786) 将软锰矿(主要成分是MnO2)与浓盐酸混合加热,产生了一种黄绿色、有刺激性气味的气体。受当时流行学说的影响,舍勒未能确认这种气体。
氯气的发现和确认
舍勒 (1742~1786)
瑞典化学家
直到1810年,英国化学家戴维( S.H.Davy,1778----1829)才确认这种气体是一种新元素组成的单质----氯气。
戴维(1778~1829)美国化学家
新华网报道:2005年3月29日,京沪高速公路淮安段一辆满载液氯的液罐车和对面来车相撞 ,大量液氯外泄。据目击者描述 : ”一股黄绿色的气体就像探照灯,光一样,‘唰’地射向高空,足有5米高,并有刺鼻的味道,眼睛也熏得有些睁不开 。”
事发后消防队员不断地用水枪喷射,但时值西南风,氯气迅速向西南方扩散 ,造成350 人中毒进医院救治, 另有28人中毒死亡的特大事故,附近居民采取应急措施,疏散到一高坡上。
导入新课
氯气的有哪些物理性质呢?
二、氯气的物理性质
通常状况下,氯气呈黄绿色,有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水(1:2)。
实验操作
实验室闻气体的方法
氯气既然有毒,那我们如何闻氯气的气味?
在瓶口轻轻扇动,
方法:一扇
三闻
二飘
使极少量气体飘入鼻孔,
仔细辨别气味。
小结:实验室无论闻什么物质的气味都是采用这个方法。
结构决定性质
从原子结构分析
易得电子 → 具有强氧化性 → Cl2是强氧化剂
Cl
最外层得到
1个电子
Cl—
氯气有哪些化学性质呢?
二、氯气的化学性质
[实验] 钠、铁、铜在氯气中燃烧,观察实验现象
实验现象 反应方程式
钠
铁
铜
剧烈燃烧,产生大量白烟
结论:氯气的氧化性很强,与变价金属反应时,通常将其氧化为高价态。
剧烈燃烧,产生大量棕褐色烟,溶于水后形成黄色溶液
剧烈燃烧,产生大量棕黄色烟,溶于水后形成蓝绿色溶液
二、氯气的化学性质
1. 与金属单质反应:
Cu + Cl2 CuCl2
Δ
2Na + Cl2 2NaCl
Δ
2Fe+ 3Cl2 2FeCl3
Δ
[实验2-7]
在空气中点燃氢气,然后把导管缓慢伸入盛满氯气的集气瓶中,观察实验现象。
氢气在氯气中点燃
现象
方程式
用途
工业上制盐酸
H2 + Cl2 2HCl
安静地燃烧,发出苍白色火焰,集气瓶口有白雾
2.与非金属单质反应
解析:产物HCl在空气中与水蒸气结合,呈现雾状,所以瓶口有白雾。
思考:白雾是怎么形成的?
Cl2与H2混合,光照射发生爆炸
注意:
【思考与讨论】
我们以前学过的燃烧反应,都是物质在氧气中的燃烧。通过H2在Cl2中的燃烧,你对燃烧的条件及其本质有什么新的认识
燃烧不一定要有氧气参加,物质并不是只有在氧气中才可以燃烧。燃烧的本质是氧化还原反应。
燃烧的定义:任何发光发热的剧烈的化学反应。
燃烧不一定有氧气参加,物质并不是只有在氧气中才可以燃烧。
燃烧的本质是氧化还原反应,所有发光发热的剧烈的化学反应都称为燃烧。
定义:任何发光发热的剧烈的化学反应叫燃烧。
通过H2在Cl2中的燃烧的实验,你对燃烧的条件及其本质有什么新的认识?
1、不能用金属跟氯气直接反应制得的氯化物的是( )
A.NaCl B.MgCl2
C.CuCl2 D.FeCl2
D
小试牛刀
2.下列对Cl2的性质叙述不正确的是( )
A.黄绿色 B.不溶于水
C.有毒 D.不支持燃烧
3.下列关于对燃烧现象的认识中,不正确的是( )
A.燃烧一定是氧化还原反应 B.燃烧一定发光放热
C.燃烧一定是化学反应 D.燃烧一定有氧气参与
小试牛刀
BD
D
燃烧:任何发光发热的剧烈的化学反应
课堂小结
一、氯气的物理性质
黄绿色有强烈刺激性气味,有毒,易液化,密度比空气大,能溶于水
二、氯气的化学性质
1. 与金属单质反应:
氯气的氧化性很强,与变价金属反应时,通常将其氧化为高价态。
2.与非金属单质反应
