”精品作业“1.4 常见的碱 第1课时(基础版)(含答案)
文档属性
| 名称 | ”精品作业“1.4 常见的碱 第1课时(基础版)(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 289.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-10-03 00:00:00 | ||
图片预览



文档简介
“精品作业”1.4.1 常见的碱(基础版)
一.选择题(共15小题)
1.滴有酚酞的Ca(OH)2溶液与下列各物质恰好完全反应仍显红色的是( )
A.稀H2SO4 B.CuCl2溶液 C.CO2 D.Na2CO3溶液
2.为研究碱的化学性质,小江进行了如下实验,试管中溶液始终保持红色的是( )
B. C. D.
3.对于碱,下列说法正确的是( )
A.碱一定含有H元素 B.可使酚酞变红的都是碱溶液
C.所有非金属氧化物都可与碱溶液反应 D.酸与碱反应一定不产生沉淀
4.为研究碱的化学性质,小明进行了如下实验,其中实验现象描述错误的是( )
溶液呈红色 B.有白色沉淀生成 C.无明显变化 D.有蓝色沉淀生成
5.下列选项中物质的名称、俗名、化学式完全一致的是( )
A.氯化钠 食盐 NaCl B.氢氧化钙 熟石灰 CaOH
C.氢氧化钠 纯碱 NaOH D.碳酸氢钠 苏打 NaHCO3
6.在①硫酸②氯化铁③碳酸钾三种物质中,跟氢氧化钙溶液、氢氧化钠溶液都能发生反应,且反应能表现出不同碱之间相似性质的组合是( )
A.①② B.①③ C.②③ D.①②③
7.下列物质暴露在空气中一段时间,溶液的溶质质量分数会因为化学变化而变小的是( )
A.浓盐酸 B.石灰水 C.氢氧化钠溶液 D.浓硫酸
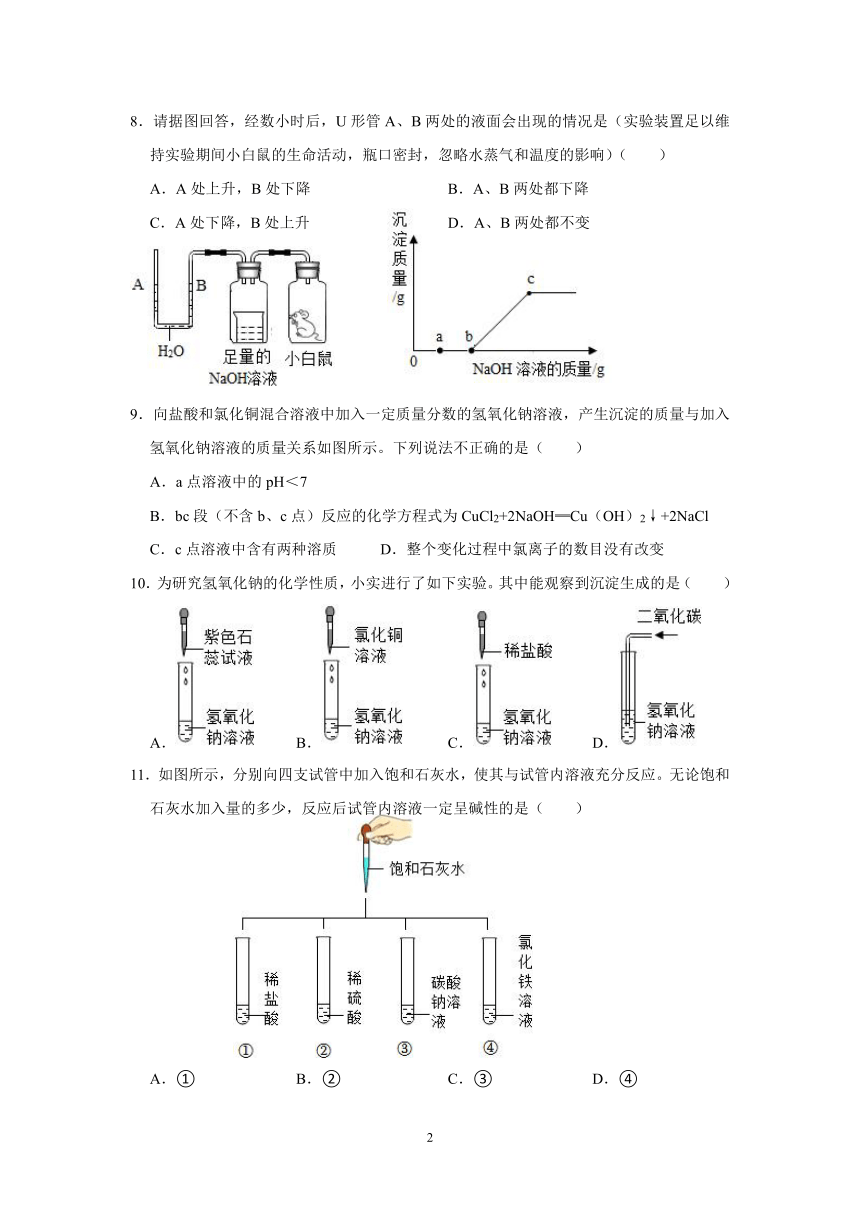
8.请据图回答,经数小时后,U形管A、B两处的液面会出现的情况是(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度的影响)( )
A.A处上升,B处下降 B.A、B两处都下降
C.A处下降,B处上升 D.A、B两处都不变
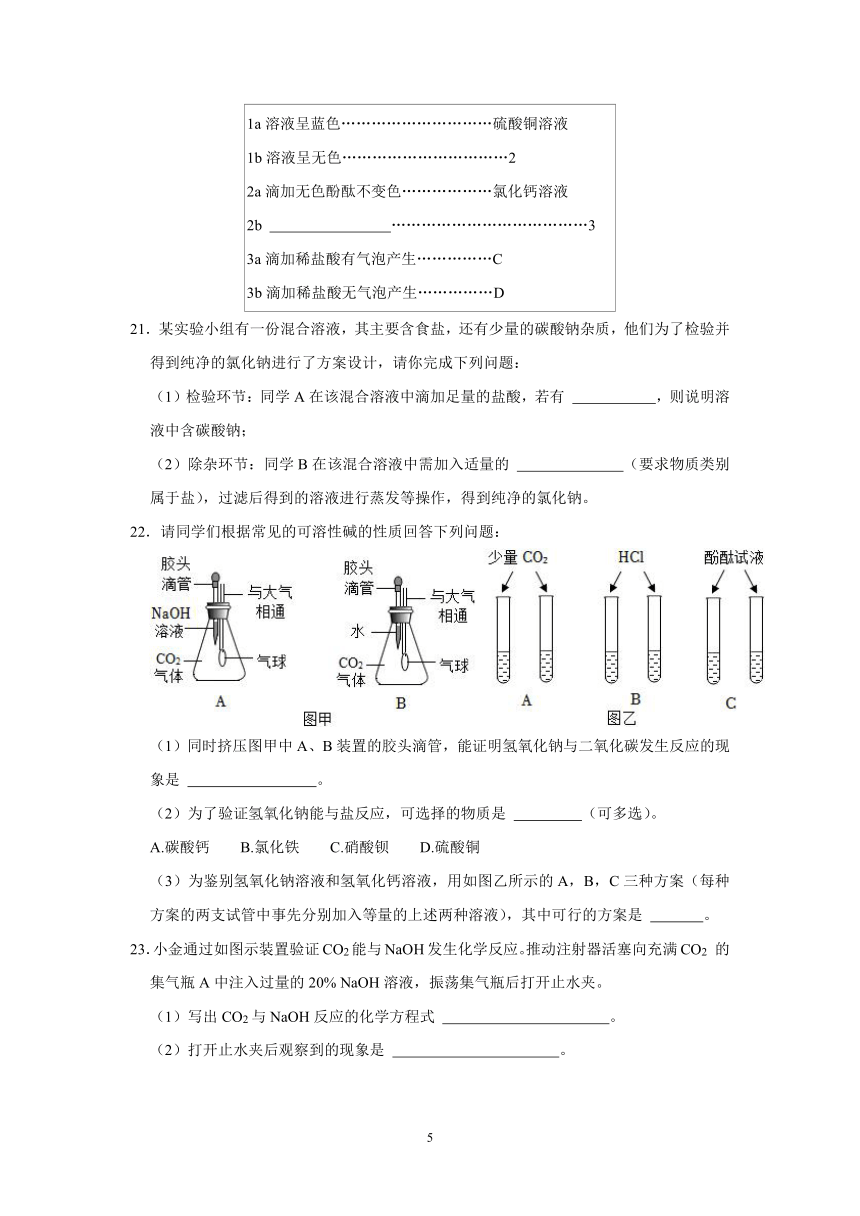
9.向盐酸和氯化铜混合溶液中加入一定质量分数的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法不正确的是( )
A.a点溶液中的pH<7
B.bc段(不含b、c点)反应的化学方程式为CuCl2+2NaOH═Cu(OH)2↓+2NaCl
C.c点溶液中含有两种溶质 D.整个变化过程中氯离子的数目没有改变
10.为研究氢氧化钠的化学性质,小实进行了如下实验。其中能观察到沉淀生成的是( )
A. B. C. D.
11.如图所示,分别向四支试管中加入饱和石灰水,使其与试管内溶液充分反应。无论饱和石灰水加入量的多少,反应后试管内溶液一定呈碱性的是( )
A.① B.② C.③ D.④
12.现有下列4种物质:①浓盐酸;②生石灰;③浓硫酸;④烧碱。它们长期露置在空气中,其中会发生化学变化且质量增加的是( )
A.②④ B.①②④ C.②③④ D.⑧③
13.小金搜集了一些日常生活用品并分析了其有效成分,如表所示。下列分析错误的是( )
物品名称 洁厕灵 炉具清洁剂 食品干燥剂 苏打粉
有效成分 盐酸 氢氧化钠 氧化钙 碳酸钠
A.生活中可用洁厕灵清除水垢[水垢主要成分为CaCO3和Mg(OH)2]
B.若洁厕灵与炉具清洁剂混合后呈碱性,则溶液中阴离子都是OH﹣
C.食品干燥剂在吸水过程中会放热
D.苏打粉溶于水后所得溶液呈碱性
14.向硫酸镁溶液中逐滴滴入溶质质量分数为20%的氢氧化钠溶液,反应生成氢氧化镁沉淀和硫酸钠溶液,溶液的总质量与滴入氢氧化钠溶液的质量关系曲线如图所示。下列说法正确的是( )
A.A点时溶液中的溶质为NaOH、Na2SO4
B.B点时溶液的pH=7
C.原溶液中硫酸镁的质量分数为7.5%
D.A点时锥形瓶内所得溶液的溶质质量分数为12.4%
15.已知,电磁铁的磁性随电流的增大而增强。如图,电源电压保持不变,
弹簧秤下挂着一块铁。现在盛有硫酸铜溶液的烧杯中,
逐渐滴入氢氧化钡溶液可发现弹簧秤的示数( )
A.逐渐变小,最后趋于稳定
B.一直保持不变
C.先变小,后变大,最后趋于稳定
D.先变大,后变小,最后趋于稳定
二、填空题
16.根据碱的四条化学性质回答下列问题:
(1)碱溶液能使酚酞溶液变红的离子是 。
(2)图中的X代表一类物质,则X为 (填写物质类别)。
17.某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,用图总结了NaOH的四条化学性质。
(1)为了验证反应③能够发生,你选择的物质是
A.Na2CO3 B.HCl C.FeCl3 D.Ba(NO3)2
(2)依据反应④,NaOH溶液可以吸收工业尾气中的SO2气体,其化学方程式为: 。
18.小科在做“碱和盐的性质”实验时,将NaOH溶液加入到CaCl2溶液中有白色沉淀产生。白色沉淀是怎么产生的呢?
(1)小陈认为是NaOH 溶液变质导致的,氢氧化钠溶液容易变质的原因是
。(用化学方程式表示)。
(2)小科认为是氢氧化钙溶解度小导致的。为了验证猜想:取该白色沉淀少许,加水后静置,取上层清液,向其中通入 气体,观察到产生白色沉淀,从而证明其猜想是正确的。
19.图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈 色。
(2)性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是 (填化学式)。
(3)依据性质③,除去硫酸厂在生产过程中产生的三氧化硫气体,化学方程式
。
20.某同学参照生物的二歧分类检索表,对一些化学物质进行区分。现有A、B、C、D四种溶液,它们分别是氢氧化钠溶液、硫酸铜溶液、碳酸钠溶液和氯化钙溶液中的一种。他制作了如图所示的分类检索表,请帮他将图中“ ”中的内容补充完整,并指明氢氧化钠所处的位置 (选填“2”、“3”、“C”、“D”)
1a溶液呈蓝色…………………………硫酸铜溶液 1b溶液呈无色……………………………2 2a滴加无色酚酞不变色………………氯化钙溶液 2b …………………………………3 3a滴加稀盐酸有气泡产生……………C 3b滴加稀盐酸无气泡产生……………D
21.某实验小组有一份混合溶液,其主要含食盐,还有少量的碳酸钠杂质,他们为了检验并得到纯净的氯化钠进行了方案设计,请你完成下列问题:
(1)检验环节:同学A在该混合溶液中滴加足量的盐酸,若有 ,则说明溶液中含碳酸钠;
(2)除杂环节:同学B在该混合溶液中需加入适量的 (要求物质类别属于盐),过滤后得到的溶液进行蒸发等操作,得到纯净的氯化钠。
22.请同学们根据常见的可溶性碱的性质回答下列问题:
(1)同时挤压图甲中A、B装置的胶头滴管,能证明氢氧化钠与二氧化碳发生反应的现象是 。
(2)为了验证氢氧化钠能与盐反应,可选择的物质是 (可多选)。
A.碳酸钙 B.氯化铁 C.硝酸钡 D.硫酸铜
(3)为鉴别氢氧化钠溶液和氢氧化钙溶液,用如图乙所示的A,B,C三种方案(每种方案的两支试管中事先分别加入等量的上述两种溶液),其中可行的方案是 。
23.小金通过如图示装置验证CO2能与NaOH发生化学反应。推动注射器活塞向充满CO2 的集气瓶A中注入过量的20% NaOH溶液,振荡集气瓶后打开止水夹。
(1)写出CO2与NaOH反应的化学方程式 。
(2)打开止水夹后观察到的现象是 。
24.在实验室,某同学将氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量。加入氢氧化钠溶液的质量(横轴)与混合溶液中溶质质量(纵轴)的关系如图所示。
(1)实验中,观察到的现象为 。
(2)向反应后的溶液中加入适量BaCl2溶液,恰好完全反应后溶液中的溶质有
。
25.某科学兴趣小组设计了一个“彩灯游戏”,规则是:在“电源开关”处填入一种物质,使其与四条支路上的灯笼对应的物质均能发生反应,并产生不同的现象,四盏彩灯才会同时亮起。
电源开关处的物质是(填化学式) ,Cu(NO3)2处对应的现象是 。
三、实验探究题
26.小滨利用图示装置和药品验证可溶性碱的性质。装置气密性良好,实验前弹簧夹处于关闭状态。(资料:碳酸铜遇水会出现蓝色沉淀物)。
(1)验证可溶性碱能与酸反应。打开活塞a,向锥形瓶中逐滴滴入稀盐酸。Ba(OH)2溶液与稀盐酸恰好完全反应的实验现象是 。
(2)验证可溶性碱能与CO2反应。完成(1)后,打开活塞b,向锥形瓶中滴入足量的NaOH溶液后,立即关闭活塞b。然后 (填实验操作)观察到 现象可证明NaOH与CO2发生反应。
(3)验证可溶性碱能与盐溶液反应。完成(2)后,装置乙中锥形瓶内的溶液呈红色,取少量该溶液于试管中,滴入足量的CuSO4溶液,观察到有蓝色沉淀生成。据上述实验现象能否验证NaOH溶液与CuSO4溶液反应,判断并说明理由 。
27.在某些食品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”(如图)。如果将小纸袋拿出来放在空气中,经过一段时间后,会发现纸袋内的白色固体颗粒黏在一起成为块状。同学们在老师的指导下,对纸袋内的物质进行了探究。【提出问题】白色块状固体的成分是什么?
【猜想假设】同学们猜想该固体有CaO、Ca(OH)2中的一种或两种。你认为还可能有 。
【实验验证】
序号 实验操作 实验现象 实验结论
实验1 取样品于试管中,加水溶解,用手触摸试管外壁。 试管外壁 ,试管底部有白色固体 样品中一定含有CaO
实验2 将实验1中液体过滤,取少量滤液于试管中,向其中通入 气体。 滤液变浑浊 样品中一定含有Ca(OH)2
实验3 取少量实验2中的滤渣,加入足量的稀盐酸。 样品中含有你猜想的物质
【反思评价】同学们经过讨论,认为滤液中一定含有Ca(OH)2,样品中不一定含有Ca(OH)2。理由用化学方程式表示为 。
【拓展应用】(1)若证明实验2滤液中Ca(OH)2的存在,选用下列物质中的 (填字母)也可达到实验目的。A.稀硝酸 B.酚酞溶液 C.碳酸钠溶液
(2)实验室中,易与空气中某些物质反应的药品更要 保存。
28.实验课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,依次开展了以下探究,请完成其中的三个空。
[提出问题1]该氢氧化钠溶液是否变质了呢?
[实验探究1]
实验操作 实验现象 实验结论
取少量该溶液于试管中,向溶液中滴加足量的稀盐酸,并不断振荡。 氢氧化钠溶液一定变质了。
[提出问题2]该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]猜想1:氢氧化钠溶液部分变质。猜想2:氢氧化钠溶液全部变质。
[实验探究2]
实验步骤 实验现象 实验结论
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 有白色沉淀生成。 说明原溶液中一定有碳酸钠。
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 溶液变红色。 说明原溶液中一定有 。
[实验结论]该氢氧化钠溶液部分变质。猜想2正确。
[思考与讨论]有同学认为,探究1已经证明了碳酸钠的存在,所以实验探究2中的实验步骤(1)是多余,只要如实验步骤(2),样品溶于水后,直接滴入酚酞即可的。该同学的看法是否正确?为什么? 。
29.化学兴趣小组同学为探究NaOH与CO2是否发生反应,设计了如下探究实验。
【方案一】从反应物角度探究NaOH与CO2是否发生反应。
(1)小诚同学设计图1所示装置进行实验,将氢氧化钠溶液滴入试管中,一段时间后打开止水夹K,观察到B中导管红墨水液面上升。小刘同学认为此现象不足以证明NaOH与CO2发生了反应,他的理由是 。
(2)小施同学在老师的指导下设计图2所示装置验证小刘同学的观点。实验时分别迅速将注射器内的液体全部注入到装满CO2的甲乙烧瓶中,关闭注射器活塞,测得烧瓶内压强与时间的关系如图3所示。
①乙装置注射器中的液体X为 。
②该实验能证明NaOH与CO2发生反应的依据是 。
【方案二】从生成物角度探究NaOH与CO2是否发生反应。
【查阅资料】常温下,NaOH与Na2CO3在乙醇中的溶解度(g)如表。
NaOH Na2CO3
17.3 <0.01
小珊同学根据上述资料设计如表所示实验证明NaOH与CO2发生反应。
实验操作 实验现象 实验结论
将CO2气体通入到 中 观察到溶液变浑浊 NaOH与CO2发生反应
30.某兴趣小组同学将CO2分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象。为探究CO2和NaOH是否发生了化学反应,小江设计了如图所示的A、B两个实验方案,验证CO2与NaOH溶液发生了化学反应。实验现象为A中试管内液面上升,B中气球胀大。
(1)小江认为上述实验是可行的,其共同原理是 。
(2)小南提出质疑,她认为上述实验不严谨,其理由是 ,要得到科学严谨的结论,仍利用该装置,补做的对比实验是 。
(3)要验证B装置中的CO2和NaOH溶液发生了反应,下一步的操作是: 。
四、解答题
31.在学校科学实验创新比赛中,科学兴趣做了如下实验,装置如图。(已知1体积水恰好能溶解1体积二氧化碳)
【实验设计】三颈烧瓶中充满二氧化碳气体,A颈、C颈分别连接装有一定量的水和氢氧化钠浓溶液的注射器,B颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
【实验操作】先通过A颈往瓶内缓慢注入20mL水,观察小气球形状的变化;过一段时间后再通过B颈往瓶内缓慢注入20mL氢氧化钠浓溶液,再次观察小气球形状的变化。
请描述整个过程中小气球形状的变化情况,并对此作出合理的解释。
32.小明在化学晚会上观看了“瓶吞鸡蛋”的魔术(如图1),看到鸡蛋被吞进瓶内小明思考:瓶能吞蛋,能不能吐蛋呢?他进行了如图2实验,注射器中的试剂P是稀盐酸,结果鸡蛋真的吐了出来。请结合化学反应、压强等科学知识解释“瓶吞鸡蛋”和“瓶吐鸡蛋”的原因。
33.盛有氢氧化钠溶液的容器中有一支燃着的蜡烛,蜡烛燃烧会产生二氧化碳和水,现用一只杯子将蜡烛罩住,如图所示。过一会,可观察到怎样的现象?并简要解释产生这一现象的原因。
现象: 。
解释: 。
参考答案与试题解析
一.选择题(共15小题)
1.D。2.C。3.A。4.B。5.A。6.A。7.B。8.C。9.C。10.B。
11.C。12.A。13.B。14.D。15.C。
二、填空题
填空题(共10小题)
16.(1)氢氧根离子;(2)酸。
17.(1)C;(2)SO2+2NaOH=Na2SO3+H2O。
18.(1)2NaOH+CO2═Na2CO3+H2O;(2)CO2。
19.(1)红;(2)NaCl、NaOH;(3)SO3+2NaOH=Na2SO4+H2O。
20.滴加无色酚酞变红色;D。
21.(1)气泡产生;(2)BaCl2溶液。
22.(1)A中气球大于B中气球;(2)BD;(3)A。
23.(1)2NaOH+CO2═Na2CO3+H2O。
(2)氯化钙溶液流入A集气瓶中,并且产生白色沉淀。
24.(1)开始没有现象,之后有蓝色沉淀生成;(2)NaOH、NaCl。
25.Ba(OH)2;产生蓝色沉淀。
三.实验探究题
26.(1)溶液由红色变成无色;
(2)打开弹簧夹;装置甲中的液体进入装置乙,且乙装置内产生白色沉淀;
(3)不能,因为碳酸钠也能与硫酸铜反应生成蓝色的碳酸铜沉淀。
27.猜想假设:CaCO3;
实验验证:实验1:发热;实验2:二氧化碳;实验3:固体全溶,有气泡产生;
反思评价:CaO+H2O=Ca(OH)2;
拓展应用:(1)BC;(2)密封。
28.实验课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,依次开展了以下探究,请完成其中的三个空。
[提出问题1]该氢氧化钠溶液是否变质了呢?
[实验探究1]
实验操作 实验现象 实验结论
取少量该溶液于试管中,向溶液中滴加足量的稀盐酸,并不断振荡。 产生气泡 氢氧化钠溶液一定变质了。
[提出问题2]该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。
猜想2:氢氧化钠溶液全部变质。
[实验探究2]
实验步骤 实验现象 实验结论
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 有白色沉淀生成。 说明原溶液中一定有碳酸钠。
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 溶液变红色。 说明原溶液中一定有 氢氧化钠 。
[实验结论]该氢氧化钠溶液部分变质。猜想2正确。
[思考与讨论]有同学认为,探究1已经证明了碳酸钠的存在,所以实验探究2中的实验步骤(1)是多余,只要如实验步骤(2),样品溶于水后,直接滴入酚酞即可的。该同学的看法是否正确?为什么? 不正确,因为碳酸钠溶液显碱性,也能使酚酞试液变红色 。
【分析】氢氧化钠溶液和碳酸钠溶液都是显碱性溶液,都能使酚酞试液变红色;
氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,和氯化钙反应生成碳酸钙沉淀和氯化钠。
【解答】解:[实验探究1]
实验操作 实验现象 实验结论
取少量该溶液于试管中,向溶液中滴加足量的稀盐酸,并不断振荡。 产生气泡 氢氧化钠溶液一定变质了。
[实验探究2]
实验步骤 实验现象 实验结论
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 有白色沉淀生成。 说明原溶液中一定有碳酸钠。
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 溶液变红色。 说明原溶液中一定有氢氧化钠。
[思考与讨论]不正确,因为碳酸钠溶液显碱性,也能使酚酞试液变红色。
29.【方案一】(1)二氧化碳会溶于水并与水反应;
(2)①45mL蒸馏水;②最终甲烧瓶内压强比乙烧瓶更小;
【方案二】NaOH的乙醇溶液。
30.(1) CO2与氢氧化钠反应,使内部气压降低 。
(2) CO2可溶于水,造成内部气压降低 ,
将氢氧化钠溶液换成等体积水进行上述实验 。
(3) 向B装置中的液体内滴加稀盐酸 。
四、计算题(共1小题)
31.1体积水恰好能溶解1体积二氧化碳,开始气球没有明显变化,过一段时间后氢氧化钠与二氧化碳反应导致瓶内压强变小,气球变大。
32.氢氧化钠能与二氧化碳反应生成碳酸钠和水,使瓶内的压强减小,在外界大气压的作用下,鸡蛋进入瓶内。酸能和碳酸钠反应生成二氧化碳从而使瓶内压强增大。可以加入的试剂是稀盐酸或稀硫酸,碳酸钠和酸反应生成二氧化碳气体,生成的二氧化碳使瓶内的压强增大,蛋被吐出。
33.蜡烛逐渐熄灭,杯子内液面上升;随着反应的进行,氧气被消耗,生成的二氧化碳不能燃烧、不能支持燃烧,蜡烛会逐渐熄灭;二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,使杯子内压强减小,故杯子内液面上升。
一.选择题(共15小题)
1.滴有酚酞的Ca(OH)2溶液与下列各物质恰好完全反应仍显红色的是( )
A.稀H2SO4 B.CuCl2溶液 C.CO2 D.Na2CO3溶液
2.为研究碱的化学性质,小江进行了如下实验,试管中溶液始终保持红色的是( )
B. C. D.
3.对于碱,下列说法正确的是( )
A.碱一定含有H元素 B.可使酚酞变红的都是碱溶液
C.所有非金属氧化物都可与碱溶液反应 D.酸与碱反应一定不产生沉淀
4.为研究碱的化学性质,小明进行了如下实验,其中实验现象描述错误的是( )
溶液呈红色 B.有白色沉淀生成 C.无明显变化 D.有蓝色沉淀生成
5.下列选项中物质的名称、俗名、化学式完全一致的是( )
A.氯化钠 食盐 NaCl B.氢氧化钙 熟石灰 CaOH
C.氢氧化钠 纯碱 NaOH D.碳酸氢钠 苏打 NaHCO3
6.在①硫酸②氯化铁③碳酸钾三种物质中,跟氢氧化钙溶液、氢氧化钠溶液都能发生反应,且反应能表现出不同碱之间相似性质的组合是( )
A.①② B.①③ C.②③ D.①②③
7.下列物质暴露在空气中一段时间,溶液的溶质质量分数会因为化学变化而变小的是( )
A.浓盐酸 B.石灰水 C.氢氧化钠溶液 D.浓硫酸
8.请据图回答,经数小时后,U形管A、B两处的液面会出现的情况是(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度的影响)( )
A.A处上升,B处下降 B.A、B两处都下降
C.A处下降,B处上升 D.A、B两处都不变
9.向盐酸和氯化铜混合溶液中加入一定质量分数的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。下列说法不正确的是( )
A.a点溶液中的pH<7
B.bc段(不含b、c点)反应的化学方程式为CuCl2+2NaOH═Cu(OH)2↓+2NaCl
C.c点溶液中含有两种溶质 D.整个变化过程中氯离子的数目没有改变
10.为研究氢氧化钠的化学性质,小实进行了如下实验。其中能观察到沉淀生成的是( )
A. B. C. D.
11.如图所示,分别向四支试管中加入饱和石灰水,使其与试管内溶液充分反应。无论饱和石灰水加入量的多少,反应后试管内溶液一定呈碱性的是( )
A.① B.② C.③ D.④
12.现有下列4种物质:①浓盐酸;②生石灰;③浓硫酸;④烧碱。它们长期露置在空气中,其中会发生化学变化且质量增加的是( )
A.②④ B.①②④ C.②③④ D.⑧③
13.小金搜集了一些日常生活用品并分析了其有效成分,如表所示。下列分析错误的是( )
物品名称 洁厕灵 炉具清洁剂 食品干燥剂 苏打粉
有效成分 盐酸 氢氧化钠 氧化钙 碳酸钠
A.生活中可用洁厕灵清除水垢[水垢主要成分为CaCO3和Mg(OH)2]
B.若洁厕灵与炉具清洁剂混合后呈碱性,则溶液中阴离子都是OH﹣
C.食品干燥剂在吸水过程中会放热
D.苏打粉溶于水后所得溶液呈碱性
14.向硫酸镁溶液中逐滴滴入溶质质量分数为20%的氢氧化钠溶液,反应生成氢氧化镁沉淀和硫酸钠溶液,溶液的总质量与滴入氢氧化钠溶液的质量关系曲线如图所示。下列说法正确的是( )
A.A点时溶液中的溶质为NaOH、Na2SO4
B.B点时溶液的pH=7
C.原溶液中硫酸镁的质量分数为7.5%
D.A点时锥形瓶内所得溶液的溶质质量分数为12.4%
15.已知,电磁铁的磁性随电流的增大而增强。如图,电源电压保持不变,
弹簧秤下挂着一块铁。现在盛有硫酸铜溶液的烧杯中,
逐渐滴入氢氧化钡溶液可发现弹簧秤的示数( )
A.逐渐变小,最后趋于稳定
B.一直保持不变
C.先变小,后变大,最后趋于稳定
D.先变大,后变小,最后趋于稳定
二、填空题
16.根据碱的四条化学性质回答下列问题:
(1)碱溶液能使酚酞溶液变红的离子是 。
(2)图中的X代表一类物质,则X为 (填写物质类别)。
17.某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,用图总结了NaOH的四条化学性质。
(1)为了验证反应③能够发生,你选择的物质是
A.Na2CO3 B.HCl C.FeCl3 D.Ba(NO3)2
(2)依据反应④,NaOH溶液可以吸收工业尾气中的SO2气体,其化学方程式为: 。
18.小科在做“碱和盐的性质”实验时,将NaOH溶液加入到CaCl2溶液中有白色沉淀产生。白色沉淀是怎么产生的呢?
(1)小陈认为是NaOH 溶液变质导致的,氢氧化钠溶液容易变质的原因是
。(用化学方程式表示)。
(2)小科认为是氢氧化钙溶解度小导致的。为了验证猜想:取该白色沉淀少许,加水后静置,取上层清液,向其中通入 气体,观察到产生白色沉淀,从而证明其猜想是正确的。
19.图1是关于氢氧化钠化学性质的思维导图,请据图回答问题。
(1)性质①,将无色酚酞溶液滴入氢氧化钠溶液中,溶液呈 色。
(2)性质②,将氢氧化钠溶液滴入稀盐酸中、图2表示该反应过程中溶液pH的变化曲线,n点溶液中的溶质是 (填化学式)。
(3)依据性质③,除去硫酸厂在生产过程中产生的三氧化硫气体,化学方程式
。
20.某同学参照生物的二歧分类检索表,对一些化学物质进行区分。现有A、B、C、D四种溶液,它们分别是氢氧化钠溶液、硫酸铜溶液、碳酸钠溶液和氯化钙溶液中的一种。他制作了如图所示的分类检索表,请帮他将图中“ ”中的内容补充完整,并指明氢氧化钠所处的位置 (选填“2”、“3”、“C”、“D”)
1a溶液呈蓝色…………………………硫酸铜溶液 1b溶液呈无色……………………………2 2a滴加无色酚酞不变色………………氯化钙溶液 2b …………………………………3 3a滴加稀盐酸有气泡产生……………C 3b滴加稀盐酸无气泡产生……………D
21.某实验小组有一份混合溶液,其主要含食盐,还有少量的碳酸钠杂质,他们为了检验并得到纯净的氯化钠进行了方案设计,请你完成下列问题:
(1)检验环节:同学A在该混合溶液中滴加足量的盐酸,若有 ,则说明溶液中含碳酸钠;
(2)除杂环节:同学B在该混合溶液中需加入适量的 (要求物质类别属于盐),过滤后得到的溶液进行蒸发等操作,得到纯净的氯化钠。
22.请同学们根据常见的可溶性碱的性质回答下列问题:
(1)同时挤压图甲中A、B装置的胶头滴管,能证明氢氧化钠与二氧化碳发生反应的现象是 。
(2)为了验证氢氧化钠能与盐反应,可选择的物质是 (可多选)。
A.碳酸钙 B.氯化铁 C.硝酸钡 D.硫酸铜
(3)为鉴别氢氧化钠溶液和氢氧化钙溶液,用如图乙所示的A,B,C三种方案(每种方案的两支试管中事先分别加入等量的上述两种溶液),其中可行的方案是 。
23.小金通过如图示装置验证CO2能与NaOH发生化学反应。推动注射器活塞向充满CO2 的集气瓶A中注入过量的20% NaOH溶液,振荡集气瓶后打开止水夹。
(1)写出CO2与NaOH反应的化学方程式 。
(2)打开止水夹后观察到的现象是 。
24.在实验室,某同学将氢氧化钠溶液逐滴滴入硫酸和硫酸铜的混合溶液中,直至过量。加入氢氧化钠溶液的质量(横轴)与混合溶液中溶质质量(纵轴)的关系如图所示。
(1)实验中,观察到的现象为 。
(2)向反应后的溶液中加入适量BaCl2溶液,恰好完全反应后溶液中的溶质有
。
25.某科学兴趣小组设计了一个“彩灯游戏”,规则是:在“电源开关”处填入一种物质,使其与四条支路上的灯笼对应的物质均能发生反应,并产生不同的现象,四盏彩灯才会同时亮起。
电源开关处的物质是(填化学式) ,Cu(NO3)2处对应的现象是 。
三、实验探究题
26.小滨利用图示装置和药品验证可溶性碱的性质。装置气密性良好,实验前弹簧夹处于关闭状态。(资料:碳酸铜遇水会出现蓝色沉淀物)。
(1)验证可溶性碱能与酸反应。打开活塞a,向锥形瓶中逐滴滴入稀盐酸。Ba(OH)2溶液与稀盐酸恰好完全反应的实验现象是 。
(2)验证可溶性碱能与CO2反应。完成(1)后,打开活塞b,向锥形瓶中滴入足量的NaOH溶液后,立即关闭活塞b。然后 (填实验操作)观察到 现象可证明NaOH与CO2发生反应。
(3)验证可溶性碱能与盐溶液反应。完成(2)后,装置乙中锥形瓶内的溶液呈红色,取少量该溶液于试管中,滴入足量的CuSO4溶液,观察到有蓝色沉淀生成。据上述实验现象能否验证NaOH溶液与CuSO4溶液反应,判断并说明理由 。
27.在某些食品的包装袋内,有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”(如图)。如果将小纸袋拿出来放在空气中,经过一段时间后,会发现纸袋内的白色固体颗粒黏在一起成为块状。同学们在老师的指导下,对纸袋内的物质进行了探究。【提出问题】白色块状固体的成分是什么?
【猜想假设】同学们猜想该固体有CaO、Ca(OH)2中的一种或两种。你认为还可能有 。
【实验验证】
序号 实验操作 实验现象 实验结论
实验1 取样品于试管中,加水溶解,用手触摸试管外壁。 试管外壁 ,试管底部有白色固体 样品中一定含有CaO
实验2 将实验1中液体过滤,取少量滤液于试管中,向其中通入 气体。 滤液变浑浊 样品中一定含有Ca(OH)2
实验3 取少量实验2中的滤渣,加入足量的稀盐酸。 样品中含有你猜想的物质
【反思评价】同学们经过讨论,认为滤液中一定含有Ca(OH)2,样品中不一定含有Ca(OH)2。理由用化学方程式表示为 。
【拓展应用】(1)若证明实验2滤液中Ca(OH)2的存在,选用下列物质中的 (填字母)也可达到实验目的。A.稀硝酸 B.酚酞溶液 C.碳酸钠溶液
(2)实验室中,易与空气中某些物质反应的药品更要 保存。
28.实验课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,依次开展了以下探究,请完成其中的三个空。
[提出问题1]该氢氧化钠溶液是否变质了呢?
[实验探究1]
实验操作 实验现象 实验结论
取少量该溶液于试管中,向溶液中滴加足量的稀盐酸,并不断振荡。 氢氧化钠溶液一定变质了。
[提出问题2]该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]猜想1:氢氧化钠溶液部分变质。猜想2:氢氧化钠溶液全部变质。
[实验探究2]
实验步骤 实验现象 实验结论
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 有白色沉淀生成。 说明原溶液中一定有碳酸钠。
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 溶液变红色。 说明原溶液中一定有 。
[实验结论]该氢氧化钠溶液部分变质。猜想2正确。
[思考与讨论]有同学认为,探究1已经证明了碳酸钠的存在,所以实验探究2中的实验步骤(1)是多余,只要如实验步骤(2),样品溶于水后,直接滴入酚酞即可的。该同学的看法是否正确?为什么? 。
29.化学兴趣小组同学为探究NaOH与CO2是否发生反应,设计了如下探究实验。
【方案一】从反应物角度探究NaOH与CO2是否发生反应。
(1)小诚同学设计图1所示装置进行实验,将氢氧化钠溶液滴入试管中,一段时间后打开止水夹K,观察到B中导管红墨水液面上升。小刘同学认为此现象不足以证明NaOH与CO2发生了反应,他的理由是 。
(2)小施同学在老师的指导下设计图2所示装置验证小刘同学的观点。实验时分别迅速将注射器内的液体全部注入到装满CO2的甲乙烧瓶中,关闭注射器活塞,测得烧瓶内压强与时间的关系如图3所示。
①乙装置注射器中的液体X为 。
②该实验能证明NaOH与CO2发生反应的依据是 。
【方案二】从生成物角度探究NaOH与CO2是否发生反应。
【查阅资料】常温下,NaOH与Na2CO3在乙醇中的溶解度(g)如表。
NaOH Na2CO3
17.3 <0.01
小珊同学根据上述资料设计如表所示实验证明NaOH与CO2发生反应。
实验操作 实验现象 实验结论
将CO2气体通入到 中 观察到溶液变浑浊 NaOH与CO2发生反应
30.某兴趣小组同学将CO2分别通入澄清石灰水和氢氧化钠溶液中,观察到前者变浑浊,后者无明显现象。为探究CO2和NaOH是否发生了化学反应,小江设计了如图所示的A、B两个实验方案,验证CO2与NaOH溶液发生了化学反应。实验现象为A中试管内液面上升,B中气球胀大。
(1)小江认为上述实验是可行的,其共同原理是 。
(2)小南提出质疑,她认为上述实验不严谨,其理由是 ,要得到科学严谨的结论,仍利用该装置,补做的对比实验是 。
(3)要验证B装置中的CO2和NaOH溶液发生了反应,下一步的操作是: 。
四、解答题
31.在学校科学实验创新比赛中,科学兴趣做了如下实验,装置如图。(已知1体积水恰好能溶解1体积二氧化碳)
【实验设计】三颈烧瓶中充满二氧化碳气体,A颈、C颈分别连接装有一定量的水和氢氧化钠浓溶液的注射器,B颈插有两端开口的玻璃导管(伸入瓶内的一端连有小气球),装置气密性良好。
【实验操作】先通过A颈往瓶内缓慢注入20mL水,观察小气球形状的变化;过一段时间后再通过B颈往瓶内缓慢注入20mL氢氧化钠浓溶液,再次观察小气球形状的变化。
请描述整个过程中小气球形状的变化情况,并对此作出合理的解释。
32.小明在化学晚会上观看了“瓶吞鸡蛋”的魔术(如图1),看到鸡蛋被吞进瓶内小明思考:瓶能吞蛋,能不能吐蛋呢?他进行了如图2实验,注射器中的试剂P是稀盐酸,结果鸡蛋真的吐了出来。请结合化学反应、压强等科学知识解释“瓶吞鸡蛋”和“瓶吐鸡蛋”的原因。
33.盛有氢氧化钠溶液的容器中有一支燃着的蜡烛,蜡烛燃烧会产生二氧化碳和水,现用一只杯子将蜡烛罩住,如图所示。过一会,可观察到怎样的现象?并简要解释产生这一现象的原因。
现象: 。
解释: 。
参考答案与试题解析
一.选择题(共15小题)
1.D。2.C。3.A。4.B。5.A。6.A。7.B。8.C。9.C。10.B。
11.C。12.A。13.B。14.D。15.C。
二、填空题
填空题(共10小题)
16.(1)氢氧根离子;(2)酸。
17.(1)C;(2)SO2+2NaOH=Na2SO3+H2O。
18.(1)2NaOH+CO2═Na2CO3+H2O;(2)CO2。
19.(1)红;(2)NaCl、NaOH;(3)SO3+2NaOH=Na2SO4+H2O。
20.滴加无色酚酞变红色;D。
21.(1)气泡产生;(2)BaCl2溶液。
22.(1)A中气球大于B中气球;(2)BD;(3)A。
23.(1)2NaOH+CO2═Na2CO3+H2O。
(2)氯化钙溶液流入A集气瓶中,并且产生白色沉淀。
24.(1)开始没有现象,之后有蓝色沉淀生成;(2)NaOH、NaCl。
25.Ba(OH)2;产生蓝色沉淀。
三.实验探究题
26.(1)溶液由红色变成无色;
(2)打开弹簧夹;装置甲中的液体进入装置乙,且乙装置内产生白色沉淀;
(3)不能,因为碳酸钠也能与硫酸铜反应生成蓝色的碳酸铜沉淀。
27.猜想假设:CaCO3;
实验验证:实验1:发热;实验2:二氧化碳;实验3:固体全溶,有气泡产生;
反思评价:CaO+H2O=Ca(OH)2;
拓展应用:(1)BC;(2)密封。
28.实验课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,依次开展了以下探究,请完成其中的三个空。
[提出问题1]该氢氧化钠溶液是否变质了呢?
[实验探究1]
实验操作 实验现象 实验结论
取少量该溶液于试管中,向溶液中滴加足量的稀盐酸,并不断振荡。 产生气泡 氢氧化钠溶液一定变质了。
[提出问题2]该氢氧化钠溶液是全部变质还是部分变质呢?
[猜想与假设]
猜想1:氢氧化钠溶液部分变质。
猜想2:氢氧化钠溶液全部变质。
[实验探究2]
实验步骤 实验现象 实验结论
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 有白色沉淀生成。 说明原溶液中一定有碳酸钠。
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 溶液变红色。 说明原溶液中一定有 氢氧化钠 。
[实验结论]该氢氧化钠溶液部分变质。猜想2正确。
[思考与讨论]有同学认为,探究1已经证明了碳酸钠的存在,所以实验探究2中的实验步骤(1)是多余,只要如实验步骤(2),样品溶于水后,直接滴入酚酞即可的。该同学的看法是否正确?为什么? 不正确,因为碳酸钠溶液显碱性,也能使酚酞试液变红色 。
【分析】氢氧化钠溶液和碳酸钠溶液都是显碱性溶液,都能使酚酞试液变红色;
氢氧化钠和二氧化碳反应生成碳酸钠和水,碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,和氯化钙反应生成碳酸钙沉淀和氯化钠。
【解答】解:[实验探究1]
实验操作 实验现象 实验结论
取少量该溶液于试管中,向溶液中滴加足量的稀盐酸,并不断振荡。 产生气泡 氢氧化钠溶液一定变质了。
[实验探究2]
实验步骤 实验现象 实验结论
(1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡。 有白色沉淀生成。 说明原溶液中一定有碳酸钠。
(2)取步骤(1)试管中的少量上层清液,滴加酚酞溶液。 溶液变红色。 说明原溶液中一定有氢氧化钠。
[思考与讨论]不正确,因为碳酸钠溶液显碱性,也能使酚酞试液变红色。
29.【方案一】(1)二氧化碳会溶于水并与水反应;
(2)①45mL蒸馏水;②最终甲烧瓶内压强比乙烧瓶更小;
【方案二】NaOH的乙醇溶液。
30.(1) CO2与氢氧化钠反应,使内部气压降低 。
(2) CO2可溶于水,造成内部气压降低 ,
将氢氧化钠溶液换成等体积水进行上述实验 。
(3) 向B装置中的液体内滴加稀盐酸 。
四、计算题(共1小题)
31.1体积水恰好能溶解1体积二氧化碳,开始气球没有明显变化,过一段时间后氢氧化钠与二氧化碳反应导致瓶内压强变小,气球变大。
32.氢氧化钠能与二氧化碳反应生成碳酸钠和水,使瓶内的压强减小,在外界大气压的作用下,鸡蛋进入瓶内。酸能和碳酸钠反应生成二氧化碳从而使瓶内压强增大。可以加入的试剂是稀盐酸或稀硫酸,碳酸钠和酸反应生成二氧化碳气体,生成的二氧化碳使瓶内的压强增大,蛋被吐出。
33.蜡烛逐渐熄灭,杯子内液面上升;随着反应的进行,氧气被消耗,生成的二氧化碳不能燃烧、不能支持燃烧,蜡烛会逐渐熄灭;二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,使杯子内压强减小,故杯子内液面上升。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
