河北省尚义县2023-2024学年高二上学期9月月考化学试题(含解析)
文档属性
| 名称 | 河北省尚义县2023-2024学年高二上学期9月月考化学试题(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 839.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-02 20:50:17 | ||
图片预览




文档简介
尚义县2023-2024学年高二上学期9月月考
化学
注意事项:
1. 本试卷共100分,考试时间75分钟。
2. 请将各题答案填在答题卡上。
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Mg-24 Al-27 S-32 Cl-35.5 V-51 Fe-56 Co-59 Cu-64 Zn-65
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1. 下列实验方案不能达到相应实验目的的是( )
A. 用装置①验证升高温度可以加快反应速率
B. 用装置②探究浓度对化学反应速率的影响
C. 用装置③比较、对分解速率的影响
D. 用装置④探究温度对化学平衡的影响
2. 在溶液中存在如下平衡: ,下列措施中能使平衡正向移动的是( )
A. 加热 B. 加压 C. 加 D. 加水稀释
3. 我国科学家通过对月壤样本的研究提出,未来在月球可利用月壤做催化剂进行人工光合作用,其中涉及的反应之一为(该条件下所有物质均为气态)。下列说法正确的是( )
A. 月壤可以改变该化学反应的限度
B. 通过控制反应条件,使和充分反应生成
C. 达平衡后,反应就停止了,正逆反应速率均为0
D. 将从体系中分离能减慢反应速率
4. 下列平衡常数的表达式书写正确的是( )
A.
B.
C.
D.
5. 工业合成氨 中,所采取的措施既有利于合成氨又能用勒夏特列原理解释的是( )
A. 高温 B. 高压 C. 加入催化剂 D. 原料气净化
6. 甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳和氢气反应可以合成甲醇,反应如下: 。下列措施中能提高平衡时转化率的是( )
A. 升温 B. 等容下通入
C. 加压 D. 增大和的初始投料比
7. 反应体系中存在平衡:,下列操作不能使平衡发生移动的是( )
A. 加入少量铁粉 B. 加入浓KSCN溶液
C. 加 D. 升温
8. 某温度下,在一个2L的密闭容器中加入和进行如下反应:,反应2min后达到平衡,测得生成,下列说法正确的是( )
A. 前2min,C的平均反应速率为
B. 反应的前后压强之比为
C. 平衡时A的平衡转化率是70%
D. 增大压强,平衡正向移动,化学平衡常数增大
9. 下列说法正确的是( )
A. 冰在室温下能自动融化成水,这是熵增的过程 B. 吸热反应一定不能自发进行
C. 非自发反应一定不能实现 D. ,的反应,低温能自发进行
10. 在一个容积不变的密闭容器中发生反应:,已知:。若该反应在恒温()、恒容的密闭体系中进行,时测得的下列数据中,不可以作为判断t时刻反应是否达到平衡状态的依据的是( )
A. t时刻及其前后、、、的浓度
B. t时刻,、、、的浓度
C. t时刻及其前后容器中的压强
D. t时刻,消耗的速率与生成的速率
11. 在密闭容器中反应 达到平衡,下列操作能使容器内气体颜色变浅的是( )
A. 升高温度 B. 缩小容器体积
C. 容器体积不变,充入 D. 保持压强不变,充入氮气
12. 工业上苯乙烯的生产主要采用乙苯脱氢工艺:。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是( )
A. 时刻,、和的物质的量之比为
B. 该反应的
C. 反应进行到时,Q<K(Q为浓度商)
D. 催化剂存在时(其他条件不变),、和苯乙烯的平衡产率都增大
13. 是一种重要的化工原料,以HCl为原料,用氧化制取,可提高效益,减少污染。反应为:实验测得在不同压强下,总反应的HCl平衡转化率随温度变化的曲线如图,下列说法正确的是( )
A. 速率: B. 平衡常数:
C. D.
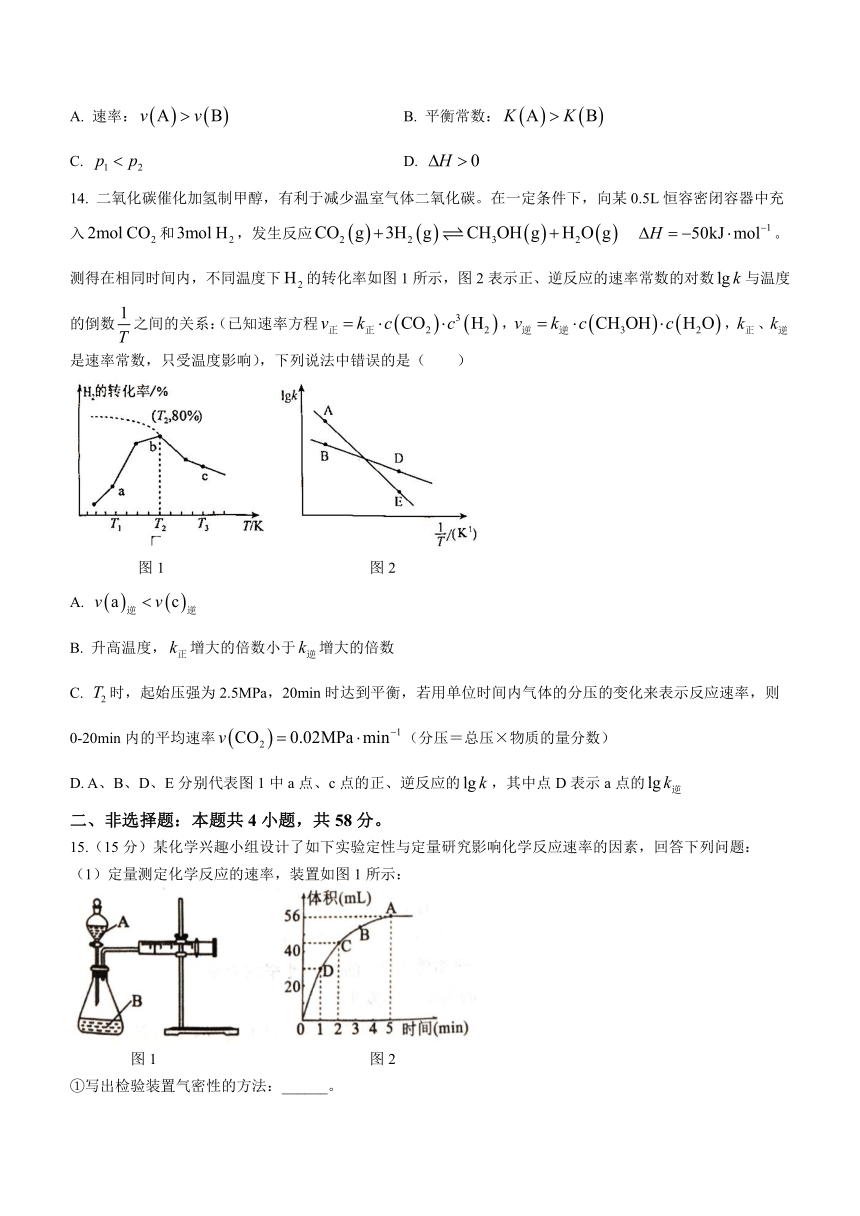
14. 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。在一定条件下,向某0.5L恒容密闭容器中充入和,发生反应 。测得在相同时间内,不同温度下的转化率如图1所示,图2表示正、逆反应的速率常数的对数与温度的倒数之间的关系:(已知速率方程,,、是速率常数,只受温度影响),下列说法中错误的是( )
图1 图2
A.
B. 升高温度,增大的倍数小于增大的倍数
C. 时,起始压强为2.5MPa,20min时达到平衡,若用单位时间内气体的分压的变化来表示反应速率,则0-20min内的平均速率(分压=总压×物质的量分数)
D. A、B、D、E分别代表图1中a点、c点的正、逆反应的,其中点D表示a点的
二、非选择题:本题共4小题,共58分。
15.(15分)某化学兴趣小组设计了如下实验定性与定量研究影响化学反应速率的因素,回答下列问题:
(1)定量测定化学反应的速率,装置如图1所示:
图1 图2
①写出检验装置气密性的方法:______。
②在装置B中加入固体,从装置A中加入的双氧水(),产生气体如图2所示:(不考虑溶液体积变化,气体体积已经转化为标准状况)
A、B、C、D各点产生的平均反应速率最大的是______(填字母)。用物质的量浓度的变化表示0~5min化学反应的平均速率______。
(2)探究浓度对化学反应速率的影响。
将3支试管分别编号为①②③,实验记录的数据如表所示。
试管编号 加溶液 加 加溶液 出现浑浊的时间
① 3mL 3mL 5滴 33s
② 2mL 5滴 28s
③ 5mL 5滴 16s
①该反应的化学方程式是____________。
②______,______。
③实验得出的结论是____________。
(3)把去掉氧化物膜的镁条投入到盛有盐酸的敞口容器里,产生的速率如图所示:
①写出时间T以前反应速率逐渐加快的原因是____________。
②写出时间T以后反应速率逐渐减慢的原因是____________。
16.(11分)勒夏特列原理是化学平衡移动的基本原理,在工农业生产中有着广泛的应用,回答下列问题:
(1)已知钾的金属性强于钠,选取适宜的温度,工业上可以利用钠制取钾,其反应原理为:,利用勒夏特列原理进行解释______。
(2)氮化硅()陶瓷能大幅度提高发动机的热效率,工业制备氮化硅陶瓷的反应原理为: 。
①在温度不变、体积恒定的密闭容器中加入、和,发生上述反应,不能表示上述反应达到化学平衡状态的是______(填字母)。
A. 混合气体的密度保持不变 B. HCl气体的物质的量分数保持不变
C. HCl的生成速率等于的消耗速率的六倍 D. 固体的质量不再发生变化
②能提高化学反应速率,同时能提高的平衡转化率可以采取的措施是____________(答出两条)。
(3)将纯净的氨基甲酸铵固体置于密闭真空容器中(容器体积可变,固体足量),在某温度下发生分解反应:,达到化学平衡状态。
①用物质的量浓度表示该反应的化学平衡常数表达式______。
②增大容器的体积,该化学平衡向______(填“正反应方向”“逆反应方向”或“不”)移动。再次达到化学平衡状态时,的质量______(填“减小”“增大”或“不变”,下同),______。
③在温度,压强为P的恒压容器中,该反应达到化学平衡状态,此时用平衡分压表示的平衡常数______。
17.(16分)氮氧化合物是大气污染物,利用甲烷()与反应可以消除氮氧化合物,反应如下: ,回答下列问题:
(1)为了加快化学反应速率,同时提高的平衡浓度,可以采取的措施是____________。
(2)温度为和时,在体积为2L的某刚性密闭容器中,加入和气体,发生上述反应,测得有关数据如表:
时间/min 0 10 20 40 50
0.50 0.35 0.25 0.10 0.10
0.50 0.30 0.218 a 0.15
①温度为时,在0~10min内用表示的平均反应速率______。
②温度______(填“大于”或“小于”),______mol。
③______0(填“大于”或“小于”),分析原因是____________。
(3)在,100kPa下用氦气作为稀释气体发生:
(主反应①)
同时能发生下列两个副反应:
(副反应②) (副反应③)
在以上反应体系中转化为、和NO的选择性用S表示(),各反应的的选择性S随平衡转化率的变化曲线如图所示:
其中曲线b代表的反应是______(填“①”、“②”或“③”),理由是____________。
18.(16分)空气中的、CO和是常见的大气污染物,合理利用可以变废为宝。回答下列问题:
(1)在某恒温刚性密闭容器中发生反应:
该反应的速率表达式为(k只与温度有关,m、n待测),时测得有关实验数据如下:
序号 速率
Ⅰ 0.0060 0.0010
Ⅱ 0.0060 0.0020
Ⅲ 0.0010 0.0060
Ⅳ 0.0020 0.0060
①______,______。若升高温度速率常数k将______(填“增大”“减小”或“不变”,下同)。
②该反应在时能自发进行反应,若升高温度该反应的化学平衡常数将______。
③该反应的基元反应可以表示为:
Ⅰ. ____________(慢) Ⅱ. (快)
写出反应Ⅰ的化学方程式____________。正反应的活化能Ⅰ______Ⅱ(填“大于”“小于”或“等于”)。
(2)一定温度下,在一体积可变的密闭容器中,充入和,发生反应Ⅰ.
Ⅱ.
达到平衡时,测定,。
①若缩小容器体积增大压强,反应Ⅱ将______(填“正反应方向”“逆反应方向”或“不”)移动。
②达到平衡时,可用气体的物质的量表示反应Ⅱ的化学平衡常数,在此表达式中______mol,______mol。
③为了提高甲醇的选择性,除使用高效催化剂和增大压强外,还可以采取的措施是____________。
尚义县2023-2024学年高二上学期9月月考
化学参考答案
1. A 【解析】A. ①中滴加了氯化铁溶液作催化剂,不能说明是温度的影响导致反应速率加快的,故A符合题意。
2. A 【解析】A. 该反应为吸热反应,升温,平衡正移,故A正确;
B. 改变压强只对有气体参加的反应有影响,故B错误;
D. 加水稀释,平衡逆移,故D错误。
3. D 【解析】A. 月壤做催化剂,催化剂可以加快化学反应速率,但不可以改变该化学反应的限度,故A错误;
B. 该反应是可逆反应,反应物不能完全转化为生成物,故和反应不可得到,故B错误;
D. 将从体系中分离,生成物浓度减小,减慢反应速率,故D正确。
4. C 【解析】化学平衡常数等于生成物的浓度幂次方的乘积与反应物浓度的幂次方的乘积比值,固体和纯液体不代入平衡常数。
A. 该反应平衡常数表达式为:,故A错误;
B. 该反应平衡常数表达式为:,故B错误;
D. 该反应平衡常数表达式为:,故D错误。
5. B 【解析】A. 升高温度,平衡逆移,氨气产率降低,不能用平衡移动原理解释,故A错误;
B. 增大压强,平衡正向移动,有利于提高原料转化率,能用平衡移动原理解释,故B正确;
C. 加入催化剂,平衡不移动,不能用平衡移动原理解释,故C错误;
D. 原料气净化是防止催化剂中毒,不能用勒夏特列原理解释,故D错误。
6. C 【解析】A. 该反应为放热反应,升温,平衡逆移,平衡时转化率减小,故A错误;
B. 等容下通入,平衡逆移,平衡时转化率减小,故B错误;
C. 该反应为气体体积减小的反应,加压,平衡正移,平衡时转化率增大,故C正确;
D. 增大和的初始投料比,平衡时转化率减小,转化率增大,故D错误。
7. C 【解析】该反应的实质为:,加平衡不移动。
8. B 【解析】
起始(mol) 4 2 0 0
转化(mol) 1.2 0.8 1.6 0.8
平衡(mol) 2.8 1.2 1.6 0.8
A. 由于C的状态是固体,不能用固体表示化学反应速率,故A错误;
B. 温度与体积一定时,压强之比等于物质的量之比,反应前后的压强之比为:,故B正确;
C. 达到平衡时,消耗,则A的转化率为,故C错误;
D. 增大压强,平衡正向移动,化学平衡常数不变,故D错误。
9. A 【解析】A. 同种物质的熵值:气态>液态>固态,故A正确;
D. 根据,反应自发进行,,的反应自发进行,需要在高温下进行,故D错误。
10. C 【解析】A. 对比t时刻及其前后、、、的浓度,当、、、的浓度不再变化的时候,说明达到化学平衡状态,故A不符合题意;
B. 知道t时刻、、、的浓度,代入公式Q,根据计算结果与的关系可判断是否达到化学平衡状态,即可以作为判断t时刻反应是否达到平衡状态的依据,故B不符合题意;
C. 该反应在反应过程中压强一直不变,测定t时刻及其前后容器中的压强无法判断是否达到化学平衡状态,即不可以作为判断t时刻反应是否达到平衡状态的依据,故C符合题意;
D. t时刻,消耗的速率是正反应方向的速率,生成的速率是逆反应方向的速率,若消耗的速率与生成的速率相等时,说明反应达到化学平衡状态,即可以作为判断t时刻反应是否达到平衡状态的依据,故D不符合题意。
11. D 【解析】A. 升高温度,平衡逆向移动,浓度增大,颜色变深,故A错误;
B、C能使平衡正向移动,但浓度增大,颜色变深,故B、C错误。
12. C 【解析】A. 时刻,反应达平衡,、和的物质的量之比不一定为,故A错误;
C. 反应进行到时,反应正向进行,故Q<K,故C正确;
D. 催化剂能降低反应的活化能,使反应的、都增大;催化剂不能使平衡移动,苯乙烯的平衡产率不变,故D错误。
13. B 【解析】A. 由图像可知反应温度:,故,故A错误;
B. 由于该反应的正反应是放热反应,在压强不变时,升高温度,化学平衡向吸热的逆反应方向移动,导致化学平衡常数减小。由图像可知反应温度:,所以化学平衡常数:,故B正确;
C. 该反应的正反应是气体体积缩小的反应,在其它条件不变时,增大压强,化学平衡向气体体积减小的正向移动,导致反应物HCl的转化率增大。由于在相同温度下HCl的转化率:,所以压强大小关系为:,故C错误;
D. 升高温度,HCl的平衡转化率降低,平衡逆向移动,正向为放热反应,故D错误。
14. D 【解析】根据图1可知,c的温度高于a点,温度高,反应速率快,则,故A不符合题意;
B. ,升高温度,平衡逆移,K减小,增大的倍数小于增大的倍数,故B不符合题意;
C. 时,起始压强2.5MPa,则的起始分压为,的起始分压为,20min时达到平衡,的转化率为80%,列三段式有
起始分压/MPa 1 1.5 0 0
变化分压/MPa 0.4 1.2 0.4 0.4
平衡分压/MPa 0.6 0.3 0.4 0.4
则,故C不符合题意;
D. 温度升高,正逆反应速率均增大,图中横坐标是温度的倒数,由右向左是升高温度,速率常数的对数随温度升高均是增大的,但温度对吸热反应方向速率影响更大,该反应逆向吸热,则逆反应方向的速率变化更大,斜率更大,A、E所在的这条线表示的是逆反应速率常数的对数与温度倒数的关系,由于a点温度较c点低,则E点表示a点的,故D符合题意。
15.(15分,除标注外每空2分)
(1)①关闭分液漏斗的活塞,轻轻向外拉动注射器的活塞,一段时间后,活塞能回到原来的位置,证明装置的气密性良好(合理即可得分)
②D(1分) 0.05
(2)① ②4(1分) 1(1分)
③其他条件不变时,增大反应物浓度能够加快化学反应速率(合理即可得分)
(3)①该反应为放热反应,T以前随着温度升高反应速率加快
②T以后,随着反应进行逐渐减小,反应速率逐渐变慢
16.(11分,除标注外每空1分)
(1)及时移走,降低生成物浓度,化学平衡正向移动,钠就能制取钾(2分,合理即可)
(2)①C ②升高温度,增大氮气或氢气的浓度(2分)
(3)① ②正反应方向 减小 不变 ③(2分)
17.(16分,每空2分)
(1)增大浓度,增大压强,增加生成物浓度等(合理即可)
(2)①0.015 ②小于 0.15
③小于 升高温度,增加,平衡逆向移动,所以正反应为放热反应
(3)③ a选择性最高是主反应①,反应条件变化是增大容器体积,副反应③随条件变化正向移动,选择性增加,所以b代表副反应③
18.(16分,除标注外每空2分)
(1)①2 1 增大(1分) ②减小(1分) ③ 大于(1分)
(2)①逆反应方向(1分) ②0.6 0.4
③降低甲醇的浓度、适当降低温度(忽略容器体积变化,合理即可)
化学
注意事项:
1. 本试卷共100分,考试时间75分钟。
2. 请将各题答案填在答题卡上。
可能用到的相对原子质量:H-1 Li-7 C-12 N-14 O-16 Mg-24 Al-27 S-32 Cl-35.5 V-51 Fe-56 Co-59 Cu-64 Zn-65
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1. 下列实验方案不能达到相应实验目的的是( )
A. 用装置①验证升高温度可以加快反应速率
B. 用装置②探究浓度对化学反应速率的影响
C. 用装置③比较、对分解速率的影响
D. 用装置④探究温度对化学平衡的影响
2. 在溶液中存在如下平衡: ,下列措施中能使平衡正向移动的是( )
A. 加热 B. 加压 C. 加 D. 加水稀释
3. 我国科学家通过对月壤样本的研究提出,未来在月球可利用月壤做催化剂进行人工光合作用,其中涉及的反应之一为(该条件下所有物质均为气态)。下列说法正确的是( )
A. 月壤可以改变该化学反应的限度
B. 通过控制反应条件,使和充分反应生成
C. 达平衡后,反应就停止了,正逆反应速率均为0
D. 将从体系中分离能减慢反应速率
4. 下列平衡常数的表达式书写正确的是( )
A.
B.
C.
D.
5. 工业合成氨 中,所采取的措施既有利于合成氨又能用勒夏特列原理解释的是( )
A. 高温 B. 高压 C. 加入催化剂 D. 原料气净化
6. 甲醇是重要的化工原料,应用前景广阔。研究表明,二氧化碳和氢气反应可以合成甲醇,反应如下: 。下列措施中能提高平衡时转化率的是( )
A. 升温 B. 等容下通入
C. 加压 D. 增大和的初始投料比
7. 反应体系中存在平衡:,下列操作不能使平衡发生移动的是( )
A. 加入少量铁粉 B. 加入浓KSCN溶液
C. 加 D. 升温
8. 某温度下,在一个2L的密闭容器中加入和进行如下反应:,反应2min后达到平衡,测得生成,下列说法正确的是( )
A. 前2min,C的平均反应速率为
B. 反应的前后压强之比为
C. 平衡时A的平衡转化率是70%
D. 增大压强,平衡正向移动,化学平衡常数增大
9. 下列说法正确的是( )
A. 冰在室温下能自动融化成水,这是熵增的过程 B. 吸热反应一定不能自发进行
C. 非自发反应一定不能实现 D. ,的反应,低温能自发进行
10. 在一个容积不变的密闭容器中发生反应:,已知:。若该反应在恒温()、恒容的密闭体系中进行,时测得的下列数据中,不可以作为判断t时刻反应是否达到平衡状态的依据的是( )
A. t时刻及其前后、、、的浓度
B. t时刻,、、、的浓度
C. t时刻及其前后容器中的压强
D. t时刻,消耗的速率与生成的速率
11. 在密闭容器中反应 达到平衡,下列操作能使容器内气体颜色变浅的是( )
A. 升高温度 B. 缩小容器体积
C. 容器体积不变,充入 D. 保持压强不变,充入氮气
12. 工业上苯乙烯的生产主要采用乙苯脱氢工艺:。某条件下无催化剂存在时,该反应的正、逆反应速率v随时间t的变化关系如图所示。下列说法正确的是( )
A. 时刻,、和的物质的量之比为
B. 该反应的
C. 反应进行到时,Q<K(Q为浓度商)
D. 催化剂存在时(其他条件不变),、和苯乙烯的平衡产率都增大
13. 是一种重要的化工原料,以HCl为原料,用氧化制取,可提高效益,减少污染。反应为:实验测得在不同压强下,总反应的HCl平衡转化率随温度变化的曲线如图,下列说法正确的是( )
A. 速率: B. 平衡常数:
C. D.
14. 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。在一定条件下,向某0.5L恒容密闭容器中充入和,发生反应 。测得在相同时间内,不同温度下的转化率如图1所示,图2表示正、逆反应的速率常数的对数与温度的倒数之间的关系:(已知速率方程,,、是速率常数,只受温度影响),下列说法中错误的是( )
图1 图2
A.
B. 升高温度,增大的倍数小于增大的倍数
C. 时,起始压强为2.5MPa,20min时达到平衡,若用单位时间内气体的分压的变化来表示反应速率,则0-20min内的平均速率(分压=总压×物质的量分数)
D. A、B、D、E分别代表图1中a点、c点的正、逆反应的,其中点D表示a点的
二、非选择题:本题共4小题,共58分。
15.(15分)某化学兴趣小组设计了如下实验定性与定量研究影响化学反应速率的因素,回答下列问题:
(1)定量测定化学反应的速率,装置如图1所示:
图1 图2
①写出检验装置气密性的方法:______。
②在装置B中加入固体,从装置A中加入的双氧水(),产生气体如图2所示:(不考虑溶液体积变化,气体体积已经转化为标准状况)
A、B、C、D各点产生的平均反应速率最大的是______(填字母)。用物质的量浓度的变化表示0~5min化学反应的平均速率______。
(2)探究浓度对化学反应速率的影响。
将3支试管分别编号为①②③,实验记录的数据如表所示。
试管编号 加溶液 加 加溶液 出现浑浊的时间
① 3mL 3mL 5滴 33s
② 2mL 5滴 28s
③ 5mL 5滴 16s
①该反应的化学方程式是____________。
②______,______。
③实验得出的结论是____________。
(3)把去掉氧化物膜的镁条投入到盛有盐酸的敞口容器里,产生的速率如图所示:
①写出时间T以前反应速率逐渐加快的原因是____________。
②写出时间T以后反应速率逐渐减慢的原因是____________。
16.(11分)勒夏特列原理是化学平衡移动的基本原理,在工农业生产中有着广泛的应用,回答下列问题:
(1)已知钾的金属性强于钠,选取适宜的温度,工业上可以利用钠制取钾,其反应原理为:,利用勒夏特列原理进行解释______。
(2)氮化硅()陶瓷能大幅度提高发动机的热效率,工业制备氮化硅陶瓷的反应原理为: 。
①在温度不变、体积恒定的密闭容器中加入、和,发生上述反应,不能表示上述反应达到化学平衡状态的是______(填字母)。
A. 混合气体的密度保持不变 B. HCl气体的物质的量分数保持不变
C. HCl的生成速率等于的消耗速率的六倍 D. 固体的质量不再发生变化
②能提高化学反应速率,同时能提高的平衡转化率可以采取的措施是____________(答出两条)。
(3)将纯净的氨基甲酸铵固体置于密闭真空容器中(容器体积可变,固体足量),在某温度下发生分解反应:,达到化学平衡状态。
①用物质的量浓度表示该反应的化学平衡常数表达式______。
②增大容器的体积,该化学平衡向______(填“正反应方向”“逆反应方向”或“不”)移动。再次达到化学平衡状态时,的质量______(填“减小”“增大”或“不变”,下同),______。
③在温度,压强为P的恒压容器中,该反应达到化学平衡状态,此时用平衡分压表示的平衡常数______。
17.(16分)氮氧化合物是大气污染物,利用甲烷()与反应可以消除氮氧化合物,反应如下: ,回答下列问题:
(1)为了加快化学反应速率,同时提高的平衡浓度,可以采取的措施是____________。
(2)温度为和时,在体积为2L的某刚性密闭容器中,加入和气体,发生上述反应,测得有关数据如表:
时间/min 0 10 20 40 50
0.50 0.35 0.25 0.10 0.10
0.50 0.30 0.218 a 0.15
①温度为时,在0~10min内用表示的平均反应速率______。
②温度______(填“大于”或“小于”),______mol。
③______0(填“大于”或“小于”),分析原因是____________。
(3)在,100kPa下用氦气作为稀释气体发生:
(主反应①)
同时能发生下列两个副反应:
(副反应②) (副反应③)
在以上反应体系中转化为、和NO的选择性用S表示(),各反应的的选择性S随平衡转化率的变化曲线如图所示:
其中曲线b代表的反应是______(填“①”、“②”或“③”),理由是____________。
18.(16分)空气中的、CO和是常见的大气污染物,合理利用可以变废为宝。回答下列问题:
(1)在某恒温刚性密闭容器中发生反应:
该反应的速率表达式为(k只与温度有关,m、n待测),时测得有关实验数据如下:
序号 速率
Ⅰ 0.0060 0.0010
Ⅱ 0.0060 0.0020
Ⅲ 0.0010 0.0060
Ⅳ 0.0020 0.0060
①______,______。若升高温度速率常数k将______(填“增大”“减小”或“不变”,下同)。
②该反应在时能自发进行反应,若升高温度该反应的化学平衡常数将______。
③该反应的基元反应可以表示为:
Ⅰ. ____________(慢) Ⅱ. (快)
写出反应Ⅰ的化学方程式____________。正反应的活化能Ⅰ______Ⅱ(填“大于”“小于”或“等于”)。
(2)一定温度下,在一体积可变的密闭容器中,充入和,发生反应Ⅰ.
Ⅱ.
达到平衡时,测定,。
①若缩小容器体积增大压强,反应Ⅱ将______(填“正反应方向”“逆反应方向”或“不”)移动。
②达到平衡时,可用气体的物质的量表示反应Ⅱ的化学平衡常数,在此表达式中______mol,______mol。
③为了提高甲醇的选择性,除使用高效催化剂和增大压强外,还可以采取的措施是____________。
尚义县2023-2024学年高二上学期9月月考
化学参考答案
1. A 【解析】A. ①中滴加了氯化铁溶液作催化剂,不能说明是温度的影响导致反应速率加快的,故A符合题意。
2. A 【解析】A. 该反应为吸热反应,升温,平衡正移,故A正确;
B. 改变压强只对有气体参加的反应有影响,故B错误;
D. 加水稀释,平衡逆移,故D错误。
3. D 【解析】A. 月壤做催化剂,催化剂可以加快化学反应速率,但不可以改变该化学反应的限度,故A错误;
B. 该反应是可逆反应,反应物不能完全转化为生成物,故和反应不可得到,故B错误;
D. 将从体系中分离,生成物浓度减小,减慢反应速率,故D正确。
4. C 【解析】化学平衡常数等于生成物的浓度幂次方的乘积与反应物浓度的幂次方的乘积比值,固体和纯液体不代入平衡常数。
A. 该反应平衡常数表达式为:,故A错误;
B. 该反应平衡常数表达式为:,故B错误;
D. 该反应平衡常数表达式为:,故D错误。
5. B 【解析】A. 升高温度,平衡逆移,氨气产率降低,不能用平衡移动原理解释,故A错误;
B. 增大压强,平衡正向移动,有利于提高原料转化率,能用平衡移动原理解释,故B正确;
C. 加入催化剂,平衡不移动,不能用平衡移动原理解释,故C错误;
D. 原料气净化是防止催化剂中毒,不能用勒夏特列原理解释,故D错误。
6. C 【解析】A. 该反应为放热反应,升温,平衡逆移,平衡时转化率减小,故A错误;
B. 等容下通入,平衡逆移,平衡时转化率减小,故B错误;
C. 该反应为气体体积减小的反应,加压,平衡正移,平衡时转化率增大,故C正确;
D. 增大和的初始投料比,平衡时转化率减小,转化率增大,故D错误。
7. C 【解析】该反应的实质为:,加平衡不移动。
8. B 【解析】
起始(mol) 4 2 0 0
转化(mol) 1.2 0.8 1.6 0.8
平衡(mol) 2.8 1.2 1.6 0.8
A. 由于C的状态是固体,不能用固体表示化学反应速率,故A错误;
B. 温度与体积一定时,压强之比等于物质的量之比,反应前后的压强之比为:,故B正确;
C. 达到平衡时,消耗,则A的转化率为,故C错误;
D. 增大压强,平衡正向移动,化学平衡常数不变,故D错误。
9. A 【解析】A. 同种物质的熵值:气态>液态>固态,故A正确;
D. 根据,反应自发进行,,的反应自发进行,需要在高温下进行,故D错误。
10. C 【解析】A. 对比t时刻及其前后、、、的浓度,当、、、的浓度不再变化的时候,说明达到化学平衡状态,故A不符合题意;
B. 知道t时刻、、、的浓度,代入公式Q,根据计算结果与的关系可判断是否达到化学平衡状态,即可以作为判断t时刻反应是否达到平衡状态的依据,故B不符合题意;
C. 该反应在反应过程中压强一直不变,测定t时刻及其前后容器中的压强无法判断是否达到化学平衡状态,即不可以作为判断t时刻反应是否达到平衡状态的依据,故C符合题意;
D. t时刻,消耗的速率是正反应方向的速率,生成的速率是逆反应方向的速率,若消耗的速率与生成的速率相等时,说明反应达到化学平衡状态,即可以作为判断t时刻反应是否达到平衡状态的依据,故D不符合题意。
11. D 【解析】A. 升高温度,平衡逆向移动,浓度增大,颜色变深,故A错误;
B、C能使平衡正向移动,但浓度增大,颜色变深,故B、C错误。
12. C 【解析】A. 时刻,反应达平衡,、和的物质的量之比不一定为,故A错误;
C. 反应进行到时,反应正向进行,故Q<K,故C正确;
D. 催化剂能降低反应的活化能,使反应的、都增大;催化剂不能使平衡移动,苯乙烯的平衡产率不变,故D错误。
13. B 【解析】A. 由图像可知反应温度:,故,故A错误;
B. 由于该反应的正反应是放热反应,在压强不变时,升高温度,化学平衡向吸热的逆反应方向移动,导致化学平衡常数减小。由图像可知反应温度:,所以化学平衡常数:,故B正确;
C. 该反应的正反应是气体体积缩小的反应,在其它条件不变时,增大压强,化学平衡向气体体积减小的正向移动,导致反应物HCl的转化率增大。由于在相同温度下HCl的转化率:,所以压强大小关系为:,故C错误;
D. 升高温度,HCl的平衡转化率降低,平衡逆向移动,正向为放热反应,故D错误。
14. D 【解析】根据图1可知,c的温度高于a点,温度高,反应速率快,则,故A不符合题意;
B. ,升高温度,平衡逆移,K减小,增大的倍数小于增大的倍数,故B不符合题意;
C. 时,起始压强2.5MPa,则的起始分压为,的起始分压为,20min时达到平衡,的转化率为80%,列三段式有
起始分压/MPa 1 1.5 0 0
变化分压/MPa 0.4 1.2 0.4 0.4
平衡分压/MPa 0.6 0.3 0.4 0.4
则,故C不符合题意;
D. 温度升高,正逆反应速率均增大,图中横坐标是温度的倒数,由右向左是升高温度,速率常数的对数随温度升高均是增大的,但温度对吸热反应方向速率影响更大,该反应逆向吸热,则逆反应方向的速率变化更大,斜率更大,A、E所在的这条线表示的是逆反应速率常数的对数与温度倒数的关系,由于a点温度较c点低,则E点表示a点的,故D符合题意。
15.(15分,除标注外每空2分)
(1)①关闭分液漏斗的活塞,轻轻向外拉动注射器的活塞,一段时间后,活塞能回到原来的位置,证明装置的气密性良好(合理即可得分)
②D(1分) 0.05
(2)① ②4(1分) 1(1分)
③其他条件不变时,增大反应物浓度能够加快化学反应速率(合理即可得分)
(3)①该反应为放热反应,T以前随着温度升高反应速率加快
②T以后,随着反应进行逐渐减小,反应速率逐渐变慢
16.(11分,除标注外每空1分)
(1)及时移走,降低生成物浓度,化学平衡正向移动,钠就能制取钾(2分,合理即可)
(2)①C ②升高温度,增大氮气或氢气的浓度(2分)
(3)① ②正反应方向 减小 不变 ③(2分)
17.(16分,每空2分)
(1)增大浓度,增大压强,增加生成物浓度等(合理即可)
(2)①0.015 ②小于 0.15
③小于 升高温度,增加,平衡逆向移动,所以正反应为放热反应
(3)③ a选择性最高是主反应①,反应条件变化是增大容器体积,副反应③随条件变化正向移动,选择性增加,所以b代表副反应③
18.(16分,除标注外每空2分)
(1)①2 1 增大(1分) ②减小(1分) ③ 大于(1分)
(2)①逆反应方向(1分) ②0.6 0.4
③降低甲醇的浓度、适当降低温度(忽略容器体积变化,合理即可)
同课章节目录
