人教版九年级上册化学5.3利用化学方程式的简单计算同步练习(含答案)
文档属性
| 名称 | 人教版九年级上册化学5.3利用化学方程式的简单计算同步练习(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 326.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-06 00:00:00 | ||
图片预览


文档简介
人教版九年级上册化学5.3利用化学方程式的简单计算同步练习
一、单选题
1.Fe2O3、ZnO、CuO的固体混合物9.6g,在一定条件下用足量的CO将其全部还原为金属单质,并将生成的二氧化碳用足量的澄清石灰水吸收,产生了10g白色沉淀,则原混合物中金属元素的总质量为
A.5.2g B.6.4g C.8g D.9g
2.甲和乙在一定条件下反应生成丙和丁,结合微观示意图分析,下列结论正确的是
A.该反应前后元素化合价均没有发生改变 B.该反应没有涉及到单质
C.反应前后原子和分子的种类均发生了改变 D.生成物丙和丁的质量比为9∶10
3.在化学反应A+B=C+D中,已知25gA跟10gB恰好完全反应,生成5gC,则10gA与足量的B反应,可生成D的质量为
A.12g B.8g C.10g D.4g
4.已知:在同温同压下,相同体积的任何气体所含的分子数目都相同。常温下二氧化硫气体和硫化氢气体混合,发生反应生成硫和水。现将一定体积的硫化氢和二氧化硫混合,充分反应,恢复到常温,若反应后气体的总体积是反应前的1/3,则原混合气体中硫化氢和二氧化硫的体积比可能为
A.1:5 B.2:3 C.4:5 D.2:1
5.现将足量氢气通过45g灼热的氧化铜和铜的混合物(铜和氢气不反应)。完全反应后称量剩余固体质量为37g。计算原混合物中氧化铜的质量为
A.20g B.32g C.40g D.42g
6.镁在氧气与氮气的混合气体中燃烧不仅生成氧化镁,还有少量的镁与氮气化合生成氮化镁(Mg3N2)。由此推知8g镁在氧气与氮气的混和气体中完全燃烧后所得产物的质量可能是
A.13.3g B.12g C.11.1g D.无法确定
7.以CO2和H2为原料合成C2H4是综合利用二氧化碳、实现“碳中和”的研究热点。相关反应的微观示意图如下所示。
关于该反应,下列说法正滩的是
A.参加反成的甲和乙的质量比为11:1 B.生成丙和丁的分子个数比为1:2
C.反应物和生成物共涉及两种氧化物 D.反应前后元素的化合价都不变
8.实验室有一瓶氢氧化钙和碳酸钙的混合物,某同学取一定量的样品于烧杯中,向其中加入73g质量分数20%的稀盐酸,恰好完全反应,测得烧杯中溶剂质量为63.8g,则反应过程中产生二氧化碳的质量为
A.2.2g B.3.3g C.4.4g D.6.6g
9.甲烷是天然气的主要成分。利用太阳能可将甲烷在高温熔融盐环境中转化为H2,反应原理如图所示,下列说法正确的是
A.整个过程中,只有Zn的化合价发生变化
B.过程①的化学反应为
C.理论上过程①与过程②中产生H2的质量比为1:2
D.当参加反应的CH4与H2O质量比为8:9时,理论上可不补充ZnO
10.将10g CaCO3固体煅烧一段时间,冷却后测得剩余固体中钙元素的质量分数为59.7%。下列说法错误的是
A.未分解CaCO3的质量是2.5 g
B.剩余固体的质量是6.7 g
C.煅烧过程中共产生CO2 3.3 g
D.剩余固体可能是纯净物
11.在反应2A+B=3C+D中,A和B的相对分子质量之比为5:1,已知20克A与一定量B恰好完全反应,生成5克D,则在此反应中B和C的质量比是
A.4:9 B.3:5 C.1:3 D.2:17
12.下列叙述完全符合质量守恒定律的是
A.水结成冰前后质量保持不变
B.50mL水和50mL乙醇混合后总体积小于100mL
C.在100g过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与4.8g氧气完全反应可生成4.4g二氧化碳
二、非选择题
13.在宏观、微观和符号之间建立联系是化学学科的特点。
(1)在一氧化碳、铁和氯化钠三种物质中,由分子构成的是 (填化学式)。
(2)在符号①Fe3+、②H2CO3、③中,表示阳离子的是 (填数字序号)。
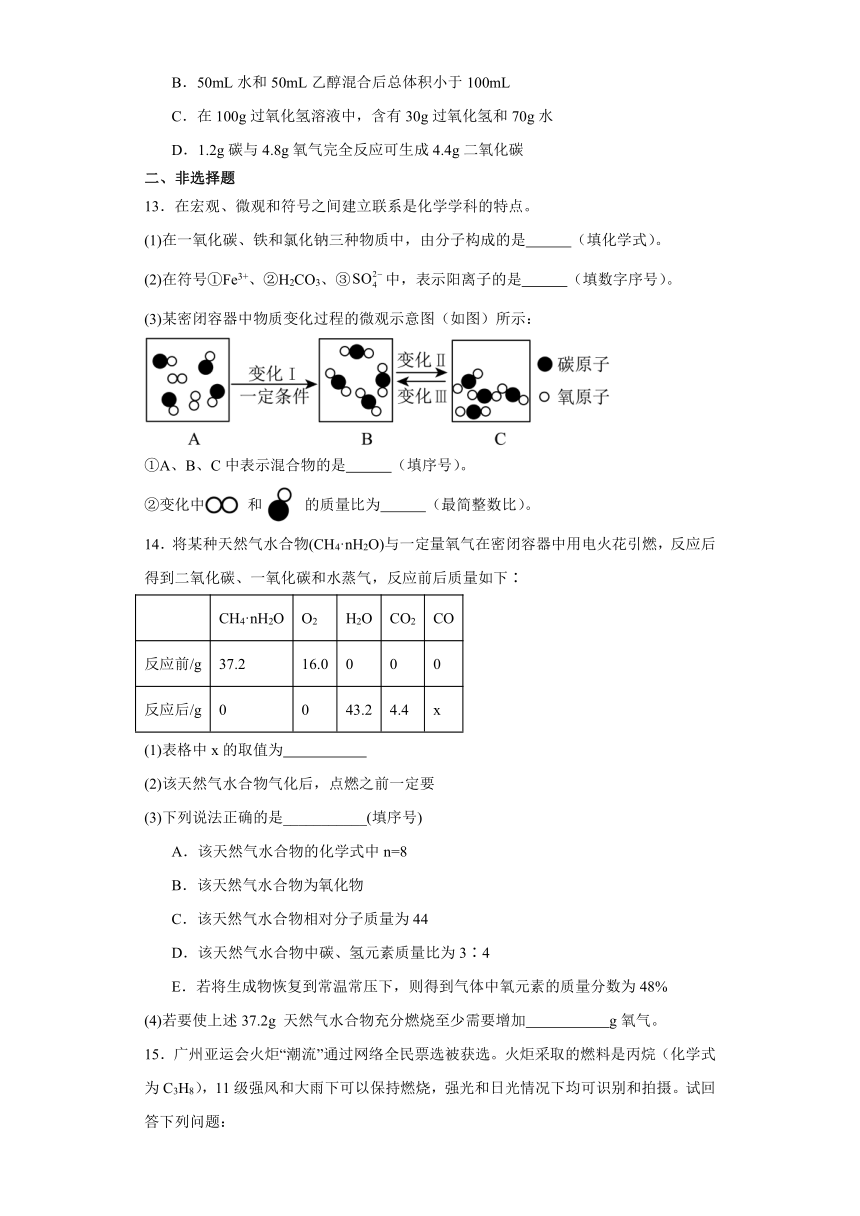
(3)某密闭容器中物质变化过程的微观示意图(如图)所示:
①A、B、C中表示混合物的是 (填序号)。
②变化中 和 的质量比为 (最简整数比)。
14.将某种天然气水合物(CH4·nH2O)与一定量氧气在密闭容器中用电火花引燃,反应后得到二氧化碳、一氧化碳和水蒸气,反应前后质量如下∶
CH4·nH2O O2 H2O CO2 CO
反应前/g 37.2 16.0 0 0 0
反应后/g 0 0 43.2 4.4 x
(1)表格中x的取值为
(2)该天然气水合物气化后,点燃之前一定要
(3)下列说法正确的是___________(填序号)
A.该天然气水合物的化学式中n=8
B.该天然气水合物为氧化物
C.该天然气水合物相对分子质量为44
D.该天然气水合物中碳、氢元素质量比为3∶4
E.若将生成物恢复到常温常压下,则得到气体中氧元素的质量分数为48%
(4)若要使上述37.2g 天然气水合物充分燃烧至少需要增加 g氧气。
15.广州亚运会火炬“潮流”通过网络全民票选被获选。火炬采取的燃料是丙烷(化学式为C3H8),11级强风和大雨下可以保持燃烧,强光和日光情况下均可识别和拍摄。试回答下列问题:
(1)亚运火炬的外壳主要材料轻薄高品质的铝合金材料。工业上制取金属铝的方法是:通电分解氧化铝(Al2O3)得到单质铝,同时生成了氧气。则反应的化学方程式为 ,发生反应的基本类型是 。
(2)当火炬点燃后,所发生反应的化学方程式为 ,所用燃料符合“绿色亚运”的要求,原因是 。
(3)我国游泳健将张琳是广州亚运首棒火炬手,他从国家主席胡锦涛手中接过的火炬“潮流”,在规定时间内燃烧丙烷在标准状况下体积为16.7L,丙烷的密度为1.98g/L,则完全燃烧可生成水的质量是多少?
16.神舟十一号飞船与天宫二号交会对接。太空中可使用过氧化钠作为氧气再生剂,Na2O2是一种淡黄色固体,常温下能与水和二氧化碳发生化学反应。
(1)在常温下,过氧化钠Na2O2能与航天员呼出的CO2反应生成碳酸钠和氧气,发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,可是有同学认为该反应还可能生成碳酸氢钠(化学式为NaHCO3)和氧气,你认为他的说法是否正确,请简述你的看法和理由 。
(2)常温下,过氧化钠也能与水发生反应,可以产生氧气,同时生成氢氧化钠,请写出该反应的化学方程式为 ;
(3)若中国空间站内两位航天员在一定时间内所排出CO2的质量为88g,完全吸收这些排出物,则需要消耗过氧化钠的质量为 g,同时产生通常状况下氧气的体积为 L(通常状况下的氧气密度为1.43g/L,计算结果确到0.1)。
参考答案:
1.C
2.D
3.A
4.C
5.C
6.B
7.C
8.C
9.D
10.D
11.D
12.D
13.(1)CO
(2)①
(3) A 4:7
14.(1)5.6
(2)检验纯度
(3)D
(4)解:设若要使上述37.2g 天然气水合物充分燃烧至少需要氧气的质量为x。
x=19.2g
19.2g-16.0g=3.2g
答:若要使上述37.2g 天然气水合物充分燃烧至少需要增加氧气的质量为3.2g。
15. 分解反应 当丙烷完全燃烧生成水和二氧化碳,则不会污染空气 54g
16. 不正确;因为反应物中不含H元素 156 22.4
一、单选题
1.Fe2O3、ZnO、CuO的固体混合物9.6g,在一定条件下用足量的CO将其全部还原为金属单质,并将生成的二氧化碳用足量的澄清石灰水吸收,产生了10g白色沉淀,则原混合物中金属元素的总质量为
A.5.2g B.6.4g C.8g D.9g
2.甲和乙在一定条件下反应生成丙和丁,结合微观示意图分析,下列结论正确的是
A.该反应前后元素化合价均没有发生改变 B.该反应没有涉及到单质
C.反应前后原子和分子的种类均发生了改变 D.生成物丙和丁的质量比为9∶10
3.在化学反应A+B=C+D中,已知25gA跟10gB恰好完全反应,生成5gC,则10gA与足量的B反应,可生成D的质量为
A.12g B.8g C.10g D.4g
4.已知:在同温同压下,相同体积的任何气体所含的分子数目都相同。常温下二氧化硫气体和硫化氢气体混合,发生反应生成硫和水。现将一定体积的硫化氢和二氧化硫混合,充分反应,恢复到常温,若反应后气体的总体积是反应前的1/3,则原混合气体中硫化氢和二氧化硫的体积比可能为
A.1:5 B.2:3 C.4:5 D.2:1
5.现将足量氢气通过45g灼热的氧化铜和铜的混合物(铜和氢气不反应)。完全反应后称量剩余固体质量为37g。计算原混合物中氧化铜的质量为
A.20g B.32g C.40g D.42g
6.镁在氧气与氮气的混合气体中燃烧不仅生成氧化镁,还有少量的镁与氮气化合生成氮化镁(Mg3N2)。由此推知8g镁在氧气与氮气的混和气体中完全燃烧后所得产物的质量可能是
A.13.3g B.12g C.11.1g D.无法确定
7.以CO2和H2为原料合成C2H4是综合利用二氧化碳、实现“碳中和”的研究热点。相关反应的微观示意图如下所示。
关于该反应,下列说法正滩的是
A.参加反成的甲和乙的质量比为11:1 B.生成丙和丁的分子个数比为1:2
C.反应物和生成物共涉及两种氧化物 D.反应前后元素的化合价都不变
8.实验室有一瓶氢氧化钙和碳酸钙的混合物,某同学取一定量的样品于烧杯中,向其中加入73g质量分数20%的稀盐酸,恰好完全反应,测得烧杯中溶剂质量为63.8g,则反应过程中产生二氧化碳的质量为
A.2.2g B.3.3g C.4.4g D.6.6g
9.甲烷是天然气的主要成分。利用太阳能可将甲烷在高温熔融盐环境中转化为H2,反应原理如图所示,下列说法正确的是
A.整个过程中,只有Zn的化合价发生变化
B.过程①的化学反应为
C.理论上过程①与过程②中产生H2的质量比为1:2
D.当参加反应的CH4与H2O质量比为8:9时,理论上可不补充ZnO
10.将10g CaCO3固体煅烧一段时间,冷却后测得剩余固体中钙元素的质量分数为59.7%。下列说法错误的是
A.未分解CaCO3的质量是2.5 g
B.剩余固体的质量是6.7 g
C.煅烧过程中共产生CO2 3.3 g
D.剩余固体可能是纯净物
11.在反应2A+B=3C+D中,A和B的相对分子质量之比为5:1,已知20克A与一定量B恰好完全反应,生成5克D,则在此反应中B和C的质量比是
A.4:9 B.3:5 C.1:3 D.2:17
12.下列叙述完全符合质量守恒定律的是
A.水结成冰前后质量保持不变
B.50mL水和50mL乙醇混合后总体积小于100mL
C.在100g过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与4.8g氧气完全反应可生成4.4g二氧化碳
二、非选择题
13.在宏观、微观和符号之间建立联系是化学学科的特点。
(1)在一氧化碳、铁和氯化钠三种物质中,由分子构成的是 (填化学式)。
(2)在符号①Fe3+、②H2CO3、③中,表示阳离子的是 (填数字序号)。
(3)某密闭容器中物质变化过程的微观示意图(如图)所示:
①A、B、C中表示混合物的是 (填序号)。
②变化中 和 的质量比为 (最简整数比)。
14.将某种天然气水合物(CH4·nH2O)与一定量氧气在密闭容器中用电火花引燃,反应后得到二氧化碳、一氧化碳和水蒸气,反应前后质量如下∶
CH4·nH2O O2 H2O CO2 CO
反应前/g 37.2 16.0 0 0 0
反应后/g 0 0 43.2 4.4 x
(1)表格中x的取值为
(2)该天然气水合物气化后,点燃之前一定要
(3)下列说法正确的是___________(填序号)
A.该天然气水合物的化学式中n=8
B.该天然气水合物为氧化物
C.该天然气水合物相对分子质量为44
D.该天然气水合物中碳、氢元素质量比为3∶4
E.若将生成物恢复到常温常压下,则得到气体中氧元素的质量分数为48%
(4)若要使上述37.2g 天然气水合物充分燃烧至少需要增加 g氧气。
15.广州亚运会火炬“潮流”通过网络全民票选被获选。火炬采取的燃料是丙烷(化学式为C3H8),11级强风和大雨下可以保持燃烧,强光和日光情况下均可识别和拍摄。试回答下列问题:
(1)亚运火炬的外壳主要材料轻薄高品质的铝合金材料。工业上制取金属铝的方法是:通电分解氧化铝(Al2O3)得到单质铝,同时生成了氧气。则反应的化学方程式为 ,发生反应的基本类型是 。
(2)当火炬点燃后,所发生反应的化学方程式为 ,所用燃料符合“绿色亚运”的要求,原因是 。
(3)我国游泳健将张琳是广州亚运首棒火炬手,他从国家主席胡锦涛手中接过的火炬“潮流”,在规定时间内燃烧丙烷在标准状况下体积为16.7L,丙烷的密度为1.98g/L,则完全燃烧可生成水的质量是多少?
16.神舟十一号飞船与天宫二号交会对接。太空中可使用过氧化钠作为氧气再生剂,Na2O2是一种淡黄色固体,常温下能与水和二氧化碳发生化学反应。
(1)在常温下,过氧化钠Na2O2能与航天员呼出的CO2反应生成碳酸钠和氧气,发生反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2,可是有同学认为该反应还可能生成碳酸氢钠(化学式为NaHCO3)和氧气,你认为他的说法是否正确,请简述你的看法和理由 。
(2)常温下,过氧化钠也能与水发生反应,可以产生氧气,同时生成氢氧化钠,请写出该反应的化学方程式为 ;
(3)若中国空间站内两位航天员在一定时间内所排出CO2的质量为88g,完全吸收这些排出物,则需要消耗过氧化钠的质量为 g,同时产生通常状况下氧气的体积为 L(通常状况下的氧气密度为1.43g/L,计算结果确到0.1)。
参考答案:
1.C
2.D
3.A
4.C
5.C
6.B
7.C
8.C
9.D
10.D
11.D
12.D
13.(1)CO
(2)①
(3) A 4:7
14.(1)5.6
(2)检验纯度
(3)D
(4)解:设若要使上述37.2g 天然气水合物充分燃烧至少需要氧气的质量为x。
x=19.2g
19.2g-16.0g=3.2g
答:若要使上述37.2g 天然气水合物充分燃烧至少需要增加氧气的质量为3.2g。
15. 分解反应 当丙烷完全燃烧生成水和二氧化碳,则不会污染空气 54g
16. 不正确;因为反应物中不含H元素 156 22.4
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
