第2章 物质转化与材料利用 精品作业测试卷(图像题,含答案)
文档属性
| 名称 | 第2章 物质转化与材料利用 精品作业测试卷(图像题,含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 526.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2023-10-07 00:00:00 | ||
图片预览


文档简介
2023初三《科学》第二章精品作业测试卷
(图像题)
一.选择题(共15小题)
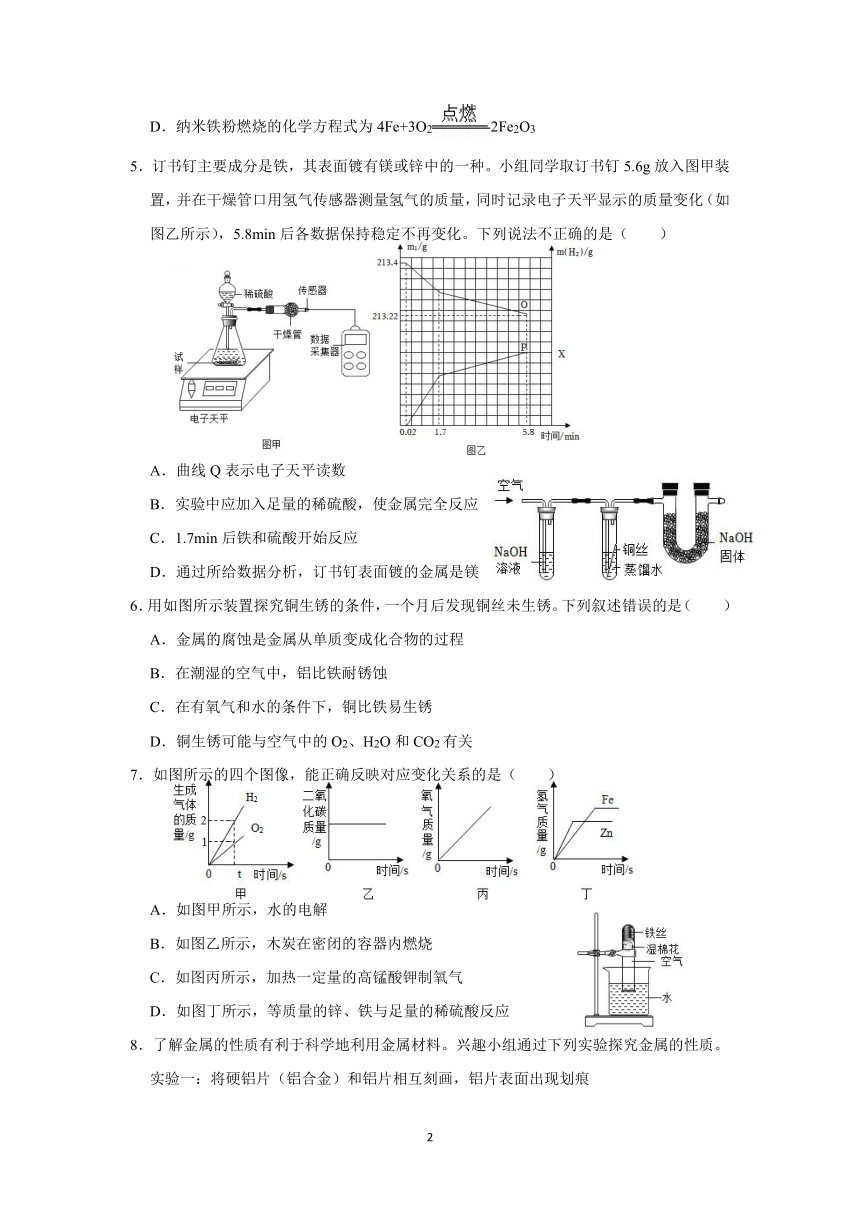
1.为验证铜与稀硝酸反应的还原产物是NO而不是NO2。某同学设计了如图所示的装置,下列叙述错误的是( )
A.应先打开活塞,再从U形管右侧加入稀硝酸
B.加入的稀硝酸应充满U形管左侧
C.关闭活塞后铜丝会全部溶解
D.反应停止后打开活塞,气体变成红棕色
2.下图是木炭在氧气中燃烧的实验示意图,以下说法正确的是( )
A.夹持木炭的仪器是镊子
B.木炭在氧气中燃烧发出白光
C.红热木炭伸入瓶中快速伸到底
D.木炭燃烧生成白灰
3.搞怪化学衫、创意元素钟表等也有化学用语,以下分析正确的是( )
A.图1衬衫的“Fe”与稀硫酸反应后生成硫酸铁:FeSO4
B.创意钟表里全是非金属元素
C.图3衬衫表示的化学方程式:Mg+ZnSO4=MgSO4+Zn
D.图4对应的微粒符号:Na+
4.纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧,生成一种黑色的氧化物,如图是纳米铁粉在锥形瓶中燃烧的实验。下列说法错误的是( )
A.激光手电照射使纳米铁粉温度达到着火点
B.锥形瓶中放水可防止生成物溅落炸裂瓶底
C.气球先变大,说明该反应为放热反应
D.纳米铁粉燃烧的化学方程式为4Fe+3O22Fe2O3
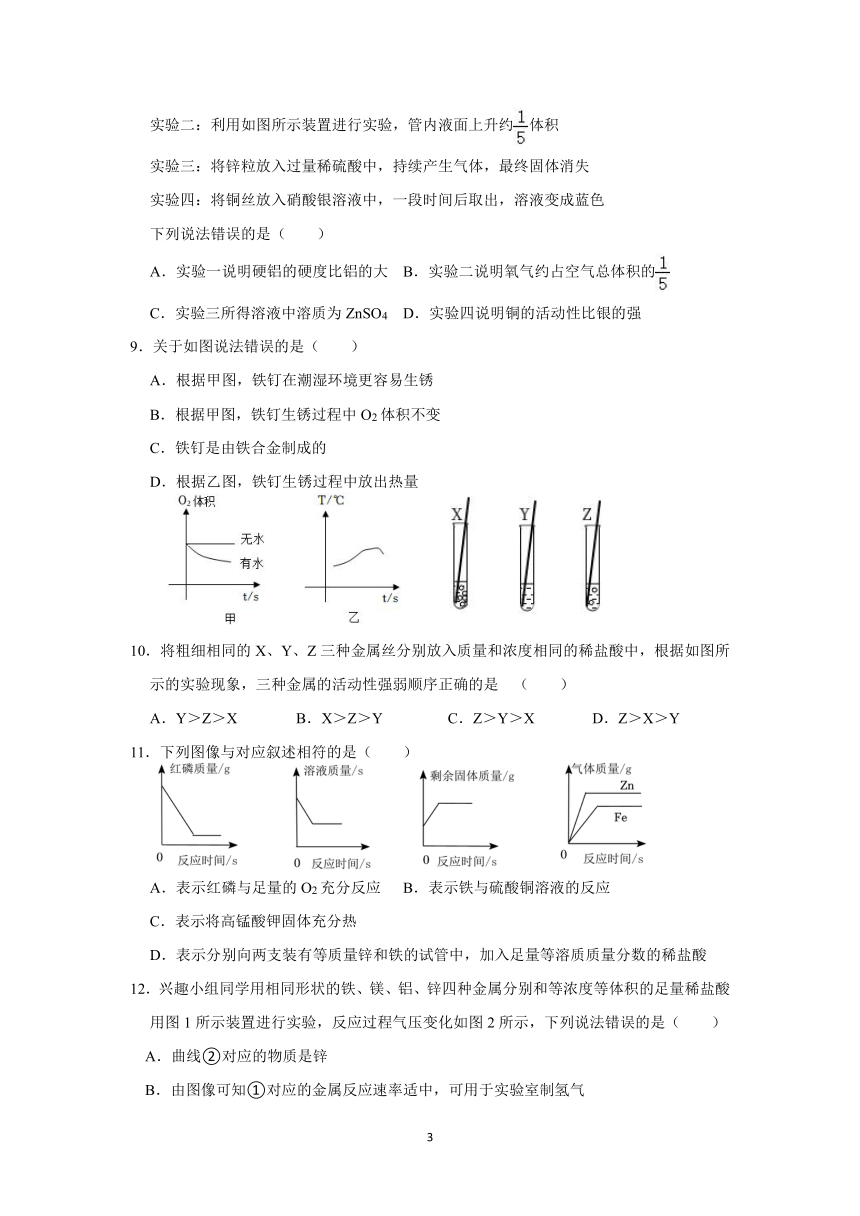
5.订书钉主要成分是铁,其表面镀有镁或锌中的一种。小组同学取订书钉5.6g放入图甲装置,并在干燥管口用氢气传感器测量氢气的质量,同时记录电子天平显示的质量变化(如图乙所示),5.8min后各数据保持稳定不再变化。下列说法不正确的是( )
A.曲线Q表示电子天平读数
B.实验中应加入足量的稀硫酸,使金属完全反应
C.1.7min后铁和硫酸开始反应
D.通过所给数据分析,订书钉表面镀的金属是镁
6.用如图所示装置探究铜生锈的条件,一个月后发现铜丝未生锈。下列叙述错误的是( )
A.金属的腐蚀是金属从单质变成化合物的过程
B.在潮湿的空气中,铝比铁耐锈蚀
C.在有氧气和水的条件下,铜比铁易生锈
D.铜生锈可能与空气中的O2、H2O和CO2有关
7.如图所示的四个图像,能正确反映对应变化关系的是( )
A.如图甲所示,水的电解
B.如图乙所示,木炭在密闭的容器内燃烧
C.如图丙所示,加热一定量的高锰酸钾制氧气
D.如图丁所示,等质量的锌、铁与足量的稀硫酸反应
8.了解金属的性质有利于科学地利用金属材料。兴趣小组通过下列实验探究金属的性质。
实验一:将硬铝片(铝合金)和铝片相互刻画,铝片表面出现划痕
实验二:利用如图所示装置进行实验,管内液面上升约体积
实验三:将锌粒放入过量稀硫酸中,持续产生气体,最终固体消失
实验四:将铜丝放入硝酸银溶液中,一段时间后取出,溶液变成蓝色
下列说法错误的是( )
A.实验一说明硬铝的硬度比铝的大 B.实验二说明氧气约占空气总体积的
C.实验三所得溶液中溶质为ZnSO4 D.实验四说明铜的活动性比银的强
9.关于如图说法错误的是( )
A.根据甲图,铁钉在潮湿环境更容易生锈
B.根据甲图,铁钉生锈过程中O2体积不变
C.铁钉是由铁合金制成的
D.根据乙图,铁钉生锈过程中放出热量
10.将粗细相同的X、Y、Z三种金属丝分别放入质量和浓度相同的稀盐酸中,根据如图所示的实验现象,三种金属的活动性强弱顺序正确的是 ( )
A.Y>Z>X B.X>Z>Y C.Z>Y>X D.Z>X>Y
11.下列图像与对应叙述相符的是( )
A.表示红磷与足量的O2充分反应 B.表示铁与硫酸铜溶液的反应
C.表示将高锰酸钾固体充分热
D.表示分别向两支装有等质量锌和铁的试管中,加入足量等溶质质量分数的稀盐酸
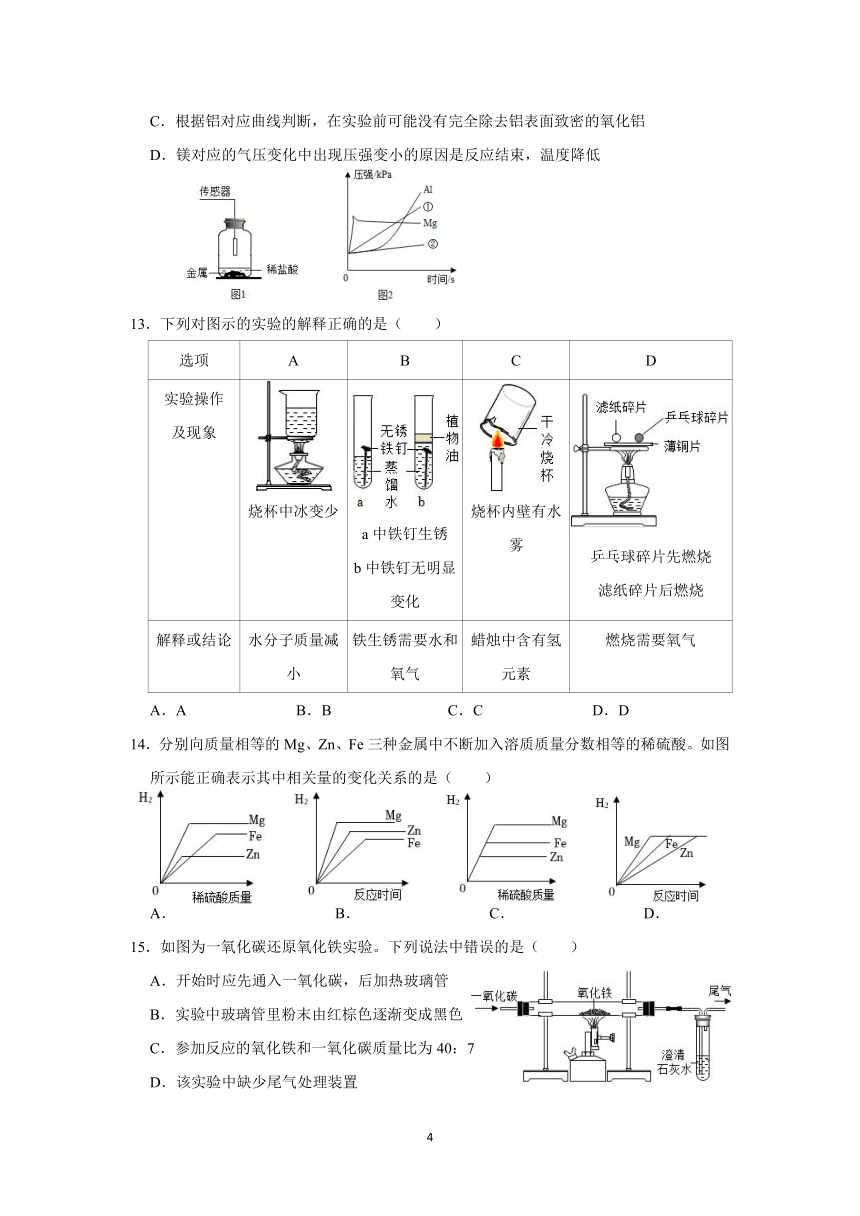
12.兴趣小组同学用相同形状的铁、镁、铝、锌四种金属分别和等浓度等体积的足量稀盐酸用图1所示装置进行实验,反应过程气压变化如图2所示,下列说法错误的是( )
A.曲线②对应的物质是锌
B.由图像可知①对应的金属反应速率适中,可用于实验室制氢气
C.根据铝对应曲线判断,在实验前可能没有完全除去铝表面致密的氧化铝
D.镁对应的气压变化中出现压强变小的原因是反应结束,温度降低
13.下列对图示的实验的解释正确的是( )
选项 A B C D
实验操作 及现象 烧杯中冰变少 a中铁钉生锈 b中铁钉无明显变化 烧杯内壁有水雾 乒乓球碎片先燃烧 滤纸碎片后燃烧
解释或结论 水分子质量减小 铁生锈需要水和氧气 蜡烛中含有氢元素 燃烧需要氧气
A.A B.B C.C D.D
14.分别向质量相等的Mg、Zn、Fe三种金属中不断加入溶质质量分数相等的稀硫酸。如图所示能正确表示其中相关量的变化关系的是( )
B. C. D.
15.如图为一氧化碳还原氧化铁实验。下列说法中错误的是( )
A.开始时应先通入一氧化碳,后加热玻璃管
B.实验中玻璃管里粉末由红棕色逐渐变成黑色
C.参加反应的氧化铁和一氧化碳质量比为40:7
D.该实验中缺少尾气处理装置
二.填空题(共8小题)
16.甲、乙两图分别表示硫、铁丝在氧气中燃烧的示意图。
(1)图乙中夹持铁丝的仪器名称是 ,图甲中发生
的化学反应的化学方程式为 。
(2)图甲中水的作用是 (填字母,下同);图乙中水的作用是 。
A.吸收热量 B.隔绝空气 C.吸收有害气体 D.防止生成物掉落炸裂瓶底
(3)图乙中的铁丝绕成螺旋状的原因是 (填字母)。
A.美观 B.增大受热面积,更易引燃 C.方便夹持
17.人体中质量分数在0.01%以下的元素称为微量元素。如图表示部分元素在人体中的质量分数及有关元素信息。
(1)图1中钙元素为 (填“常量”或“微量”)元素;人体缺乏钙元素会患有的疾病是 。
(2)图2为钠原子结构示意图,在化学反应中钠原子容易 (填“得”或“失”)电子,形成的离子符号为 。
(3)以铁元素为主要成分的生铁比纯铁硬度 (填“大”或“小”)。
(4)钾在空气中加热发生化合反应生成超氧化钾(KO2)的化学方程式为
。
18.有限的元素可以组成种类繁多的物质,依据表中的元素回答下列问题。
元素名称 钠 钙 氧 氯 碳 氢
元素符号 Na Ca O Cl C H
(1)写出厨房里常见的一种调味品的名称是 。
(2)若某物质可以改良酸性土壤,则该物质的化学式为 。
(3)生成物全为单质的分解反应是 。
(4)A、B、C、D都是由上表中的元素组成的常见物质。其中C是钠盐,且C、D都是由三种元素组成,B的固体升华时可作制冷剂。他们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“→”表示某一种物质经一步反应可转化为另一种物质)。
①图中反应③的化学方程式可以为 。
②A物质可以是 (填字母序号)。
a.单质 b.氧化物 c.酸 d.碱 e.盐
19.金属材料在生产、生活中有越来越广泛的用途。
(1)下列物质中属于金属材料的是 (填序号)。
①四氧化三铁 ②硫酸铜 ③不锈钢 ④生铁 ⑤铝合金 ⑥焊锡
(2)铁是生产、生活中使用最多的金属材料。铁生锈的必要条件是 。
(3)图甲是探究影响铁锈蚀快慢因素的实验。为了探究氯化钠是否可以加快铁的锈蚀,试管①中的物质X和试管②中的物质Y分别是 。
(4)图乙是金属性质的实验。步骤①体现了铜具有 性,步骤②验证了三种金属活动性强弱的依据是 。
20.A~E是初中化学常见的物质,它们之间的转化关系如图(部分物质已略去)。已知A、B组成元素相同且常温下均为液体;D是相对分子质量为16的含碳化合物。则A转化为B的化学方程式为 ;C转化为B的化学方程式为
;C的一种用途是 。
21.金属材料广泛应用于生活和生产中。
(1)不法分子常用假“金元宝”(铜锌合金)蒙骗人们,下列鉴别真假元宝办法中错误的是 。A.加盐酸 B.测密度 C.用火烧 D.看颜色
(2)某化学兴趣小组同学在实验室将一定质量的锌粉放入盛有硝酸银、硝酸铜和硝酸镁的混合溶液中,充分反应后过滤,得到滤渣和滤液,滤液呈无色。
①滤渣中可能含有的金属是 。②滤液中一定含有的阳离子是 。
(3)往盛有4.0g久置的铝片的烧杯中滴加稀盐酸,让其充分反应,放出氢气的质量与所滴加稀盐酸的质量关系如图所示。请回答下列问题并计算:
①刚开始滴加稀盐酸时,没有氢气放出的原因是 。
②该铝片中铝的质量分数为 。
22.“价﹣﹣类”二维图可表示元素化合价与物质类别之间的关系,图中a、b、c、d、e、f代表常见的含碳物质。
(1)a是沼气的主要成分,写出它燃烧的化学方程式 。
(2)下列关于物质及其转化的说法中与事实相符的有 。
①b和d反应生成c;②d和水反应生成e;③物质f可能难溶于水;
④由b到f至少要经过三步反应;⑤由f到d实现一步转化只能通过与酸反应来实现
23.金属及金属材料具有广泛的应用。
Ⅰ.纽扣电池是生活中常用的电源。纽扣电池的金属外壳可以加工得很薄,说明金属具有
性。
Ⅱ.运用手持技术探究金属与酸的反应。向250mL的烧瓶内注入25mL某浓度的稀硫酸(足量),分别剪取相同长度和宽度、质量的镁、铝、锌、铁、铜金属片,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡皮塞(见图1),点击采集,得到如图2所示的变化曲线。
(1)曲线b对应的金属是铁,反应的化学方程式为 。
(2)下列说法不正确的是 (填字母)。
A.曲线a对应的金属是铜。B.曲线d对应的反应速率适中适合实验室制取气体。
C.曲线e在0~100s段几乎没有上升,可能是该金属活动性比较弱。
D.曲线c在18s左右达到最高点后又略下降的原因是反应结束,温度降低,压强下降。
E.如延长横坐标时间,曲线c、d、e最终将交于一点。
三.科学探究题(共4小题)
24.金属材料的广泛应用,极大地促进了社会发展。某小组同学以“认识金属”为主题开展学习。(一)认识金属的化学性质活动一:验证金属活动性
(1)如图1实验,发现铜、铁两种金属与稀硫酸反应现象不同,原因是 。
(2)除上述实验外,验证铜、铁两种金属活动性强弱关系,还可以使用的试剂为 。
活动二:探究金属与氧气反应的快慢
如表数据是在一定温度下,相同形状的金属镁和镍分别在表面生成氧化物薄膜的实验记录:
反应时间/h 1 4 9 16 25
镁表面氧化薄膜层厚/nm 0.05a 0.2a 0.45a 0.8a 1.25a
镍表面氧化薄膜层厚/nm b 2b 3b 4b 5b
注:a和b均为与温度有关的常数,nm表示纳米。
(3)镁与镍比较, 生成氧化物薄膜的速度更快。
(二)认识金属的制备
如图2是实验室模拟工业炼铁的装置。
(1)实验过程中,装置A玻璃管中发生反应的化学方程式为 。
(2)装置B的作用有:检验二氧化碳; 。
(三)认识金属的锈蚀
如图3所示,若要探究铁生锈的条件,还应该补充的实验是 (可“文字叙述”或“画图”)。
25.铁是现代化学工业的基础,人类进步所必不可少的金属材料。
(1)看图1回答,铁元素为 元素(填“金属或非金属”)。
(2)健康人体内,总量4~5g的铁元素主要以化合物形式存在,缺铁会患 (填字母)。a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
【实验一】兴趣小组通过图2实验研究铁的冶炼
(3)该装置有一明显不当之处,你的改进方案是 。
(4)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式 。
(5)实验一段时间后,观察到B处澄清石灰水变 ,A处红棕色固体变为黑色,小明将所得的黑色固体物质放入足量的稀盐酸中,发现有少量气泡。写出反应的化学方程式 。
【资料1】已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。
Fe2O3Fe3O4FeOFe
【资料2】实验研究表明:该实验得到是四氧化三铁与铁粉的混合物。同时实验说明温度对CO和Fe2O3反应有影响。
【实验二】兴趣小组继续用图3实验研究一氧化碳和四氧化三铁的反应
【资料3】氢氧化钠溶液可以与二氧化碳反应,吸收二氧化碳。
(6)从安全与规范的角度考虑,装置C后面应连接 (选填装置序号)。
(7)四氧化三铁的质量为2.32g,充分反应。请计算产生单质铁的质量。(写出解题过程)
26.某兴趣小组为证明CO作还原剂表现还原性,采用如图所示装置进行实验。
【查询资料】
Ⅰ.用甲酸与浓硫酸微热可生成CO,化学方程为HCOOHCO↑+H2O。
Ⅱ.HCOOH:熔点8.6℃,沸点100.8℃。
【实验装置】
请回答:
(1)仪器a的名称是 ,仪器b的名称是 ;
(2)该兴趣小组方框A中需选择 (填“A1”、“A2”或“A3”)装置生成CO气体,然后与B装置对接完成实验;
(3)写出B装置硬质玻璃管中发生反应的化学方程式 ;
(4)B装置硬质玻璃管中的现象是 ,从C装置中出现
现象同样可以证明CO具有还原性;
(5)该小组经过交流讨论,得出该装置存在一定缺陷,具体是 。
27.金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。
【探索性质】
(1)河南省博物院展馆中的汉代金缕玉衣是我国重要的黄金文物。金缕玉衣所用的金丝直径仅为0.08mm,金能制成金丝是利用了其 性。
(2)铁、铜、银是初中化学实验中常见的金属,以下实验可以判断三种金属的活动性顺序,则金属A为 。
【变废为宝】(3)近年来,我国非常重视“绿色发展”,为减少污染并变废为宝,某化学兴趣小组在实验室模拟探究工业废水的综合利用时,设计了以下流程图并完成了回收铜和硫酸锌的实验。
①加入过量A时发生的反应方程式是 。
②固体X的成分是 。
③若试剂B为稀硫酸,可以判断稀硫酸适量的现象是 。
【模拟炼铁】(4)当今,“有一种速度叫中国速度,
有一种骄傲叫中国高铁”,修建高铁需要消耗大量的钢铁,
下列为实验室模拟炼铁并检验气体产物的实验。
①A装置玻璃管内反应的现象为 。
②从环保角度考虑,尾气的处理方法除了点燃,还可以收集,收集尾气的方法最好为 (填“向上排空气法”“向下排空气法”或“排水法”)。
【工业应用】
(5)铝的利用距今还不到200年,现在铝的年产量得到大幅度的提高。工业上可利用“铝热反应”焊接钢轨,其原理是在高温下铝与氧化铁反应生成铁和氧化铝。若用10.8kg铝与氧化铁反应来制取铁,理论上生成铁的质量是多少?
2023初三《科学》第二章精品作业测试卷
(图像题)参考答案与试题解析
一.选择题(共15小题)
1.C。2.B。3.C。4.D。5.D。6.C。7.D。8.C。9.B。10.B。
11.B。12.A。13.C。14.C。15.C。
一.填空题(共8小题)
16.(1)坩埚钳;铁+氧气四氧化三铁。(2)C;D。(3)B。
17.(1)常量;佝偻病、骨质疏松;(2)失;Na+;(3)大;(4)K+O2KO2。
18.(1)氯化钠或醋酸等;(2)Ca(OH)2;(3)2H2O2H2↑+O2↑;
(4)①Na2CO3+2HCl═2NaCl+H2O+CO2↑;②abce。
19.(1)③④⑤⑥;(2)铁与水、氧气同时接触;(3)X是氧气,Y是氯化钠溶液;
(4)延展;在金属活动性顺序表中,前面的金属和后面金属的盐溶液反应,把其从盐溶液中置换出来,A试管无明显现象,说明铁比铜活泼;B试管铜丝表面变银白色,无色溶液变蓝色,说明铜比银活泼。
20.2H2O22H2O+O2↑;CO2+2NaOH=Na2CO3+H2O(合理即可);灭火。
21.(1)D;(2)①锌;②Zn2+、Mg2+;(3)①铝片表面有一层致密的氧化铝薄膜,稀盐酸先和氧化铝反应生成氯化铝和水;②90%。
22.(1)CH4+2O2CO2+2H2O;(2)①②③。
23.Ⅰ、延展;Ⅱ、(1)Fe+2HCl=FeCl2+H2↑;(2)CE。
三.科学探究题(共4小题)
24.(一)(1)在金属活动性顺序中,铁排在氢前面,铜排在氢后面;(2)铁与硫酸铜溶液(合理即可);(3)镁或Mg;
(二)(1)Fe2O3+3CO2Fe+3CO2;
(2)收集一氧化碳,防止一氧化碳扩散到空气中,污染空气;
(三)A试管中的铁钉与氧气和水同时接触,发生锈蚀;B试管中的铁钉
只与氧气接触,没有锈蚀,还需要设计一个铁钉只与水接触的对比实验,探究铁的锈蚀是否与水有关,图示为;故答案为:将无锈的铁钉全部浸没在煮沸迅速冷却后的蒸馏水中,水面上用植物油液封或。
25.(1)金属;(2)c;(3)在末端加一个燃着的酒精灯;(4)Fe2O3+3CO2Fe+3CO2;
(5)浑浊;Fe+2HCl=FeCl2+H2↑;(6)E;(7)1.68g。
26.(1)分液漏斗;锥形瓶;(2)A2;(3)CO+CuOCu+CO2;
(4)黑色固体变为红色;澄清石灰水变浑浊;(5)C装置后面缺少尾气处理装置。
27.(1)延展;(2)铜(或Cu);
(3)①Zn+CuSO4=ZnSO4+Cu;②Cu、Zn;③逐滴滴加稀硫酸至不再有气泡产生为止;
(4)①红棕色粉末变黑色;②排水法;(5)22.4kg。
(图像题)
一.选择题(共15小题)
1.为验证铜与稀硝酸反应的还原产物是NO而不是NO2。某同学设计了如图所示的装置,下列叙述错误的是( )
A.应先打开活塞,再从U形管右侧加入稀硝酸
B.加入的稀硝酸应充满U形管左侧
C.关闭活塞后铜丝会全部溶解
D.反应停止后打开活塞,气体变成红棕色
2.下图是木炭在氧气中燃烧的实验示意图,以下说法正确的是( )
A.夹持木炭的仪器是镊子
B.木炭在氧气中燃烧发出白光
C.红热木炭伸入瓶中快速伸到底
D.木炭燃烧生成白灰
3.搞怪化学衫、创意元素钟表等也有化学用语,以下分析正确的是( )
A.图1衬衫的“Fe”与稀硫酸反应后生成硫酸铁:FeSO4
B.创意钟表里全是非金属元素
C.图3衬衫表示的化学方程式:Mg+ZnSO4=MgSO4+Zn
D.图4对应的微粒符号:Na+
4.纳米铁粉在空气中不易自燃,但稍加热即可剧烈燃烧,生成一种黑色的氧化物,如图是纳米铁粉在锥形瓶中燃烧的实验。下列说法错误的是( )
A.激光手电照射使纳米铁粉温度达到着火点
B.锥形瓶中放水可防止生成物溅落炸裂瓶底
C.气球先变大,说明该反应为放热反应
D.纳米铁粉燃烧的化学方程式为4Fe+3O22Fe2O3
5.订书钉主要成分是铁,其表面镀有镁或锌中的一种。小组同学取订书钉5.6g放入图甲装置,并在干燥管口用氢气传感器测量氢气的质量,同时记录电子天平显示的质量变化(如图乙所示),5.8min后各数据保持稳定不再变化。下列说法不正确的是( )
A.曲线Q表示电子天平读数
B.实验中应加入足量的稀硫酸,使金属完全反应
C.1.7min后铁和硫酸开始反应
D.通过所给数据分析,订书钉表面镀的金属是镁
6.用如图所示装置探究铜生锈的条件,一个月后发现铜丝未生锈。下列叙述错误的是( )
A.金属的腐蚀是金属从单质变成化合物的过程
B.在潮湿的空气中,铝比铁耐锈蚀
C.在有氧气和水的条件下,铜比铁易生锈
D.铜生锈可能与空气中的O2、H2O和CO2有关
7.如图所示的四个图像,能正确反映对应变化关系的是( )
A.如图甲所示,水的电解
B.如图乙所示,木炭在密闭的容器内燃烧
C.如图丙所示,加热一定量的高锰酸钾制氧气
D.如图丁所示,等质量的锌、铁与足量的稀硫酸反应
8.了解金属的性质有利于科学地利用金属材料。兴趣小组通过下列实验探究金属的性质。
实验一:将硬铝片(铝合金)和铝片相互刻画,铝片表面出现划痕
实验二:利用如图所示装置进行实验,管内液面上升约体积
实验三:将锌粒放入过量稀硫酸中,持续产生气体,最终固体消失
实验四:将铜丝放入硝酸银溶液中,一段时间后取出,溶液变成蓝色
下列说法错误的是( )
A.实验一说明硬铝的硬度比铝的大 B.实验二说明氧气约占空气总体积的
C.实验三所得溶液中溶质为ZnSO4 D.实验四说明铜的活动性比银的强
9.关于如图说法错误的是( )
A.根据甲图,铁钉在潮湿环境更容易生锈
B.根据甲图,铁钉生锈过程中O2体积不变
C.铁钉是由铁合金制成的
D.根据乙图,铁钉生锈过程中放出热量
10.将粗细相同的X、Y、Z三种金属丝分别放入质量和浓度相同的稀盐酸中,根据如图所示的实验现象,三种金属的活动性强弱顺序正确的是 ( )
A.Y>Z>X B.X>Z>Y C.Z>Y>X D.Z>X>Y
11.下列图像与对应叙述相符的是( )
A.表示红磷与足量的O2充分反应 B.表示铁与硫酸铜溶液的反应
C.表示将高锰酸钾固体充分热
D.表示分别向两支装有等质量锌和铁的试管中,加入足量等溶质质量分数的稀盐酸
12.兴趣小组同学用相同形状的铁、镁、铝、锌四种金属分别和等浓度等体积的足量稀盐酸用图1所示装置进行实验,反应过程气压变化如图2所示,下列说法错误的是( )
A.曲线②对应的物质是锌
B.由图像可知①对应的金属反应速率适中,可用于实验室制氢气
C.根据铝对应曲线判断,在实验前可能没有完全除去铝表面致密的氧化铝
D.镁对应的气压变化中出现压强变小的原因是反应结束,温度降低
13.下列对图示的实验的解释正确的是( )
选项 A B C D
实验操作 及现象 烧杯中冰变少 a中铁钉生锈 b中铁钉无明显变化 烧杯内壁有水雾 乒乓球碎片先燃烧 滤纸碎片后燃烧
解释或结论 水分子质量减小 铁生锈需要水和氧气 蜡烛中含有氢元素 燃烧需要氧气
A.A B.B C.C D.D
14.分别向质量相等的Mg、Zn、Fe三种金属中不断加入溶质质量分数相等的稀硫酸。如图所示能正确表示其中相关量的变化关系的是( )
B. C. D.
15.如图为一氧化碳还原氧化铁实验。下列说法中错误的是( )
A.开始时应先通入一氧化碳,后加热玻璃管
B.实验中玻璃管里粉末由红棕色逐渐变成黑色
C.参加反应的氧化铁和一氧化碳质量比为40:7
D.该实验中缺少尾气处理装置
二.填空题(共8小题)
16.甲、乙两图分别表示硫、铁丝在氧气中燃烧的示意图。
(1)图乙中夹持铁丝的仪器名称是 ,图甲中发生
的化学反应的化学方程式为 。
(2)图甲中水的作用是 (填字母,下同);图乙中水的作用是 。
A.吸收热量 B.隔绝空气 C.吸收有害气体 D.防止生成物掉落炸裂瓶底
(3)图乙中的铁丝绕成螺旋状的原因是 (填字母)。
A.美观 B.增大受热面积,更易引燃 C.方便夹持
17.人体中质量分数在0.01%以下的元素称为微量元素。如图表示部分元素在人体中的质量分数及有关元素信息。
(1)图1中钙元素为 (填“常量”或“微量”)元素;人体缺乏钙元素会患有的疾病是 。
(2)图2为钠原子结构示意图,在化学反应中钠原子容易 (填“得”或“失”)电子,形成的离子符号为 。
(3)以铁元素为主要成分的生铁比纯铁硬度 (填“大”或“小”)。
(4)钾在空气中加热发生化合反应生成超氧化钾(KO2)的化学方程式为
。
18.有限的元素可以组成种类繁多的物质,依据表中的元素回答下列问题。
元素名称 钠 钙 氧 氯 碳 氢
元素符号 Na Ca O Cl C H
(1)写出厨房里常见的一种调味品的名称是 。
(2)若某物质可以改良酸性土壤,则该物质的化学式为 。
(3)生成物全为单质的分解反应是 。
(4)A、B、C、D都是由上表中的元素组成的常见物质。其中C是钠盐,且C、D都是由三种元素组成,B的固体升华时可作制冷剂。他们之间有如图所示转化关系(部分反应物、生成物及反应条件已略去,“→”表示某一种物质经一步反应可转化为另一种物质)。
①图中反应③的化学方程式可以为 。
②A物质可以是 (填字母序号)。
a.单质 b.氧化物 c.酸 d.碱 e.盐
19.金属材料在生产、生活中有越来越广泛的用途。
(1)下列物质中属于金属材料的是 (填序号)。
①四氧化三铁 ②硫酸铜 ③不锈钢 ④生铁 ⑤铝合金 ⑥焊锡
(2)铁是生产、生活中使用最多的金属材料。铁生锈的必要条件是 。
(3)图甲是探究影响铁锈蚀快慢因素的实验。为了探究氯化钠是否可以加快铁的锈蚀,试管①中的物质X和试管②中的物质Y分别是 。
(4)图乙是金属性质的实验。步骤①体现了铜具有 性,步骤②验证了三种金属活动性强弱的依据是 。
20.A~E是初中化学常见的物质,它们之间的转化关系如图(部分物质已略去)。已知A、B组成元素相同且常温下均为液体;D是相对分子质量为16的含碳化合物。则A转化为B的化学方程式为 ;C转化为B的化学方程式为
;C的一种用途是 。
21.金属材料广泛应用于生活和生产中。
(1)不法分子常用假“金元宝”(铜锌合金)蒙骗人们,下列鉴别真假元宝办法中错误的是 。A.加盐酸 B.测密度 C.用火烧 D.看颜色
(2)某化学兴趣小组同学在实验室将一定质量的锌粉放入盛有硝酸银、硝酸铜和硝酸镁的混合溶液中,充分反应后过滤,得到滤渣和滤液,滤液呈无色。
①滤渣中可能含有的金属是 。②滤液中一定含有的阳离子是 。
(3)往盛有4.0g久置的铝片的烧杯中滴加稀盐酸,让其充分反应,放出氢气的质量与所滴加稀盐酸的质量关系如图所示。请回答下列问题并计算:
①刚开始滴加稀盐酸时,没有氢气放出的原因是 。
②该铝片中铝的质量分数为 。
22.“价﹣﹣类”二维图可表示元素化合价与物质类别之间的关系,图中a、b、c、d、e、f代表常见的含碳物质。
(1)a是沼气的主要成分,写出它燃烧的化学方程式 。
(2)下列关于物质及其转化的说法中与事实相符的有 。
①b和d反应生成c;②d和水反应生成e;③物质f可能难溶于水;
④由b到f至少要经过三步反应;⑤由f到d实现一步转化只能通过与酸反应来实现
23.金属及金属材料具有广泛的应用。
Ⅰ.纽扣电池是生活中常用的电源。纽扣电池的金属外壳可以加工得很薄,说明金属具有
性。
Ⅱ.运用手持技术探究金属与酸的反应。向250mL的烧瓶内注入25mL某浓度的稀硫酸(足量),分别剪取相同长度和宽度、质量的镁、铝、锌、铁、铜金属片,打磨后投入烧瓶中,迅速塞紧带有压强传感器的橡皮塞(见图1),点击采集,得到如图2所示的变化曲线。
(1)曲线b对应的金属是铁,反应的化学方程式为 。
(2)下列说法不正确的是 (填字母)。
A.曲线a对应的金属是铜。B.曲线d对应的反应速率适中适合实验室制取气体。
C.曲线e在0~100s段几乎没有上升,可能是该金属活动性比较弱。
D.曲线c在18s左右达到最高点后又略下降的原因是反应结束,温度降低,压强下降。
E.如延长横坐标时间,曲线c、d、e最终将交于一点。
三.科学探究题(共4小题)
24.金属材料的广泛应用,极大地促进了社会发展。某小组同学以“认识金属”为主题开展学习。(一)认识金属的化学性质活动一:验证金属活动性
(1)如图1实验,发现铜、铁两种金属与稀硫酸反应现象不同,原因是 。
(2)除上述实验外,验证铜、铁两种金属活动性强弱关系,还可以使用的试剂为 。
活动二:探究金属与氧气反应的快慢
如表数据是在一定温度下,相同形状的金属镁和镍分别在表面生成氧化物薄膜的实验记录:
反应时间/h 1 4 9 16 25
镁表面氧化薄膜层厚/nm 0.05a 0.2a 0.45a 0.8a 1.25a
镍表面氧化薄膜层厚/nm b 2b 3b 4b 5b
注:a和b均为与温度有关的常数,nm表示纳米。
(3)镁与镍比较, 生成氧化物薄膜的速度更快。
(二)认识金属的制备
如图2是实验室模拟工业炼铁的装置。
(1)实验过程中,装置A玻璃管中发生反应的化学方程式为 。
(2)装置B的作用有:检验二氧化碳; 。
(三)认识金属的锈蚀
如图3所示,若要探究铁生锈的条件,还应该补充的实验是 (可“文字叙述”或“画图”)。
25.铁是现代化学工业的基础,人类进步所必不可少的金属材料。
(1)看图1回答,铁元素为 元素(填“金属或非金属”)。
(2)健康人体内,总量4~5g的铁元素主要以化合物形式存在,缺铁会患 (填字母)。a.骨质疏松 b.甲状腺疾病 c.贫血症 d.侏儒症
【实验一】兴趣小组通过图2实验研究铁的冶炼
(3)该装置有一明显不当之处,你的改进方案是 。
(4)试写出一氧化碳和氧化铁在高温下生成铁的化学反应方程式 。
(5)实验一段时间后,观察到B处澄清石灰水变 ,A处红棕色固体变为黑色,小明将所得的黑色固体物质放入足量的稀盐酸中,发现有少量气泡。写出反应的化学方程式 。
【资料1】已知铁的氧化物均能逐步失去其中的氧,最终被还原为铁。
Fe2O3Fe3O4FeOFe
【资料2】实验研究表明:该实验得到是四氧化三铁与铁粉的混合物。同时实验说明温度对CO和Fe2O3反应有影响。
【实验二】兴趣小组继续用图3实验研究一氧化碳和四氧化三铁的反应
【资料3】氢氧化钠溶液可以与二氧化碳反应,吸收二氧化碳。
(6)从安全与规范的角度考虑,装置C后面应连接 (选填装置序号)。
(7)四氧化三铁的质量为2.32g,充分反应。请计算产生单质铁的质量。(写出解题过程)
26.某兴趣小组为证明CO作还原剂表现还原性,采用如图所示装置进行实验。
【查询资料】
Ⅰ.用甲酸与浓硫酸微热可生成CO,化学方程为HCOOHCO↑+H2O。
Ⅱ.HCOOH:熔点8.6℃,沸点100.8℃。
【实验装置】
请回答:
(1)仪器a的名称是 ,仪器b的名称是 ;
(2)该兴趣小组方框A中需选择 (填“A1”、“A2”或“A3”)装置生成CO气体,然后与B装置对接完成实验;
(3)写出B装置硬质玻璃管中发生反应的化学方程式 ;
(4)B装置硬质玻璃管中的现象是 ,从C装置中出现
现象同样可以证明CO具有还原性;
(5)该小组经过交流讨论,得出该装置存在一定缺陷,具体是 。
27.金属材料的使用作为一个时代的标志,见证了人类文明发展的过程。
【探索性质】
(1)河南省博物院展馆中的汉代金缕玉衣是我国重要的黄金文物。金缕玉衣所用的金丝直径仅为0.08mm,金能制成金丝是利用了其 性。
(2)铁、铜、银是初中化学实验中常见的金属,以下实验可以判断三种金属的活动性顺序,则金属A为 。
【变废为宝】(3)近年来,我国非常重视“绿色发展”,为减少污染并变废为宝,某化学兴趣小组在实验室模拟探究工业废水的综合利用时,设计了以下流程图并完成了回收铜和硫酸锌的实验。
①加入过量A时发生的反应方程式是 。
②固体X的成分是 。
③若试剂B为稀硫酸,可以判断稀硫酸适量的现象是 。
【模拟炼铁】(4)当今,“有一种速度叫中国速度,
有一种骄傲叫中国高铁”,修建高铁需要消耗大量的钢铁,
下列为实验室模拟炼铁并检验气体产物的实验。
①A装置玻璃管内反应的现象为 。
②从环保角度考虑,尾气的处理方法除了点燃,还可以收集,收集尾气的方法最好为 (填“向上排空气法”“向下排空气法”或“排水法”)。
【工业应用】
(5)铝的利用距今还不到200年,现在铝的年产量得到大幅度的提高。工业上可利用“铝热反应”焊接钢轨,其原理是在高温下铝与氧化铁反应生成铁和氧化铝。若用10.8kg铝与氧化铁反应来制取铁,理论上生成铁的质量是多少?
2023初三《科学》第二章精品作业测试卷
(图像题)参考答案与试题解析
一.选择题(共15小题)
1.C。2.B。3.C。4.D。5.D。6.C。7.D。8.C。9.B。10.B。
11.B。12.A。13.C。14.C。15.C。
一.填空题(共8小题)
16.(1)坩埚钳;铁+氧气四氧化三铁。(2)C;D。(3)B。
17.(1)常量;佝偻病、骨质疏松;(2)失;Na+;(3)大;(4)K+O2KO2。
18.(1)氯化钠或醋酸等;(2)Ca(OH)2;(3)2H2O2H2↑+O2↑;
(4)①Na2CO3+2HCl═2NaCl+H2O+CO2↑;②abce。
19.(1)③④⑤⑥;(2)铁与水、氧气同时接触;(3)X是氧气,Y是氯化钠溶液;
(4)延展;在金属活动性顺序表中,前面的金属和后面金属的盐溶液反应,把其从盐溶液中置换出来,A试管无明显现象,说明铁比铜活泼;B试管铜丝表面变银白色,无色溶液变蓝色,说明铜比银活泼。
20.2H2O22H2O+O2↑;CO2+2NaOH=Na2CO3+H2O(合理即可);灭火。
21.(1)D;(2)①锌;②Zn2+、Mg2+;(3)①铝片表面有一层致密的氧化铝薄膜,稀盐酸先和氧化铝反应生成氯化铝和水;②90%。
22.(1)CH4+2O2CO2+2H2O;(2)①②③。
23.Ⅰ、延展;Ⅱ、(1)Fe+2HCl=FeCl2+H2↑;(2)CE。
三.科学探究题(共4小题)
24.(一)(1)在金属活动性顺序中,铁排在氢前面,铜排在氢后面;(2)铁与硫酸铜溶液(合理即可);(3)镁或Mg;
(二)(1)Fe2O3+3CO2Fe+3CO2;
(2)收集一氧化碳,防止一氧化碳扩散到空气中,污染空气;
(三)A试管中的铁钉与氧气和水同时接触,发生锈蚀;B试管中的铁钉
只与氧气接触,没有锈蚀,还需要设计一个铁钉只与水接触的对比实验,探究铁的锈蚀是否与水有关,图示为;故答案为:将无锈的铁钉全部浸没在煮沸迅速冷却后的蒸馏水中,水面上用植物油液封或。
25.(1)金属;(2)c;(3)在末端加一个燃着的酒精灯;(4)Fe2O3+3CO2Fe+3CO2;
(5)浑浊;Fe+2HCl=FeCl2+H2↑;(6)E;(7)1.68g。
26.(1)分液漏斗;锥形瓶;(2)A2;(3)CO+CuOCu+CO2;
(4)黑色固体变为红色;澄清石灰水变浑浊;(5)C装置后面缺少尾气处理装置。
27.(1)延展;(2)铜(或Cu);
(3)①Zn+CuSO4=ZnSO4+Cu;②Cu、Zn;③逐滴滴加稀硫酸至不再有气泡产生为止;
(4)①红棕色粉末变黑色;②排水法;(5)22.4kg。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
