九年级化学上册人教版第三单元物质构成的奥秘单元复习课件(共32张PPT)
文档属性
| 名称 | 九年级化学上册人教版第三单元物质构成的奥秘单元复习课件(共32张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-07 12:09:06 | ||
图片预览






文档简介
(共32张PPT)
第三单元 物质构成的奥秘
单元复习
知识结构
知识点讲解
01
02
知识点典例
03
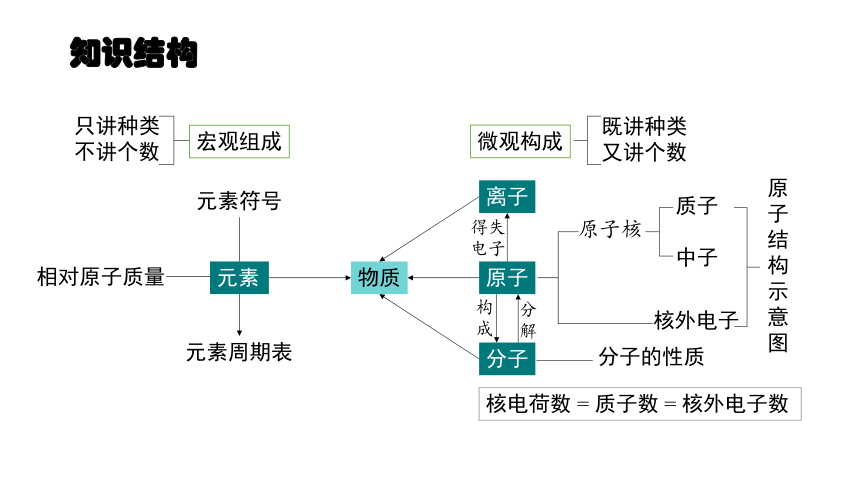
知识结构
宏观组成
物质
元素
元素符号
微观构成
离子
原子
分子
相对原子质量
元素周期表
原子核
核外电子
质子
中子
得失电子
构成
分解
核电荷数 = 质子数 = 核外电子数
分子的性质
原子结构示意图
既讲种类又讲个数
只讲种类不讲个数
0
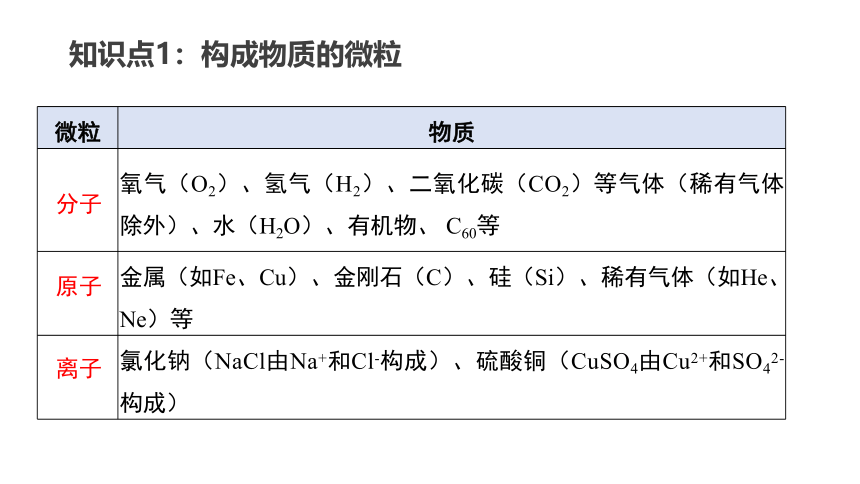
知识点1:构成物质的微粒
微粒 物质
氧气(O2)、氢气(H2)、二氧化碳(CO2)等气体(稀有气体除外)、水(H2O)、有机物、 C60等
金属(如Fe、Cu)、金刚石(C)、硅(Si)、稀有气体(如He、Ne)等
氯化钠(NaCl由Na+和Cl-构成)、硫酸铜(CuSO4由Cu2+和SO42-构成)
分子
离子
原子
分子和原子的区别与联系
加热
O
Hg
O
Hg
氧化汞分子
O
O
Hg
Hg
+
汞原子
氧原子
Hg
Hg
O
O
+
汞原子
氧分子
分子 原子
定义
区别 化学变化中分子可分,原子不可分 联系 分子可以分为原子,原子可以互相结合成分子 原子是化学变化中的最小粒子
由分子构成的物质,分子是保持其物质化学性质的最小粒子
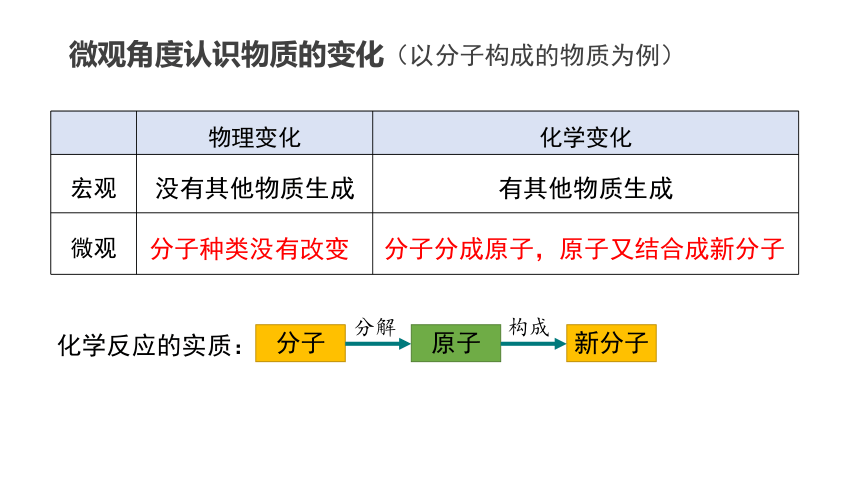
微观角度认识物质的变化(以分子构成的物质为例)
物理变化 化学变化
宏观 没有其他物质生成 有其他物质生成
微观
分子
原子
新分子
分解
构成
化学反应的实质:
分子种类没有改变
分子分成原子,原子又结合成新分子
微观角度认识物质的组成(以分子构成的物质为例)
混合物 纯净物
宏观 含有两种或两种以上的物质,如空气 只含有一种物质,
如氧气
微观 含有_________分子, 如空气中含有氧气分子、氮气分子、二氧化碳分子等 只含有_______分子,
如氧气中只含有氧分子一种分子
多种
一种
【知识点典例】
1.下列物质由分子构成的是( )
A.硫酸铜 B.液氧 C.金刚石 D.银
2.(2023 牡丹江)下列物质由原子直接构成的是( )
A.氯化钠 B.过氧化氢 C.汞 D.C60
B
C
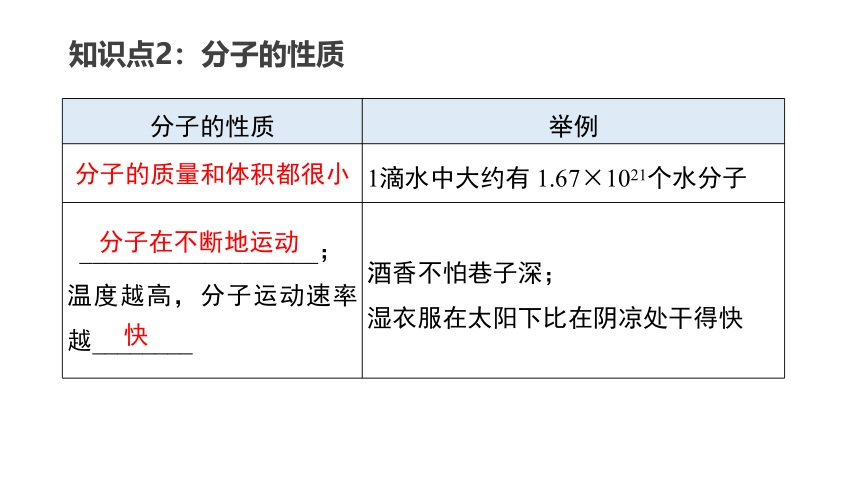
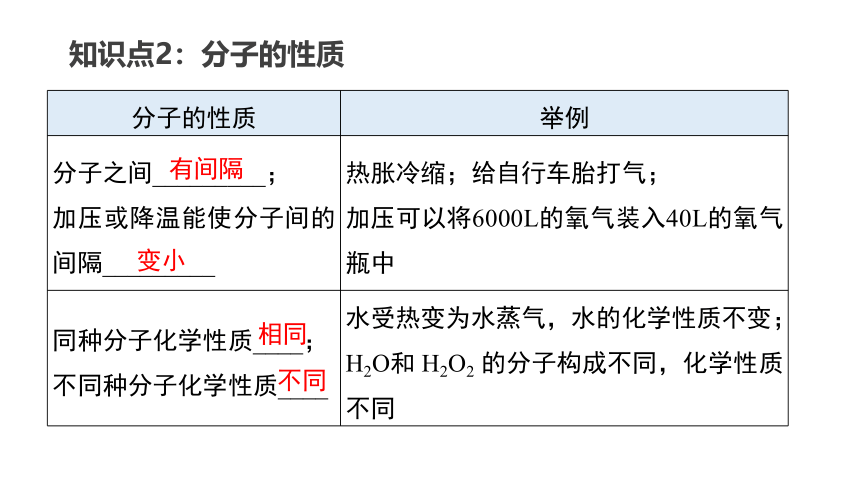
知识点2:分子的性质
分子的性质 举例
1滴水中大约有 1.67×1021个水分子
___________________; 温度越高,分子运动速率越________ 酒香不怕巷子深;
湿衣服在太阳下比在阴凉处干得快
分子的质量和体积都很小
分子在不断地运动
快
知识点2:分子的性质
分子的性质 举例
分子之间_________; 加压或降温能使分子间的间隔_________ 热胀冷缩;给自行车胎打气;
加压可以将6000L的氧气装入40L的氧气瓶中
同种分子化学性质____; 不同种分子化学性质____ 水受热变为水蒸气,水的化学性质不变;
H2O和 H2O2 的分子构成不同,化学性质不同
有间隔
变小
相同
不同
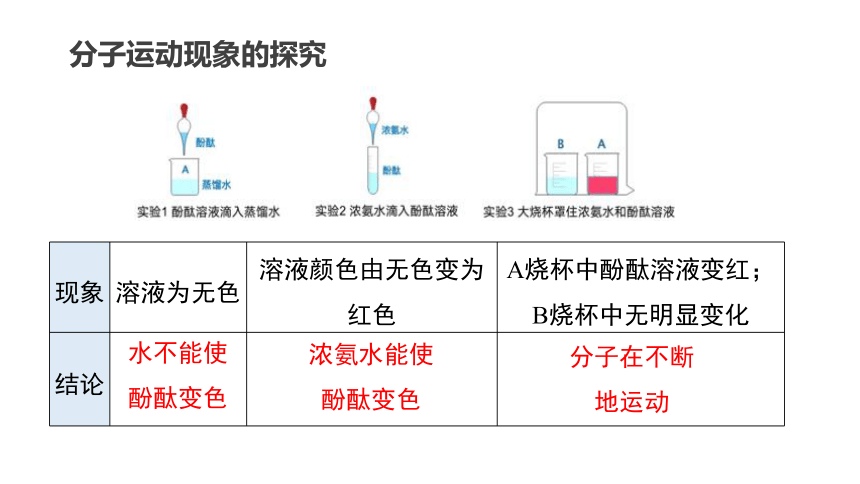
分子运动现象的探究
现象 溶液为无色 溶液颜色由无色变为红色 A烧杯中酚酞溶液变红;
B烧杯中无明显变化
结论
水不能使酚酞变色
浓氨水能使酚酞变色
分子在不断地运动
【知识点典例】
1.下列客观实对应的微观解释错误的是( )
A.端午时节,粽叶飘香——分子总是在不断运动着
B.蔗糖放入水中溶解——蔗糖分子分解了
C.氧气和液氧都能支持燃烧——构成物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大
B
【知识点典例】
2.(2023· 温州)如图为安装在宾馆、仓库等处天花板的自动喷水灭火装置。室内起火时,密封在装置内的液体体积膨胀,冲破水管阀门,实现喷水灭火。起火时,液体体积膨胀是因为液体分子( )
质量变大 B. 间隔变大
C. 数量变多 D.引力变大
B
【知识点典例】
3.(2023 营口)“航天点亮梦想”。航天工业曾用液氢作火箭燃料,氢气液化过程中发生改变的是( )
A.分子种类 B.原子种类
C.原子大小 D.分子间隔
D
知识点3:原子
→每个质子带1个单位正电荷
→不带电
质子
中子
原子核
核外电子
原子
→每个电子带1个单位负电荷
电中性
【特别提醒】原子核中不一定有中子;
同一原子中质子数和中子数不一定相等。
核电荷数
= 质子数
= 核外电子数
+11
简明描述原子结构的模型——原子结构示意图
2 8 1
表示原子核及核内的质子数(核电荷数)
数字“1”表示最外层电子数
表示电子层以及电子层上的电子数
钠原子结构示意图
原子种类 最外层电子数 得失电子 化学性质 举例
< 4 易失去 不稳定 Na、Mg、Al
> 4 易得到 不稳定 O、S、Cl
稀有气体 8(氦为2) 不易得失 稳定 He、Ne、Ar
总结:元素的化学性质与相应原子的最外层电子数密切相关,一般情况下,最外层电子数相等的原子化学性质相似。
原子结构与其化学性质的关系
金属
非金属
1.定义:以一种碳原子的质量的1/12作为标准,其他原子的质量与它相比较所得的比,就是这种原子的相对原子质量。
2.公式:某原子的相对原子质量=
某原子的实际质量
一个碳-12原子质量
特别提醒:相对原子质量( Ar )是一个 “比值”,单位为“1” ,通常省略不写。
相对原子质量(符号为Ar)
3.近似计算:相对原子质量≈质子数+中子数。
【知识点典例】
1.(2023 温州)古人通过往铜中加入锡( Sn)熔合制成青铜器。锡的相对原子质量为119,质子数为50。则锡原子的核外电子数为( )
169 B. 119 C. 69 D. 50
2.质子数与中子数都为6的碳原子质量为a kg ,某原子质量为b kg ,则该元素的相对原子质量为_____________。
D
12b/a
知识点4:离子
阴离子
阳离子
离子
失e-
原子
得e-
2
+11
8
2
+17
8
8
钠离子的结构示意图
氯离子的结构示意图
带电的原子(或原子团)
带负电
带正电
离子符号
镁离子:__________。
Mg2+
离子和原子的区别与联系
原子 离子 阳离子 阴离子
结构 质子数___电子数 质子数____电子数 质子数___电子数
电性
联系 =
〉
〈
不带电
带正电
带负电
【知识点典例】
1.(2023·营口节选)如图为几种原子的结构示意图:
①图中具有相对稳定结构的原子是 _________(填字母序号);
②B原子在化学反应中容易 _________ (填“得到”或“失去”)电子,成为 _________ (填“阴”或“阳”)离子;
③C中x的值是 _________ .
A
失去
阳
6
【知识点典例】
2.下列关于Na、Na+两种粒子的判断中, 正确的是( )
①质子数相同 ②核外电子数相等
③质量几乎相等 ④Na +比Na稳定
A.①②③ B.②③④
C.①③④ D .①②③④
C
知识点5:元素及元素周期表
1.元素是________(即__________)相同的一类原子的总称。
2.元素符号书写规则:一大二小。
如:N(氮元素)、Na (钠元素) 、Ne (氖元素) ;
H(氢元素)、He (氦元素) 、Hg (汞元素)。
理解:元素为宏观概念,只讲种类,不讲个数;
不同元素的本质区别是质子数不同。
质子数
核电荷数
知识点5:元素及元素周期表
3.元素符号的意义
【特别提醒】元素属于宏观概念,只讲种类,不讲个数。当元素符号前面有数字时,只表示微观意义,如 2Fe只能表示2个铁原子。
Fe
宏观
表示铁元素
表示铁这种物质
微观
一个铁原子
O
宏观
表示氧元素
微观
一个氧原子
知识点5:元素及元素周期表
4.元素含量
地壳中的元素分布
0
0
生物细胞中元素分布
Al
Si
O
Fe
Ca
O
C
H
N
Ca
P
知识点5:元素及元素周期表
固体:“石”字旁(碳、硅、硫)
气体:“气”字头(氧、氢、氮)
液体:“氵”字旁(溴)
元素
金属元素:“钅”字旁(铁、铜、银)
非金属元素
稀有气体元素(氦、氖、氩)
5.元素的分类
6.元素周期表
人物 俄国化学家_________发现了元素周期律,并编制了元素周期表 排列依据 按元素原子__________依次递增的顺序给元素编号 结构 横行(周期) 元素周期表有____个横行(电子层数相同)
纵列(族) 有_____个纵列,_____个族(最外层电子数数相同)
单元格 包含信息 门捷列夫
核电荷数
7
18
16
【知识点典例】
1.(2023 锦州)在原子中,能决定元素种类的是( )
A. 电子层数 B. 质子数 C. 中子数 D. 核外电子数
2. (2023 株洲)地壳中含量最多的金属元素是( )
A.Si B.Fe C.Al D.O
B
C
【知识点典例】
3.(2023 营口)稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法错误的是( )
A.铈的原子序数是58
B.铈属于非金属元素
C.铈原子中的质子数是58
D.铈元素的相对原子质量是140.1
B
【知识点典例】
4. (2023 潍坊)科学家利用“基因剪刀”技术降低了水稻中砷的含量。如图是砷元素在元素周期表中的信息及原子结构示意图。下列说法错误的是( )
A.砷属于非金属元素
B.砷的原子序数为33
C.砷原子的相对原子质量为74.92g
D.x=5,砷与磷元素化学性质相似
C
第三单元 物质构成的奥秘
单元复习
知识结构
知识点讲解
01
02
知识点典例
03
知识结构
宏观组成
物质
元素
元素符号
微观构成
离子
原子
分子
相对原子质量
元素周期表
原子核
核外电子
质子
中子
得失电子
构成
分解
核电荷数 = 质子数 = 核外电子数
分子的性质
原子结构示意图
既讲种类又讲个数
只讲种类不讲个数
0
知识点1:构成物质的微粒
微粒 物质
氧气(O2)、氢气(H2)、二氧化碳(CO2)等气体(稀有气体除外)、水(H2O)、有机物、 C60等
金属(如Fe、Cu)、金刚石(C)、硅(Si)、稀有气体(如He、Ne)等
氯化钠(NaCl由Na+和Cl-构成)、硫酸铜(CuSO4由Cu2+和SO42-构成)
分子
离子
原子
分子和原子的区别与联系
加热
O
Hg
O
Hg
氧化汞分子
O
O
Hg
Hg
+
汞原子
氧原子
Hg
Hg
O
O
+
汞原子
氧分子
分子 原子
定义
区别 化学变化中分子可分,原子不可分 联系 分子可以分为原子,原子可以互相结合成分子 原子是化学变化中的最小粒子
由分子构成的物质,分子是保持其物质化学性质的最小粒子
微观角度认识物质的变化(以分子构成的物质为例)
物理变化 化学变化
宏观 没有其他物质生成 有其他物质生成
微观
分子
原子
新分子
分解
构成
化学反应的实质:
分子种类没有改变
分子分成原子,原子又结合成新分子
微观角度认识物质的组成(以分子构成的物质为例)
混合物 纯净物
宏观 含有两种或两种以上的物质,如空气 只含有一种物质,
如氧气
微观 含有_________分子, 如空气中含有氧气分子、氮气分子、二氧化碳分子等 只含有_______分子,
如氧气中只含有氧分子一种分子
多种
一种
【知识点典例】
1.下列物质由分子构成的是( )
A.硫酸铜 B.液氧 C.金刚石 D.银
2.(2023 牡丹江)下列物质由原子直接构成的是( )
A.氯化钠 B.过氧化氢 C.汞 D.C60
B
C
知识点2:分子的性质
分子的性质 举例
1滴水中大约有 1.67×1021个水分子
___________________; 温度越高,分子运动速率越________ 酒香不怕巷子深;
湿衣服在太阳下比在阴凉处干得快
分子的质量和体积都很小
分子在不断地运动
快
知识点2:分子的性质
分子的性质 举例
分子之间_________; 加压或降温能使分子间的间隔_________ 热胀冷缩;给自行车胎打气;
加压可以将6000L的氧气装入40L的氧气瓶中
同种分子化学性质____; 不同种分子化学性质____ 水受热变为水蒸气,水的化学性质不变;
H2O和 H2O2 的分子构成不同,化学性质不同
有间隔
变小
相同
不同
分子运动现象的探究
现象 溶液为无色 溶液颜色由无色变为红色 A烧杯中酚酞溶液变红;
B烧杯中无明显变化
结论
水不能使酚酞变色
浓氨水能使酚酞变色
分子在不断地运动
【知识点典例】
1.下列客观实对应的微观解释错误的是( )
A.端午时节,粽叶飘香——分子总是在不断运动着
B.蔗糖放入水中溶解——蔗糖分子分解了
C.氧气和液氧都能支持燃烧——构成物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大
B
【知识点典例】
2.(2023· 温州)如图为安装在宾馆、仓库等处天花板的自动喷水灭火装置。室内起火时,密封在装置内的液体体积膨胀,冲破水管阀门,实现喷水灭火。起火时,液体体积膨胀是因为液体分子( )
质量变大 B. 间隔变大
C. 数量变多 D.引力变大
B
【知识点典例】
3.(2023 营口)“航天点亮梦想”。航天工业曾用液氢作火箭燃料,氢气液化过程中发生改变的是( )
A.分子种类 B.原子种类
C.原子大小 D.分子间隔
D
知识点3:原子
→每个质子带1个单位正电荷
→不带电
质子
中子
原子核
核外电子
原子
→每个电子带1个单位负电荷
电中性
【特别提醒】原子核中不一定有中子;
同一原子中质子数和中子数不一定相等。
核电荷数
= 质子数
= 核外电子数
+11
简明描述原子结构的模型——原子结构示意图
2 8 1
表示原子核及核内的质子数(核电荷数)
数字“1”表示最外层电子数
表示电子层以及电子层上的电子数
钠原子结构示意图
原子种类 最外层电子数 得失电子 化学性质 举例
< 4 易失去 不稳定 Na、Mg、Al
> 4 易得到 不稳定 O、S、Cl
稀有气体 8(氦为2) 不易得失 稳定 He、Ne、Ar
总结:元素的化学性质与相应原子的最外层电子数密切相关,一般情况下,最外层电子数相等的原子化学性质相似。
原子结构与其化学性质的关系
金属
非金属
1.定义:以一种碳原子的质量的1/12作为标准,其他原子的质量与它相比较所得的比,就是这种原子的相对原子质量。
2.公式:某原子的相对原子质量=
某原子的实际质量
一个碳-12原子质量
特别提醒:相对原子质量( Ar )是一个 “比值”,单位为“1” ,通常省略不写。
相对原子质量(符号为Ar)
3.近似计算:相对原子质量≈质子数+中子数。
【知识点典例】
1.(2023 温州)古人通过往铜中加入锡( Sn)熔合制成青铜器。锡的相对原子质量为119,质子数为50。则锡原子的核外电子数为( )
169 B. 119 C. 69 D. 50
2.质子数与中子数都为6的碳原子质量为a kg ,某原子质量为b kg ,则该元素的相对原子质量为_____________。
D
12b/a
知识点4:离子
阴离子
阳离子
离子
失e-
原子
得e-
2
+11
8
2
+17
8
8
钠离子的结构示意图
氯离子的结构示意图
带电的原子(或原子团)
带负电
带正电
离子符号
镁离子:__________。
Mg2+
离子和原子的区别与联系
原子 离子 阳离子 阴离子
结构 质子数___电子数 质子数____电子数 质子数___电子数
电性
联系 =
〉
〈
不带电
带正电
带负电
【知识点典例】
1.(2023·营口节选)如图为几种原子的结构示意图:
①图中具有相对稳定结构的原子是 _________(填字母序号);
②B原子在化学反应中容易 _________ (填“得到”或“失去”)电子,成为 _________ (填“阴”或“阳”)离子;
③C中x的值是 _________ .
A
失去
阳
6
【知识点典例】
2.下列关于Na、Na+两种粒子的判断中, 正确的是( )
①质子数相同 ②核外电子数相等
③质量几乎相等 ④Na +比Na稳定
A.①②③ B.②③④
C.①③④ D .①②③④
C
知识点5:元素及元素周期表
1.元素是________(即__________)相同的一类原子的总称。
2.元素符号书写规则:一大二小。
如:N(氮元素)、Na (钠元素) 、Ne (氖元素) ;
H(氢元素)、He (氦元素) 、Hg (汞元素)。
理解:元素为宏观概念,只讲种类,不讲个数;
不同元素的本质区别是质子数不同。
质子数
核电荷数
知识点5:元素及元素周期表
3.元素符号的意义
【特别提醒】元素属于宏观概念,只讲种类,不讲个数。当元素符号前面有数字时,只表示微观意义,如 2Fe只能表示2个铁原子。
Fe
宏观
表示铁元素
表示铁这种物质
微观
一个铁原子
O
宏观
表示氧元素
微观
一个氧原子
知识点5:元素及元素周期表
4.元素含量
地壳中的元素分布
0
0
生物细胞中元素分布
Al
Si
O
Fe
Ca
O
C
H
N
Ca
P
知识点5:元素及元素周期表
固体:“石”字旁(碳、硅、硫)
气体:“气”字头(氧、氢、氮)
液体:“氵”字旁(溴)
元素
金属元素:“钅”字旁(铁、铜、银)
非金属元素
稀有气体元素(氦、氖、氩)
5.元素的分类
6.元素周期表
人物 俄国化学家_________发现了元素周期律,并编制了元素周期表 排列依据 按元素原子__________依次递增的顺序给元素编号 结构 横行(周期) 元素周期表有____个横行(电子层数相同)
纵列(族) 有_____个纵列,_____个族(最外层电子数数相同)
单元格 包含信息 门捷列夫
核电荷数
7
18
16
【知识点典例】
1.(2023 锦州)在原子中,能决定元素种类的是( )
A. 电子层数 B. 质子数 C. 中子数 D. 核外电子数
2. (2023 株洲)地壳中含量最多的金属元素是( )
A.Si B.Fe C.Al D.O
B
C
【知识点典例】
3.(2023 营口)稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法错误的是( )
A.铈的原子序数是58
B.铈属于非金属元素
C.铈原子中的质子数是58
D.铈元素的相对原子质量是140.1
B
【知识点典例】
4. (2023 潍坊)科学家利用“基因剪刀”技术降低了水稻中砷的含量。如图是砷元素在元素周期表中的信息及原子结构示意图。下列说法错误的是( )
A.砷属于非金属元素
B.砷的原子序数为33
C.砷原子的相对原子质量为74.92g
D.x=5,砷与磷元素化学性质相似
C
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
