人教版 高中化学 选择性必修3 4.1糖类同步练习(含答案)
文档属性
| 名称 | 人教版 高中化学 选择性必修3 4.1糖类同步练习(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 863.0KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-07 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
4.1糖类同步练习-人教版高中化学选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.糖类、油脂、蛋白质都是与生命息息相关的物质,下列说法正确的是
A.葡萄糖是单糖,蔗糖是二糖,它们是同系物,淀粉和纤维素是同分异构体
B.淀粉、纤维素、油脂、蛋白质都是高分子化合物,都能发生水解反应
C.油脂在碱性条件下的水解反应为皂化反应
D.植物油、矿物油、甘油都可用于萃取碘水中的碘
2.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述正确的是
①油脂不能使溴的四氯化碳溶液褪色
②汽油、柴油和植物油都是碳氢化合物
③葡萄糖、麦芽糖在一定条件下既能发生水解反应,又能发生银镜反应
④葡萄糖和果糖互为同分异构体
⑤加热、紫外线、酒精、福尔马林、饱和硫酸钠溶液会使蛋白质发生盐析,具有可逆性
⑥可用碘水检验淀粉是否水解完全
⑦淀粉和纤维素的组成都是(C6H10O5)n,不是同分异构体,且水解最终产物都是葡萄糖
⑧醋酸纤维素、油脂和蛋白质在一定条件下都能水解
⑨淀粉、棉花、羊毛、蚕丝、油脂都属于高分子化合物.
A.②③⑤⑦ B.②③④⑥⑧ C.①②④⑨ D.④⑥⑦⑧
3.下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
A 检验某有机物A中是否含有氯原子 取2mL有机物A于试管中加入5mL20%KOH醇溶液混合后加热,再滴加AgNO3溶液 若不产生白色沉淀,则该有机物A中不含有氯原子:若产生白色沉淀,则该有机物A中含有氯原子
B 探究浓度对化学反应速率的影响 取2mL0.01mol·L-1KMnO4溶液分别加入2支试管中,向2支试管中分别加入2mL0.1mol·L-1H2C2O4溶液和2mL0.2mol·L-1H2C2O4溶液 加入2mL0.2mol·L-1H2C2O4溶液的试管褪色快,则浓度越大化学反应速率越快
C 检测一定量H2还原Fe2O3的产物 将剩余固体产物溶解在稀盐酸中,分别滴加亚铁氰化钾溶液和铁氰化钾溶液 若滴加亚铁氰化钾溶液,产生蓝色沉淀,则产物含Fe3O4;若滴加铁氰化钾溶液,产生蓝色沉淀,则产物含FeO
D 检验麦芽糖是否发生了水解 向麦芽糖溶液中加入几滴稀硫酸,水浴加热几分钟后。取适量水解液于另一试管中,先加入足量NaOH溶液,再向其中加入新制的Cu(OH)2悬浊液加热 生成砖红色沉淀,则麦芽糖发生了水解
A.A B.B C.C D.D
4.对于淀粉和纤维素的叙述,正确的是
A.因为都属于糖,所以都具有甜味
B.人体内有催化淀粉和纤维素水解的酶
C.两者都能在一定条件下水解生成葡萄糖
D.因为二者都是由多个单糖分子按照一定的方式在分子间脱水结合而成,所以都用(C6H10O5)n表示,因此它们是同分异构体。
5.生活离不开化学。下列有关说法正确的是
A.聚氯乙烯塑料制品可用于食品包装
B.苏打溶液显碱性,故苏打常用作胃酸中和剂
C.通过煤的气化和液化等化学变化后再使用,可有效提高燃料的利用率
D.淀粉和纤维素互为同分异构体
6.化学是以实验为基础的一门学科,下列实验的操作方法和结论正确的是
A.在试管中加入2mL10%的溶液,然后加入5滴5%的NaOH溶液得到新制,再加入几滴葡萄糖溶液加热煮沸,产生砖红色沉淀
B.用稀氨水清洗做过银镜反应的试管,是因为银可以与稀氨水生成银氨溶液
C.乙烷中混有乙烯可以用酸性高锰酸钾溶液除去乙烯
D.用热NaOH溶液清洗盛过油脂的试管,是因为油脂在碱性条件下可以水解
7.下列由实验得出的结论正确的是
选项 实验 结论
A 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 生成的一氯甲烷具有酸性
B 向淀粉溶液中加少量稀硫酸,加热4~5min。冷却后向其中加入新制Cu(OH)2悬浊液,加热至沸腾,无砖红色沉淀 淀粉没有发生水解
C 乙烯能使酸性高锰酸钾溶液褪色 可以用酸性高锰酸钾溶液除去乙烷中的乙烯,并得到干燥纯净的乙烷
D 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 发生加成反应,产物无色、可溶于四氯化碳
A.A B.B C.C D.D
8.下列物质中,不属于糖类的是
A.蔗糖 B.淀粉 C.纤维素 D.蛋白质
9.下列对相关实验操作及现象的描述存在错误的是
选项 实验操作 现象
A 向FeSO4溶液中滴加K3[Fe(CN)6]溶液 出现蓝色沉淀
B 向淀粉溶液中先滴加稀硫酸,加热一段时间再加入稍过量的NaOH溶液,最后加入新制的Cu(OH)2悬浊液并加热 出现砖红色沉淀
C 将乙醇蒸气通过炽热的CuO固体粉末 黑色的固体变为紫红色
D 向AlCl3溶液中通入过量的NH3 先出现白色沉淀,后沉淀溶解
A.A B.B C.C D.D
10.某学生设计了如下实验方案用以检验淀粉水解的情况:
下列结论中正确的是
A.淀粉尚有部分未水解
B.淀粉已完全水解
C.淀粉没有水解
D.淀粉已发生水解,但不知是否完全水解
二、填空题
11.按要求写出方程式。
(1)与足量的氢气一定条件下反应: 。
(2)苯酚中加足量浓溴水: 。
(3)乙醛与新制的银氨溶液水浴加热: 。
(4)纤维素在酸或酶的作用下水解: 。
12.按要求回答下列问题:
(1)下列5种物质:a.乙烯;b.苯;c.甲苯;d.溴乙烷;e.聚乙烯。
①互为同系物的是 (填序号,下同)。
②分子中所有原子在同一平面内的是 。
③从上述5种物质中选出2种,使其能通过一步反应发生转化。写出任意一个符合上述要求的反应的化学方程式: 。
(2)分子式为的芳香族化合物有多种同分异构体。写出其中符合下列要求的同分异构体的结构简式。
①能与溶液作用显色: (任写一种)。
②分子中有4种不同化学环境的氢原子: 、 。
(3)①淀粉或纤维素在酸的作用下彻底发生水解反应,均可得到的产物是 。
②若要证明淀粉在水解过程中是否完全发生反应,可采取的实验方法: 。
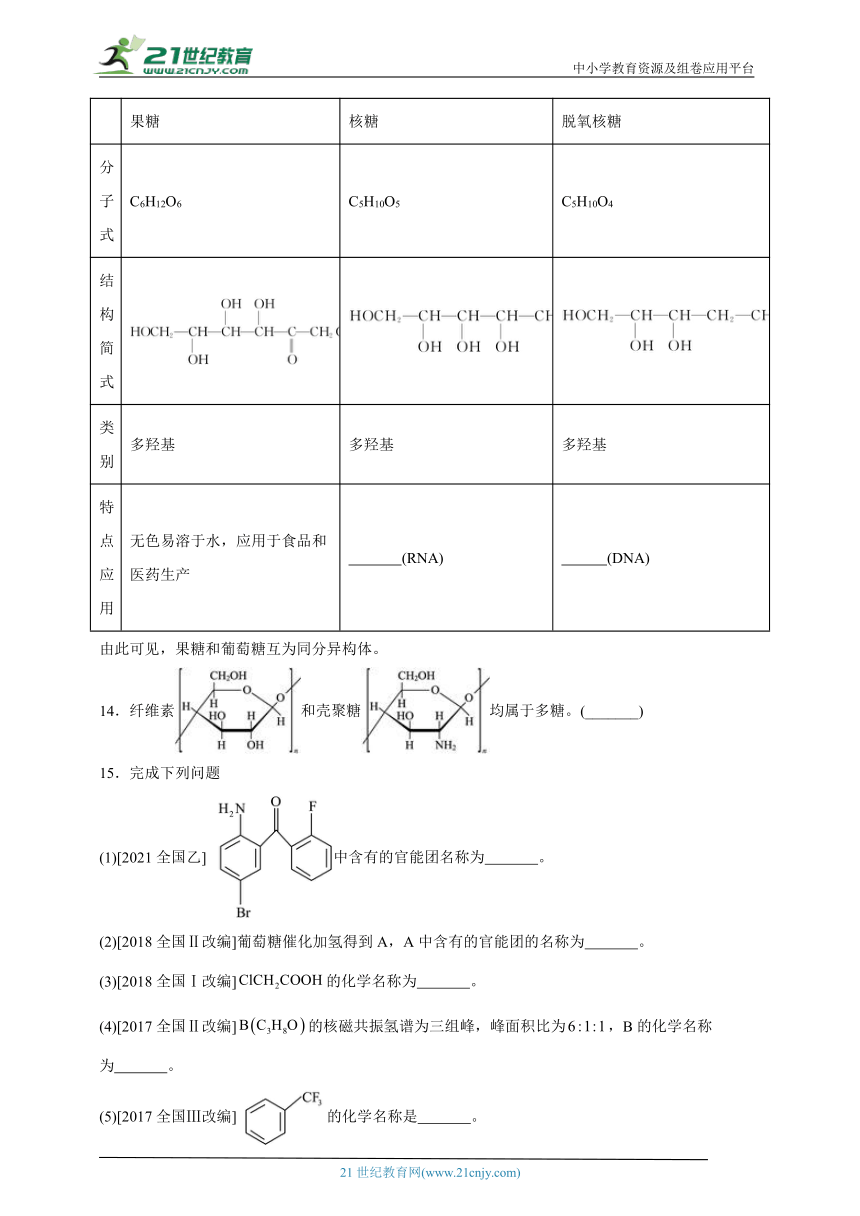
13.果糖、核糖与脱氧核糖
果糖 核糖 脱氧核糖
分子式 C6H12O6 C5H10O5 C5H10O4
结构简式
类别 多羟基 多羟基 多羟基
特点应用 无色易溶于水,应用于食品和医药生产 (RNA) (DNA)
由此可见,果糖和葡萄糖互为同分异构体。
14.纤维素和壳聚糖均属于多糖。(_______)
15.完成下列问题
(1)[2021全国乙] 中含有的官能团名称为 。
(2)[2018全国Ⅱ改编]葡萄糖催化加氢得到A,A中含有的官能团的名称为 。
(3)[2018全国Ⅰ改编]的化学名称为 。
(4)[2017全国Ⅱ改编]的核磁共振氢谱为三组峰,峰面积比为,B的化学名称为 。
(5)[2017全国Ⅲ改编] 的化学名称是 。
16.传统酿酒的原理可简单表示如下。请根据题意填空;
(1)混合物A遇碘水变蓝,说明混合物A中含 (填“淀粉”或“葡萄糖”);
(2)乙醇(CH3CH2OH)中官能团的名称是 (填“羟基”或“羧基”);
(3)炒菜时放一些酒和醋,能使菜味香可口。请完成该反应的化学方程式:CH3COOH+CH3CH2OH 。
17.淀粉是人体主要的供能物质之一,而且还是酿酒的原料,请回答下列问题。
(1)淀粉在人体内水解成葡萄糖,葡萄糖氧化时产生能量。写出葡萄糖在人体内氧化最终生成CO2和H2O的化学反应方程式 。
(2)淀粉酿酒的原理是淀粉在糖化酶的作用下水解成葡萄糖等,葡萄糖等在酒化酶的作用下分解生成乙醇,写出其中的化学反应方程式 。
18.葡萄糖分子中含有的官能团是什么?可发生哪些反应?
19.淀粉和纤维素是常见的多糖,在一定条件下它们都可以水解生成葡萄糖。
(1)淀粉在浓硫酸作用下水解生成葡萄糖的化学方程式为 。
(2)某学生设计了如下实验方案用以检验淀粉水解的情况:
下列结论正确的是_______。
A.淀粉尚有部分未水解 B.淀粉已完全水解
C.淀粉没有水解 D.淀粉已水解,但不知是否完全水解
(3)一种测定饮料中糖类物质含量(所有糖类物质以葡萄糖计算)的方法如下:
取某无色饮料20.00mL加入稀硫酸煮沸,充分反应后,冷却,加入适量的氢氧化钠溶液并稀释至100.00mL。取10.00mL稀释液,加入30.00mL0.0150mol/L标准I2溶液,置于暗处15分钟。然后滴加2~3滴淀粉溶液作指示剂,再用0.01200mol/LNa2S2O3标准溶液滴定反应所剩余的I2,当溶液由蓝色变为无色且半分钟不变时,反应达到终点,共消耗Na2S2O3标推溶液25.00mL。
已知:a.I2在碱性条件下能与葡萄糖反应:C6H12O6+I2+3NaOH=C6H11O7Na+2NaI+2H2O
b.Na2S2O3与I2能发牛如下反应:I2+2Na2S2O3=2NaI+Na2S4O6
①配制100.00mL0.01500mol/LI2标准溶液,所必需的玻璃仪器有烧杯、玻璃棒、 和 。
②向饮料中加入稀硫酸并充分煮沸的目的是 。
③计算该饮料中糖类物质的含量(单位mg/mL)(写出计算过程)。 。
20.糖类的定义:分子中有两个或两个以上 的 或 以及水解后可以生成 或 的有机化合物。
糖类的分类: 、 、 。
三、实验题
21.葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见表:
物质名称 葡萄糖酸钙 葡萄糖酸 溴化钙 氯化钙
水中的溶解性 可溶于冷水 易溶于热水 可溶 易溶 易溶
乙醇中的溶解性 微溶 微溶 可溶 可溶
实验流程如图:
C6H12O6溶液悬浊液Ca(C6H11O7)2
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,图中装置最适合的是 。
A.B.C.
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是 。
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是 ;本实验中不宜用CaCl2替代CaCO3,理由是 。
(3)第③步需趁热过滤,其原因是 。
(4)第④步加入乙醇的作用是 。
(5)第⑥步中,下列洗涤剂最合适的是_______。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
22.氧化亚铜是大型水面舰艇防护涂层的重要原料.某小组通过查阅资料,进行如图研究.
I.Cu2O的制取
(1)葡萄糖还原法制Cu2O的化学方程式为
(2)实验室用此方法制取并获得少量Cu2O固体,需要的玻璃仪器除试管、酒精灯、烧杯外,还需要
Ⅱ.检验样品中是否含有CuO
方案1:将制得的Cu2O样品溶于足量稀硫酸.
(3)甲同学认为若溶液变为蓝色,则说明样品中含有CuO杂质.乙同学认为此推论不合理,用化学用语解释原因
(4)甲同学通过反思,认为将定性检验改为定量测定便能确定样品中是否含有CuO杂质,应测量的数据是
方案2:丙同学认为采用如下装置(所加药品均足量)进行实验,通过测定c装置反应后固体的质量以及d装置反应前后增重的质量,可计算,从而确定样品中是否含有氧化铜.
(5)装置a中所加的酸是
(填化学式),装置e中碱石灰的作用是
(6)点燃装置c中酒精灯之前需进行的操作是
(7)熄灭酒精灯之后,仍需通一段时间H2至试管冷却,原因是 .
23.葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
相关物质的溶解性见下表:
物质名称 葡萄糖酸钙 葡萄糖酸 溴化钙
水中的溶解性 可溶于冷水易溶于热水 可溶 易溶
乙醇中的溶解性 微溶 微溶 可溶
(1)第①步中溴水氧化葡萄糖时,下列装置中最适合的是 。
葡萄糖的氧化也可用其他试剂,下列物质中最适合的是 。
a.新制Cu(OH)2悬浊液 b.酸性KMnO4溶液
c.O2/葡萄糖氧化酶 d.银氨溶液
(2)第②步中CaCO3固体需过量的原因是 。
(3)第③步需趁热过滤,其原因是 。
(4)第④步加入乙醇的作用是 。
参考答案:
1.C
2.D
3.B
4.C
5.C
6.D
7.D
8.D
9.D
10.D
11.(1)
(2)
(3)CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag+3NH3+H2O
(4)(C6H10O5)n+nH2OnC6H12O6
12. bc ab 葡萄糖 向水解液中加入碘水,若不变蓝色,则淀粉全部水解
13. 酮 醛 醛 核糖核酸 脱氧核糖核酸
14.错误
15.(1)氨基、羰基、溴原子、氟原子
(2)羟基
(3)氯乙酸
(4)2-丙醇(或异丙醇)
(5)三氟甲苯
16. 淀粉 羟基
17. C6H12O6+6O2→6CO2+6H2O (C6H10O5)n+nH2OnC6H12O6、C6H12O62C2H5OH+2CO2↑
18.醛基:加成反应、氧化反应、还原反应;羟基:酯化反应
19.(1)(C6H10O5)n+nH2OnC6H12O6(葡萄糖)
(2)D
(3) 胶头滴管 100mL容量瓶 将饮料中的糖类物质都转化为葡萄糖 27.00mg/mL
20. 羟基 醛 酮 多羟基醛 多羟基酮 单糖 低聚糖 多糖
21.(1) B C
(2) 提高葡萄糖的转化率 氯化钙难以与葡萄糖酸直接反应得到葡萄糖酸钙,便于后面的分离
(3)葡萄糖酸钙冷却后会结晶,如不趁热过滤会损失产品
(4)可降低葡萄糖酸钙在溶液中的溶解度,有利于葡萄糖酸钙的析出
(5)D
22.(1)
(2)漏斗、玻璃棒
(3)Cu2O + H2SO4=CuSO4+Cu + H2O
(4)Cu2O样品的质量、反应后剩余固体(Cu)的质量
(5) H2SO4 防止空气中的水进入d装置,m(H2O)测定不准确
(6)打开K1,关闭K2,通一段时间氢气后验纯,打开K2,关闭K1
(7)防止生成的Cu单质在高温下又被氧气氧化为CuO,导致测定数据不准确
23. B c 使葡萄糖酸全部转化成葡萄糖酸钙 葡萄糖酸钙冷却后会结晶析出,如不趁热过滤会损失产品 葡萄糖酸钙在乙醇中的溶解度比在水中小,有利于葡萄糖酸钙结晶析出减少产品损失
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
4.1糖类同步练习-人教版高中化学选择性必修3
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.糖类、油脂、蛋白质都是与生命息息相关的物质,下列说法正确的是
A.葡萄糖是单糖,蔗糖是二糖,它们是同系物,淀粉和纤维素是同分异构体
B.淀粉、纤维素、油脂、蛋白质都是高分子化合物,都能发生水解反应
C.油脂在碱性条件下的水解反应为皂化反应
D.植物油、矿物油、甘油都可用于萃取碘水中的碘
2.糖类、脂肪和蛋白质是维持人体生命活动所必需的三大营养物质.以下叙述正确的是
①油脂不能使溴的四氯化碳溶液褪色
②汽油、柴油和植物油都是碳氢化合物
③葡萄糖、麦芽糖在一定条件下既能发生水解反应,又能发生银镜反应
④葡萄糖和果糖互为同分异构体
⑤加热、紫外线、酒精、福尔马林、饱和硫酸钠溶液会使蛋白质发生盐析,具有可逆性
⑥可用碘水检验淀粉是否水解完全
⑦淀粉和纤维素的组成都是(C6H10O5)n,不是同分异构体,且水解最终产物都是葡萄糖
⑧醋酸纤维素、油脂和蛋白质在一定条件下都能水解
⑨淀粉、棉花、羊毛、蚕丝、油脂都属于高分子化合物.
A.②③⑤⑦ B.②③④⑥⑧ C.①②④⑨ D.④⑥⑦⑧
3.下列方案设计、现象和结论都正确的是
目的 方案设计 现象和结论
A 检验某有机物A中是否含有氯原子 取2mL有机物A于试管中加入5mL20%KOH醇溶液混合后加热,再滴加AgNO3溶液 若不产生白色沉淀,则该有机物A中不含有氯原子:若产生白色沉淀,则该有机物A中含有氯原子
B 探究浓度对化学反应速率的影响 取2mL0.01mol·L-1KMnO4溶液分别加入2支试管中,向2支试管中分别加入2mL0.1mol·L-1H2C2O4溶液和2mL0.2mol·L-1H2C2O4溶液 加入2mL0.2mol·L-1H2C2O4溶液的试管褪色快,则浓度越大化学反应速率越快
C 检测一定量H2还原Fe2O3的产物 将剩余固体产物溶解在稀盐酸中,分别滴加亚铁氰化钾溶液和铁氰化钾溶液 若滴加亚铁氰化钾溶液,产生蓝色沉淀,则产物含Fe3O4;若滴加铁氰化钾溶液,产生蓝色沉淀,则产物含FeO
D 检验麦芽糖是否发生了水解 向麦芽糖溶液中加入几滴稀硫酸,水浴加热几分钟后。取适量水解液于另一试管中,先加入足量NaOH溶液,再向其中加入新制的Cu(OH)2悬浊液加热 生成砖红色沉淀,则麦芽糖发生了水解
A.A B.B C.C D.D
4.对于淀粉和纤维素的叙述,正确的是
A.因为都属于糖,所以都具有甜味
B.人体内有催化淀粉和纤维素水解的酶
C.两者都能在一定条件下水解生成葡萄糖
D.因为二者都是由多个单糖分子按照一定的方式在分子间脱水结合而成,所以都用(C6H10O5)n表示,因此它们是同分异构体。
5.生活离不开化学。下列有关说法正确的是
A.聚氯乙烯塑料制品可用于食品包装
B.苏打溶液显碱性,故苏打常用作胃酸中和剂
C.通过煤的气化和液化等化学变化后再使用,可有效提高燃料的利用率
D.淀粉和纤维素互为同分异构体
6.化学是以实验为基础的一门学科,下列实验的操作方法和结论正确的是
A.在试管中加入2mL10%的溶液,然后加入5滴5%的NaOH溶液得到新制,再加入几滴葡萄糖溶液加热煮沸,产生砖红色沉淀
B.用稀氨水清洗做过银镜反应的试管,是因为银可以与稀氨水生成银氨溶液
C.乙烷中混有乙烯可以用酸性高锰酸钾溶液除去乙烯
D.用热NaOH溶液清洗盛过油脂的试管,是因为油脂在碱性条件下可以水解
7.下列由实验得出的结论正确的是
选项 实验 结论
A 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 生成的一氯甲烷具有酸性
B 向淀粉溶液中加少量稀硫酸,加热4~5min。冷却后向其中加入新制Cu(OH)2悬浊液,加热至沸腾,无砖红色沉淀 淀粉没有发生水解
C 乙烯能使酸性高锰酸钾溶液褪色 可以用酸性高锰酸钾溶液除去乙烷中的乙烯,并得到干燥纯净的乙烷
D 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 发生加成反应,产物无色、可溶于四氯化碳
A.A B.B C.C D.D
8.下列物质中,不属于糖类的是
A.蔗糖 B.淀粉 C.纤维素 D.蛋白质
9.下列对相关实验操作及现象的描述存在错误的是
选项 实验操作 现象
A 向FeSO4溶液中滴加K3[Fe(CN)6]溶液 出现蓝色沉淀
B 向淀粉溶液中先滴加稀硫酸,加热一段时间再加入稍过量的NaOH溶液,最后加入新制的Cu(OH)2悬浊液并加热 出现砖红色沉淀
C 将乙醇蒸气通过炽热的CuO固体粉末 黑色的固体变为紫红色
D 向AlCl3溶液中通入过量的NH3 先出现白色沉淀,后沉淀溶解
A.A B.B C.C D.D
10.某学生设计了如下实验方案用以检验淀粉水解的情况:
下列结论中正确的是
A.淀粉尚有部分未水解
B.淀粉已完全水解
C.淀粉没有水解
D.淀粉已发生水解,但不知是否完全水解
二、填空题
11.按要求写出方程式。
(1)与足量的氢气一定条件下反应: 。
(2)苯酚中加足量浓溴水: 。
(3)乙醛与新制的银氨溶液水浴加热: 。
(4)纤维素在酸或酶的作用下水解: 。
12.按要求回答下列问题:
(1)下列5种物质:a.乙烯;b.苯;c.甲苯;d.溴乙烷;e.聚乙烯。
①互为同系物的是 (填序号,下同)。
②分子中所有原子在同一平面内的是 。
③从上述5种物质中选出2种,使其能通过一步反应发生转化。写出任意一个符合上述要求的反应的化学方程式: 。
(2)分子式为的芳香族化合物有多种同分异构体。写出其中符合下列要求的同分异构体的结构简式。
①能与溶液作用显色: (任写一种)。
②分子中有4种不同化学环境的氢原子: 、 。
(3)①淀粉或纤维素在酸的作用下彻底发生水解反应,均可得到的产物是 。
②若要证明淀粉在水解过程中是否完全发生反应,可采取的实验方法: 。
13.果糖、核糖与脱氧核糖
果糖 核糖 脱氧核糖
分子式 C6H12O6 C5H10O5 C5H10O4
结构简式
类别 多羟基 多羟基 多羟基
特点应用 无色易溶于水,应用于食品和医药生产 (RNA) (DNA)
由此可见,果糖和葡萄糖互为同分异构体。
14.纤维素和壳聚糖均属于多糖。(_______)
15.完成下列问题
(1)[2021全国乙] 中含有的官能团名称为 。
(2)[2018全国Ⅱ改编]葡萄糖催化加氢得到A,A中含有的官能团的名称为 。
(3)[2018全国Ⅰ改编]的化学名称为 。
(4)[2017全国Ⅱ改编]的核磁共振氢谱为三组峰,峰面积比为,B的化学名称为 。
(5)[2017全国Ⅲ改编] 的化学名称是 。
16.传统酿酒的原理可简单表示如下。请根据题意填空;
(1)混合物A遇碘水变蓝,说明混合物A中含 (填“淀粉”或“葡萄糖”);
(2)乙醇(CH3CH2OH)中官能团的名称是 (填“羟基”或“羧基”);
(3)炒菜时放一些酒和醋,能使菜味香可口。请完成该反应的化学方程式:CH3COOH+CH3CH2OH 。
17.淀粉是人体主要的供能物质之一,而且还是酿酒的原料,请回答下列问题。
(1)淀粉在人体内水解成葡萄糖,葡萄糖氧化时产生能量。写出葡萄糖在人体内氧化最终生成CO2和H2O的化学反应方程式 。
(2)淀粉酿酒的原理是淀粉在糖化酶的作用下水解成葡萄糖等,葡萄糖等在酒化酶的作用下分解生成乙醇,写出其中的化学反应方程式 。
18.葡萄糖分子中含有的官能团是什么?可发生哪些反应?
19.淀粉和纤维素是常见的多糖,在一定条件下它们都可以水解生成葡萄糖。
(1)淀粉在浓硫酸作用下水解生成葡萄糖的化学方程式为 。
(2)某学生设计了如下实验方案用以检验淀粉水解的情况:
下列结论正确的是_______。
A.淀粉尚有部分未水解 B.淀粉已完全水解
C.淀粉没有水解 D.淀粉已水解,但不知是否完全水解
(3)一种测定饮料中糖类物质含量(所有糖类物质以葡萄糖计算)的方法如下:
取某无色饮料20.00mL加入稀硫酸煮沸,充分反应后,冷却,加入适量的氢氧化钠溶液并稀释至100.00mL。取10.00mL稀释液,加入30.00mL0.0150mol/L标准I2溶液,置于暗处15分钟。然后滴加2~3滴淀粉溶液作指示剂,再用0.01200mol/LNa2S2O3标准溶液滴定反应所剩余的I2,当溶液由蓝色变为无色且半分钟不变时,反应达到终点,共消耗Na2S2O3标推溶液25.00mL。
已知:a.I2在碱性条件下能与葡萄糖反应:C6H12O6+I2+3NaOH=C6H11O7Na+2NaI+2H2O
b.Na2S2O3与I2能发牛如下反应:I2+2Na2S2O3=2NaI+Na2S4O6
①配制100.00mL0.01500mol/LI2标准溶液,所必需的玻璃仪器有烧杯、玻璃棒、 和 。
②向饮料中加入稀硫酸并充分煮沸的目的是 。
③计算该饮料中糖类物质的含量(单位mg/mL)(写出计算过程)。 。
20.糖类的定义:分子中有两个或两个以上 的 或 以及水解后可以生成 或 的有机化合物。
糖类的分类: 、 、 。
三、实验题
21.葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7+CaCO3→Ca(C6H11O7)2(葡萄糖酸钙)+H2O+CO2↑
相关物质的溶解性见表:
物质名称 葡萄糖酸钙 葡萄糖酸 溴化钙 氯化钙
水中的溶解性 可溶于冷水 易溶于热水 可溶 易溶 易溶
乙醇中的溶解性 微溶 微溶 可溶 可溶
实验流程如图:
C6H12O6溶液悬浊液Ca(C6H11O7)2
请回答下列问题:
(1)第①步中溴水氧化葡萄糖时,图中装置最适合的是 。
A.B.C.
制备葡萄糖酸钙的过程中,葡萄糖的氧化也可用其它试剂,下列物质中最适合的是 。
A.新制Cu(OH)2悬浊液 B.酸性KMnO4溶液
C.O2/葡萄糖氧化酶 D.[Ag(NH3)2]OH溶液
(2)第②步充分反应后CaCO3固体需有剩余,其目的是 ;本实验中不宜用CaCl2替代CaCO3,理由是 。
(3)第③步需趁热过滤,其原因是 。
(4)第④步加入乙醇的作用是 。
(5)第⑥步中,下列洗涤剂最合适的是_______。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
22.氧化亚铜是大型水面舰艇防护涂层的重要原料.某小组通过查阅资料,进行如图研究.
I.Cu2O的制取
(1)葡萄糖还原法制Cu2O的化学方程式为
(2)实验室用此方法制取并获得少量Cu2O固体,需要的玻璃仪器除试管、酒精灯、烧杯外,还需要
Ⅱ.检验样品中是否含有CuO
方案1:将制得的Cu2O样品溶于足量稀硫酸.
(3)甲同学认为若溶液变为蓝色,则说明样品中含有CuO杂质.乙同学认为此推论不合理,用化学用语解释原因
(4)甲同学通过反思,认为将定性检验改为定量测定便能确定样品中是否含有CuO杂质,应测量的数据是
方案2:丙同学认为采用如下装置(所加药品均足量)进行实验,通过测定c装置反应后固体的质量以及d装置反应前后增重的质量,可计算,从而确定样品中是否含有氧化铜.
(5)装置a中所加的酸是
(填化学式),装置e中碱石灰的作用是
(6)点燃装置c中酒精灯之前需进行的操作是
(7)熄灭酒精灯之后,仍需通一段时间H2至试管冷却,原因是 .
23.葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:
相关物质的溶解性见下表:
物质名称 葡萄糖酸钙 葡萄糖酸 溴化钙
水中的溶解性 可溶于冷水易溶于热水 可溶 易溶
乙醇中的溶解性 微溶 微溶 可溶
(1)第①步中溴水氧化葡萄糖时,下列装置中最适合的是 。
葡萄糖的氧化也可用其他试剂,下列物质中最适合的是 。
a.新制Cu(OH)2悬浊液 b.酸性KMnO4溶液
c.O2/葡萄糖氧化酶 d.银氨溶液
(2)第②步中CaCO3固体需过量的原因是 。
(3)第③步需趁热过滤,其原因是 。
(4)第④步加入乙醇的作用是 。
参考答案:
1.C
2.D
3.B
4.C
5.C
6.D
7.D
8.D
9.D
10.D
11.(1)
(2)
(3)CH3CHO+2Ag(NH3)2OHCH3COONH4+2Ag+3NH3+H2O
(4)(C6H10O5)n+nH2OnC6H12O6
12. bc ab 葡萄糖 向水解液中加入碘水,若不变蓝色,则淀粉全部水解
13. 酮 醛 醛 核糖核酸 脱氧核糖核酸
14.错误
15.(1)氨基、羰基、溴原子、氟原子
(2)羟基
(3)氯乙酸
(4)2-丙醇(或异丙醇)
(5)三氟甲苯
16. 淀粉 羟基
17. C6H12O6+6O2→6CO2+6H2O (C6H10O5)n+nH2OnC6H12O6、C6H12O62C2H5OH+2CO2↑
18.醛基:加成反应、氧化反应、还原反应;羟基:酯化反应
19.(1)(C6H10O5)n+nH2OnC6H12O6(葡萄糖)
(2)D
(3) 胶头滴管 100mL容量瓶 将饮料中的糖类物质都转化为葡萄糖 27.00mg/mL
20. 羟基 醛 酮 多羟基醛 多羟基酮 单糖 低聚糖 多糖
21.(1) B C
(2) 提高葡萄糖的转化率 氯化钙难以与葡萄糖酸直接反应得到葡萄糖酸钙,便于后面的分离
(3)葡萄糖酸钙冷却后会结晶,如不趁热过滤会损失产品
(4)可降低葡萄糖酸钙在溶液中的溶解度,有利于葡萄糖酸钙的析出
(5)D
22.(1)
(2)漏斗、玻璃棒
(3)Cu2O + H2SO4=CuSO4+Cu + H2O
(4)Cu2O样品的质量、反应后剩余固体(Cu)的质量
(5) H2SO4 防止空气中的水进入d装置,m(H2O)测定不准确
(6)打开K1,关闭K2,通一段时间氢气后验纯,打开K2,关闭K1
(7)防止生成的Cu单质在高温下又被氧气氧化为CuO,导致测定数据不准确
23. B c 使葡萄糖酸全部转化成葡萄糖酸钙 葡萄糖酸钙冷却后会结晶析出,如不趁热过滤会损失产品 葡萄糖酸钙在乙醇中的溶解度比在水中小,有利于葡萄糖酸钙结晶析出减少产品损失
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
