2024人教版新教材高中化学选择性必修2同步练习--第1课时 原子结构与元素周期表(含解析)
文档属性
| 名称 | 2024人教版新教材高中化学选择性必修2同步练习--第1课时 原子结构与元素周期表(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 517.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-08 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2024人教版新教材高中化学选择性必修2
第二节 原子结构与元素的性质
第1课时 原子结构与元素周期表
基础过关练
题组一 原子结构与元素周期表
1.(2020山东济宁期末)周期表中共有18个纵列,从左到右分别为1~18列,按这种规定,下列说法正确的是( )
A.第1列是碱金属元素
B.只有第2列元素基态原子的价层电子排布为ns2
C.第1列和第18列所含元素种数不同
D.第8列没有非金属元素
2.(2021山东日照莒县期中)具有以下结构的基态原子,对应元素一定是主族元素的是( )
A.4s1 B.4p3
C.3d34s2 D.3d104s2
3.元素周期表长周期从左到右有18列,碱金属元素在第1列,稀有气体元素在第18列。按这种规定,下列说法正确的是( )
A.第9列元素中没有非金属元素
B.第15列元素原子的最外层电子排布是ns2np5
C.原子最外层电子排布为ns2的元素一定在第2列
D.元素周期表每一周期元素原子的最外层电子排布均是从ns1 过渡到ns2np6
题组二 元素周期表的分区
4.关于元素周期表中元素的分区,下列说法正确的是( )
A.元素周期表的d区元素不全是副族元素
B.元素周期表的d区包含所有的过渡元素
C.过渡元素包括d区、f区、ds区的元素
D.ds区元素不都是副族元素5.(2021山西汾阳期末)元素周期表中,有非金属元素的区域为( )
A.只有s区 B.只有p区
C.s区、d区和ds区 D.s区和p区
6.闪烁着银白色光泽的金属钛(22Ti)因具有密度小、强度大、无磁性等优良的机械性能,被广泛地应用于军事、医学等领域,号称“崛起的第三金属”。已知钛有48Ti、49Ti、50Ti等核素,下列关于金属钛的叙述中不正确的是( )
A.上述钛原子中,中子数不可能为22
B.钛元素在元素周期表中位于第四周期
C.钛的不同核素在元素周期表中处于不同的位置
D.钛元素是d区的过渡元素
7.A~M元素在周期表中的位置如图所示:
下列叙述正确的是( )
A.K位于元素周期表中第四周期第ⅡB族,属于ds区元素
B.J位于元素周期表中第四周期第ⅣB族,属于d区元素
C.F位于元素周期表中第三周期第ⅡA族,属于s区元素
D.I位于元素周期表中第三周期第ⅦA族,属于ds区元素
能力提升练
题组一 核外电子排布与元素周期表的分区
1.(2022辽宁县级重点高中协作体期末)下列关于元素的分区说法正确的是( )
A.所有的金属元素都分布在d区和ds区
B.所有的非金属元素都分布在p区
C.元素周期表中第ⅢB族到第ⅡB族10个纵列的元素都是金属元素
D.最外层电子数为2的元素都分布在s区
2.已知某元素+3价基态离子的电子排布式为1s22s22p63s23p63d3,该元素在元素周期表中的位置和所在区是( )
A.第三周期第ⅥB族;p区
B.第三周期第ⅢB族;ds区
C.第四周期第ⅥB族;d区
D.第四周期第ⅢB族;f区
3.(2022福建永泰一中期中)下列关于原子核外电子排布与元素在周期表中位置关系的叙述正确的是( )
A.基态原子核外N层上只有一个电子的元素一定是第ⅠA族元素
B.基态原子价层电子排布式为(n-1)d6~8ns2的元素不一定是副族元素
C.基态原子最外层的p能级上半充满的元素一定位于p区
D.基态原子核外价层电子排布式为(n-1)dxnsy的元素的族序数一定为x+y
4.已知某些元素在周期表中的位置如图所示:
下列说法正确的是( )
A.表中五种元素位于5个不同的区
B.元素4的基态原子价层电子排布式为3d104s2,与它具有相同最外层电子数的元素只可能位于ds区
C.元素1、2、3的基态原子中,未成对电子数之比为1∶2∶4
D.元素5的原子结构示意图为
5.格哈德·多马克将一种磺胺药应用于医学,因此荣获1939年诺贝尔生理学或医学奖。已知该物质的结构为,其中W、X、Y、Z、M为原子序数依次增大的短周期元素,Z和M为同主族元素。则下列说法中不正确的是( )
A.基态M原子的价层电子排布式为3s23p4
B.基态Y原子的电子排布图为
C.基态Z原子核外未成对电子数是成对电子数的3倍
D.基态X原子核外s能级电子总数是p能级电子总数的2倍
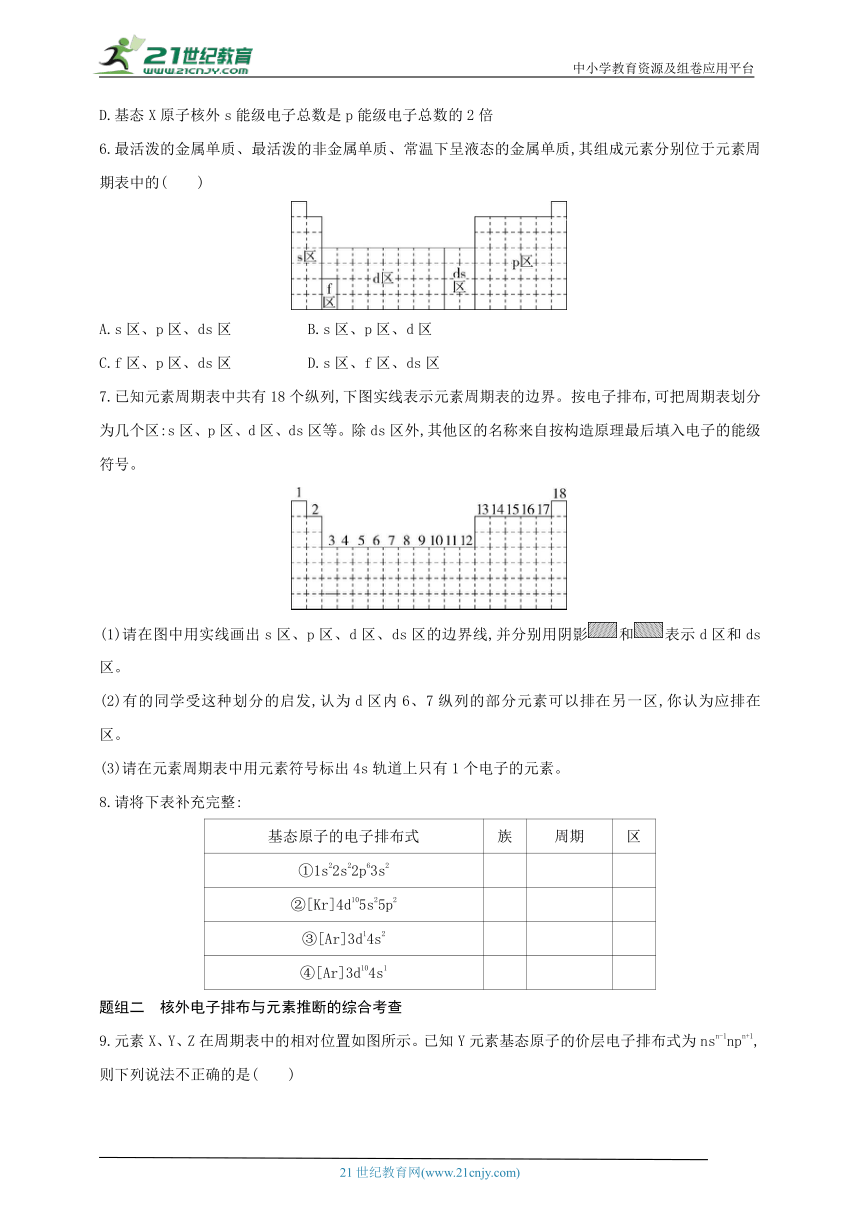
6.最活泼的金属单质、最活泼的非金属单质、常温下呈液态的金属单质,其组成元素分别位于元素周期表中的( )
A.s区、p区、ds区 B.s区、p区、d区
C.f区、p区、ds区 D.s区、f区、ds区
7.已知元素周期表中共有18个纵列,下图实线表示元素周期表的边界。按电子排布,可把周期表划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入电子的能级符号。
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影和表示d区和ds区。
(2)有的同学受这种划分的启发,认为d区内6、7纵列的部分元素可以排在另一区,你认为应排在 区。
(3)请在元素周期表中用元素符号标出4s轨道上只有1个电子的元素。
8.请将下表补充完整:
基态原子的电子排布式 族 周期 区
①1s22s22p63s2
②[Kr]4d105s25p2
③[Ar]3d14s2
④[Ar]3d104s1
题组二 核外电子排布与元素推断的综合考查
9.元素X、Y、Z在周期表中的相对位置如图所示。已知Y元素基态原子的价层电子排布式为nsn-1npn+1,则下列说法不正确的是( )
A.Y元素基态原子的价层电子排布式为4s24p4
B.Y元素在元素周期表的第三周期第ⅥA族
C.X元素所在周期中所含非金属元素种数最多
D.Z元素基态原子的电子排布式为1s22s22p63s23p63d104s24p3
10.(2021山东青岛黄岛期末)现有五种前四周期元素,结构信息见下表,回答下列问题。
元素 结构信息
A 基态原子有6个原子轨道填充满电子,有3个未成对电子
B M层比L层少两个电子
C 基态原子核外有17种不同运动状态的电子
D 基态原子的价层电子排布式为3dx4s2,在常见化合物中其最高正价为+7价
E 基态原子的M层全充满,N层没有成对电子,只有1个未成对电子
(1)A、B、C三种元素最高价氧化物的水化物酸性由强到弱的顺序为
(用最高价氧化物的水化物的化学式表示)。
(2)D在元素周期表中的位置为 ,其基态原子的简化电子排布式为 。
(3)写出基态B原子价层电子的轨道表示式: 。
(4)E位于元素周期表的 区,基态原子填有电子的轨道数为 。
答案全解全析
基础过关练
1.D 第1列为第ⅠA族元素,其中H是非金属元素,A错误。基态原子价层电子排布为ns2的并非只有第ⅡA族元素,还有He元素,B错误。第1列为第ⅠA族,含有H、Li、Na、K、Rb、Cs、Fr 7种元素;第18列为0族,含有He、Ne、Ar、Kr、Xe、Rn、Og 7种元素,故这两列所含元素种数相同,C错误。第8列无非金属元素,D正确。
2.B 具有4s1结构的原子可能是Cr(3d54s1),Cr不是主族元素,A错误;具有4p3结构的基态原子,其对应元素一定是主族元素,B正确;具有3d34s2结构的基态原子对应元素为V,V不是主族元素,C错误;具有3d104s2结构的基态原子对应元素可能为Zn元素,不是主族元素,D错误。
3.A 第9列元素是过渡元素,没有非金属元素,A项正确;第15列元素原子的最外层电子排布是ns2np3,B项错误;原子最外层电子排布为ns2的元素也可能是过渡元素或0族元素He,C项错误;第一周期元素原子最外层电子排布是从1s1过渡到1s2,D项错误。
4.C d区包括ⅢB~ⅦB族(镧系和锕系除外)元素和第Ⅷ族元素,ds区包括ⅠB族和ⅡB族元素,过渡元素包括所有的副族元素,即包括了d区、f区、ds区的元素,故C正确。
5.D s区除氢元素外均为金属元素;p区包含0族元素、ⅢA族~ⅦA族元素,含有金属元素与非金属元素;d区、ds区全部为金属元素;f区为镧系元素和锕系元素,全部为金属元素。
6.C 22Ti的原子序数为22,位于第四周期第ⅣB族,属于d区的过渡元素;根据三种核素的质量数可知,其中子数最小为26;钛的三种核素的质子数均为22,故在元素周期表中处于同一位置。
7.C K位于元素周期表中第四周期第ⅠB族,属于ds区元素,A错误;J位于元素周期表中第四周期第ⅥB族,属于d区元素,B错误;F位于元素周期表中第三周期第ⅡA族,属于s区元素,C正确;I位于元素周期表中第三周期第ⅦA族,属于p区元素,D错误。
能力提升练
1.C s区同时存在金属元素和非金属元素(H),A、B两项错误;He的最外层电子数是2,位于p区,D项错误。
2.C 某元素+3价基态离子的电子排布式为1s22s22p63s23p63d3,其原子核外电子数为21+3=24,为Cr元素,位于元素周期表第四周期第ⅥB族,属于d区元素,故选C。
3.C 基态原子的N层上只有一个电子的元素,可能为K、Cr或Cu,K为主族元素,Cr、Cu为副族元素,故A错误;基态原子的价层电子排布式为(n-1)d6~8ns2的元素为第Ⅷ族元素,故B错误;基态原子最外层的p能级上半充满的元素,其电子最后填充p能级,属于p区,故C正确;基态原子核外价层电子排布式为(n-1)dxnsy的元素的族序数不一定为x+y,例如ⅠB族、ⅡB族元素,族序数为y,故D错误。
4.D H(元素1)位于s区,O(元素2)、Ge(元素5)位于p区,Mn(元素3)位于d区,Zn(元素4)位于ds区,则表中五种元素位于4个不同的区,A项错误;元素4为Zn元素,其基态原子价层电子排布式为3d104s2,最外层电子排布式为4s2,与它具有相同最外层电子数的元素可能位于ds区、s区、p区(He)、d区、f区,B项错误;元素1的价层电子排布式为1s1,元素2的价层电子排布式为2s22p4,元素3的价层电子排布式为3d54s2,则元素1、2、3的基态原子中,未成对电子数分别为1、2、5,未成对电子数之比为1∶2∶5,C项错误;元素5为Ge,其基态原子的电子排布式为1s22s22p63s23p63d104s24p2,则其原子结构示意图为,D项正确。
5.C 根据给定物质的结构,结合W、X、Y、Z、M为原子序数依次增大的短周期元素,Z和M为同主族元素,可知W、X、Y、Z、M分别为H、C、N、O、S。基态硫原子的价层电子排布式为3s23p4,故A正确;基态氮原子的电子排布图为 ,故B正确;Z为氧元素,其基态原子的电子排布式为1s22s22p4,基态Z原子核外成对电子数是未成对电子数的3倍,故C错误;X为碳元素,其基态原子的电子排布式为1s22s22p2,因此基态碳原子核外s能级电子总数是p能级电子总数的2倍,故D正确。
6.A 理论上最活泼的金属单质是Fr,但由于其具有放射性,故一般认为最活泼的金属单质是Cs,而Cs元素和Fr元素都属于第ⅠA族元素,位于s区;最活泼的非金属元素是氟,在第ⅦA族,位于p区;常温下呈液态的金属单质为Hg,汞元素原子的价层电子排布式为5d106s2,属于第ⅡB族元素,位于ds区。
7.答案 (1)如图:
(2)ds (3)见上图
解析 (2)ds区元素原子价层电子排布式为(n-1)d10ns1和(n-1)d10ns2,而d区内6纵列部分元素的价层电子排布式为 (n-1)d5ns1,7纵列部分元素的价层电子排布式为(n-1)d5ns2,因此类比可以放在ds区。(3)4s轨道上只有1个电子,即4s1,元素原子的电子排布式可能为1s22s22p63s23p64s1(K)、1s22s22p63s23p63d54s1(Cr)或1s22s22p63s23p63d104s1(Cu),分别标在元素周期表中相应位置即可。
8.答案 ①ⅡA 三 s ②ⅣA 五 p ③ⅢB 四 d ④ⅠB 四 ds
解析 ①最后一个电子填充在s轨道,属于s区元素,为主族元素,在第三周期第ⅡA族。 ②最后一个电子填充在p轨道,属于p区元素,为主族元素,在第五周期第ⅣA族。③最后一个电子填充在d轨道,且d轨道上电子数小于10,属于d区元素,为副族元素,在第四周期第ⅢB族。④最后一个电子填充在d轨道,且d轨道上电子数等于10,属于ds区元素,为副族元素,在第四周期第ⅠB族。
9.A 因为Y元素原子的价层电子排布式中出现了np能级,所以其ns能级已经充满且只能为2个电子,则n-1=2,n=3,即Y元素原子的价层电子排布式为3s23p4,故A项错误,B项正确。Y为S元素,X为F元素,第二周期所含非金属元素种数最多,故C项正确。Z为As元素,基态砷原子的电子排布式为1s22s22p63s23p63d104s24p3,故D项正确。
误区警示 对价层电子认识的误区提醒
(1)价层电子不一定是最外层电子,主族元素的价层电子是最外层电子,对于过渡元素还包括部分内层电子。
(2)元素的价层电子数不一定等于其所在族的族序数。
10.答案 (1)HClO4>H2SO4>H3PO4 (2)第四周期第ⅦB族 [Ar]3d54s2 (3)
(4)ds 15
解析 A的基态原子有6个原子轨道填充满电子,有3个未成对电子,A为P;B原子的M层比L层少两个电子,B为S;C的基态原子核外有17种不同运动状态的电子,C为Cl;D的基态原子的价层电子排布式为3dx4s2,在常见化合物中其最高正价为+7价,则价层电子排布式为3d54s2,D为Mn;E的基态原子的M层全充满,N层没有成对电子,只有1个未成对电子,E的价层电子排布式为3d104s1,E为Cu。(1)由以上分析知,A为P,B为S,C为Cl。A、B、C三种元素最高价氧化物的水化物酸性由强到弱的顺序为HClO4>H2SO4>H3PO4。(2)D为锰元素,其在元素周期表中的位置为第四周期第ⅦB族,其基态原子的简化电子排布式为[Ar]3d54s2。(3)B为硫元素,其基态原子的价层电子的轨道表示式为。(4)E为铜元素,位于元素周期表的ds区,其基态原子的电子排布式为1s22s22p63s23p63d104s1,填有电子的轨道数为15。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024人教版新教材高中化学选择性必修2
第二节 原子结构与元素的性质
第1课时 原子结构与元素周期表
基础过关练
题组一 原子结构与元素周期表
1.(2020山东济宁期末)周期表中共有18个纵列,从左到右分别为1~18列,按这种规定,下列说法正确的是( )
A.第1列是碱金属元素
B.只有第2列元素基态原子的价层电子排布为ns2
C.第1列和第18列所含元素种数不同
D.第8列没有非金属元素
2.(2021山东日照莒县期中)具有以下结构的基态原子,对应元素一定是主族元素的是( )
A.4s1 B.4p3
C.3d34s2 D.3d104s2
3.元素周期表长周期从左到右有18列,碱金属元素在第1列,稀有气体元素在第18列。按这种规定,下列说法正确的是( )
A.第9列元素中没有非金属元素
B.第15列元素原子的最外层电子排布是ns2np5
C.原子最外层电子排布为ns2的元素一定在第2列
D.元素周期表每一周期元素原子的最外层电子排布均是从ns1 过渡到ns2np6
题组二 元素周期表的分区
4.关于元素周期表中元素的分区,下列说法正确的是( )
A.元素周期表的d区元素不全是副族元素
B.元素周期表的d区包含所有的过渡元素
C.过渡元素包括d区、f区、ds区的元素
D.ds区元素不都是副族元素5.(2021山西汾阳期末)元素周期表中,有非金属元素的区域为( )
A.只有s区 B.只有p区
C.s区、d区和ds区 D.s区和p区
6.闪烁着银白色光泽的金属钛(22Ti)因具有密度小、强度大、无磁性等优良的机械性能,被广泛地应用于军事、医学等领域,号称“崛起的第三金属”。已知钛有48Ti、49Ti、50Ti等核素,下列关于金属钛的叙述中不正确的是( )
A.上述钛原子中,中子数不可能为22
B.钛元素在元素周期表中位于第四周期
C.钛的不同核素在元素周期表中处于不同的位置
D.钛元素是d区的过渡元素
7.A~M元素在周期表中的位置如图所示:
下列叙述正确的是( )
A.K位于元素周期表中第四周期第ⅡB族,属于ds区元素
B.J位于元素周期表中第四周期第ⅣB族,属于d区元素
C.F位于元素周期表中第三周期第ⅡA族,属于s区元素
D.I位于元素周期表中第三周期第ⅦA族,属于ds区元素
能力提升练
题组一 核外电子排布与元素周期表的分区
1.(2022辽宁县级重点高中协作体期末)下列关于元素的分区说法正确的是( )
A.所有的金属元素都分布在d区和ds区
B.所有的非金属元素都分布在p区
C.元素周期表中第ⅢB族到第ⅡB族10个纵列的元素都是金属元素
D.最外层电子数为2的元素都分布在s区
2.已知某元素+3价基态离子的电子排布式为1s22s22p63s23p63d3,该元素在元素周期表中的位置和所在区是( )
A.第三周期第ⅥB族;p区
B.第三周期第ⅢB族;ds区
C.第四周期第ⅥB族;d区
D.第四周期第ⅢB族;f区
3.(2022福建永泰一中期中)下列关于原子核外电子排布与元素在周期表中位置关系的叙述正确的是( )
A.基态原子核外N层上只有一个电子的元素一定是第ⅠA族元素
B.基态原子价层电子排布式为(n-1)d6~8ns2的元素不一定是副族元素
C.基态原子最外层的p能级上半充满的元素一定位于p区
D.基态原子核外价层电子排布式为(n-1)dxnsy的元素的族序数一定为x+y
4.已知某些元素在周期表中的位置如图所示:
下列说法正确的是( )
A.表中五种元素位于5个不同的区
B.元素4的基态原子价层电子排布式为3d104s2,与它具有相同最外层电子数的元素只可能位于ds区
C.元素1、2、3的基态原子中,未成对电子数之比为1∶2∶4
D.元素5的原子结构示意图为
5.格哈德·多马克将一种磺胺药应用于医学,因此荣获1939年诺贝尔生理学或医学奖。已知该物质的结构为,其中W、X、Y、Z、M为原子序数依次增大的短周期元素,Z和M为同主族元素。则下列说法中不正确的是( )
A.基态M原子的价层电子排布式为3s23p4
B.基态Y原子的电子排布图为
C.基态Z原子核外未成对电子数是成对电子数的3倍
D.基态X原子核外s能级电子总数是p能级电子总数的2倍
6.最活泼的金属单质、最活泼的非金属单质、常温下呈液态的金属单质,其组成元素分别位于元素周期表中的( )
A.s区、p区、ds区 B.s区、p区、d区
C.f区、p区、ds区 D.s区、f区、ds区
7.已知元素周期表中共有18个纵列,下图实线表示元素周期表的边界。按电子排布,可把周期表划分为几个区:s区、p区、d区、ds区等。除ds区外,其他区的名称来自按构造原理最后填入电子的能级符号。
(1)请在图中用实线画出s区、p区、d区、ds区的边界线,并分别用阴影和表示d区和ds区。
(2)有的同学受这种划分的启发,认为d区内6、7纵列的部分元素可以排在另一区,你认为应排在 区。
(3)请在元素周期表中用元素符号标出4s轨道上只有1个电子的元素。
8.请将下表补充完整:
基态原子的电子排布式 族 周期 区
①1s22s22p63s2
②[Kr]4d105s25p2
③[Ar]3d14s2
④[Ar]3d104s1
题组二 核外电子排布与元素推断的综合考查
9.元素X、Y、Z在周期表中的相对位置如图所示。已知Y元素基态原子的价层电子排布式为nsn-1npn+1,则下列说法不正确的是( )
A.Y元素基态原子的价层电子排布式为4s24p4
B.Y元素在元素周期表的第三周期第ⅥA族
C.X元素所在周期中所含非金属元素种数最多
D.Z元素基态原子的电子排布式为1s22s22p63s23p63d104s24p3
10.(2021山东青岛黄岛期末)现有五种前四周期元素,结构信息见下表,回答下列问题。
元素 结构信息
A 基态原子有6个原子轨道填充满电子,有3个未成对电子
B M层比L层少两个电子
C 基态原子核外有17种不同运动状态的电子
D 基态原子的价层电子排布式为3dx4s2,在常见化合物中其最高正价为+7价
E 基态原子的M层全充满,N层没有成对电子,只有1个未成对电子
(1)A、B、C三种元素最高价氧化物的水化物酸性由强到弱的顺序为
(用最高价氧化物的水化物的化学式表示)。
(2)D在元素周期表中的位置为 ,其基态原子的简化电子排布式为 。
(3)写出基态B原子价层电子的轨道表示式: 。
(4)E位于元素周期表的 区,基态原子填有电子的轨道数为 。
答案全解全析
基础过关练
1.D 第1列为第ⅠA族元素,其中H是非金属元素,A错误。基态原子价层电子排布为ns2的并非只有第ⅡA族元素,还有He元素,B错误。第1列为第ⅠA族,含有H、Li、Na、K、Rb、Cs、Fr 7种元素;第18列为0族,含有He、Ne、Ar、Kr、Xe、Rn、Og 7种元素,故这两列所含元素种数相同,C错误。第8列无非金属元素,D正确。
2.B 具有4s1结构的原子可能是Cr(3d54s1),Cr不是主族元素,A错误;具有4p3结构的基态原子,其对应元素一定是主族元素,B正确;具有3d34s2结构的基态原子对应元素为V,V不是主族元素,C错误;具有3d104s2结构的基态原子对应元素可能为Zn元素,不是主族元素,D错误。
3.A 第9列元素是过渡元素,没有非金属元素,A项正确;第15列元素原子的最外层电子排布是ns2np3,B项错误;原子最外层电子排布为ns2的元素也可能是过渡元素或0族元素He,C项错误;第一周期元素原子最外层电子排布是从1s1过渡到1s2,D项错误。
4.C d区包括ⅢB~ⅦB族(镧系和锕系除外)元素和第Ⅷ族元素,ds区包括ⅠB族和ⅡB族元素,过渡元素包括所有的副族元素,即包括了d区、f区、ds区的元素,故C正确。
5.D s区除氢元素外均为金属元素;p区包含0族元素、ⅢA族~ⅦA族元素,含有金属元素与非金属元素;d区、ds区全部为金属元素;f区为镧系元素和锕系元素,全部为金属元素。
6.C 22Ti的原子序数为22,位于第四周期第ⅣB族,属于d区的过渡元素;根据三种核素的质量数可知,其中子数最小为26;钛的三种核素的质子数均为22,故在元素周期表中处于同一位置。
7.C K位于元素周期表中第四周期第ⅠB族,属于ds区元素,A错误;J位于元素周期表中第四周期第ⅥB族,属于d区元素,B错误;F位于元素周期表中第三周期第ⅡA族,属于s区元素,C正确;I位于元素周期表中第三周期第ⅦA族,属于p区元素,D错误。
能力提升练
1.C s区同时存在金属元素和非金属元素(H),A、B两项错误;He的最外层电子数是2,位于p区,D项错误。
2.C 某元素+3价基态离子的电子排布式为1s22s22p63s23p63d3,其原子核外电子数为21+3=24,为Cr元素,位于元素周期表第四周期第ⅥB族,属于d区元素,故选C。
3.C 基态原子的N层上只有一个电子的元素,可能为K、Cr或Cu,K为主族元素,Cr、Cu为副族元素,故A错误;基态原子的价层电子排布式为(n-1)d6~8ns2的元素为第Ⅷ族元素,故B错误;基态原子最外层的p能级上半充满的元素,其电子最后填充p能级,属于p区,故C正确;基态原子核外价层电子排布式为(n-1)dxnsy的元素的族序数不一定为x+y,例如ⅠB族、ⅡB族元素,族序数为y,故D错误。
4.D H(元素1)位于s区,O(元素2)、Ge(元素5)位于p区,Mn(元素3)位于d区,Zn(元素4)位于ds区,则表中五种元素位于4个不同的区,A项错误;元素4为Zn元素,其基态原子价层电子排布式为3d104s2,最外层电子排布式为4s2,与它具有相同最外层电子数的元素可能位于ds区、s区、p区(He)、d区、f区,B项错误;元素1的价层电子排布式为1s1,元素2的价层电子排布式为2s22p4,元素3的价层电子排布式为3d54s2,则元素1、2、3的基态原子中,未成对电子数分别为1、2、5,未成对电子数之比为1∶2∶5,C项错误;元素5为Ge,其基态原子的电子排布式为1s22s22p63s23p63d104s24p2,则其原子结构示意图为,D项正确。
5.C 根据给定物质的结构,结合W、X、Y、Z、M为原子序数依次增大的短周期元素,Z和M为同主族元素,可知W、X、Y、Z、M分别为H、C、N、O、S。基态硫原子的价层电子排布式为3s23p4,故A正确;基态氮原子的电子排布图为 ,故B正确;Z为氧元素,其基态原子的电子排布式为1s22s22p4,基态Z原子核外成对电子数是未成对电子数的3倍,故C错误;X为碳元素,其基态原子的电子排布式为1s22s22p2,因此基态碳原子核外s能级电子总数是p能级电子总数的2倍,故D正确。
6.A 理论上最活泼的金属单质是Fr,但由于其具有放射性,故一般认为最活泼的金属单质是Cs,而Cs元素和Fr元素都属于第ⅠA族元素,位于s区;最活泼的非金属元素是氟,在第ⅦA族,位于p区;常温下呈液态的金属单质为Hg,汞元素原子的价层电子排布式为5d106s2,属于第ⅡB族元素,位于ds区。
7.答案 (1)如图:
(2)ds (3)见上图
解析 (2)ds区元素原子价层电子排布式为(n-1)d10ns1和(n-1)d10ns2,而d区内6纵列部分元素的价层电子排布式为 (n-1)d5ns1,7纵列部分元素的价层电子排布式为(n-1)d5ns2,因此类比可以放在ds区。(3)4s轨道上只有1个电子,即4s1,元素原子的电子排布式可能为1s22s22p63s23p64s1(K)、1s22s22p63s23p63d54s1(Cr)或1s22s22p63s23p63d104s1(Cu),分别标在元素周期表中相应位置即可。
8.答案 ①ⅡA 三 s ②ⅣA 五 p ③ⅢB 四 d ④ⅠB 四 ds
解析 ①最后一个电子填充在s轨道,属于s区元素,为主族元素,在第三周期第ⅡA族。 ②最后一个电子填充在p轨道,属于p区元素,为主族元素,在第五周期第ⅣA族。③最后一个电子填充在d轨道,且d轨道上电子数小于10,属于d区元素,为副族元素,在第四周期第ⅢB族。④最后一个电子填充在d轨道,且d轨道上电子数等于10,属于ds区元素,为副族元素,在第四周期第ⅠB族。
9.A 因为Y元素原子的价层电子排布式中出现了np能级,所以其ns能级已经充满且只能为2个电子,则n-1=2,n=3,即Y元素原子的价层电子排布式为3s23p4,故A项错误,B项正确。Y为S元素,X为F元素,第二周期所含非金属元素种数最多,故C项正确。Z为As元素,基态砷原子的电子排布式为1s22s22p63s23p63d104s24p3,故D项正确。
误区警示 对价层电子认识的误区提醒
(1)价层电子不一定是最外层电子,主族元素的价层电子是最外层电子,对于过渡元素还包括部分内层电子。
(2)元素的价层电子数不一定等于其所在族的族序数。
10.答案 (1)HClO4>H2SO4>H3PO4 (2)第四周期第ⅦB族 [Ar]3d54s2 (3)
(4)ds 15
解析 A的基态原子有6个原子轨道填充满电子,有3个未成对电子,A为P;B原子的M层比L层少两个电子,B为S;C的基态原子核外有17种不同运动状态的电子,C为Cl;D的基态原子的价层电子排布式为3dx4s2,在常见化合物中其最高正价为+7价,则价层电子排布式为3d54s2,D为Mn;E的基态原子的M层全充满,N层没有成对电子,只有1个未成对电子,E的价层电子排布式为3d104s1,E为Cu。(1)由以上分析知,A为P,B为S,C为Cl。A、B、C三种元素最高价氧化物的水化物酸性由强到弱的顺序为HClO4>H2SO4>H3PO4。(2)D为锰元素,其在元素周期表中的位置为第四周期第ⅦB族,其基态原子的简化电子排布式为[Ar]3d54s2。(3)B为硫元素,其基态原子的价层电子的轨道表示式为。(4)E为铜元素,位于元素周期表的ds区,其基态原子的电子排布式为1s22s22p63s23p63d104s1,填有电子的轨道数为15。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
