2024科粤版九年级化学上学期单元测试卷--第二章空气、物质的构成测试卷(含答案)
文档属性
| 名称 | 2024科粤版九年级化学上学期单元测试卷--第二章空气、物质的构成测试卷(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-08 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024科粤版九年级化学上学期单元测试卷
第二章 空气、物质的构成
时间:45分钟 满分:100分
可能用到的相对原子质量:C—12
一、选择题(每小题3分,共36分,每小题只有一个选项符合题意)
1.航天活动中需要“人造空气”来供航天员呼吸,这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气,还有二氧化碳。下列关于“人造空气”的说法不正确的是 ( )
A.“人造空气”比空气中的氮气含量低
B.氮气对航天员呼吸没有任何作用,因此“人造空气”可以不需要氮气
C.“人造空气”中的氧气和空气中的氧气化学性质相同
D.潜水员在水下用的“人造空气”用氦气代替氮气,与氦气的化学性质不活泼
有关
2.下列说法错误的是 ( )
A.氮气化学性质稳定,任何情况下都不能与其他物质反应
B.氮气不支持呼吸,故可用作粮食的保护气
C.氦气的密度小且化学性质稳定,通常用于填充气球
D.工业生产排放到空气中的有害气体和烟尘会污染空气
3.下列各组物质中,前者属于纯净物,后者属于混合物的是 ( )
A.二氧化碳、澄清石灰水
B.五氧化二磷、冰水共存物
C.矿泉水、河水
D.净化后的空气、被污染的空气
4.下列化学符号既表示一种物质,又表示一个原子,还表示一种元素的是 ( )
A.H2 B.Cu C.NaCl D.H2O
5.万物皆化学,从微观视角对生活中的下列现象解释正确的是 ( )
A.水蒸发为水蒸气,所占体积变大——水分子的体积变大
B.阳光下比阴凉处湿衣服干得快——温度升高,分子间的间隔变大
C.空气比水容易压缩——气体分子间的间隔比液体分子间的间隔大
D.河水在冬天结冰后停止流动——固体物质中的分子是静止不动的
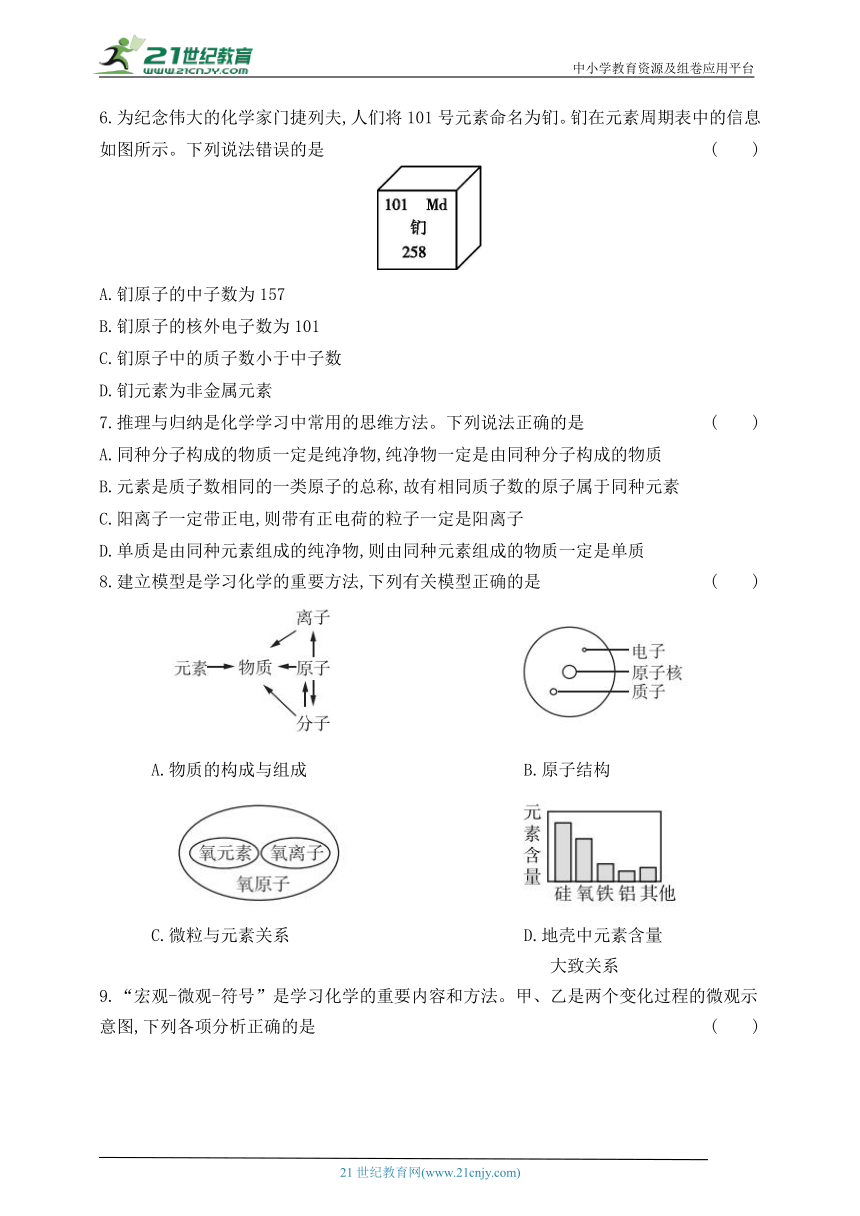
6.为纪念伟大的化学家门捷列夫,人们将101号元素命名为钔。钔在元素周期表中的信息如图所示。下列说法错误的是 ( )
A.钔原子的中子数为157
B.钔原子的核外电子数为101
C.钔原子中的质子数小于中子数
D.钔元素为非金属元素
7.推理与归纳是化学学习中常用的思维方法。下列说法正确的是 ( )
A.同种分子构成的物质一定是纯净物,纯净物一定是由同种分子构成的物质
B.元素是质子数相同的一类原子的总称,故有相同质子数的原子属于同种元素
C.阳离子一定带正电,则带有正电荷的粒子一定是阳离子
D.单质是由同种元素组成的纯净物,则由同种元素组成的物质一定是单质
8.建立模型是学习化学的重要方法,下列有关模型正确的是 ( )
A.物质的构成与组成 B.原子结构
C.微粒与元素关系 D.地壳中元素含量
大致关系
9.“宏观-微观-符号”是学习化学的重要内容和方法。甲、乙是两个变化过程的微观示意图,下列各项分析正确的是 ( )
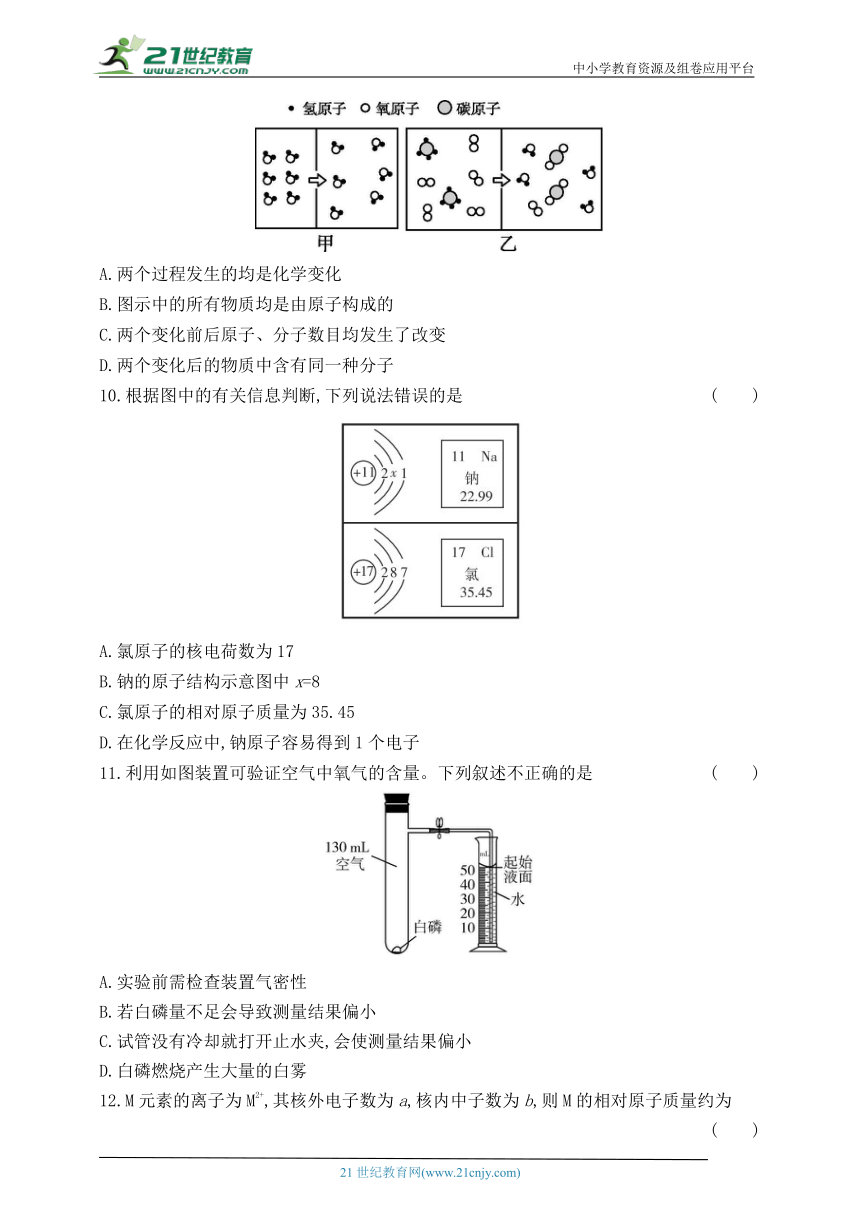
A.两个过程发生的均是化学变化
B.图示中的所有物质均是由原子构成的
C.两个变化前后原子、分子数目均发生了改变
D.两个变化后的物质中含有同一种分子
10.根据图中的有关信息判断,下列说法错误的是 ( )
A.氯原子的核电荷数为17
B.钠的原子结构示意图中x=8
C.氯原子的相对原子质量为35.45
D.在化学反应中,钠原子容易得到1个电子
11.利用如图装置可验证空气中氧气的含量。下列叙述不正确的是 ( )
A.实验前需检查装置气密性
B.若白磷量不足会导致测量结果偏小
C.试管没有冷却就打开止水夹,会使测量结果偏小
D.白磷燃烧产生大量的白雾
12.M元素的离子为M2+,其核外电子数为a,核内中子数为b,则M的相对原子质量约为 ( )
A.a+b+2 B.a+b-2
C.a+b D.b+2
二、填空及简答题(共34分)
13.(3分)成语是中华民族艺术宝库中的瑰宝。请用元素符号填写下列成语,要求元素符号表示的元素名称要与成语中的字相同或谐音。示例:高山(S)水、雪中送(C)。
群之马; 石心肠; 根结底。
14.(4分)空气是由多种气体组成的混合物,是一种宝贵的自然资源。
(1)空气中稀有气体的体积分数大约为 。
(2)夏天,从冰箱中拿出来的汽水放在桌上一段时间后,外壁有水珠出现,说明空气中含有 。
(3)空气质量日报可以及时、准确反映空气质量状况。空气质量级别分为六级,级别越高则空气污染程度越 (填“轻”或“重”)。请你提出一条防治空气污染的合理建议: 。
15.(4分)科学研究证实,物质从宏观上讲是由元素组成的,从微观上讲是由微粒构成的,例如铁是由铁原子构成的。请你在下列空格里,用“元素”“原子”“分子”或“离子”填空。
(1)水是由氧、氢两种 组成的。
(2)保持氢气化学性质的最小微粒是氢 。
(3)化学变化中的最小微粒是 。
(4)用于配制生理盐水的氯化钠晶体是由 构成的。
16.(6分)根据图示回答下列问题:
图1 蔗糖溶于水 图2 氢气燃烧的示意图
(1)图1中从微观角度获得的一条信息是 。
(2)图2中第一个框内的物质是 (填“混合物”或“化合物”,下同),第三个框内的物质是 。
(3)图1发生的是 (填“物理”或“化学”,下一空同)变化,图2发生的是 变化;从图2的微观示意图中能得到的信息是 。
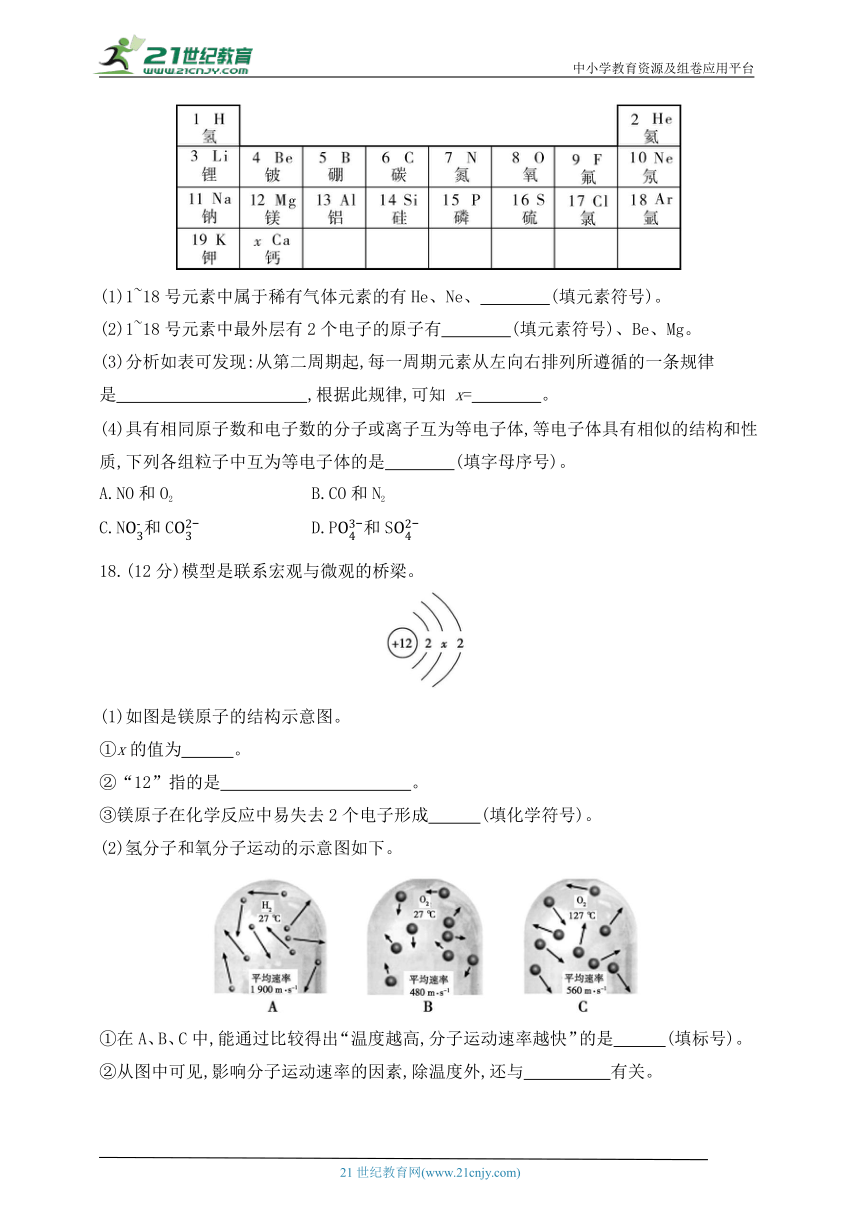
17.(5分)如下是元素周期表的部分信息,请回答下列问题:
(1)1~18号元素中属于稀有气体元素的有He、Ne、 (填元素符号)。
(2)1~18号元素中最外层有2个电子的原子有 (填元素符号)、Be、Mg。
(3)分析如表可发现:从第二周期起,每一周期元素从左向右排列所遵循的一条规律是 ,根据此规律,可知 x= 。
(4)具有相同原子数和电子数的分子或离子互为等电子体,等电子体具有相似的结构和性质,下列各组粒子中互为等电子体的是 (填字母序号)。
A.NO和O2 B.CO和N2
C.N和C D.P和S
18.(12分)模型是联系宏观与微观的桥梁。
(1)如图是镁原子的结构示意图。
①x的值为 。
②“12”指的是 。
③镁原子在化学反应中易失去2个电子形成 (填化学符号)。
(2)氢分子和氧分子运动的示意图如下。
①在A、B、C中,能通过比较得出“温度越高,分子运动速率越快”的是 (填标号)。
②从图中可见,影响分子运动速率的因素,除温度外,还与 有关。
③举一个能说明“温度升高,分子运动速率加快”的生活事例: 。
三、实验与探究题(共24分)
19.(10分)“微粒运动实验”再探究。
【实验回顾】图甲为分子运动现象的实验。
图甲
该实验利用的浓氨水的化学性质是 。 可以观察到的现象是 (填序号)。
A.烧杯A内溶液表面很快变红,液体内部由上而下缓慢变红
B.烧杯A内溶液表面和内部几乎同时很快变红
C.烧杯B内溶液表面很快变红,液体内部由上而下缓慢变红
D.烧杯B内溶液表面和内部几乎同时很快变红
【问题提出】酚酞微粒是否在运动
图乙
【实验探究】如图乙所示,将一条用水湿透的滤纸条放入图甲实验已变红的溶液中,可以观察到的现象是 。
【表达交流】同学们讨论后认为,只利用图甲中药品,不用滤纸条,改用胶头滴管也能完成实验探究,则操作步骤和现象是 。
【实验结论】由本实验可以得出有关微粒运动的结论是 (不定项选择)。
A.有的微粒是运动的,有的微粒是静止的
B.微粒都在不停地运动,但运动速率可能不同
C.微粒的运动速率与微粒的种类有关
D.微粒的运动速率与所处介质有关
E.微粒的运动速率与温度有关
20.(14分)某实验小组对教材中测定空气中氧气体积分数的实验进行了改进,并取得成功(装置如图所示)。
【实验准备】具支试管和小气球内空气的总体积为50 mL,注射器中留下的空气体积为50 mL,该装置气密性良好。
【实验探究】装入药品,按图所示连接好仪器。用酒精灯在红磷部位加热,加热时不断推拉注射器活塞,气球忽大忽小,并不断将气球中的气体全部挤入试管中。
【现象分析】
(1)实验开始时若将注射器活塞向内推,可观察到气球变 (填“大”或“小”)。
(2)加热试管底部,红磷被引燃,反应的现象是 ,足量的红磷在试管中未能全部燃烧,说明试管内剩余气体具有的化学性质为 ,写出红磷燃烧的文字表达式 。
(3)实验结束后,停止加热,待试管冷却至室温,注射器活塞稳定后,读取注射器内剩余气体的体积约为 mL。
【得出结论】氧气约占空气总体积的五分之一。
【反思评价】实验中,加热时不断推拉注射器活塞的目的是 ,此实验与教材中实验比较的优点为 。
四、分析与计算题(共6分)
21.(6分)已知A原子的质量为3.986×10-26 kg,A原子中的质子数与中子数相等。已知1个碳12原子的质量为1.993×10-26 kg。
(1)A原子的相对原子质量是多少
(2)A原子中的中子数是多少
(3)A原子中的核外电子数是多少
第二章 空气、物质的构成
1 2 3 4 5 6 7 8 9 10 11 12
B A A B C D B A D D D A
1.B 空气中各成分按体积计算,大约是氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%。所以“人造空气”比空气中的氮气含量低,A正确;氮气对航天员呼吸没有任何作用,但人体长期吸入纯氧会影响人体健康,所以“人造空气”还需要氮气,B错误;“人造空气”中的氧气与空气中的氧气属于同一种物质,化学性质相同,C正确;潜水员在水下用的“人造空气”用氦气代替氮气,与氦气的化学性质不活泼有关,D正确。
2.A 氮气化学性质稳定,一般不能与其他物质反应,但在一定条件下能与其他物质反应,故A错误;氮气不支持呼吸,可用作粮食的保护气,故B正确;氦气的密度小且化学性质稳定,通常可用于填充气球,故C正确;工业生产排放到空气中的有害气体和烟尘会污染空气,故D正确。
3.A 纯净物是由一种物质组成的,混合物是由两种或两种以上的物质组成的。“冰水共存物”属于纯净物,故B错误;矿泉水、河水、净化后的空气、被污染的空气都是混合物,故C、D错误。
4.B H2表示氢气,也可表示一个氢分子,不能表示氢元素或一个原子;Cu表示铜单质、一个铜原子或铜元素;NaCl表示氯化钠这种物质;H2O表示水这种物质,也表示一个水分子。
5.C 水蒸发为水蒸气,所占体积变大,是由于分子间间隔变大,分子体积无变化,A错误;阳光下比阴凉处湿衣服干得快,是由于温度升高,分子的运动速率变大,B错误;空气比水容易压缩,是由于气体分子间的间隔比液体分子间的间隔大,C正确;构成物质的分子都是在不停运动的,与物质的状态无关,D错误。
6.D 根据元素周期表中单元格中信息可知,左上角的数字为101,表示原子序数为101;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为101,核外电子数为101;中子数=258-101=157,大于质子数;钔带有“钅”字旁,故钔为金属元素。故D错误。
7.B 分子、原子、离子都可以构成物质,纯净物不一定是同种分子构成的物质,A错误;有相同质子数的一类原子统称为元素,故B正确;带有正电荷的粒子有质子、阳离子,质子不属于阳离子,C错误;同种元素组成的物质不一定是单质,如氧气(O2)和臭氧(O3)的混合气体由氧元素组成,但是属于混合物,D错误。
8.A 物质是由元素组成的,同时也是由分子、原子或离子构成的,A项模型与事实相符;原子核由质子和中子构成,模型中质子不在原子核内,B项模型与事实不符;氧原子和氧离子都属于氧元素,C项模型与事实不符;地壳中元素含量由多到少前四位元素依次是氧、硅、铝、铁,D项模型与事实不符。
9.D 甲图所示变化中分子种类没有改变,不属于化学变化,A错误;两个图示中物质均由分子构成,B错误;甲、乙图示中分子、原子数目都未改变,C错误;两个变化后的物质中均含有这种分子,D正确。
10.D 由原子结构示意图可知氯原子的核电荷数为17;根据电子层的电子排布特点可知,x的值为8;氯原子的相对原子质量为35.45;在化学反应中,钠原子易失去1个电子。故选D。
11.D 实验前要检查装置气密性,防止漏气,故A正确;白磷的作用是消耗试管中的氧气,若白磷量不足,则氧气消耗不尽,导致测量结果偏小,故B正确;试管没有冷却到室温,剩余气体在受热状态下,体积膨胀,造成测量结果偏小,故C正确;白磷燃烧生成P2O5固体,现象为产生大量白烟,故D错误。故选D。
12.A 由M2+的核外电子数为a,可知M原子的核外电子数为a+2,由于原子中质子数等于核外电子数,所以其质子数等于a+2。相对原子质量≈质子数+中子数,可知M元素的相对原子质量约为a+b+2。故选A。
13.(每空1分)He Fe Si
14.(每空1分)(1)0.94% (2)水蒸气 (3)重 工业生产中的废气处理达标后再排放(合理即可)
15.(每空1分)(1)元素 (2)分子 (3)原子 (4)离子
【解题思路】(1)在化学上,从宏观角度描述物质的组成用元素表示。(2)氢气是由氢分子构成的,由分子构成的物质,保持其化学性质的最小微粒是它的分子。(3)在化学变化中,分子可分成原子,原子不可再分,因此原子是化学变化中的最小微粒。(4)氯化钠晶体是由钠离子和氯离子构成的。
16.(每空1分)(1)分子在不断运动(或分子间有间隔或分子很小) (2)混合物 化合物 (3)物理 化学 化学变化中分子本身发生变化(合理即可)
【解题思路】(1)图1反映的是物质的溶解过程,可以体现的微观信息主要有分子在不断运动、分子之间有间隔、分子很小等。(2)图2第一个框中含有两种物质的分子,依据混合物由两种或两种以上物质组成,可知该框中物质是混合物;第三个框中的分子只有一种,且每个分子中有两种原子,所以该物质是化合物。(3)图1没有生成新物质,为物理变化;图2生成了新物质,为化学变化,化学变化中分子本身发生了变化。
17.(每空1分)(1)Ar (2)He (3)原子序数依次递增 20 (4)BCD
【解题思路】(3)分析表可发现:从第二周期起,每一周期元素从左向右排列所遵循的一条规律是原子序数依次递增,根据此规律,可知 x=20。(4)A.NO和O2核外电子数分别是15、16,不互为等电子体;B.CO和N2核外电子数和原子数都相同,分别都是14、2,互为等电子体;C.N和C核外电子数和原子数都相同,分别都是32、4,互为等电子体;D.P和S核外电子数和原子数都相同,分别都是50、5,互为等电子体。
18.(每空2分)(1)①8 ②镁原子的质子数为12(或其他合理答案) ③Mg2+ (2)①BC ②分子种类(或其他合理答案) ③湿衣服在阳光下比在阴凉处干得快(或其他合理答案)
【解题思路】(1)①原子中核内质子数=核外电子数,由原子结构示意图可知该原子核内有12个质子,所以核外有12个电子,则x=12-2-2=8;②原子核内的12表示的是质子数;③镁原子最外层只有 2个电子,化学反应中易失去2个电子形成镁离子,化学符号是Mg2+。(2)①由B、C两个图示可知,127 ℃时氧分子的运动速率比27 ℃时的运动速率快,能体现温度越高,分子运动速率越快;②相同温度下,氢分子和氧分子的运动速率不同,说明分子种类也能影响运动速率;③温度越高,分子运动速率越快,例如,湿衣服在阳光下比在阴凉处干得快等。
19.(每空2分)【实验回顾】能使酚酞溶液变红 C
【实验探究】滤纸条由下往上逐渐变红
【表达交流】用胶头滴管吸取变红的酚酞溶液滴入浓氨水中,溶液逐渐全部变红
【实验结论】BCD
【解题思路】【实验回顾】浓氨水具有挥发性,能挥发出氨气,氨气溶于水形成氨水,氨水能使酚酞溶液变红,所以该实验利用了氨水能使酚酞溶液变红的化学性质。可以观察到的现象:烧杯B内溶液表面很快变红,液体内部由上而下缓慢变红。【实验结论】此实验没有涉及微粒的运动速率与温度的关系。
20.(每空2分)【现象分析】(1)大 (2)产生大量白烟,放出热量 不燃烧,且不支持燃烧 红磷+氧气五氧化二磷 (3)30
【反思评价】使装置中的氧气完全反应 实验结果更准确,更环保
【解题思路】【现象分析】(1)实验开始时,若将注射器向内推,因为装置气密性良好,故试管中气体压强增大,可观察到气球变大。(2)加热试管底部,红磷被引燃,反应现象是产生大量白烟,放出热量;足量的红磷在试管中未能全部燃烧,说明试管内剩余气体的化学性质为不燃烧,且不支持燃烧;红磷点燃后和氧气反应生成五氧化二磷。(3)待注射器活塞稳定后,读取注射器内剩余气体的体积约为50 mL-
100 mL×=30 mL。
【反思评价】实验中,加热时不断推拉注射器活塞的目的是使装置中的氧气完全反应,此实验与教材中实验比较的优点为实验结果更准确,更环保。
21.解:(1)A原子的相对原子质量==24。(2分)
(2)A原子中的质子数与中子数相等,A原子的相对原子质量为24,则A原子中的中子数是24÷2=12。(2分)
(3)原子中,质子数=核外电子数,A原子中的质子数=中子数=12,故A原子中的核外电子数是12。(2分)
【解题思路】(1)根据相对原子质量的概念公式,计算A原子的相对原子质量,某原子的相对原子质量=;(2)根据相对原子质量≈质子数+中子数,计算A原子中的中子数;(3)根据原子中质子数=核外电子数,分析求A原子中的核外电子数。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2024科粤版九年级化学上学期单元测试卷
第二章 空气、物质的构成
时间:45分钟 满分:100分
可能用到的相对原子质量:C—12
一、选择题(每小题3分,共36分,每小题只有一个选项符合题意)
1.航天活动中需要“人造空气”来供航天员呼吸,这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气,还有二氧化碳。下列关于“人造空气”的说法不正确的是 ( )
A.“人造空气”比空气中的氮气含量低
B.氮气对航天员呼吸没有任何作用,因此“人造空气”可以不需要氮气
C.“人造空气”中的氧气和空气中的氧气化学性质相同
D.潜水员在水下用的“人造空气”用氦气代替氮气,与氦气的化学性质不活泼
有关
2.下列说法错误的是 ( )
A.氮气化学性质稳定,任何情况下都不能与其他物质反应
B.氮气不支持呼吸,故可用作粮食的保护气
C.氦气的密度小且化学性质稳定,通常用于填充气球
D.工业生产排放到空气中的有害气体和烟尘会污染空气
3.下列各组物质中,前者属于纯净物,后者属于混合物的是 ( )
A.二氧化碳、澄清石灰水
B.五氧化二磷、冰水共存物
C.矿泉水、河水
D.净化后的空气、被污染的空气
4.下列化学符号既表示一种物质,又表示一个原子,还表示一种元素的是 ( )
A.H2 B.Cu C.NaCl D.H2O
5.万物皆化学,从微观视角对生活中的下列现象解释正确的是 ( )
A.水蒸发为水蒸气,所占体积变大——水分子的体积变大
B.阳光下比阴凉处湿衣服干得快——温度升高,分子间的间隔变大
C.空气比水容易压缩——气体分子间的间隔比液体分子间的间隔大
D.河水在冬天结冰后停止流动——固体物质中的分子是静止不动的
6.为纪念伟大的化学家门捷列夫,人们将101号元素命名为钔。钔在元素周期表中的信息如图所示。下列说法错误的是 ( )
A.钔原子的中子数为157
B.钔原子的核外电子数为101
C.钔原子中的质子数小于中子数
D.钔元素为非金属元素
7.推理与归纳是化学学习中常用的思维方法。下列说法正确的是 ( )
A.同种分子构成的物质一定是纯净物,纯净物一定是由同种分子构成的物质
B.元素是质子数相同的一类原子的总称,故有相同质子数的原子属于同种元素
C.阳离子一定带正电,则带有正电荷的粒子一定是阳离子
D.单质是由同种元素组成的纯净物,则由同种元素组成的物质一定是单质
8.建立模型是学习化学的重要方法,下列有关模型正确的是 ( )
A.物质的构成与组成 B.原子结构
C.微粒与元素关系 D.地壳中元素含量
大致关系
9.“宏观-微观-符号”是学习化学的重要内容和方法。甲、乙是两个变化过程的微观示意图,下列各项分析正确的是 ( )
A.两个过程发生的均是化学变化
B.图示中的所有物质均是由原子构成的
C.两个变化前后原子、分子数目均发生了改变
D.两个变化后的物质中含有同一种分子
10.根据图中的有关信息判断,下列说法错误的是 ( )
A.氯原子的核电荷数为17
B.钠的原子结构示意图中x=8
C.氯原子的相对原子质量为35.45
D.在化学反应中,钠原子容易得到1个电子
11.利用如图装置可验证空气中氧气的含量。下列叙述不正确的是 ( )
A.实验前需检查装置气密性
B.若白磷量不足会导致测量结果偏小
C.试管没有冷却就打开止水夹,会使测量结果偏小
D.白磷燃烧产生大量的白雾
12.M元素的离子为M2+,其核外电子数为a,核内中子数为b,则M的相对原子质量约为 ( )
A.a+b+2 B.a+b-2
C.a+b D.b+2
二、填空及简答题(共34分)
13.(3分)成语是中华民族艺术宝库中的瑰宝。请用元素符号填写下列成语,要求元素符号表示的元素名称要与成语中的字相同或谐音。示例:高山(S)水、雪中送(C)。
群之马; 石心肠; 根结底。
14.(4分)空气是由多种气体组成的混合物,是一种宝贵的自然资源。
(1)空气中稀有气体的体积分数大约为 。
(2)夏天,从冰箱中拿出来的汽水放在桌上一段时间后,外壁有水珠出现,说明空气中含有 。
(3)空气质量日报可以及时、准确反映空气质量状况。空气质量级别分为六级,级别越高则空气污染程度越 (填“轻”或“重”)。请你提出一条防治空气污染的合理建议: 。
15.(4分)科学研究证实,物质从宏观上讲是由元素组成的,从微观上讲是由微粒构成的,例如铁是由铁原子构成的。请你在下列空格里,用“元素”“原子”“分子”或“离子”填空。
(1)水是由氧、氢两种 组成的。
(2)保持氢气化学性质的最小微粒是氢 。
(3)化学变化中的最小微粒是 。
(4)用于配制生理盐水的氯化钠晶体是由 构成的。
16.(6分)根据图示回答下列问题:
图1 蔗糖溶于水 图2 氢气燃烧的示意图
(1)图1中从微观角度获得的一条信息是 。
(2)图2中第一个框内的物质是 (填“混合物”或“化合物”,下同),第三个框内的物质是 。
(3)图1发生的是 (填“物理”或“化学”,下一空同)变化,图2发生的是 变化;从图2的微观示意图中能得到的信息是 。
17.(5分)如下是元素周期表的部分信息,请回答下列问题:
(1)1~18号元素中属于稀有气体元素的有He、Ne、 (填元素符号)。
(2)1~18号元素中最外层有2个电子的原子有 (填元素符号)、Be、Mg。
(3)分析如表可发现:从第二周期起,每一周期元素从左向右排列所遵循的一条规律是 ,根据此规律,可知 x= 。
(4)具有相同原子数和电子数的分子或离子互为等电子体,等电子体具有相似的结构和性质,下列各组粒子中互为等电子体的是 (填字母序号)。
A.NO和O2 B.CO和N2
C.N和C D.P和S
18.(12分)模型是联系宏观与微观的桥梁。
(1)如图是镁原子的结构示意图。
①x的值为 。
②“12”指的是 。
③镁原子在化学反应中易失去2个电子形成 (填化学符号)。
(2)氢分子和氧分子运动的示意图如下。
①在A、B、C中,能通过比较得出“温度越高,分子运动速率越快”的是 (填标号)。
②从图中可见,影响分子运动速率的因素,除温度外,还与 有关。
③举一个能说明“温度升高,分子运动速率加快”的生活事例: 。
三、实验与探究题(共24分)
19.(10分)“微粒运动实验”再探究。
【实验回顾】图甲为分子运动现象的实验。
图甲
该实验利用的浓氨水的化学性质是 。 可以观察到的现象是 (填序号)。
A.烧杯A内溶液表面很快变红,液体内部由上而下缓慢变红
B.烧杯A内溶液表面和内部几乎同时很快变红
C.烧杯B内溶液表面很快变红,液体内部由上而下缓慢变红
D.烧杯B内溶液表面和内部几乎同时很快变红
【问题提出】酚酞微粒是否在运动
图乙
【实验探究】如图乙所示,将一条用水湿透的滤纸条放入图甲实验已变红的溶液中,可以观察到的现象是 。
【表达交流】同学们讨论后认为,只利用图甲中药品,不用滤纸条,改用胶头滴管也能完成实验探究,则操作步骤和现象是 。
【实验结论】由本实验可以得出有关微粒运动的结论是 (不定项选择)。
A.有的微粒是运动的,有的微粒是静止的
B.微粒都在不停地运动,但运动速率可能不同
C.微粒的运动速率与微粒的种类有关
D.微粒的运动速率与所处介质有关
E.微粒的运动速率与温度有关
20.(14分)某实验小组对教材中测定空气中氧气体积分数的实验进行了改进,并取得成功(装置如图所示)。
【实验准备】具支试管和小气球内空气的总体积为50 mL,注射器中留下的空气体积为50 mL,该装置气密性良好。
【实验探究】装入药品,按图所示连接好仪器。用酒精灯在红磷部位加热,加热时不断推拉注射器活塞,气球忽大忽小,并不断将气球中的气体全部挤入试管中。
【现象分析】
(1)实验开始时若将注射器活塞向内推,可观察到气球变 (填“大”或“小”)。
(2)加热试管底部,红磷被引燃,反应的现象是 ,足量的红磷在试管中未能全部燃烧,说明试管内剩余气体具有的化学性质为 ,写出红磷燃烧的文字表达式 。
(3)实验结束后,停止加热,待试管冷却至室温,注射器活塞稳定后,读取注射器内剩余气体的体积约为 mL。
【得出结论】氧气约占空气总体积的五分之一。
【反思评价】实验中,加热时不断推拉注射器活塞的目的是 ,此实验与教材中实验比较的优点为 。
四、分析与计算题(共6分)
21.(6分)已知A原子的质量为3.986×10-26 kg,A原子中的质子数与中子数相等。已知1个碳12原子的质量为1.993×10-26 kg。
(1)A原子的相对原子质量是多少
(2)A原子中的中子数是多少
(3)A原子中的核外电子数是多少
第二章 空气、物质的构成
1 2 3 4 5 6 7 8 9 10 11 12
B A A B C D B A D D D A
1.B 空气中各成分按体积计算,大约是氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%。所以“人造空气”比空气中的氮气含量低,A正确;氮气对航天员呼吸没有任何作用,但人体长期吸入纯氧会影响人体健康,所以“人造空气”还需要氮气,B错误;“人造空气”中的氧气与空气中的氧气属于同一种物质,化学性质相同,C正确;潜水员在水下用的“人造空气”用氦气代替氮气,与氦气的化学性质不活泼有关,D正确。
2.A 氮气化学性质稳定,一般不能与其他物质反应,但在一定条件下能与其他物质反应,故A错误;氮气不支持呼吸,可用作粮食的保护气,故B正确;氦气的密度小且化学性质稳定,通常可用于填充气球,故C正确;工业生产排放到空气中的有害气体和烟尘会污染空气,故D正确。
3.A 纯净物是由一种物质组成的,混合物是由两种或两种以上的物质组成的。“冰水共存物”属于纯净物,故B错误;矿泉水、河水、净化后的空气、被污染的空气都是混合物,故C、D错误。
4.B H2表示氢气,也可表示一个氢分子,不能表示氢元素或一个原子;Cu表示铜单质、一个铜原子或铜元素;NaCl表示氯化钠这种物质;H2O表示水这种物质,也表示一个水分子。
5.C 水蒸发为水蒸气,所占体积变大,是由于分子间间隔变大,分子体积无变化,A错误;阳光下比阴凉处湿衣服干得快,是由于温度升高,分子的运动速率变大,B错误;空气比水容易压缩,是由于气体分子间的间隔比液体分子间的间隔大,C正确;构成物质的分子都是在不停运动的,与物质的状态无关,D错误。
6.D 根据元素周期表中单元格中信息可知,左上角的数字为101,表示原子序数为101;根据原子中原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为101,核外电子数为101;中子数=258-101=157,大于质子数;钔带有“钅”字旁,故钔为金属元素。故D错误。
7.B 分子、原子、离子都可以构成物质,纯净物不一定是同种分子构成的物质,A错误;有相同质子数的一类原子统称为元素,故B正确;带有正电荷的粒子有质子、阳离子,质子不属于阳离子,C错误;同种元素组成的物质不一定是单质,如氧气(O2)和臭氧(O3)的混合气体由氧元素组成,但是属于混合物,D错误。
8.A 物质是由元素组成的,同时也是由分子、原子或离子构成的,A项模型与事实相符;原子核由质子和中子构成,模型中质子不在原子核内,B项模型与事实不符;氧原子和氧离子都属于氧元素,C项模型与事实不符;地壳中元素含量由多到少前四位元素依次是氧、硅、铝、铁,D项模型与事实不符。
9.D 甲图所示变化中分子种类没有改变,不属于化学变化,A错误;两个图示中物质均由分子构成,B错误;甲、乙图示中分子、原子数目都未改变,C错误;两个变化后的物质中均含有这种分子,D正确。
10.D 由原子结构示意图可知氯原子的核电荷数为17;根据电子层的电子排布特点可知,x的值为8;氯原子的相对原子质量为35.45;在化学反应中,钠原子易失去1个电子。故选D。
11.D 实验前要检查装置气密性,防止漏气,故A正确;白磷的作用是消耗试管中的氧气,若白磷量不足,则氧气消耗不尽,导致测量结果偏小,故B正确;试管没有冷却到室温,剩余气体在受热状态下,体积膨胀,造成测量结果偏小,故C正确;白磷燃烧生成P2O5固体,现象为产生大量白烟,故D错误。故选D。
12.A 由M2+的核外电子数为a,可知M原子的核外电子数为a+2,由于原子中质子数等于核外电子数,所以其质子数等于a+2。相对原子质量≈质子数+中子数,可知M元素的相对原子质量约为a+b+2。故选A。
13.(每空1分)He Fe Si
14.(每空1分)(1)0.94% (2)水蒸气 (3)重 工业生产中的废气处理达标后再排放(合理即可)
15.(每空1分)(1)元素 (2)分子 (3)原子 (4)离子
【解题思路】(1)在化学上,从宏观角度描述物质的组成用元素表示。(2)氢气是由氢分子构成的,由分子构成的物质,保持其化学性质的最小微粒是它的分子。(3)在化学变化中,分子可分成原子,原子不可再分,因此原子是化学变化中的最小微粒。(4)氯化钠晶体是由钠离子和氯离子构成的。
16.(每空1分)(1)分子在不断运动(或分子间有间隔或分子很小) (2)混合物 化合物 (3)物理 化学 化学变化中分子本身发生变化(合理即可)
【解题思路】(1)图1反映的是物质的溶解过程,可以体现的微观信息主要有分子在不断运动、分子之间有间隔、分子很小等。(2)图2第一个框中含有两种物质的分子,依据混合物由两种或两种以上物质组成,可知该框中物质是混合物;第三个框中的分子只有一种,且每个分子中有两种原子,所以该物质是化合物。(3)图1没有生成新物质,为物理变化;图2生成了新物质,为化学变化,化学变化中分子本身发生了变化。
17.(每空1分)(1)Ar (2)He (3)原子序数依次递增 20 (4)BCD
【解题思路】(3)分析表可发现:从第二周期起,每一周期元素从左向右排列所遵循的一条规律是原子序数依次递增,根据此规律,可知 x=20。(4)A.NO和O2核外电子数分别是15、16,不互为等电子体;B.CO和N2核外电子数和原子数都相同,分别都是14、2,互为等电子体;C.N和C核外电子数和原子数都相同,分别都是32、4,互为等电子体;D.P和S核外电子数和原子数都相同,分别都是50、5,互为等电子体。
18.(每空2分)(1)①8 ②镁原子的质子数为12(或其他合理答案) ③Mg2+ (2)①BC ②分子种类(或其他合理答案) ③湿衣服在阳光下比在阴凉处干得快(或其他合理答案)
【解题思路】(1)①原子中核内质子数=核外电子数,由原子结构示意图可知该原子核内有12个质子,所以核外有12个电子,则x=12-2-2=8;②原子核内的12表示的是质子数;③镁原子最外层只有 2个电子,化学反应中易失去2个电子形成镁离子,化学符号是Mg2+。(2)①由B、C两个图示可知,127 ℃时氧分子的运动速率比27 ℃时的运动速率快,能体现温度越高,分子运动速率越快;②相同温度下,氢分子和氧分子的运动速率不同,说明分子种类也能影响运动速率;③温度越高,分子运动速率越快,例如,湿衣服在阳光下比在阴凉处干得快等。
19.(每空2分)【实验回顾】能使酚酞溶液变红 C
【实验探究】滤纸条由下往上逐渐变红
【表达交流】用胶头滴管吸取变红的酚酞溶液滴入浓氨水中,溶液逐渐全部变红
【实验结论】BCD
【解题思路】【实验回顾】浓氨水具有挥发性,能挥发出氨气,氨气溶于水形成氨水,氨水能使酚酞溶液变红,所以该实验利用了氨水能使酚酞溶液变红的化学性质。可以观察到的现象:烧杯B内溶液表面很快变红,液体内部由上而下缓慢变红。【实验结论】此实验没有涉及微粒的运动速率与温度的关系。
20.(每空2分)【现象分析】(1)大 (2)产生大量白烟,放出热量 不燃烧,且不支持燃烧 红磷+氧气五氧化二磷 (3)30
【反思评价】使装置中的氧气完全反应 实验结果更准确,更环保
【解题思路】【现象分析】(1)实验开始时,若将注射器向内推,因为装置气密性良好,故试管中气体压强增大,可观察到气球变大。(2)加热试管底部,红磷被引燃,反应现象是产生大量白烟,放出热量;足量的红磷在试管中未能全部燃烧,说明试管内剩余气体的化学性质为不燃烧,且不支持燃烧;红磷点燃后和氧气反应生成五氧化二磷。(3)待注射器活塞稳定后,读取注射器内剩余气体的体积约为50 mL-
100 mL×=30 mL。
【反思评价】实验中,加热时不断推拉注射器活塞的目的是使装置中的氧气完全反应,此实验与教材中实验比较的优点为实验结果更准确,更环保。
21.解:(1)A原子的相对原子质量==24。(2分)
(2)A原子中的质子数与中子数相等,A原子的相对原子质量为24,则A原子中的中子数是24÷2=12。(2分)
(3)原子中,质子数=核外电子数,A原子中的质子数=中子数=12,故A原子中的核外电子数是12。(2分)
【解题思路】(1)根据相对原子质量的概念公式,计算A原子的相对原子质量,某原子的相对原子质量=;(2)根据相对原子质量≈质子数+中子数,计算A原子中的中子数;(3)根据原子中质子数=核外电子数,分析求A原子中的核外电子数。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
