化学人教版(2019)必修第一册1.1.1分散系及其分类(共34张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.1分散系及其分类(共34张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 33.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-08 00:00:00 | ||
图片预览





文档简介
(共34张PPT)
第一节 物质的分类
第一课时 分散系及其分类
第一章 物质及其变化
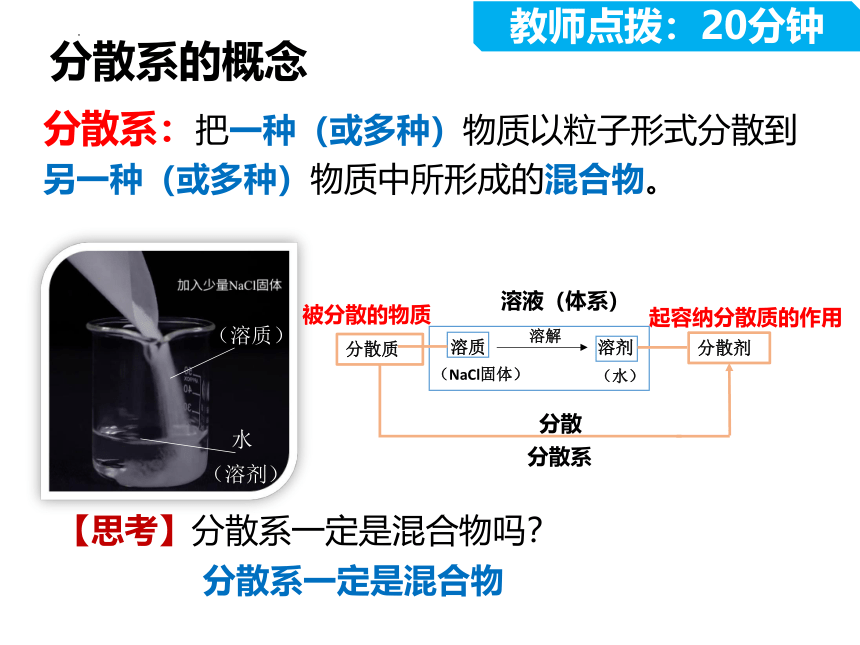
分散系:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
溶质
溶剂
(溶质)
(溶剂)
水
溶液(体系)
溶解
(NaCl固体)
(水)
分散质
分散剂
分散系
分散
分散系的概念
被分散的物质
起容纳分散质的作用
教师点拨:20分钟
【思考】分散系一定是混合物吗?
分散系一定是混合物
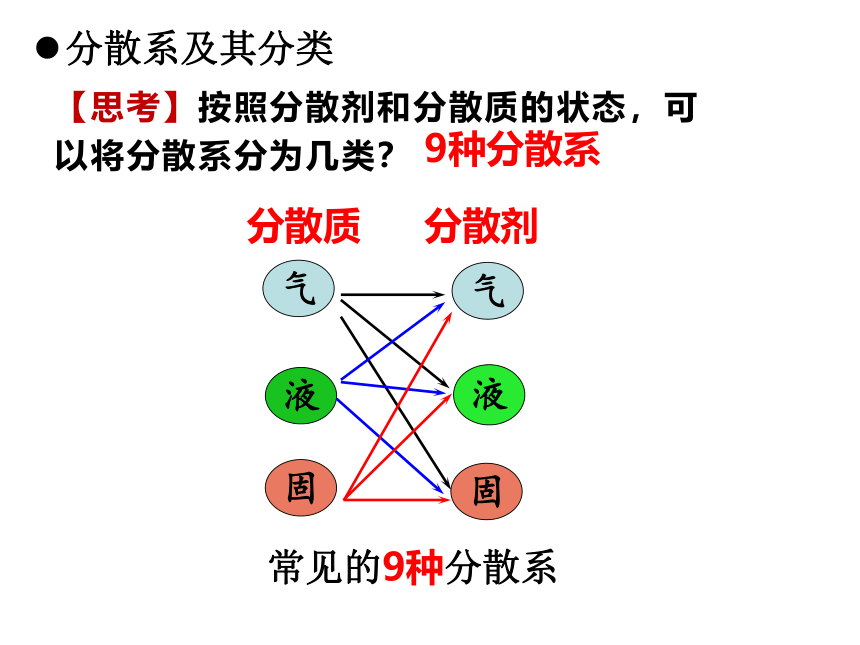
常见的9种分散系
分散质
分散剂
气
液
固
气
液
固
【思考】按照分散剂和分散质的状态,可以将分散系分为几类?
9种分散系
分散系及其分类
分散系及其分类
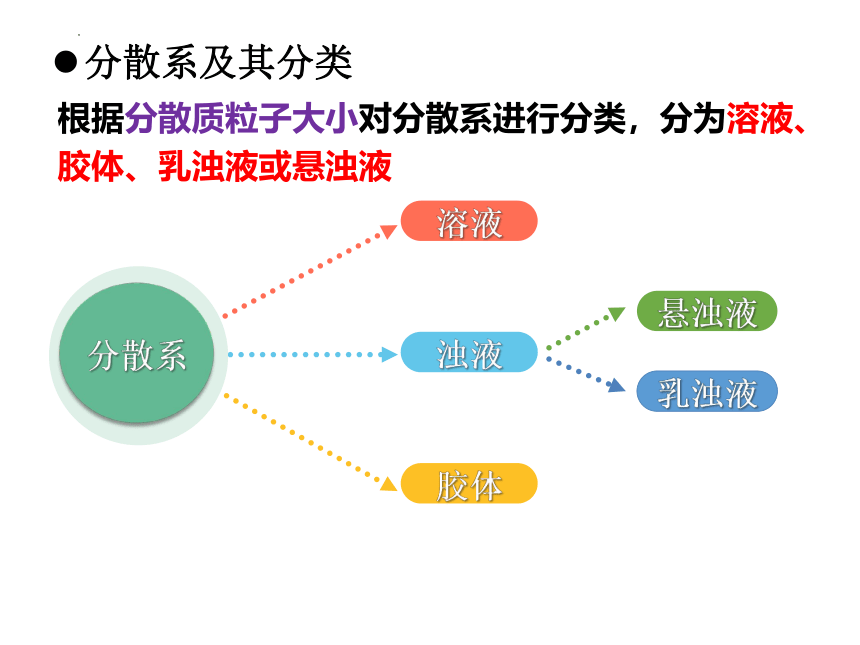
溶液
胶体
分散系
乳浊液
悬浊液
浊液
根据分散质粒子大小对分散系进行分类,分为溶液、胶体、乳浊液或悬浊液
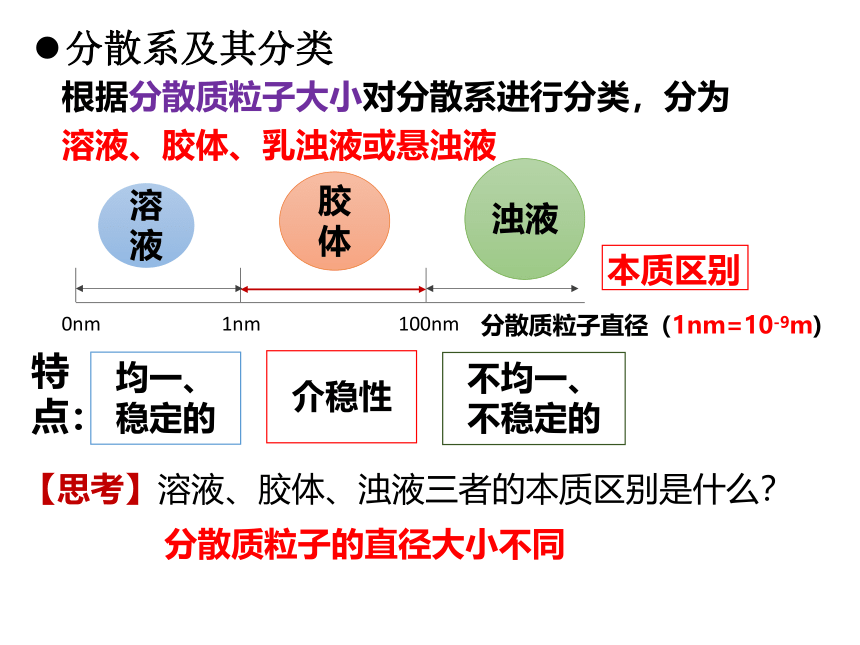
根据分散质粒子大小对分散系进行分类,分为溶液、胶体、乳浊液或悬浊液
溶液
胶体
浊液
0nm
1nm
100nm
分散质粒子直径(1nm=10-9m)
特点:
均一、稳定的
介稳性
不均一、不稳定的
本质区别
分散系及其分类
【思考】溶液、胶体、浊液三者的本质区别是什么?
分散质粒子的直径大小不同
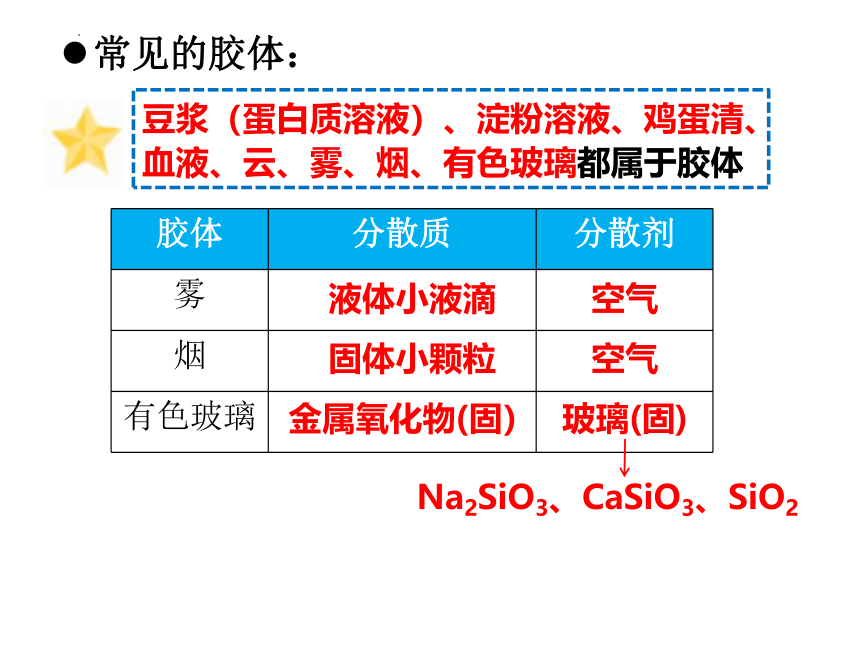
豆浆(蛋白质溶液)、淀粉溶液、鸡蛋清、血液、云、雾、烟、有色玻璃都属于胶体
常见的胶体:
胶体 分散质 分散剂
雾
烟
有色玻璃
液体小液滴
空气
固体小颗粒
空气
金属氧化物(固)
玻璃(固)
Na2SiO3、CaSiO3、SiO2
分散系及其分类
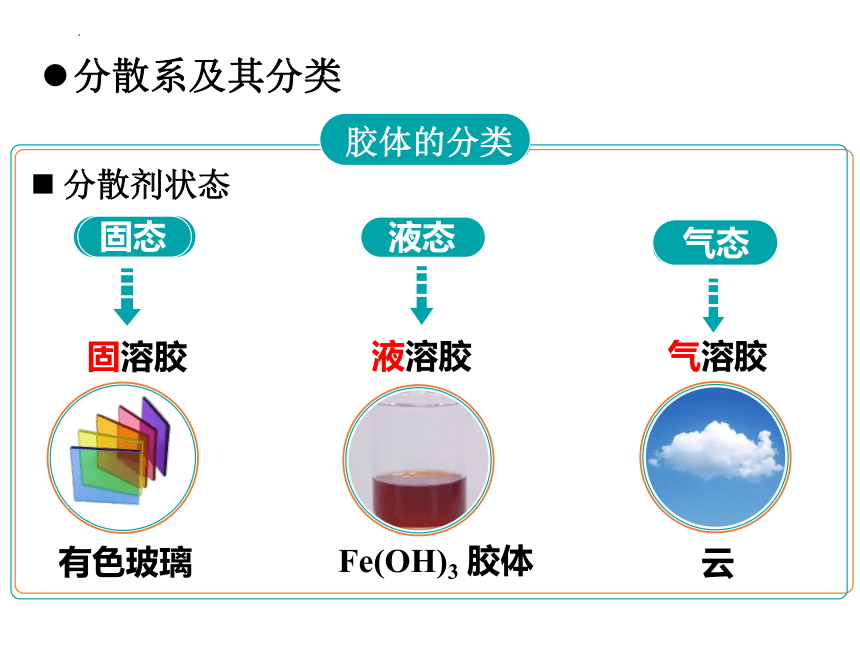
胶体的分类
分散剂状态
固溶胶
有色玻璃
固态
液溶胶
液态
气溶胶
云
气态
Fe(OH)3 胶体
取两个100 mL小烧杯,分别加入40 mL蒸馏水和40 mLCuSO4溶液。将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴FeCl3饱和溶液。继续煮沸至液体呈现红褐色,停止加热。观察制得的Fe(OH)3胶体。
胶体的制备、性质及应用
实验1-1
化学方程式:FeCl3+3H2O Fe(OH)3(胶体)+3HCl
区别:FeCl3+3NaOH=Fe(OH)3↓+3NaCl
注意事项:
1、不能使用自来水;
2、实验过程不能用玻璃棒搅拌;
3、当反应体系呈现红褐色,即制得氢氧化铁胶体,应立即停止加热,否则也容易出现浑浊,产生红褐色的氢氧化铁沉淀。
4.必须使用FeCl3饱和溶液,若浓度过低,不利于氢氧化铁胶体形成;
5.水煮沸再滴加FeCl3饱和溶液,直接加热FeCl3饱和溶液会生成氢氧化铁沉淀
氢氧化铁胶体的制备
胶体的制备、性质及应用
实验1-1
把盛有CuSO4溶液和Fe(OH)3胶体的烧杯置于暗处,分别用红色激光笔照射烧杯中的液体,在与光束垂直的方向进行观察,并记录现象。
CuSO4溶液
Fe(OH)3胶体
鉴别胶体跟溶液的方法:利用丁达尔效应
原理:胶体粒子对光的散射
现象:形成一道光亮的“通路”
(1)丁达尔效应:可见光束通过胶体时,在入射光侧面可看到一条光亮的通路
溶液:散射极其微弱
浊液:分散质粒子直径大于可见光的波长,它们对光只有反射作用,不会产生光的散射
胶体的性质
胶体的制备、性质及应用
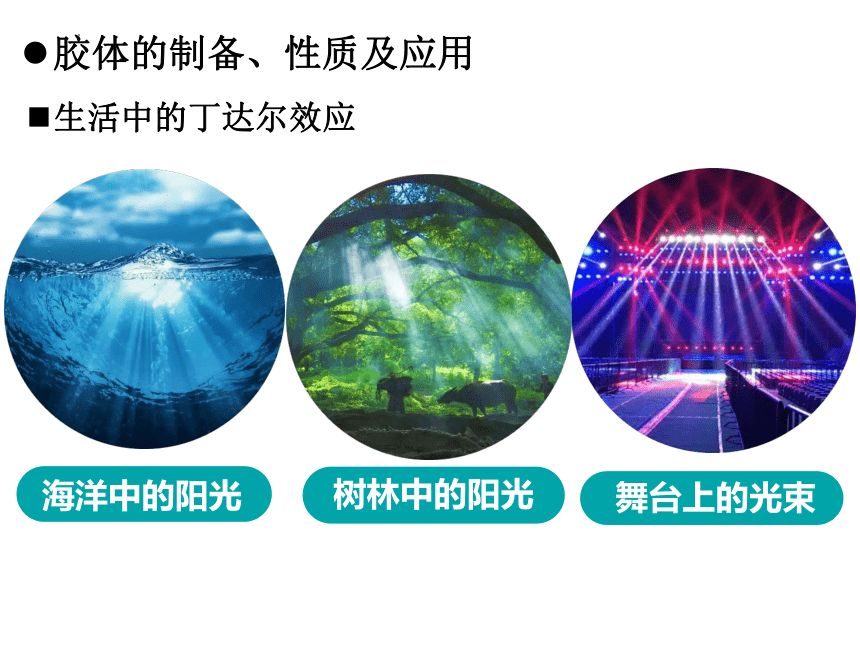
生活中的丁达尔效应
海洋中的阳光
舞台上的光束
树林中的阳光
原因①:胶体粒子可以通过吸附离子而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥,不易聚集而稳定。(主要原因)
(2)介稳性:
{[Fe(OH)3]m·nFeO+(n-x)Cl-}x+·xCl-
胶核
吸附层
胶粒
扩散层
胶核
胶体不带电,带电的是胶体粒子
胶体的性质
胶核
Fe(OH)3胶体中的1个胶体粒子不是1个Fe(OH)3分子,而是很多个Fe(OH)3分子聚集在一起形成的粒子直径在1~100nm的集合体。
胶体的性质
(2)介稳性:
胶体不带电,带电的是胶体粒子
根据胶体的介稳性,想一想如何破坏胶体的介稳性,使胶体发生聚沉?
原因②:分散剂分子对胶粒无规则的撞击,
做布朗运动。
原因①:胶体粒子可以通过吸附离子而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥,不易聚集而稳定。(主要原因)
胶体的性质
(3)聚沉:胶体的介稳性被破坏,胶体粒子聚集成为较大的颗粒而以沉淀形式从分散剂中析出。
聚沉方法
加入少量电解质(酸、碱、盐)
加热
搅拌
加入与胶体粒子带相反电荷胶粒的胶体
加快胶体粒子运动的速率,增大胶体粒子之间的碰撞机会
中和胶体粒子的电性,消除胶体粒子间的相互排斥
胶体的性质
胶体聚沉应用实例
①卤水点豆腐:盐卤/石膏
②江河入海口处形成三角洲:
有的三角洲是胶体,出现在河流入海口
这是因为河水和海水的成分不同,所含的胶体微粒就不同,当带正电的微粒与带负电微粒相遇时,就发生胶体的聚沉,产生了沉淀。
盐卤(MgCl2·6H2O)或
石膏(CaSO4·2H2O)溶液
胶体的性质
胶体聚沉应用实例
④胶体的净水作用:如明矾(KAl(SO4)2 12H2O)净水
③FeCl3溶液用于伤口止血
不同品牌的墨水不能混用!!!
胶体的性质
(4)电泳
Fe(OH)3胶体
Fe(OH)3胶体
颜色变深
颜色变浅
通电前
通电后
Fe(OH)3胶体粒子带正电荷
电泳:由于胶体粒子带有电荷,在电场作用下,胶体粒子在分散剂中作定向移动的现象。
【注意】:胶体本身不带电,带电的是胶体粒子(通过吸附某种离子带电)。
不是所有的胶体粒子都带电。如淀粉的胶粒不带电。
可应用于静电除尘
静电除尘原理是含尘气体经过高压静电场时被电分离,尘粒与负离子结合带上负电后,趋向阳极表面放电而沉积。
胶体的性质
(1)胶体与浊液分离—过滤 胶体能够通过滤纸,浊液中的微粒不能透过滤纸。
(2)胶体与溶液分离— 渗析 溶液中的粒子或小分子能够透过半透膜,胶体微粒不能透过半透膜。
胶体的性质
生活中渗析法的应用
血液实际上是一种液溶胶
血液透析又叫做人工肾,是把血液引出体外,然后借助透析机上的装置,把血液泵入透析器,通过透析器里面的透析膜进行物质交换,清除血液中多余的水分以及代谢废物,补充有益的电解质,保持酸碱平衡,再把清洁后的血液送回身体内。
血 液 透 析
【归纳总结】溶液、胶体、浊液三者的性质差异
溶液 胶体 浊液
分散质粒子的直径 <1nm 1~100nm >100nm
分散质粒子 分子或离子 许多集合体或单个高分子 巨大数目分子集合体
性 质 外观 均一、透明 均一 不均一、不透明
稳定性 稳定 介稳性 不稳定
能否透过滤纸 能 能 不能
能否透过半透膜 能 不能 不能
是否具有丁达尔效应 无 有 无
实例 食盐水、碘酒 豆浆、牛奶 泥水
1.下列现象与胶体的性质无关的是( )A.夏日的傍晚常常看到万丈霞光穿云而过美不胜收B.过滤除去氯化钠溶液中的泥沙C.食品加工厂利用豆浆中加入盐卤做豆腐D.化工厂利用静电除尘技术去除废气中的固体悬浮物
B
丁达尔效应
悬浊液
聚沉
电泳
实战演练
2.某同学在实验室进行了如图所示的实验,下列说法错误的是( )
A.利用过滤的方法,可将Z中固体与液体分离B.X、Z烧杯中分散质相同C.Z中分散系能产生丁达尔效应D.Y中放出的气体为CO2
B
溶液
胶体
CaCO3+2HCl=CaCl2+H2O+CO2↑
固体不能通过滤纸,胶体可以透过滤纸
实战演练
3、下列现象或技术应用中,不涉及胶体性质的是( )
A.在江河入海处容易形成三角洲
B.向豆浆中加入石膏容易形成美味的豆腐
C.在氯化铁饱和溶液中加入浓NaOH溶液,产生红褐色沉淀
D.清晨,在茂密的森林中,常常可以看到从枝叶间透过的一道道光柱
C
聚沉
聚沉
沉淀
丁达尔效应
实战演练
4、胶体是一种常见的分散系,按要求回答下列问题:
(1)将饱和三氯化铁溶液滴入沸水时,得到的液体是___________色,反应的化学方程式为 。
(2)用此分散系进行下列实验:
①将其装入U形管内,用石墨作电极,接通直接电源,通电一段时间后发现阴极附近颜色________,这种现象称为_______。
②向其中逐滴加入过量稀硫酸,现象是先 _ 再 。
红褐
变深
电泳
产生红褐色沉淀
沉淀溶解成棕黄色溶液
先聚沉
Fe(OH)3↓又与稀H2SO4发生中和反应
5、下列叙述正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液中的溶质微粒不能透过半透膜,胶体中的分散质粒子能透过半透膜
C.胶体区别于其他分散系的本质特征是胶体具有丁达尔效应
D.利用半透膜可除去淀粉溶液中的少量NaCl
D
胶粒带电荷,胶体呈电中性
不能
能
分散质粒子直径的大小
胶体
胶体与溶液分离—渗析
溶液中的粒子或小分子能够透过半透膜,胶体微粒不能透过半透膜。
6、朱自清先生在《荷塘月色》中写道:“溥薄的青雾浮起在荷塘里......月光是隔离树照过来的,高处丛生的灌木,落下参差的斑驳的黑影.....”月光穿过薄雾所形成的种种美景的本质原因是( )
A.发生丁达尔效应
B.光是一种胶体
C.雾是一种胶体
D.空气中的小水滴的直径介于1nm~100nm之间
D
7、下列说法正确的是( )
A.丁达尔效应不是胶体特有的现象,溶液与浊液也有
B.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有
C.胶体粒子的直径小于10-9m
D.丁达尔效应可用于区别胶体和溶液
本质区别是分散质粒子直径大小
D
1nm=10-9m
8.下列不会出现丁达尔效应的分散系是( )①鸡蛋清溶液 ②水
③淀粉溶液 ④蔗糖溶液
⑤FeCl3溶液 ⑥豆浆A.④⑤ B.③④ C.②④⑥ D.①③④
A
水、蔗糖溶液和FeCl3溶液不属于胶体,且水不是分散系,鸡蛋清溶液、淀粉溶液、豆浆属于胶体,会出现丁达尔效应。
9.淀粉溶液是一种胶体,并且淀粉遇碘单质变蓝。现将淀粉和Na2SO4的稀溶液混合,装在半透膜袋中,浸泡在盛有蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是( )A.加入BaCl2溶液产生白色沉淀
B.加入碘水不变蓝C.加入BaCl2溶液没有白色沉淀产生
D.加入碘水变蓝
B
解析:这是一个渗析实验,如果半透膜完好无损,则只有钠离子和硫酸根离子能透过半透膜,淀粉分子不能透过半透膜,故向烧杯中的液体中加入碘水不变蓝,可以证明半透膜完好无损。
10.有一胶体,在电泳实验中其胶粒向阴极移动,对这种胶体进行下列处理,不发生聚沉的是( )A.加硫酸钠溶液 B.加热
C.加硅酸胶体 D.加氢氧化铁胶体
D
解析:由题意可知胶体粒子带有正电荷,加热、加电解质溶液、加胶粒带负电荷的胶体(硅酸胶体)都能使其聚沉。
11.“纳米技术”广泛应用于催化及军事科学中,“纳米材料”是粒子直径为1~100 nm(纳米)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )①是溶液 ②是胶体 ③是浊液
④不能透过滤纸 ⑤能透过滤纸 ⑥能产生丁达尔效应 ⑦静置后,会析出黑色沉淀A.②⑤⑥ B.②⑥⑦
C.①⑤ D.③④⑦
A
解析:“纳米材料”是粒子直径为1~100 nm的材料,纳米碳就是其中的一种。属于胶体分散质微粒直径的大小,若将纳米碳均匀地分散到蒸馏水中形成分散系是胶体,具有丁达尔现象,能透过滤纸,具有介稳性,不生成沉淀,故②⑤⑥正确。
12.有人设想通过特殊的方法将碳酸钙加工成为纳米碳酸钙(即碳酸钙粒子直径达到纳米级),这将使建筑材料的性能发生巨大的变化。下列关于纳米碳酸钙的说法正确的是( )A.纳米碳酸钙是与胶体相似的分散系 B.纳米碳酸钙分散到水中所得到的分散系会产生丁达尔效应C.纳米碳酸钙的化学性质与原来碳酸钙完全不同D.纳米碳酸钙粒子不能透过滤纸
B
纳米碳酸钙是纯净物,分散系是混合物
不会发生改变
与胶体中的胶粒(微粒直径在10-9~10-7m之间)能透过滤纸一样,纳米碳酸钙粒子也能透过滤纸
第一节 物质的分类
第一课时 分散系及其分类
第一章 物质及其变化
分散系:把一种(或多种)物质以粒子形式分散到另一种(或多种)物质中所形成的混合物。
溶质
溶剂
(溶质)
(溶剂)
水
溶液(体系)
溶解
(NaCl固体)
(水)
分散质
分散剂
分散系
分散
分散系的概念
被分散的物质
起容纳分散质的作用
教师点拨:20分钟
【思考】分散系一定是混合物吗?
分散系一定是混合物
常见的9种分散系
分散质
分散剂
气
液
固
气
液
固
【思考】按照分散剂和分散质的状态,可以将分散系分为几类?
9种分散系
分散系及其分类
分散系及其分类
溶液
胶体
分散系
乳浊液
悬浊液
浊液
根据分散质粒子大小对分散系进行分类,分为溶液、胶体、乳浊液或悬浊液
根据分散质粒子大小对分散系进行分类,分为溶液、胶体、乳浊液或悬浊液
溶液
胶体
浊液
0nm
1nm
100nm
分散质粒子直径(1nm=10-9m)
特点:
均一、稳定的
介稳性
不均一、不稳定的
本质区别
分散系及其分类
【思考】溶液、胶体、浊液三者的本质区别是什么?
分散质粒子的直径大小不同
豆浆(蛋白质溶液)、淀粉溶液、鸡蛋清、血液、云、雾、烟、有色玻璃都属于胶体
常见的胶体:
胶体 分散质 分散剂
雾
烟
有色玻璃
液体小液滴
空气
固体小颗粒
空气
金属氧化物(固)
玻璃(固)
Na2SiO3、CaSiO3、SiO2
分散系及其分类
胶体的分类
分散剂状态
固溶胶
有色玻璃
固态
液溶胶
液态
气溶胶
云
气态
Fe(OH)3 胶体
取两个100 mL小烧杯,分别加入40 mL蒸馏水和40 mLCuSO4溶液。将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴FeCl3饱和溶液。继续煮沸至液体呈现红褐色,停止加热。观察制得的Fe(OH)3胶体。
胶体的制备、性质及应用
实验1-1
化学方程式:FeCl3+3H2O Fe(OH)3(胶体)+3HCl
区别:FeCl3+3NaOH=Fe(OH)3↓+3NaCl
注意事项:
1、不能使用自来水;
2、实验过程不能用玻璃棒搅拌;
3、当反应体系呈现红褐色,即制得氢氧化铁胶体,应立即停止加热,否则也容易出现浑浊,产生红褐色的氢氧化铁沉淀。
4.必须使用FeCl3饱和溶液,若浓度过低,不利于氢氧化铁胶体形成;
5.水煮沸再滴加FeCl3饱和溶液,直接加热FeCl3饱和溶液会生成氢氧化铁沉淀
氢氧化铁胶体的制备
胶体的制备、性质及应用
实验1-1
把盛有CuSO4溶液和Fe(OH)3胶体的烧杯置于暗处,分别用红色激光笔照射烧杯中的液体,在与光束垂直的方向进行观察,并记录现象。
CuSO4溶液
Fe(OH)3胶体
鉴别胶体跟溶液的方法:利用丁达尔效应
原理:胶体粒子对光的散射
现象:形成一道光亮的“通路”
(1)丁达尔效应:可见光束通过胶体时,在入射光侧面可看到一条光亮的通路
溶液:散射极其微弱
浊液:分散质粒子直径大于可见光的波长,它们对光只有反射作用,不会产生光的散射
胶体的性质
胶体的制备、性质及应用
生活中的丁达尔效应
海洋中的阳光
舞台上的光束
树林中的阳光
原因①:胶体粒子可以通过吸附离子而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥,不易聚集而稳定。(主要原因)
(2)介稳性:
{[Fe(OH)3]m·nFeO+(n-x)Cl-}x+·xCl-
胶核
吸附层
胶粒
扩散层
胶核
胶体不带电,带电的是胶体粒子
胶体的性质
胶核
Fe(OH)3胶体中的1个胶体粒子不是1个Fe(OH)3分子,而是很多个Fe(OH)3分子聚集在一起形成的粒子直径在1~100nm的集合体。
胶体的性质
(2)介稳性:
胶体不带电,带电的是胶体粒子
根据胶体的介稳性,想一想如何破坏胶体的介稳性,使胶体发生聚沉?
原因②:分散剂分子对胶粒无规则的撞击,
做布朗运动。
原因①:胶体粒子可以通过吸附离子而带有电荷,同种胶粒带同种电荷,而同种电荷会相互排斥,不易聚集而稳定。(主要原因)
胶体的性质
(3)聚沉:胶体的介稳性被破坏,胶体粒子聚集成为较大的颗粒而以沉淀形式从分散剂中析出。
聚沉方法
加入少量电解质(酸、碱、盐)
加热
搅拌
加入与胶体粒子带相反电荷胶粒的胶体
加快胶体粒子运动的速率,增大胶体粒子之间的碰撞机会
中和胶体粒子的电性,消除胶体粒子间的相互排斥
胶体的性质
胶体聚沉应用实例
①卤水点豆腐:盐卤/石膏
②江河入海口处形成三角洲:
有的三角洲是胶体,出现在河流入海口
这是因为河水和海水的成分不同,所含的胶体微粒就不同,当带正电的微粒与带负电微粒相遇时,就发生胶体的聚沉,产生了沉淀。
盐卤(MgCl2·6H2O)或
石膏(CaSO4·2H2O)溶液
胶体的性质
胶体聚沉应用实例
④胶体的净水作用:如明矾(KAl(SO4)2 12H2O)净水
③FeCl3溶液用于伤口止血
不同品牌的墨水不能混用!!!
胶体的性质
(4)电泳
Fe(OH)3胶体
Fe(OH)3胶体
颜色变深
颜色变浅
通电前
通电后
Fe(OH)3胶体粒子带正电荷
电泳:由于胶体粒子带有电荷,在电场作用下,胶体粒子在分散剂中作定向移动的现象。
【注意】:胶体本身不带电,带电的是胶体粒子(通过吸附某种离子带电)。
不是所有的胶体粒子都带电。如淀粉的胶粒不带电。
可应用于静电除尘
静电除尘原理是含尘气体经过高压静电场时被电分离,尘粒与负离子结合带上负电后,趋向阳极表面放电而沉积。
胶体的性质
(1)胶体与浊液分离—过滤 胶体能够通过滤纸,浊液中的微粒不能透过滤纸。
(2)胶体与溶液分离— 渗析 溶液中的粒子或小分子能够透过半透膜,胶体微粒不能透过半透膜。
胶体的性质
生活中渗析法的应用
血液实际上是一种液溶胶
血液透析又叫做人工肾,是把血液引出体外,然后借助透析机上的装置,把血液泵入透析器,通过透析器里面的透析膜进行物质交换,清除血液中多余的水分以及代谢废物,补充有益的电解质,保持酸碱平衡,再把清洁后的血液送回身体内。
血 液 透 析
【归纳总结】溶液、胶体、浊液三者的性质差异
溶液 胶体 浊液
分散质粒子的直径 <1nm 1~100nm >100nm
分散质粒子 分子或离子 许多集合体或单个高分子 巨大数目分子集合体
性 质 外观 均一、透明 均一 不均一、不透明
稳定性 稳定 介稳性 不稳定
能否透过滤纸 能 能 不能
能否透过半透膜 能 不能 不能
是否具有丁达尔效应 无 有 无
实例 食盐水、碘酒 豆浆、牛奶 泥水
1.下列现象与胶体的性质无关的是( )A.夏日的傍晚常常看到万丈霞光穿云而过美不胜收B.过滤除去氯化钠溶液中的泥沙C.食品加工厂利用豆浆中加入盐卤做豆腐D.化工厂利用静电除尘技术去除废气中的固体悬浮物
B
丁达尔效应
悬浊液
聚沉
电泳
实战演练
2.某同学在实验室进行了如图所示的实验,下列说法错误的是( )
A.利用过滤的方法,可将Z中固体与液体分离B.X、Z烧杯中分散质相同C.Z中分散系能产生丁达尔效应D.Y中放出的气体为CO2
B
溶液
胶体
CaCO3+2HCl=CaCl2+H2O+CO2↑
固体不能通过滤纸,胶体可以透过滤纸
实战演练
3、下列现象或技术应用中,不涉及胶体性质的是( )
A.在江河入海处容易形成三角洲
B.向豆浆中加入石膏容易形成美味的豆腐
C.在氯化铁饱和溶液中加入浓NaOH溶液,产生红褐色沉淀
D.清晨,在茂密的森林中,常常可以看到从枝叶间透过的一道道光柱
C
聚沉
聚沉
沉淀
丁达尔效应
实战演练
4、胶体是一种常见的分散系,按要求回答下列问题:
(1)将饱和三氯化铁溶液滴入沸水时,得到的液体是___________色,反应的化学方程式为 。
(2)用此分散系进行下列实验:
①将其装入U形管内,用石墨作电极,接通直接电源,通电一段时间后发现阴极附近颜色________,这种现象称为_______。
②向其中逐滴加入过量稀硫酸,现象是先 _ 再 。
红褐
变深
电泳
产生红褐色沉淀
沉淀溶解成棕黄色溶液
先聚沉
Fe(OH)3↓又与稀H2SO4发生中和反应
5、下列叙述正确的是( )
A.溶液呈电中性,胶体带有电荷
B.溶液中的溶质微粒不能透过半透膜,胶体中的分散质粒子能透过半透膜
C.胶体区别于其他分散系的本质特征是胶体具有丁达尔效应
D.利用半透膜可除去淀粉溶液中的少量NaCl
D
胶粒带电荷,胶体呈电中性
不能
能
分散质粒子直径的大小
胶体
胶体与溶液分离—渗析
溶液中的粒子或小分子能够透过半透膜,胶体微粒不能透过半透膜。
6、朱自清先生在《荷塘月色》中写道:“溥薄的青雾浮起在荷塘里......月光是隔离树照过来的,高处丛生的灌木,落下参差的斑驳的黑影.....”月光穿过薄雾所形成的种种美景的本质原因是( )
A.发生丁达尔效应
B.光是一种胶体
C.雾是一种胶体
D.空气中的小水滴的直径介于1nm~100nm之间
D
7、下列说法正确的是( )
A.丁达尔效应不是胶体特有的现象,溶液与浊液也有
B.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有
C.胶体粒子的直径小于10-9m
D.丁达尔效应可用于区别胶体和溶液
本质区别是分散质粒子直径大小
D
1nm=10-9m
8.下列不会出现丁达尔效应的分散系是( )①鸡蛋清溶液 ②水
③淀粉溶液 ④蔗糖溶液
⑤FeCl3溶液 ⑥豆浆A.④⑤ B.③④ C.②④⑥ D.①③④
A
水、蔗糖溶液和FeCl3溶液不属于胶体,且水不是分散系,鸡蛋清溶液、淀粉溶液、豆浆属于胶体,会出现丁达尔效应。
9.淀粉溶液是一种胶体,并且淀粉遇碘单质变蓝。现将淀粉和Na2SO4的稀溶液混合,装在半透膜袋中,浸泡在盛有蒸馏水的烧杯内,过一段时间后,取烧杯中液体进行实验,能证明半透膜完好无损的是( )A.加入BaCl2溶液产生白色沉淀
B.加入碘水不变蓝C.加入BaCl2溶液没有白色沉淀产生
D.加入碘水变蓝
B
解析:这是一个渗析实验,如果半透膜完好无损,则只有钠离子和硫酸根离子能透过半透膜,淀粉分子不能透过半透膜,故向烧杯中的液体中加入碘水不变蓝,可以证明半透膜完好无损。
10.有一胶体,在电泳实验中其胶粒向阴极移动,对这种胶体进行下列处理,不发生聚沉的是( )A.加硫酸钠溶液 B.加热
C.加硅酸胶体 D.加氢氧化铁胶体
D
解析:由题意可知胶体粒子带有正电荷,加热、加电解质溶液、加胶粒带负电荷的胶体(硅酸胶体)都能使其聚沉。
11.“纳米技术”广泛应用于催化及军事科学中,“纳米材料”是粒子直径为1~100 nm(纳米)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )①是溶液 ②是胶体 ③是浊液
④不能透过滤纸 ⑤能透过滤纸 ⑥能产生丁达尔效应 ⑦静置后,会析出黑色沉淀A.②⑤⑥ B.②⑥⑦
C.①⑤ D.③④⑦
A
解析:“纳米材料”是粒子直径为1~100 nm的材料,纳米碳就是其中的一种。属于胶体分散质微粒直径的大小,若将纳米碳均匀地分散到蒸馏水中形成分散系是胶体,具有丁达尔现象,能透过滤纸,具有介稳性,不生成沉淀,故②⑤⑥正确。
12.有人设想通过特殊的方法将碳酸钙加工成为纳米碳酸钙(即碳酸钙粒子直径达到纳米级),这将使建筑材料的性能发生巨大的变化。下列关于纳米碳酸钙的说法正确的是( )A.纳米碳酸钙是与胶体相似的分散系 B.纳米碳酸钙分散到水中所得到的分散系会产生丁达尔效应C.纳米碳酸钙的化学性质与原来碳酸钙完全不同D.纳米碳酸钙粒子不能透过滤纸
B
纳米碳酸钙是纯净物,分散系是混合物
不会发生改变
与胶体中的胶粒(微粒直径在10-9~10-7m之间)能透过滤纸一样,纳米碳酸钙粒子也能透过滤纸
