2024年高三化学专题复习 基于认知模型建构的大概念教学——以“有机物分子中基团间相互作用”的教学为例 课件(共24张PPT)
文档属性
| 名称 | 2024年高三化学专题复习 基于认知模型建构的大概念教学——以“有机物分子中基团间相互作用”的教学为例 课件(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-09 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
基于认知模型建构的大概念教学
——以“有机物分子中基团间相互作用”的教学为例
维生素C又叫抗坏血酸是一种水溶性维生素,在人体内会参与多种反应。能促进胶原蛋白的形成,防治坏血病,可以促进外伤愈合;具有还原性,促进胆固醇代谢及铁的吸收,抗衰老,具有增强机体免疫力和抗癌能力。Vc在人体不能合成,每人每天摄入100mg左右就能满足需要。樱桃、猕猴桃、草莓、辣椒、番茄、苦瓜含有
较多Vc。
科普小知识
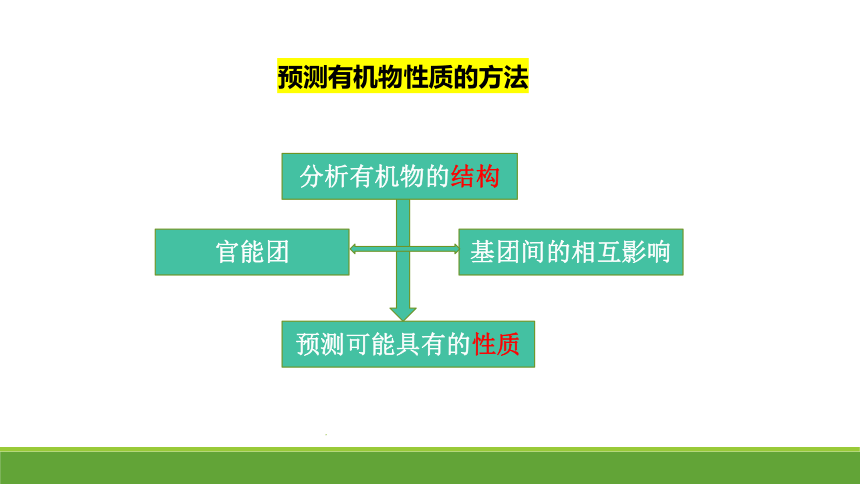
官能团
基团间的相互影响
预测可能具有的性质
分析有机物的结构
预测有机物性质的方法
学习目标:
1.知道同一分子中官能团之间存在相互影响。
2.知道分子中基团之间的相互影响会导致键的极性发生改变。
3.能从微观角度解释重要有机反应的基团间的相互影响的本源。
4.建立从化学键的角度认识有机物性质的认知模型,发展学生宏观辨识与微观探析,证据推理与模型认知的学科素养。
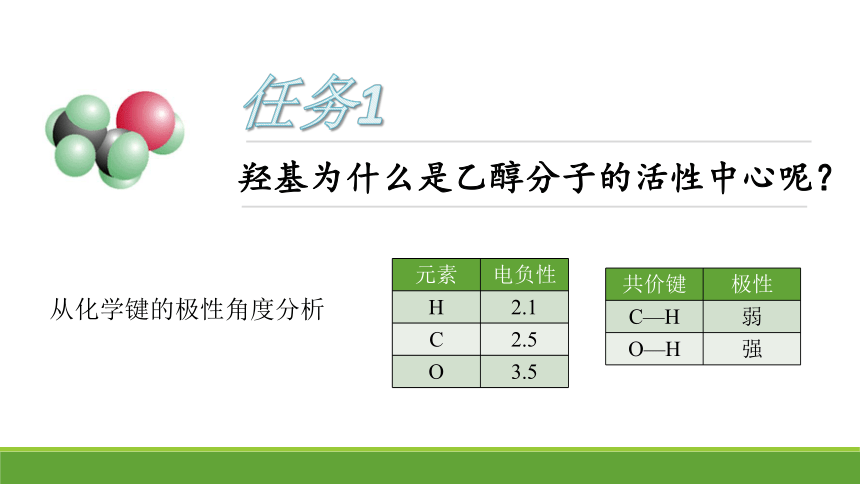
羟基为什么是乙醇分子的活性中心呢?
任务1
元素 电负性
H 2.1
C 2.5
O 3.5
共价键 极性
C—H 弱
O—H 强
从化学键的极性角度分析
羟基为什么是乙醇分子的活性中心呢?
任务1
乙醇分子中羟基极性最强,活性最强
共价键的极性影响基团的活性
注意:键的极性不是一成不变的,受分子中邻近基团或外界环境的影响,键的极性及其强度可能发生变化
比较羟基氢的活泼性
—水、乙醇和苯酚的羟基哪个更活泼?提供合理证据
任务2
CH3CH2-OH
H-OH
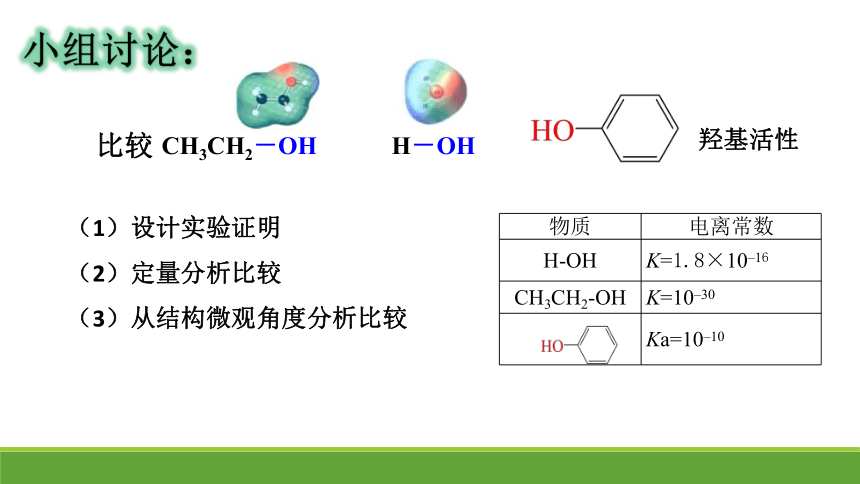
小组讨论:
CH3CH2-OH
H-OH
比较
羟基活性
(1)设计实验证明
(2)定量分析比较
(3)从结构微观角度分析比较
物质 电离常数
H-OH K=1.8×10–16
CH3CH2-OH K=10–30
Ka=10–10
H—O—H
CH3CH2O—H
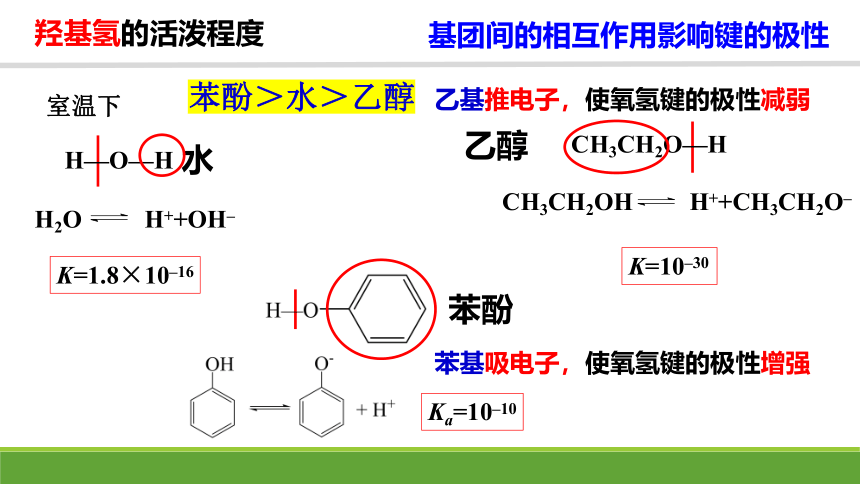
羟基氢的活泼程度
H2O H++OH–
CH3CH2OH H++CH3CH2O–
室温下
K=1.8×10–16
K=10–30
Ka=10–10
水
乙醇
苯酚
基团间的相互作用影响键的极性
苯酚>水>乙醇
乙基推电子,使氧氢键的极性减弱
苯基吸电子,使氧氢键的极性增强
电子效应
诱导效应:
在分子中引进一个原子或原子团后,可使σ键电子沿着原子链向某一方向移动,使整个分子中的成键电子云密度向某一方向偏移,使分子发生极化的效应。
诱导效比较,常以氢原子为标准。
吸电子基团:吸引电子能力(电负性较大)比氢原子强的原子或原子团
(如:–NO2、–CN、–COOH、–COOR、–CHO 、 –X、 、–OCH3、–OH、 –C6H5 、 等)
推电子基团:比氢原子弱(如:烷基)(CH3)3C–>(CH3)2C–>CH3CH2–>CH3–。
拓展视野
针对性练习1
液相中,测定一元醇的的酸性顺序如下,请根据所学知识
解释酸性顺序。
CH3OH>CH3CH2OH>
烃基是推电子基团,推电子能力(CH3)2CH—>CH3CH2—>CH3—
迁移应用1
H—O—Cl
弱酸
H—O—Cl
H—O—Cl
中强酸
最强含氧酸
强酸
O
O
O
H—O—Cl
O
O
O
元素 H C O Cl
电负性 2.1 2.5 3.5 3.0
无机含氧酸中非羟基氧的数目越多酸性越强
从化学键的极性变化角度分析HClO、HClO2、HClO3、HClO4酸性依次增强的原因
链接高考
【2022年山东高考16题节选】
的碱性随N原子电子云密度的增大而增强,
其中碱性最弱的是______。
甲基是推电子基,氯原子是吸电子基,导致N原子电子云密度 最小,
最大。
分析羟基对其他基团的影响
任务3
从结构微观角度分析羟基对其他基团是如何影响的?
1.为何乙烷很难被一般氧化剂氧化,而乙醇可以被氧化为醛或酮?
2.为何苯与溴反应需要铁作催化剂生成溴苯,而苯酚与溴反应不需要条件且生成三溴苯酚?
分析:苯酚中的羟基是如何影响苯环的?
..
δ+
δ-
δ-
δ-
苯酚中共轭效应的影响大于诱导效应,苯环被“致活”。
羟基氧原子上的p电子向苯环π键供电子,形成p-π共轭效应,提升苯环电子云密度。
氧原子的电负性比碳原子强,羟基表现吸电子的诱导效应,使苯环上的电子云密度降低,苯环活性减弱,与事实不符。
针对性练习2:
从结构的角度解释:为什么甲苯发生硝化反应的速率是苯发生硝化反应速率的4000倍?
δ+
δ-
δ-
δ-
δ-
δ+
δ+
δ-
δ+
甲基是给电子基诱导效应基团,甲基的 C—H 键与苯环的大π键形成δ-π超共轭效应,向苯环补给电子,使苯环的电子云密度升高,活性增强。
从结构的角度解释烯烃、炔烃、羧酸的a-H容易与Cl2发生取代反应。如:CH3CH=CH2、RCH2COOH(教材p90追根源)
迁移应用2
碳碳双键、碳碳三键、羧基均为吸电子基,使α-C上的C-H键极性增强,在一定条件下,α-H表现反应活性。
解密Vc的酸性
请谈一下本节收获
课堂小结
分析有机化合物性质的一般思路
【学以致用】:以甲苯为原料,设计了如下两种合成水杨酸( )的方案,请分析方案存在哪些缺陷?(已知羧基为间位定位基,甲基为邻对位定位基)
羧基为间位定位基,溴原子一般不处于邻位。
甲基为邻对位定位基团,难以控制反应只取代邻位。
可采取对位氢保护的方法
课后作业
利用本节课的收获去解决你在预习学案中尚存的问题。
2.完成合作探究学案上【巩固提升】的题目。
3.水杨酸( )是一种常用的解热镇痛药物,但酸性较强,对胃有一定的刺激性,长期服用容易引发胃溃疡。思考①为什么水杨酸酸性较强?②在确保药效的前提下,如何改变结构,降低水杨酸的酸性?
祝同学们2024金榜题名!
敬请各位专家老师批评指正!
基于认知模型建构的大概念教学
——以“有机物分子中基团间相互作用”的教学为例
维生素C又叫抗坏血酸是一种水溶性维生素,在人体内会参与多种反应。能促进胶原蛋白的形成,防治坏血病,可以促进外伤愈合;具有还原性,促进胆固醇代谢及铁的吸收,抗衰老,具有增强机体免疫力和抗癌能力。Vc在人体不能合成,每人每天摄入100mg左右就能满足需要。樱桃、猕猴桃、草莓、辣椒、番茄、苦瓜含有
较多Vc。
科普小知识
官能团
基团间的相互影响
预测可能具有的性质
分析有机物的结构
预测有机物性质的方法
学习目标:
1.知道同一分子中官能团之间存在相互影响。
2.知道分子中基团之间的相互影响会导致键的极性发生改变。
3.能从微观角度解释重要有机反应的基团间的相互影响的本源。
4.建立从化学键的角度认识有机物性质的认知模型,发展学生宏观辨识与微观探析,证据推理与模型认知的学科素养。
羟基为什么是乙醇分子的活性中心呢?
任务1
元素 电负性
H 2.1
C 2.5
O 3.5
共价键 极性
C—H 弱
O—H 强
从化学键的极性角度分析
羟基为什么是乙醇分子的活性中心呢?
任务1
乙醇分子中羟基极性最强,活性最强
共价键的极性影响基团的活性
注意:键的极性不是一成不变的,受分子中邻近基团或外界环境的影响,键的极性及其强度可能发生变化
比较羟基氢的活泼性
—水、乙醇和苯酚的羟基哪个更活泼?提供合理证据
任务2
CH3CH2-OH
H-OH
小组讨论:
CH3CH2-OH
H-OH
比较
羟基活性
(1)设计实验证明
(2)定量分析比较
(3)从结构微观角度分析比较
物质 电离常数
H-OH K=1.8×10–16
CH3CH2-OH K=10–30
Ka=10–10
H—O—H
CH3CH2O—H
羟基氢的活泼程度
H2O H++OH–
CH3CH2OH H++CH3CH2O–
室温下
K=1.8×10–16
K=10–30
Ka=10–10
水
乙醇
苯酚
基团间的相互作用影响键的极性
苯酚>水>乙醇
乙基推电子,使氧氢键的极性减弱
苯基吸电子,使氧氢键的极性增强
电子效应
诱导效应:
在分子中引进一个原子或原子团后,可使σ键电子沿着原子链向某一方向移动,使整个分子中的成键电子云密度向某一方向偏移,使分子发生极化的效应。
诱导效比较,常以氢原子为标准。
吸电子基团:吸引电子能力(电负性较大)比氢原子强的原子或原子团
(如:–NO2、–CN、–COOH、–COOR、–CHO 、 –X、 、–OCH3、–OH、 –C6H5 、 等)
推电子基团:比氢原子弱(如:烷基)(CH3)3C–>(CH3)2C–>CH3CH2–>CH3–。
拓展视野
针对性练习1
液相中,测定一元醇的的酸性顺序如下,请根据所学知识
解释酸性顺序。
CH3OH>CH3CH2OH>
烃基是推电子基团,推电子能力(CH3)2CH—>CH3CH2—>CH3—
迁移应用1
H—O—Cl
弱酸
H—O—Cl
H—O—Cl
中强酸
最强含氧酸
强酸
O
O
O
H—O—Cl
O
O
O
元素 H C O Cl
电负性 2.1 2.5 3.5 3.0
无机含氧酸中非羟基氧的数目越多酸性越强
从化学键的极性变化角度分析HClO、HClO2、HClO3、HClO4酸性依次增强的原因
链接高考
【2022年山东高考16题节选】
的碱性随N原子电子云密度的增大而增强,
其中碱性最弱的是______。
甲基是推电子基,氯原子是吸电子基,导致N原子电子云密度 最小,
最大。
分析羟基对其他基团的影响
任务3
从结构微观角度分析羟基对其他基团是如何影响的?
1.为何乙烷很难被一般氧化剂氧化,而乙醇可以被氧化为醛或酮?
2.为何苯与溴反应需要铁作催化剂生成溴苯,而苯酚与溴反应不需要条件且生成三溴苯酚?
分析:苯酚中的羟基是如何影响苯环的?
..
δ+
δ-
δ-
δ-
苯酚中共轭效应的影响大于诱导效应,苯环被“致活”。
羟基氧原子上的p电子向苯环π键供电子,形成p-π共轭效应,提升苯环电子云密度。
氧原子的电负性比碳原子强,羟基表现吸电子的诱导效应,使苯环上的电子云密度降低,苯环活性减弱,与事实不符。
针对性练习2:
从结构的角度解释:为什么甲苯发生硝化反应的速率是苯发生硝化反应速率的4000倍?
δ+
δ-
δ-
δ-
δ-
δ+
δ+
δ-
δ+
甲基是给电子基诱导效应基团,甲基的 C—H 键与苯环的大π键形成δ-π超共轭效应,向苯环补给电子,使苯环的电子云密度升高,活性增强。
从结构的角度解释烯烃、炔烃、羧酸的a-H容易与Cl2发生取代反应。如:CH3CH=CH2、RCH2COOH(教材p90追根源)
迁移应用2
碳碳双键、碳碳三键、羧基均为吸电子基,使α-C上的C-H键极性增强,在一定条件下,α-H表现反应活性。
解密Vc的酸性
请谈一下本节收获
课堂小结
分析有机化合物性质的一般思路
【学以致用】:以甲苯为原料,设计了如下两种合成水杨酸( )的方案,请分析方案存在哪些缺陷?(已知羧基为间位定位基,甲基为邻对位定位基)
羧基为间位定位基,溴原子一般不处于邻位。
甲基为邻对位定位基团,难以控制反应只取代邻位。
可采取对位氢保护的方法
课后作业
利用本节课的收获去解决你在预习学案中尚存的问题。
2.完成合作探究学案上【巩固提升】的题目。
3.水杨酸( )是一种常用的解热镇痛药物,但酸性较强,对胃有一定的刺激性,长期服用容易引发胃溃疡。思考①为什么水杨酸酸性较强?②在确保药效的前提下,如何改变结构,降低水杨酸的酸性?
祝同学们2024金榜题名!
敬请各位专家老师批评指正!
同课章节目录
