陕西省咸阳市武功县普集镇高级中学2023-2024学年高二上学期10月月考化学试题(含答案)
文档属性
| 名称 | 陕西省咸阳市武功县普集镇高级中学2023-2024学年高二上学期10月月考化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 939.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-11 00:00:00 | ||
图片预览


文档简介
普集镇高级中学2023-2024学年高二上学期10月月考
(化学)试题(卷)
总分值:100分
试题范围:选择性必修一第一至第二章 考试时间:90分钟
第I卷(选择题 共60分)
一、单选题
1.下列关于化学反应中热量变化的说法,正确的是( )
A.需要加热才能发生的反应都是吸热反应
B.放热反应在常温下一定可以发生
C.甲烷作为燃料的优点,不仅是热值高,还易充分燃烧
D.煤制气的过程可以增加煤的热值
2.实验室用锌粒与硫酸溶液制取氢气,下列措施能加快化学反应速率的是( )
A.向该硫酸溶液中加入等体积的水 B.加入等体积盐酸
C.加热溶液 D.增加锌粒质量
3.相同状况下: ; ,则和的关系为( )
A. B. C. D.
4.已知的正反应是吸热反应,反应速率为;的正反应是放热反应,反应速率为。对于上述反应,当温度升高时,和的变化情况为( )
A.都增大 B.都减小
C.增大,减小 D.减小,增大
5.已知一些燃料的燃烧热数据如下:
燃料 一氧化碳 甲烷 丙烷 乙醇
使用上述燃料最能体现“低碳经济”理念的是( )
A.甲烷 B.一氧化碳 C.丙烷 D.乙醇
6.工业上冶炼钛的有关反应如下:
①
②
③
④
⑤
下列有关推断正确的是( )
A. B.,
C. D.
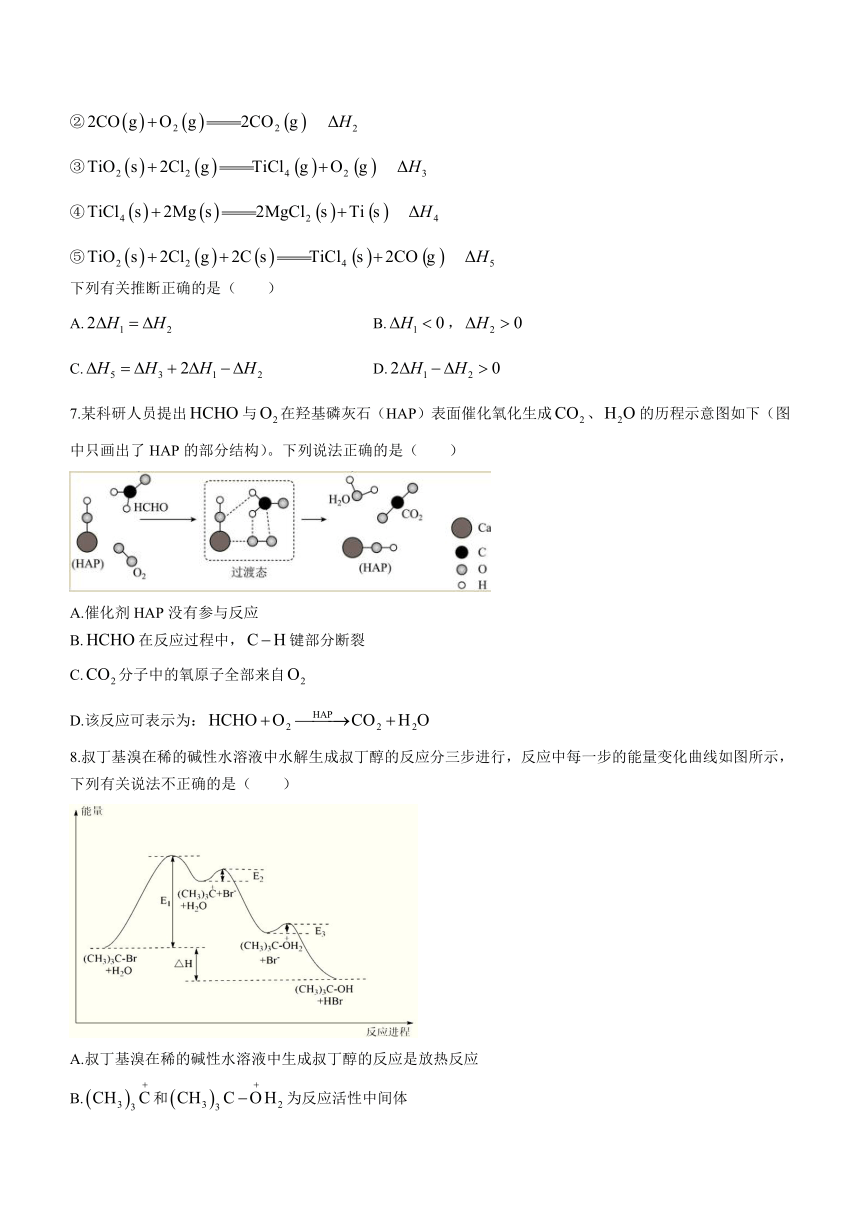
7.某科研人员提出与在羟基磷灰石(HAP)表面催化氧化生成、的历程示意图如下(图中只画出了HAP的部分结构)。下列说法正确的是( )
A.催化剂HAP没有参与反应
B.在反应过程中,键部分断裂
C.分子中的氧原子全部来自
D.该反应可表示为:
8.叔丁基溴在稀的碱性水溶液中水解生成叔丁醇的反应分三步进行,反应中每一步的能量变化曲线如图所示,下列有关说法不正确的是( )
A.叔丁基溴在稀的碱性水溶液中生成叔丁醇的反应是放热反应
B.和为反应活性中间体
C.决定叔丁基溴水解生成叔丁醇反应的速率的是第二步反应
D.第三步反应为
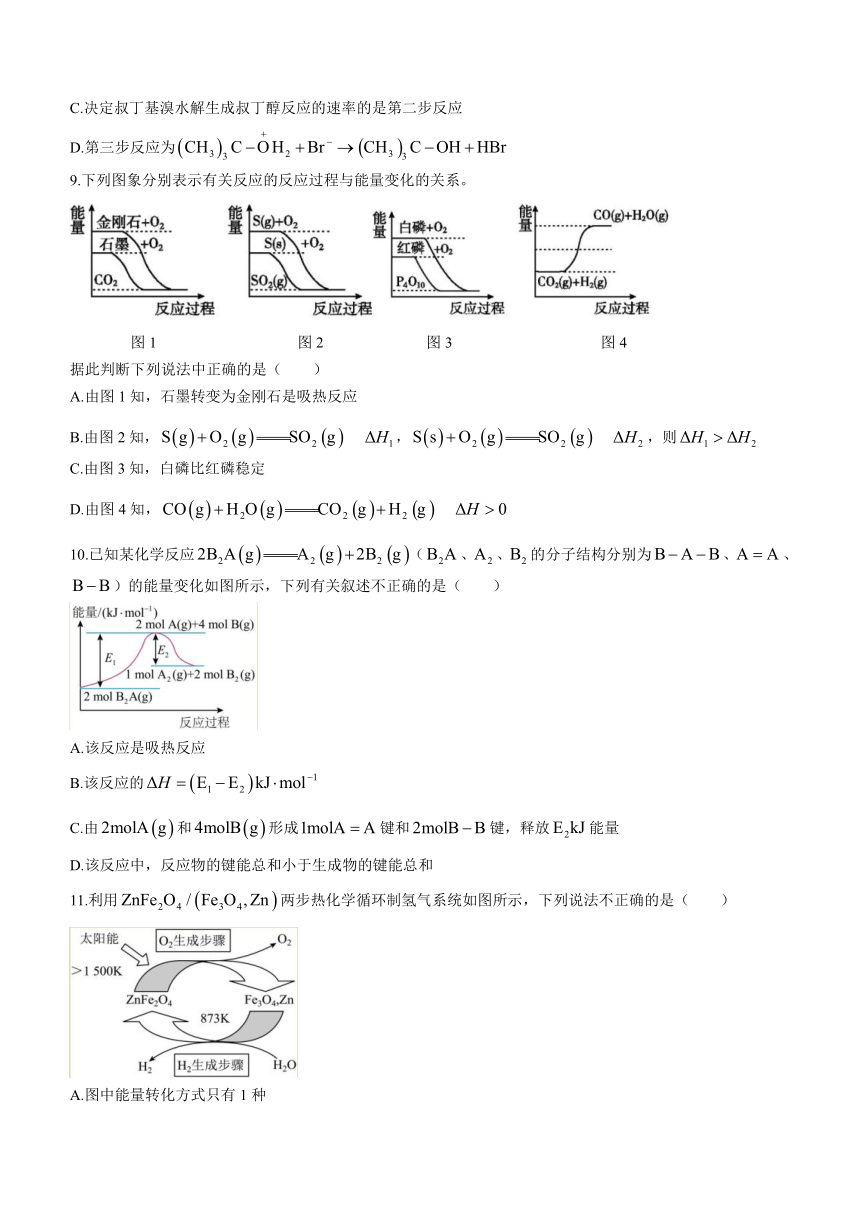
9.下列图象分别表示有关反应的反应过程与能量变化的关系。
图1 图2 图3 图4
据此判断下列说法中正确的是( )
A.由图1知,石墨转变为金刚石是吸热反应
B.由图2知, , ,则
C.由图3知,白磷比红磷稳定
D.由图4知,
10.已知某化学反应(、、的分子结构分别为、、)的能量变化如图所示,下列有关叙述不正确的是( )
A.该反应是吸热反应
B.该反应的
C.由和形成键和键,释放能量
D.该反应中,反应物的键能总和小于生成物的键能总和
11.利用两步热化学循环制氢气系统如图所示,下列说法不正确的是( )
A.图中能量转化方式只有1种
B.两步总反应为
C.氢能是一种清洁、高效、安全、可持续的新能源
D.生成步骤反应为
12.分解速率受多种因素影响。实验测得时不同条件下浓度随时间的变化如图所示。下列说法正确的是( )
甲 乙 丙 丁
A.图甲表明,其他条件相同时,浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液越小,分解速率越快
C.图丙表明,少量存在时,溶液碱性越强,分解速率越快
D.图丙和图丁表明,碱性溶液中,对分解速率的影响大
13.与盐酸反应过程中的能量变化示意图如图,下列选项正确的是( )
A.为放热反应
B.
C.
D.
14.我国科研人员提出了以为催化剂,由和转化为产品的反应历程(该反应可逆),其示意图如下:
下列说法不正确的是( )
A.总反应方程式为:
B.在反应历程中,键与键断裂吸收能量
C.催化剂不能改变该反应速率
D.反应过程中,催化剂改变反应路径,降低反应的活化能
15.在、下,将通入溶液中充分反应,测得反应放出的热量。已知在该条件下,通入溶液中充分反应放出的热量,则与溶液反应生成的热化学方程式正确的是( )
A.
B.
C.
D.
第II卷(非选择题(共40分))
二、填空题
16(8分).研究化学反应时,既要关注物质变化,又要关注能量变化。请回答以下问题.
(1)氢气在氧气中燃烧,破坏键吸收的热量,破坏键吸收的热量,形成键释放的热量,则下列关系式正确的是______。(填字母序号)
A. B.
C. D.
(2)用催化还原氮氧化物可以消除氮氧化物的污染。
已知:①
②
③
则 ______(用含a、b、c的代数式表示)。
(3)红磷和发生反应生成和,反应过程中的热量关系如图所示(图中的表示生成1mol产物的数据)。
根据如图回答下列问题:
①写出和反应生成的热化学方程式__________________;
②已知:常温时红磷比白磷稳定,比较下列反应中的大小:______(填“>”、“<”或“=”)。
i.
ii.
17.(12分)尿素是首个由无机物人工合成的有机物。
(1)工业上用和在一定条件下合成,其反应方程式__________________。
(2)在一个的密闭容器内,当起始投入量氨碳比,的转化率随时间的变化关系如下图所示。
①点的逆反应速率______点的正反应速率为(填“大于”、“小于”或“等于”)
②假设氨的起始投入量为,求从开始到达到平衡状态这段时间内______。
③的平衡转化率为__________________。
④单纯从制备的成本角度考虑,我们希望氨碳比尽可能______(“大”、“小”)因为________________________。
18.(10)化学反应速率在生产生活中有重要作用。
(1)氨的合成为氮肥的生产工业奠定了基础,其原理。
①反应一段时间后,的浓度增加了,用表示其平均反应速率为,则反应的时间为______s。
②下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是______(填字母)。
A. B.
C. D.
(2)一定温度下,氧化铁可与一氧化碳发生反应:。在盛有粉末的密闭容器中通入气体,后,生成单质铁。内______。
(3)研究反应的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物的浓度随反应时间的变化情况如图所示。
①对比实验I、II可得出:____________,化学反应速率加快。
②对比实验II、IV可得出:____________,化学反应速率加快。
③在内,实验III的平均速率______。
三、实验题
19.(10分)在保温杯式量热计中(见图)。将、溶液与、溶液混合,溶液温度从升高到,溶液比热容,溶液的密度为。(已知:反应放出的热量)
(1)通过计算,写出和反应热方程式__________________。
(2)实验中溶液过量的目的是________________________。
(3)中和热的文献值为,你认为(1)中测得的热量数值偏小的可能原因是________________________。
A.量热计的保温效果不好 B.酸碱溶液混合不迅速
C.温度计不够精确 D.用量筒量取酸和碱溶液的体积时仰视读数
(4)你认为与中和反应的和与和反应的相比,______大(填“”、“”或“一样”),原因是________________________。
(5)下列说法正确的是______(填标号)。
a.向内筒中加入稀碱时,应当缓慢而匀速地加入
b.将用量筒量取好的稀酸加入保温瓶后,应当快速用水冲洗筒内壁剩余的稀酸至保温瓶中,以免造成测量误差
c.用量筒量取稀酸或碱时,眼睛必须与液体凹面最低处相平
d.保温瓶洗净后,未及时烘干,直接进行实验,对中和反应的反应热测量无影响
参考答案:
1.C2.C3.C4.A5.A6.C7.D8.C9.A10.D11.A12.D13.C14.C15.C
16. C. 1/2(b-a)-2c P(s)+5/2Cl2(g)=PCl5(g) ΔH=-399 kJ/mol <
17.(1)2NH3+CO2═CO(NH2)2+H2O
(2) 小于 v(NH3)=0.2 mol/(L·min) NH3的平衡转化率为30% 氨碳比尽可能小 因为可以提高价格较高的NH3的转化率
18. 3 B 0.015 增大反应物浓度 升高温度 0.02
19.(1)
(2)保证醋酸完全被NaOH中和
(3)ABC
(4) ΔH1 是弱酸电离要吸热
(5)c
(化学)试题(卷)
总分值:100分
试题范围:选择性必修一第一至第二章 考试时间:90分钟
第I卷(选择题 共60分)
一、单选题
1.下列关于化学反应中热量变化的说法,正确的是( )
A.需要加热才能发生的反应都是吸热反应
B.放热反应在常温下一定可以发生
C.甲烷作为燃料的优点,不仅是热值高,还易充分燃烧
D.煤制气的过程可以增加煤的热值
2.实验室用锌粒与硫酸溶液制取氢气,下列措施能加快化学反应速率的是( )
A.向该硫酸溶液中加入等体积的水 B.加入等体积盐酸
C.加热溶液 D.增加锌粒质量
3.相同状况下: ; ,则和的关系为( )
A. B. C. D.
4.已知的正反应是吸热反应,反应速率为;的正反应是放热反应,反应速率为。对于上述反应,当温度升高时,和的变化情况为( )
A.都增大 B.都减小
C.增大,减小 D.减小,增大
5.已知一些燃料的燃烧热数据如下:
燃料 一氧化碳 甲烷 丙烷 乙醇
使用上述燃料最能体现“低碳经济”理念的是( )
A.甲烷 B.一氧化碳 C.丙烷 D.乙醇
6.工业上冶炼钛的有关反应如下:
①
②
③
④
⑤
下列有关推断正确的是( )
A. B.,
C. D.
7.某科研人员提出与在羟基磷灰石(HAP)表面催化氧化生成、的历程示意图如下(图中只画出了HAP的部分结构)。下列说法正确的是( )
A.催化剂HAP没有参与反应
B.在反应过程中,键部分断裂
C.分子中的氧原子全部来自
D.该反应可表示为:
8.叔丁基溴在稀的碱性水溶液中水解生成叔丁醇的反应分三步进行,反应中每一步的能量变化曲线如图所示,下列有关说法不正确的是( )
A.叔丁基溴在稀的碱性水溶液中生成叔丁醇的反应是放热反应
B.和为反应活性中间体
C.决定叔丁基溴水解生成叔丁醇反应的速率的是第二步反应
D.第三步反应为
9.下列图象分别表示有关反应的反应过程与能量变化的关系。
图1 图2 图3 图4
据此判断下列说法中正确的是( )
A.由图1知,石墨转变为金刚石是吸热反应
B.由图2知, , ,则
C.由图3知,白磷比红磷稳定
D.由图4知,
10.已知某化学反应(、、的分子结构分别为、、)的能量变化如图所示,下列有关叙述不正确的是( )
A.该反应是吸热反应
B.该反应的
C.由和形成键和键,释放能量
D.该反应中,反应物的键能总和小于生成物的键能总和
11.利用两步热化学循环制氢气系统如图所示,下列说法不正确的是( )
A.图中能量转化方式只有1种
B.两步总反应为
C.氢能是一种清洁、高效、安全、可持续的新能源
D.生成步骤反应为
12.分解速率受多种因素影响。实验测得时不同条件下浓度随时间的变化如图所示。下列说法正确的是( )
甲 乙 丙 丁
A.图甲表明,其他条件相同时,浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液越小,分解速率越快
C.图丙表明,少量存在时,溶液碱性越强,分解速率越快
D.图丙和图丁表明,碱性溶液中,对分解速率的影响大
13.与盐酸反应过程中的能量变化示意图如图,下列选项正确的是( )
A.为放热反应
B.
C.
D.
14.我国科研人员提出了以为催化剂,由和转化为产品的反应历程(该反应可逆),其示意图如下:
下列说法不正确的是( )
A.总反应方程式为:
B.在反应历程中,键与键断裂吸收能量
C.催化剂不能改变该反应速率
D.反应过程中,催化剂改变反应路径,降低反应的活化能
15.在、下,将通入溶液中充分反应,测得反应放出的热量。已知在该条件下,通入溶液中充分反应放出的热量,则与溶液反应生成的热化学方程式正确的是( )
A.
B.
C.
D.
第II卷(非选择题(共40分))
二、填空题
16(8分).研究化学反应时,既要关注物质变化,又要关注能量变化。请回答以下问题.
(1)氢气在氧气中燃烧,破坏键吸收的热量,破坏键吸收的热量,形成键释放的热量,则下列关系式正确的是______。(填字母序号)
A. B.
C. D.
(2)用催化还原氮氧化物可以消除氮氧化物的污染。
已知:①
②
③
则 ______(用含a、b、c的代数式表示)。
(3)红磷和发生反应生成和,反应过程中的热量关系如图所示(图中的表示生成1mol产物的数据)。
根据如图回答下列问题:
①写出和反应生成的热化学方程式__________________;
②已知:常温时红磷比白磷稳定,比较下列反应中的大小:______(填“>”、“<”或“=”)。
i.
ii.
17.(12分)尿素是首个由无机物人工合成的有机物。
(1)工业上用和在一定条件下合成,其反应方程式__________________。
(2)在一个的密闭容器内,当起始投入量氨碳比,的转化率随时间的变化关系如下图所示。
①点的逆反应速率______点的正反应速率为(填“大于”、“小于”或“等于”)
②假设氨的起始投入量为,求从开始到达到平衡状态这段时间内______。
③的平衡转化率为__________________。
④单纯从制备的成本角度考虑,我们希望氨碳比尽可能______(“大”、“小”)因为________________________。
18.(10)化学反应速率在生产生活中有重要作用。
(1)氨的合成为氮肥的生产工业奠定了基础,其原理。
①反应一段时间后,的浓度增加了,用表示其平均反应速率为,则反应的时间为______s。
②下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是______(填字母)。
A. B.
C. D.
(2)一定温度下,氧化铁可与一氧化碳发生反应:。在盛有粉末的密闭容器中通入气体,后,生成单质铁。内______。
(3)研究反应的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物的浓度随反应时间的变化情况如图所示。
①对比实验I、II可得出:____________,化学反应速率加快。
②对比实验II、IV可得出:____________,化学反应速率加快。
③在内,实验III的平均速率______。
三、实验题
19.(10分)在保温杯式量热计中(见图)。将、溶液与、溶液混合,溶液温度从升高到,溶液比热容,溶液的密度为。(已知:反应放出的热量)
(1)通过计算,写出和反应热方程式__________________。
(2)实验中溶液过量的目的是________________________。
(3)中和热的文献值为,你认为(1)中测得的热量数值偏小的可能原因是________________________。
A.量热计的保温效果不好 B.酸碱溶液混合不迅速
C.温度计不够精确 D.用量筒量取酸和碱溶液的体积时仰视读数
(4)你认为与中和反应的和与和反应的相比,______大(填“”、“”或“一样”),原因是________________________。
(5)下列说法正确的是______(填标号)。
a.向内筒中加入稀碱时,应当缓慢而匀速地加入
b.将用量筒量取好的稀酸加入保温瓶后,应当快速用水冲洗筒内壁剩余的稀酸至保温瓶中,以免造成测量误差
c.用量筒量取稀酸或碱时,眼睛必须与液体凹面最低处相平
d.保温瓶洗净后,未及时烘干,直接进行实验,对中和反应的反应热测量无影响
参考答案:
1.C2.C3.C4.A5.A6.C7.D8.C9.A10.D11.A12.D13.C14.C15.C
16. C. 1/2(b-a)-2c P(s)+5/2Cl2(g)=PCl5(g) ΔH=-399 kJ/mol <
17.(1)2NH3+CO2═CO(NH2)2+H2O
(2) 小于 v(NH3)=0.2 mol/(L·min) NH3的平衡转化率为30% 氨碳比尽可能小 因为可以提高价格较高的NH3的转化率
18. 3 B 0.015 增大反应物浓度 升高温度 0.02
19.(1)
(2)保证醋酸完全被NaOH中和
(3)ABC
(4) ΔH1 是弱酸电离要吸热
(5)c
同课章节目录
