【轻松备课】科粤版化学九年级上 第三章 3.4 物质组成的表示式 第2课时 教学课件
文档属性
| 名称 | 【轻松备课】科粤版化学九年级上 第三章 3.4 物质组成的表示式 第2课时 教学课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 645.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-11 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
3.4 物质组成的表示式
第三章 维持生命之气——氧气
第2课时
第三章 维持生命之气——氧气
1.熟知常见元素化合价。
2.能依据化合价写出物质的化学式。
3.能根据化学式推求某元素的化合价。
学 习 目 标
自 主 探 究
写出下列常见物质的化学式。
二氧化碳 一氧化碳 水 氧气 铜 氧化铜
CO2 CO H2O O2 Cu CuO
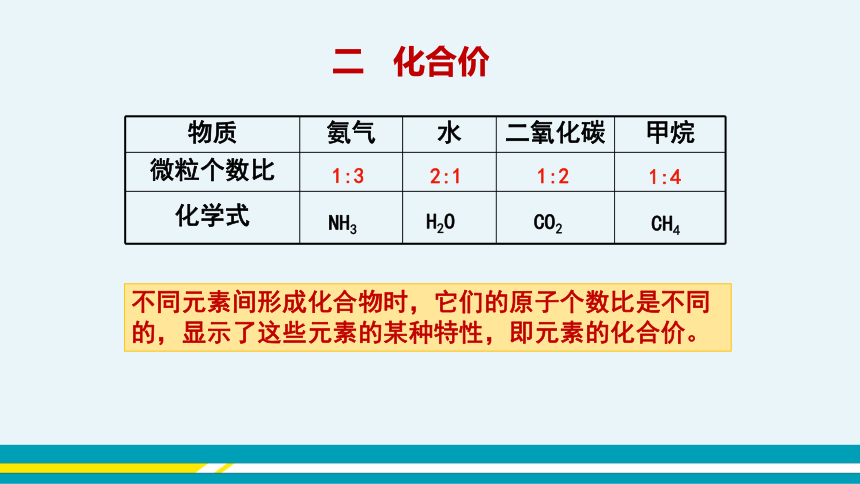
物质 氨气 水 二氧化碳 甲烷
微粒个数比
化学式
1:3
2:1
1:2
1:4
NH3
CO2
H2O
二 化合价
不同元素间形成化合物时,它们的原子个数比是不同的,显示了这些元素的某种特性,即元素的化合价。
CH4
形成化合物
化合价用来确定化合物中原子或离子之间相互结合的数目。化合价的价数越大的元素,提供原子或离子的个数越少,反之,化合价的价数越小的元素,提供原子或离子的个数就越多。
化合价是元素形成化合物时表现出来的性质。
规定:单质中元素化合价为零。
Fe
化合价标在元素符号的正上方(符号在前,数字在后)。
1.化合价的表示方法
+3
表示+3价的铁元素。
Fe3+
表示一个铁离子带3个单位的正电荷。
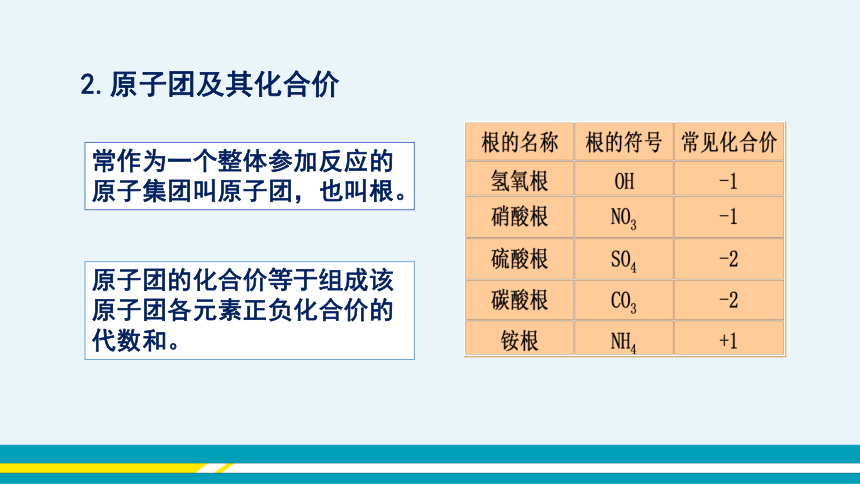
2.原子团及其化合价
常作为一个整体参加反应的原子集团叫原子团,也叫根。
原子团的化合价等于组成该原子团各元素正负化合价的代数和。
名称 符号 化合价 名称 符号 化合价
钠 Na +1 氯 Cl –1
钙 Ca +2 硫 S –2、+4、+6
钾 K +1 碳 C +2、+4
镁 Mg +2 氮 N –3、+2、+4、+5
铝 Al +3 氢氧根 OH –1
锌 Zn +2 碳酸根 CO3 –2
铁 Fe +2、+3 硝酸根 NO3 –1
铜 Cu +2 硫酸根 SO4 –2
氢 H +1 铵根 NH4 +1
氧 O –2 氯酸根 ClO3 –1
常见元素或根在化合物中的主要化合价
常见元素及根的化合价口诀
一价 氢 氯 钾 钠 银, 二价 氧 钙 钡 镁 锌,
H、Cl、K、Na、Ag, O、Ca、Ba、Mg、Zn
三 铝 四硅五价磷, 二三铁二四碳,
Al Si P, Fe C
负一硝酸氢氧根;负二硫酸碳酸根;
NO3、OH SO4 、CO3
负三记住磷酸根;正一价的是铵根
PO4 NH4
(1)在化合物里,氧元素通常显-2价,氢元素通常显+1价。
(2)化合价有正价和负价。金属与非金属形成化合物时,金属元素通常显正价,非金属元素通常显负价。许多非金属元素与氧元素形成化合物时,通常显正价。
(3)一些元素在不同的化合物中可显示不同的化合价,如、。
(4)同种元素在同一化合物中可能显示不同的化合价,如。
(5)在化合物中各元素正负化合价的代数和等于0。
(6)单质中,元素的化合价为0。
3.化合价的规律
(1)标出氯酸钾中氯元素化合价。
(2)标出O2 、P2O5、Fe2O3、Ca(CIO)2中各元素化合价。
(3)NH4NO3中氮元素的化合价。
(4)标出下列物质中红色元素的化合价。
KMnO4 K2MnO4 MnO2 N2 HNO3 Mg(NO3)2 NO NH3
4.根据化合价规律求化学式中元素化合价
NH4NO3
KCIO3
+5
0
+5 -2
+3 -2
+2 +1 -2
+7
+6
+5
0
+4
+5
+2
-3
(1)氧化钙 (2)硫化钠
Ca O
+2 -2
验证:(+2)+(-2)= 0
Na S
+1 -2
验证:(+1) ×2 +(-2)= 0
正左负右,
标价交叉,
约简复查。
2
5.根据元素化合价写出物质的化学式
(1)硫酸铝 (2)氢氧化钠
Al SO4
Na OH
+3 - 2
2
( )
验证:(+3)×2 + (-2)×3 = 0
+1 -1
验证:(+1) +(-1)= 0
3
原子团的个数不为“1”时加括号。
1.三氧化二铋(Bi2O3)俗称铋黄,是制作防火纸的材料之一。三氧化二铋中铋元素的化合价是( )
A.+6 B. +3 C. +2 D.-2
课 堂 达 标
B
2.下列硫的单质和化合物中,硫元素的化合价最高的是( )
A.S B.SO2 C.H2S D.H2SO4
3.下列物质中,氮元素化合价为+5价的是( )
A.NH3 B.NO2 C.KNO3 D.NaNO2
D
C
4.数字在化学式不同部位可表示不同的意义:①表示微粒的数目
②表示元素的化合价 ③表示离子的电荷数。请你判断下列化学式中的“2”分别表示上述哪种含义?(填序号)
Mg2+ ;2CO ;CaCO3 。
③
+2
①
②
5.氯是一种重要的“成盐元素”,在海水、盐湖和盐矿中广泛存在。
(1)卤水点豆腐时常用到氯化镁,氯化镁的化学式是____________。
(2)构成氯化钙的基本微粒是离子,则钙离子的化学符号为_____________,氯原子的结构示意图为
__________。
MgCl2
Ca2+
谢 谢 观 看
3.4 物质组成的表示式
第三章 维持生命之气——氧气
第2课时
第三章 维持生命之气——氧气
1.熟知常见元素化合价。
2.能依据化合价写出物质的化学式。
3.能根据化学式推求某元素的化合价。
学 习 目 标
自 主 探 究
写出下列常见物质的化学式。
二氧化碳 一氧化碳 水 氧气 铜 氧化铜
CO2 CO H2O O2 Cu CuO
物质 氨气 水 二氧化碳 甲烷
微粒个数比
化学式
1:3
2:1
1:2
1:4
NH3
CO2
H2O
二 化合价
不同元素间形成化合物时,它们的原子个数比是不同的,显示了这些元素的某种特性,即元素的化合价。
CH4
形成化合物
化合价用来确定化合物中原子或离子之间相互结合的数目。化合价的价数越大的元素,提供原子或离子的个数越少,反之,化合价的价数越小的元素,提供原子或离子的个数就越多。
化合价是元素形成化合物时表现出来的性质。
规定:单质中元素化合价为零。
Fe
化合价标在元素符号的正上方(符号在前,数字在后)。
1.化合价的表示方法
+3
表示+3价的铁元素。
Fe3+
表示一个铁离子带3个单位的正电荷。
2.原子团及其化合价
常作为一个整体参加反应的原子集团叫原子团,也叫根。
原子团的化合价等于组成该原子团各元素正负化合价的代数和。
名称 符号 化合价 名称 符号 化合价
钠 Na +1 氯 Cl –1
钙 Ca +2 硫 S –2、+4、+6
钾 K +1 碳 C +2、+4
镁 Mg +2 氮 N –3、+2、+4、+5
铝 Al +3 氢氧根 OH –1
锌 Zn +2 碳酸根 CO3 –2
铁 Fe +2、+3 硝酸根 NO3 –1
铜 Cu +2 硫酸根 SO4 –2
氢 H +1 铵根 NH4 +1
氧 O –2 氯酸根 ClO3 –1
常见元素或根在化合物中的主要化合价
常见元素及根的化合价口诀
一价 氢 氯 钾 钠 银, 二价 氧 钙 钡 镁 锌,
H、Cl、K、Na、Ag, O、Ca、Ba、Mg、Zn
三 铝 四硅五价磷, 二三铁二四碳,
Al Si P, Fe C
负一硝酸氢氧根;负二硫酸碳酸根;
NO3、OH SO4 、CO3
负三记住磷酸根;正一价的是铵根
PO4 NH4
(1)在化合物里,氧元素通常显-2价,氢元素通常显+1价。
(2)化合价有正价和负价。金属与非金属形成化合物时,金属元素通常显正价,非金属元素通常显负价。许多非金属元素与氧元素形成化合物时,通常显正价。
(3)一些元素在不同的化合物中可显示不同的化合价,如、。
(4)同种元素在同一化合物中可能显示不同的化合价,如。
(5)在化合物中各元素正负化合价的代数和等于0。
(6)单质中,元素的化合价为0。
3.化合价的规律
(1)标出氯酸钾中氯元素化合价。
(2)标出O2 、P2O5、Fe2O3、Ca(CIO)2中各元素化合价。
(3)NH4NO3中氮元素的化合价。
(4)标出下列物质中红色元素的化合价。
KMnO4 K2MnO4 MnO2 N2 HNO3 Mg(NO3)2 NO NH3
4.根据化合价规律求化学式中元素化合价
NH4NO3
KCIO3
+5
0
+5 -2
+3 -2
+2 +1 -2
+7
+6
+5
0
+4
+5
+2
-3
(1)氧化钙 (2)硫化钠
Ca O
+2 -2
验证:(+2)+(-2)= 0
Na S
+1 -2
验证:(+1) ×2 +(-2)= 0
正左负右,
标价交叉,
约简复查。
2
5.根据元素化合价写出物质的化学式
(1)硫酸铝 (2)氢氧化钠
Al SO4
Na OH
+3 - 2
2
( )
验证:(+3)×2 + (-2)×3 = 0
+1 -1
验证:(+1) +(-1)= 0
3
原子团的个数不为“1”时加括号。
1.三氧化二铋(Bi2O3)俗称铋黄,是制作防火纸的材料之一。三氧化二铋中铋元素的化合价是( )
A.+6 B. +3 C. +2 D.-2
课 堂 达 标
B
2.下列硫的单质和化合物中,硫元素的化合价最高的是( )
A.S B.SO2 C.H2S D.H2SO4
3.下列物质中,氮元素化合价为+5价的是( )
A.NH3 B.NO2 C.KNO3 D.NaNO2
D
C
4.数字在化学式不同部位可表示不同的意义:①表示微粒的数目
②表示元素的化合价 ③表示离子的电荷数。请你判断下列化学式中的“2”分别表示上述哪种含义?(填序号)
Mg2+ ;2CO ;CaCO3 。
③
+2
①
②
5.氯是一种重要的“成盐元素”,在海水、盐湖和盐矿中广泛存在。
(1)卤水点豆腐时常用到氯化镁,氯化镁的化学式是____________。
(2)构成氯化钙的基本微粒是离子,则钙离子的化学符号为_____________,氯原子的结构示意图为
__________。
MgCl2
Ca2+
谢 谢 观 看
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
