【轻松备课】科粤版化学九年级上 第四章 4.4 化学方程式 第1课时 教学课件
文档属性
| 名称 | 【轻松备课】科粤版化学九年级上 第四章 4.4 化学方程式 第1课时 教学课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-11 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
第四章 生命之源——水
4.4 化学方程式
第四章 生命之源——水
第1课时
1.通过碳燃烧的化学方程式,能从具体的化学方程式中获取并说出有关反应信息,总结出化学方程式表示的意义。
2.通过碳燃烧的化学方程式,能说出化学方程式的读法。
3.通过复习质量守恒定律,知道书写化学方程式遵守的原则。
4.通过练习,能正确书写简单的化学方程式。
学 习 目 标
自 主 探究
1.请你写出下列化学反应的文字表达式。
(1)碳在氧气中燃烧;
(2)磷在氧气中燃烧;
(3)电解水;
(4)过氧化氢分解;
(5)加热高锰酸钾。
2.什么是质量守恒定律,用分子、原子的知识解释质量守恒的原因。
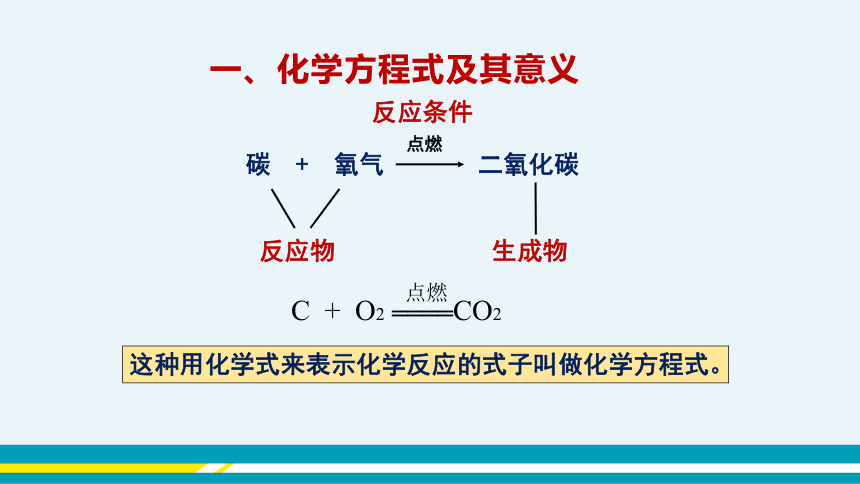
碳 + 氧气 二氧化碳
点燃
反应物
生成物
反应条件
C + O2 ════CO2
点燃
这种用化学式来表示化学反应的式子叫做化学方程式。
一、化学方程式及其意义
化学式和化学方程式有什么不同?
用元素符号和数字的组合来表示物质组成的式子叫做化学式。
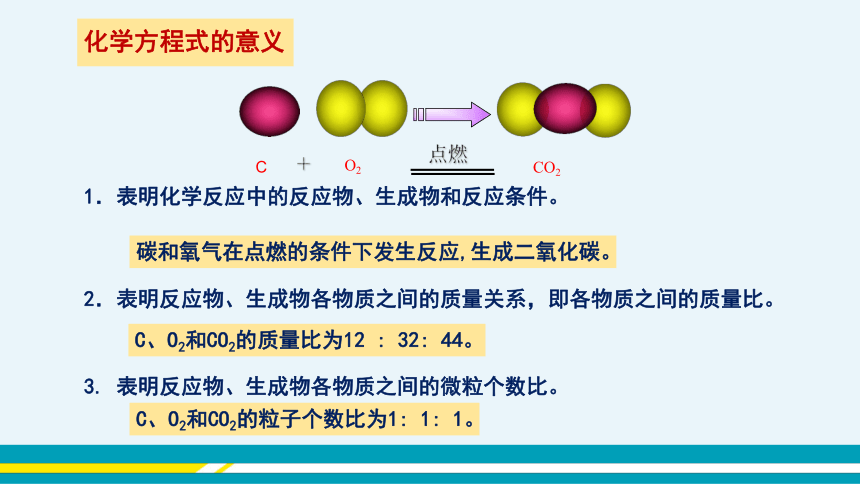
化学方程式的意义
1.表明化学反应中的反应物、生成物和反应条件。
2.表明反应物、生成物各物质之间的质量关系,即各物质之间的质量比。
碳和氧气在点燃的条件下发生反应,生成二氧化碳。
C、O2和CO2的质量比为12 : 32: 44。
C
+
CO2
O2
点燃
3. 表明反应物、生成物各物质之间的微粒个数比。
C、O2和CO2的粒子个数比为1: 1: 1。
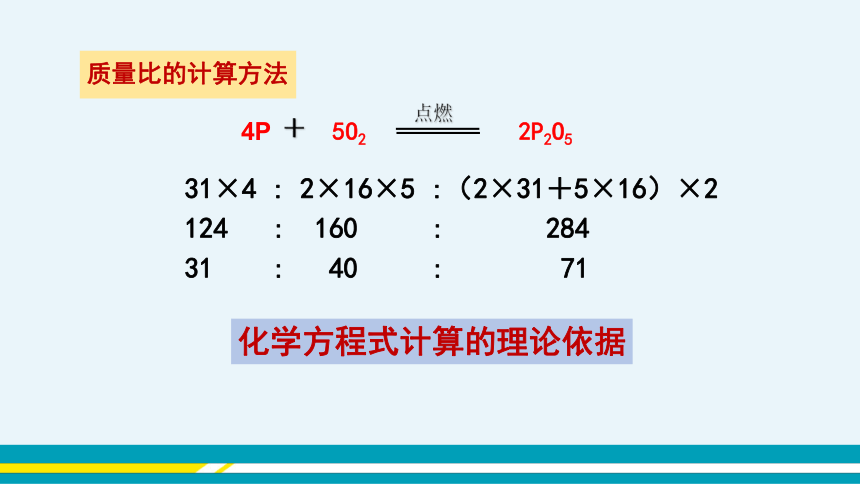
4P
+
2P2O5
5O2
点燃
31×4 : 2×16×5 :(2×31+5×16)×2
124 : 160 : 284
31 : 40 : 71
化学方程式计算的理论依据
质量比的计算方法
从化学方程式还能获得下列信息:
1.反应所属类型。
2.反应前后质量守恒等。
36 4 32
在点燃的条件下,碳和氧气反应生成二氧化碳。
在点燃的条件下,每12份质量的碳和32份质量的氧气反应生成44份质量的二氧化碳。
C
+
CO2
O2
点燃
12 32 44
化学方程式的读法
宏观上
质量上
微观上
在点燃的条件下,1个碳原子和1个氧分子恰好完全反应生成1个二氧化碳分子。
请从物质种类、质量、反应条件等方面考虑,讨论下列化学方程式提供的信息:
CuO+H2
加热
Cu+H2O
讨论交流
二、化学方程式的书写
请同学们阅读教材115页,说出书写化学方程式应遵循的原则。
(1)以科学实验的事实为根据,写出反应物和生成物的化学式。
(2)以质量守恒定律为根据,等号两边各种原子的种类和数目必须相同。
1.书写化学方程式应遵循的原则
H2 + O2 H2O + O
化学反应要尊重客观事实,不能改动反应物和生成物的化学式。
下面方程式正确吗?
×
根据科学实验事实,在左边写出反应物的化学式,右边写出生成物的化学式,如果反应物或生成物不止一种,就分别用“+”把它们连接起来,并在反应物与生成物之间画一条短横线。
P + O2 P2O5
根据质量守恒定律,进行配平,即在有关化学式前配上适当的化学计量数,使反应前后各种元素的原子个数相等。
写
配
书写化学方程式的步骤
4P + 5O2 2P2O5
点燃
4P + 5O2 2P2O5
点燃
将短横线改写成“ ”。
4P +5O2 2P2O5
注明反应发生条件以及生成物状态“↑”或“↓”。
注
等
书写化学方程式的步骤
检查化学式是否正确、化学方程式是否配平、反应条件和生成物状态符号是否标注,标注是否恰当。
查
化学方程式中一些符号的意义:
加热
产物中有气体生成
溶液中生成沉淀
反应物中有气体参与,生成气体就不用加“↑”
2CuO。
△表示 ,如
↑表示 ,如
↓表示 ,如
观察碳燃烧的化学方程式
“C+O2 CO2 ”为什么没有“↑”
2H2O2 2H2O +O2↑。
2NaOH+CuSO4==Cu(OH)2 ↓ +Na2SO4。
根据化合价的规则书写化合物的化学式:
先排列,
后标价;
约最简,
再交叉。
正确书写反应物和生成物的化学式
写出下列物质的化学式
(1)氧气、氢气、氯气、氮气
(2)氧化铝、氯化钾、氧化钙、氧化铁
(3)氢氧化钙、碳酸钠、硫酸铜、锰酸钾
O2 H2 Cl2 N2
Al2O3 KCl CaO Fe2O3
Ca(OH)2 Na2CO3 CuSO4 K2MnO4
就是在各化学式前面配上适当的化学计量数,
使左、右两边各种元素的原子个数相等。
配平时只能在各化学式前加化学计量数,
不能改动元素符号右下方的小数字;
配平化学方程式
1
各化学计量数之间为最简整数比,不能是分数,不能有约数。
2
1.红磷在氧气中燃烧生成五氧化二磷,该反应中红磷、氧气、五氧化二磷的质量比为( )
A. 4∶5∶2 B. 31∶24∶47
C. 31∶32∶142 D. 124∶160∶284
D
课 堂 达 标
2. 天然气的主要成分甲烷(CH4)在空气中燃烧的化学反应可用“CH4+2O2 CO2+2H2O”来表示。以下信息:①反应条件;②反应速率;③反应物、生成物各物质间的质量关系;④反应的微观过程;⑤反应过程中的能量变化;⑥反应体系中微观粒子的数量关系。
能从上述化学方程式中获得的是( )
A.①③④ B.②③⑤ C.①③⑥ D.②④⑥
C
3.把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下表。下列说法不正确的是( )
物质 甲 乙 丙 丁
反应前的质量(g) 4.0 2.0 3.0 2.0
反应后的质量(g) 1.2 X 2.4 5.4
A.X=2.0,乙可能是催化剂
B.甲和丙是反应物
C.参加反应的甲、丙质量比是1∶2
D.丁一定是化合物
C
4.根据已学知识判断下列反应方程式是否正确?如有错误,请指出错误之处:
(1)3Fe+2O2 Fe3O4
(2)Mg+O2 MgO2
(3)CH4+O2 CO2+H2O
加热
点燃
点燃
×
×
×
谢 谢 观 看
第四章 生命之源——水
4.4 化学方程式
第四章 生命之源——水
第1课时
1.通过碳燃烧的化学方程式,能从具体的化学方程式中获取并说出有关反应信息,总结出化学方程式表示的意义。
2.通过碳燃烧的化学方程式,能说出化学方程式的读法。
3.通过复习质量守恒定律,知道书写化学方程式遵守的原则。
4.通过练习,能正确书写简单的化学方程式。
学 习 目 标
自 主 探究
1.请你写出下列化学反应的文字表达式。
(1)碳在氧气中燃烧;
(2)磷在氧气中燃烧;
(3)电解水;
(4)过氧化氢分解;
(5)加热高锰酸钾。
2.什么是质量守恒定律,用分子、原子的知识解释质量守恒的原因。
碳 + 氧气 二氧化碳
点燃
反应物
生成物
反应条件
C + O2 ════CO2
点燃
这种用化学式来表示化学反应的式子叫做化学方程式。
一、化学方程式及其意义
化学式和化学方程式有什么不同?
用元素符号和数字的组合来表示物质组成的式子叫做化学式。
化学方程式的意义
1.表明化学反应中的反应物、生成物和反应条件。
2.表明反应物、生成物各物质之间的质量关系,即各物质之间的质量比。
碳和氧气在点燃的条件下发生反应,生成二氧化碳。
C、O2和CO2的质量比为12 : 32: 44。
C
+
CO2
O2
点燃
3. 表明反应物、生成物各物质之间的微粒个数比。
C、O2和CO2的粒子个数比为1: 1: 1。
4P
+
2P2O5
5O2
点燃
31×4 : 2×16×5 :(2×31+5×16)×2
124 : 160 : 284
31 : 40 : 71
化学方程式计算的理论依据
质量比的计算方法
从化学方程式还能获得下列信息:
1.反应所属类型。
2.反应前后质量守恒等。
36 4 32
在点燃的条件下,碳和氧气反应生成二氧化碳。
在点燃的条件下,每12份质量的碳和32份质量的氧气反应生成44份质量的二氧化碳。
C
+
CO2
O2
点燃
12 32 44
化学方程式的读法
宏观上
质量上
微观上
在点燃的条件下,1个碳原子和1个氧分子恰好完全反应生成1个二氧化碳分子。
请从物质种类、质量、反应条件等方面考虑,讨论下列化学方程式提供的信息:
CuO+H2
加热
Cu+H2O
讨论交流
二、化学方程式的书写
请同学们阅读教材115页,说出书写化学方程式应遵循的原则。
(1)以科学实验的事实为根据,写出反应物和生成物的化学式。
(2)以质量守恒定律为根据,等号两边各种原子的种类和数目必须相同。
1.书写化学方程式应遵循的原则
H2 + O2 H2O + O
化学反应要尊重客观事实,不能改动反应物和生成物的化学式。
下面方程式正确吗?
×
根据科学实验事实,在左边写出反应物的化学式,右边写出生成物的化学式,如果反应物或生成物不止一种,就分别用“+”把它们连接起来,并在反应物与生成物之间画一条短横线。
P + O2 P2O5
根据质量守恒定律,进行配平,即在有关化学式前配上适当的化学计量数,使反应前后各种元素的原子个数相等。
写
配
书写化学方程式的步骤
4P + 5O2 2P2O5
点燃
4P + 5O2 2P2O5
点燃
将短横线改写成“ ”。
4P +5O2 2P2O5
注明反应发生条件以及生成物状态“↑”或“↓”。
注
等
书写化学方程式的步骤
检查化学式是否正确、化学方程式是否配平、反应条件和生成物状态符号是否标注,标注是否恰当。
查
化学方程式中一些符号的意义:
加热
产物中有气体生成
溶液中生成沉淀
反应物中有气体参与,生成气体就不用加“↑”
2CuO。
△表示 ,如
↑表示 ,如
↓表示 ,如
观察碳燃烧的化学方程式
“C+O2 CO2 ”为什么没有“↑”
2H2O2 2H2O +O2↑。
2NaOH+CuSO4==Cu(OH)2 ↓ +Na2SO4。
根据化合价的规则书写化合物的化学式:
先排列,
后标价;
约最简,
再交叉。
正确书写反应物和生成物的化学式
写出下列物质的化学式
(1)氧气、氢气、氯气、氮气
(2)氧化铝、氯化钾、氧化钙、氧化铁
(3)氢氧化钙、碳酸钠、硫酸铜、锰酸钾
O2 H2 Cl2 N2
Al2O3 KCl CaO Fe2O3
Ca(OH)2 Na2CO3 CuSO4 K2MnO4
就是在各化学式前面配上适当的化学计量数,
使左、右两边各种元素的原子个数相等。
配平时只能在各化学式前加化学计量数,
不能改动元素符号右下方的小数字;
配平化学方程式
1
各化学计量数之间为最简整数比,不能是分数,不能有约数。
2
1.红磷在氧气中燃烧生成五氧化二磷,该反应中红磷、氧气、五氧化二磷的质量比为( )
A. 4∶5∶2 B. 31∶24∶47
C. 31∶32∶142 D. 124∶160∶284
D
课 堂 达 标
2. 天然气的主要成分甲烷(CH4)在空气中燃烧的化学反应可用“CH4+2O2 CO2+2H2O”来表示。以下信息:①反应条件;②反应速率;③反应物、生成物各物质间的质量关系;④反应的微观过程;⑤反应过程中的能量变化;⑥反应体系中微观粒子的数量关系。
能从上述化学方程式中获得的是( )
A.①③④ B.②③⑤ C.①③⑥ D.②④⑥
C
3.把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下表。下列说法不正确的是( )
物质 甲 乙 丙 丁
反应前的质量(g) 4.0 2.0 3.0 2.0
反应后的质量(g) 1.2 X 2.4 5.4
A.X=2.0,乙可能是催化剂
B.甲和丙是反应物
C.参加反应的甲、丙质量比是1∶2
D.丁一定是化合物
C
4.根据已学知识判断下列反应方程式是否正确?如有错误,请指出错误之处:
(1)3Fe+2O2 Fe3O4
(2)Mg+O2 MgO2
(3)CH4+O2 CO2+H2O
加热
点燃
点燃
×
×
×
谢 谢 观 看
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
