【轻松备课】人教版化学九年级上 第三单元 课题2 原子的结构(第2课时)教学课件
文档属性
| 名称 | 【轻松备课】人教版化学九年级上 第三单元 课题2 原子的结构(第2课时)教学课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 916.6KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览







文档简介
(共22张PPT)
第三单元 物质构成的奥秘
第三单元 物质构成的奥秘
课题2 原子的结构
第2课时
1.了解构建原子结构示意图是一种模型化的方法。
2.了解原子核外的电子是分层排布的。
3.了解典型元素(稀有气体、金属和非金属)原子核外电子排布的特点。
4.以氯化钠为例,了解离子形成的过程,知道离子是构成物质的一种粒子。
学 习 目 标
思考?电子在核外的空间里做高速的运动,它们会相互碰撞打架吗?电子在核外的排布会有什么特点?
特点:核外电子是分层运动的,这种分层运动也叫分层排布。
三、原子核外电子的排布
自 主 探 究
1.核外电子排布的特点
(1)各层最多能容纳的电子数为2n2个;
(2)第一层最多容纳2个电子,第二层最多容纳8个电子,最外层不超过8个电子(若第一层为最外层时,不超过2个电子);
(3)能量低的优先排满,依次再排能量逐步升高的电子层里。
回忆原子的构成
+11
2.原子结构示意图
电子层
原子核
质子数
各电子层上的电子数
圆圈表示
圈内数字表示
弧线表示
原子核带正电
“+”表示
最外层电子数
数字1也可以表示
2 8 1
弧线上的数字表示
第一层
第二层
第三层(最外层)
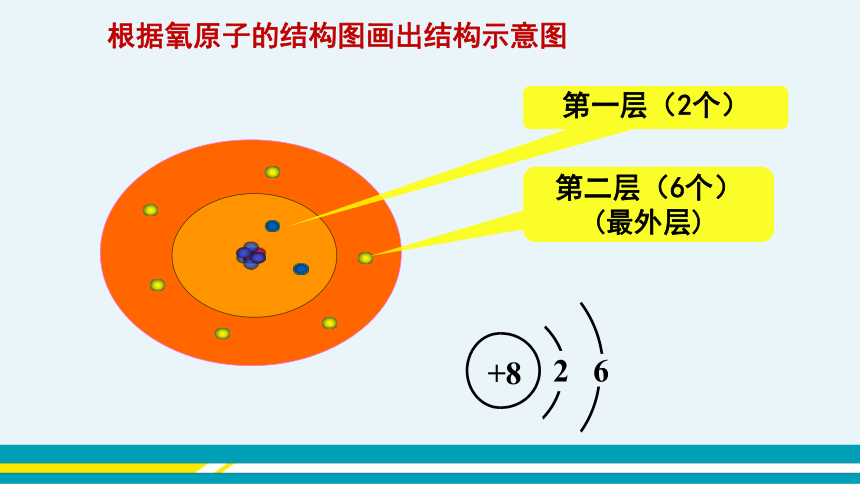
第一层(2个)
第二层(6个)
(最外层)
根据氧原子的结构图画出结构示意图
+8
2
6
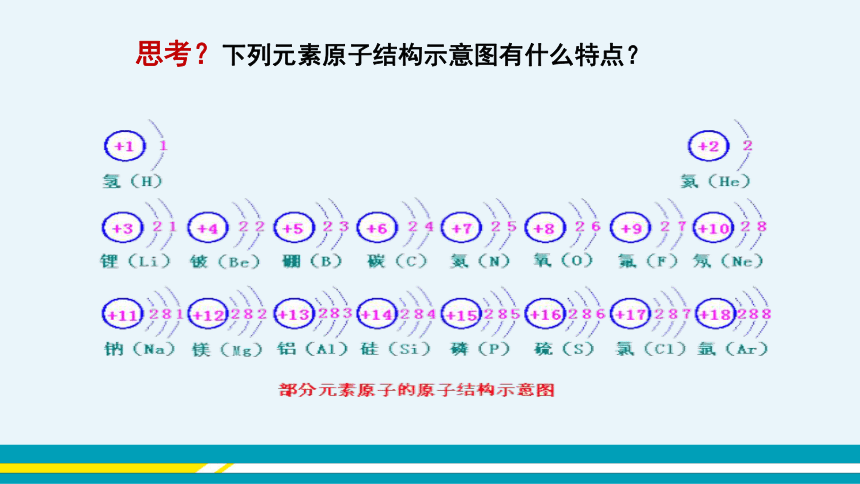
思考?下列元素原子结构示意图有什么特点?
⑴第一层最多容纳___个电子,第二层最多容纳___个电子。
2
(2)最外层不超过 个电子,只有1层的不超过___个电子。
8
8
⑶电子先排满第___层,再排第___层,排满第___层,再排第___层。(按照能量由低到高的顺序分层排布)
2
3
2
3.核外电子的排布规律
1
2
4.原子结构与元素分类和元素化学性质的关系
(1)金属元素:最外层一般少于4个电子,易失去最外层电子,化学性质活泼。
(2)非金属元素:最外层一般等于或大于4个电子,易得到电子,化学性质活泼。
(3)稀有气体元素:最外层8个电子(氦2个),称稳定结构,化学性质不活泼。
结论:1.元素的化学性质与原子的最外层电子数有着密切关系。
2.最外层电子数决定元素的化学性质。
由于金属原子、非金属原子的原子核外最外层没有达到稳定结构,在化学反应中易得失电子,从而达到稳定结构,那么,得失电子的结果怎样呢?
Na
Na+
Cl
Cl-
Na
Cl
5.离子的形成
NaCl
钠 + 氯气 氯化钠
点燃
NaCl
Na
Cl2
钠在氯气中点燃生成氯化钠的形成过程
1.离子的定义:带电的原子(或原子团)叫离子。
2.离子的分类
(1)阳离子:带正电的原子(或原子团)叫做阳离子。
①特点:电子数<质子数。
②示例:Na+、K+、Mg2+、Al3+。
(2)阴离子:带负电的原子(或原子团)叫做阴离子。
①特点:电子数>质子数。
②示例:O2-、S2-、 F- 、Cl-。
四、离子
3.离子化合物
像氯化钠由阴、阳离子靠静电作用而形成的化合物。
4.离子符号的书写
先写元素符号,然后将电荷数标注在元素符号的右上角,数字在前、符号在后,“1”省略不写。离子所带电荷数由该元素原子的最外层电子数决定。
X
n±
离子带正或负电
离子所带电荷数(得失电子数);
当n=1时略去不写
元素符号
5.离子符号表示的意义
表示一个镁离子
表示一个带2个单位正电荷的镁离子
3Mg2+
表示3个镁离子
Mg2+
熟记常见原子团(根)的符号、名称
名称: 氢氧根 硝酸根 铵根 碳酸根 硫酸根
符号: OH- NO3- NH4+ CO32- SO42-
6.构成物质的粒子
构成物质的粒子包括原子、分子、离子。
(1)由原子直接构成的物质:稀有气体(如:He、Ne等);金属(如:Hg、Fe等);少数固态非金属(如:C、Si等)。
(2)由分子构成的物质:双原子气体分子(如:H2、O2、N2等);多原子共价化合物(如:H2O、CO2、HCl等)。
(3)由离子构成的物质:离子化合物(如:NaCl、K2S、CuSO4等)。
7.离子与原子的区别和联系
原子
阴离子
阳离子
失电子
得电子
失电子
得电子
(2)联系
(1)区别
①化学性质不同:原子大多不稳定,化学性质活泼;离子结构稳定,化学性质不活泼。
②电性不同:原子不带电,离子带电。
Na
Mg
2
1
8
+11
2
2
8
+12
2
6
8
+16
2
7
8
+17
S
Cl
2
8
+11
2
8
+12
2
8
8
+16
2
8
8
+17
1.辨别下列哪些是原子结构示意图,哪些是离子结构示意图,并能够根据结构示意图写出对应的符号:
原子:核电荷数=核外电子数
离子:核电荷数≠核外电子数
Na+
Mg2+
S2-
Cl-
课 堂 达 标
Al3+
10
铝离子
2
8
+13
2.某离子带3个单位的正电荷,质子数为13,
该离子的核外电子数为_____,该离子的
名称是______,符号是____,该离子的
结构示意图是:
3.根据右边的结构图回答:
如果该图表示的是原子,X值为___,该原子的符号是____。
如果该图表示的是带两个单位正电荷的阳离子,X值为___,符号是____。
如果该图表示的是带两个单位负电荷的阴离子,X值为___,符号是____。
10
Ne
12
Mg2+
8
O2-
点评:求离子的核电荷数采用还原成原子的方法。
谢 谢 观 看
第三单元 物质构成的奥秘
第三单元 物质构成的奥秘
课题2 原子的结构
第2课时
1.了解构建原子结构示意图是一种模型化的方法。
2.了解原子核外的电子是分层排布的。
3.了解典型元素(稀有气体、金属和非金属)原子核外电子排布的特点。
4.以氯化钠为例,了解离子形成的过程,知道离子是构成物质的一种粒子。
学 习 目 标
思考?电子在核外的空间里做高速的运动,它们会相互碰撞打架吗?电子在核外的排布会有什么特点?
特点:核外电子是分层运动的,这种分层运动也叫分层排布。
三、原子核外电子的排布
自 主 探 究
1.核外电子排布的特点
(1)各层最多能容纳的电子数为2n2个;
(2)第一层最多容纳2个电子,第二层最多容纳8个电子,最外层不超过8个电子(若第一层为最外层时,不超过2个电子);
(3)能量低的优先排满,依次再排能量逐步升高的电子层里。
回忆原子的构成
+11
2.原子结构示意图
电子层
原子核
质子数
各电子层上的电子数
圆圈表示
圈内数字表示
弧线表示
原子核带正电
“+”表示
最外层电子数
数字1也可以表示
2 8 1
弧线上的数字表示
第一层
第二层
第三层(最外层)
第一层(2个)
第二层(6个)
(最外层)
根据氧原子的结构图画出结构示意图
+8
2
6
思考?下列元素原子结构示意图有什么特点?
⑴第一层最多容纳___个电子,第二层最多容纳___个电子。
2
(2)最外层不超过 个电子,只有1层的不超过___个电子。
8
8
⑶电子先排满第___层,再排第___层,排满第___层,再排第___层。(按照能量由低到高的顺序分层排布)
2
3
2
3.核外电子的排布规律
1
2
4.原子结构与元素分类和元素化学性质的关系
(1)金属元素:最外层一般少于4个电子,易失去最外层电子,化学性质活泼。
(2)非金属元素:最外层一般等于或大于4个电子,易得到电子,化学性质活泼。
(3)稀有气体元素:最外层8个电子(氦2个),称稳定结构,化学性质不活泼。
结论:1.元素的化学性质与原子的最外层电子数有着密切关系。
2.最外层电子数决定元素的化学性质。
由于金属原子、非金属原子的原子核外最外层没有达到稳定结构,在化学反应中易得失电子,从而达到稳定结构,那么,得失电子的结果怎样呢?
Na
Na+
Cl
Cl-
Na
Cl
5.离子的形成
NaCl
钠 + 氯气 氯化钠
点燃
NaCl
Na
Cl2
钠在氯气中点燃生成氯化钠的形成过程
1.离子的定义:带电的原子(或原子团)叫离子。
2.离子的分类
(1)阳离子:带正电的原子(或原子团)叫做阳离子。
①特点:电子数<质子数。
②示例:Na+、K+、Mg2+、Al3+。
(2)阴离子:带负电的原子(或原子团)叫做阴离子。
①特点:电子数>质子数。
②示例:O2-、S2-、 F- 、Cl-。
四、离子
3.离子化合物
像氯化钠由阴、阳离子靠静电作用而形成的化合物。
4.离子符号的书写
先写元素符号,然后将电荷数标注在元素符号的右上角,数字在前、符号在后,“1”省略不写。离子所带电荷数由该元素原子的最外层电子数决定。
X
n±
离子带正或负电
离子所带电荷数(得失电子数);
当n=1时略去不写
元素符号
5.离子符号表示的意义
表示一个镁离子
表示一个带2个单位正电荷的镁离子
3Mg2+
表示3个镁离子
Mg2+
熟记常见原子团(根)的符号、名称
名称: 氢氧根 硝酸根 铵根 碳酸根 硫酸根
符号: OH- NO3- NH4+ CO32- SO42-
6.构成物质的粒子
构成物质的粒子包括原子、分子、离子。
(1)由原子直接构成的物质:稀有气体(如:He、Ne等);金属(如:Hg、Fe等);少数固态非金属(如:C、Si等)。
(2)由分子构成的物质:双原子气体分子(如:H2、O2、N2等);多原子共价化合物(如:H2O、CO2、HCl等)。
(3)由离子构成的物质:离子化合物(如:NaCl、K2S、CuSO4等)。
7.离子与原子的区别和联系
原子
阴离子
阳离子
失电子
得电子
失电子
得电子
(2)联系
(1)区别
①化学性质不同:原子大多不稳定,化学性质活泼;离子结构稳定,化学性质不活泼。
②电性不同:原子不带电,离子带电。
Na
Mg
2
1
8
+11
2
2
8
+12
2
6
8
+16
2
7
8
+17
S
Cl
2
8
+11
2
8
+12
2
8
8
+16
2
8
8
+17
1.辨别下列哪些是原子结构示意图,哪些是离子结构示意图,并能够根据结构示意图写出对应的符号:
原子:核电荷数=核外电子数
离子:核电荷数≠核外电子数
Na+
Mg2+
S2-
Cl-
课 堂 达 标
Al3+
10
铝离子
2
8
+13
2.某离子带3个单位的正电荷,质子数为13,
该离子的核外电子数为_____,该离子的
名称是______,符号是____,该离子的
结构示意图是:
3.根据右边的结构图回答:
如果该图表示的是原子,X值为___,该原子的符号是____。
如果该图表示的是带两个单位正电荷的阳离子,X值为___,符号是____。
如果该图表示的是带两个单位负电荷的阴离子,X值为___,符号是____。
10
Ne
12
Mg2+
8
O2-
点评:求离子的核电荷数采用还原成原子的方法。
谢 谢 观 看
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
