【轻松备课】人教版化学九年级上 第六单元 课题3 二氧化碳和一氧化碳(第2课时)教学课件
文档属性
| 名称 | 【轻松备课】人教版化学九年级上 第六单元 课题3 二氧化碳和一氧化碳(第2课时)教学课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 12.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览








文档简介
(共23张PPT)
第 六 单 元 碳和碳的氧化物
第 2 课 时
课 题 3 二氧化碳和一氧化碳
第六单元 碳和碳的氧化物
1.通过生活实例,能说出二氧化碳的用途和自然界中的碳循环。
2.通过小组交流讨论,总结归纳温室效应的原因及危害并能说出防止温室效应进一步增强的措施。
3.通过实验,结合生活实例,记住一氧化碳的性质,能写出相关的化学方程式。
4.认识自然界中二氧化碳的循环及重要性,增强环保意识及人与自然的和谐统一意识;通过全面认识一氧化碳的性质,体会任何事物的两面性。
学 习 目 标
自 主 探 究
阅读教材119-121页,思考:
1. 二氧化碳有哪些用途,利用了二氧化碳的哪些性质?
2. 温室效应增强的原因、危害和对策。
3. 日常生活中怎样做才算是“低碳”?
二氧化碳的主要用途
用途 性质
灭火 不能燃烧一般也不支持燃烧,密度比空气大
汽水、碳酸饮料 可溶于水
温室气体肥料 能够参与光合作用
致冷剂、人工降雨 干冰升华吸热
合作交流
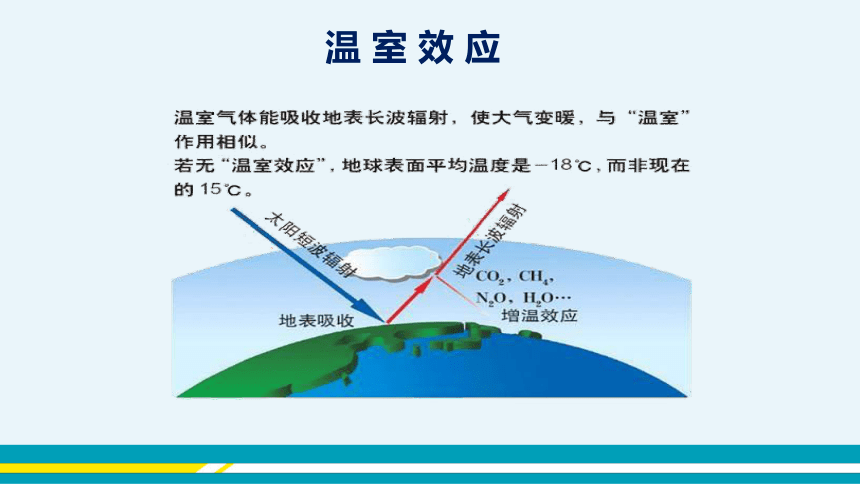
温 室 效 应
(1)改变能源结构,减少使用煤、石油、天然气等化石燃料,更多地利用太阳能、风能等清洁能源。
(2)大力植树造林,严禁乱砍滥伐。
(3)提高能源的生产效率和使用效率。
(4)采用物理或化学的方法,人工吸收二氧化碳。
减缓温室效应的措施
低碳指的是较低的二氧化碳排放量
物理性质 颜色 气味 状态 溶解性 密度
一氧化碳
无色
无味
气体
难溶于水
比空气略小
1.一氧化碳的物理性质
一氧化碳可以用什么方法收集?
可以用排水法收集
自主学习
2.一氧化碳的化学性质
(1)一氧化碳有可燃性。
点燃前要:检验纯度
化学方程式:2CO+O2====2CO2
用途:气体燃料。
燃烧现象:点燃纯净的CO,它能够燃烧,放出大量的热,火焰呈蓝色,生成能使澄清的石灰水变浑浊的气体。
点燃
思考讨论:
1.煤气的主要成分是什么?
2.煤气泄漏为什么不易被发觉?
3.煤气中毒的原因是什么?
4.怎样预防煤气中毒?
5.煤炉上放一壶水能防止煤气中毒吗?
小组合作
冬季用炭火取暖或在浴室内使用燃气热水器,由于环境比较密闭,燃料不充分燃烧,容易产生一氧化碳使人中毒。
小常识
由于一氧化碳无色无味,泄露不易被发现。
(2)一氧化碳有毒性。
一氧化碳极易与血红蛋白结合,从而使血红蛋白不能再与氧气结合,造成生物体缺氧。
预防一氧化碳中毒的措施
发生煤气泄漏应关闭阀门,开窗通风;
不能触动电器开关
一氧化碳与氧化铜反应
一氧化碳还原氧化铜的实验应怎样操作?
探究实验
实验步骤 原因
1.连接装置 ,检查装置的气密性。
2.点燃后面酒精灯。
3.先通入CO。
4.然后加热CuO。 5.停止加热CuO。
6.冷却后停止通入CO。 7 . 停止点燃尾气。
防止尾气中有毒的一氧化碳污染空气。
为了排尽玻璃管内的空气,防止一氧
化碳和氧气混合加热发生爆炸。
为了防止热的铜被氧化,防止石灰水
倒流进玻璃管中,炸裂玻璃管。
一氧化碳与氧化铜反应
黑色粉末变为红色
澄清石灰水变浑浊
有蓝色火焰出现
用途:冶金工业,例如利用一氧化碳还原性炼铁
CO + CuO ==== Cu + CO2
加热
还原剂
具有还原性
被氧化
发生氧化反应
氧化剂
具有氧化性
被还原
发生还原反应
(3)一氧化碳有还原性
总 结
2.一氧化碳的化学性质
(1)一氧化碳具有可燃性 2CO+O2====2CO2
(2)一氧化碳有毒
(3)一氧化碳具有还原性 CO+CuO ==== Cu+ CO2
加热
点燃
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
课 堂 达 标
1.下列二氧化碳的用途,既跟它的物理性质有关,又跟它的化学性质有关的是( )
A.用来灭火 B.制干冰
C.温室内做气体肥料 D.制化肥
A
2.关于C、CO、CO2三种物质,有下列说法:
①三种物质都含有碳元素,都具有还原性
②CO、CO2都是没有颜色、没有气味的气体
③CO2可用于光合作用,CO可用于人工降雨
④CO2能产生温室效应,CO易与血液中的血红蛋白结合引起中毒
⑤CO2可用来灭火,CO可用作燃料
上述说法中正确的是( )
A.①②③ B.②③④ C.②④⑤ D.①③⑤
C
3.某同学设计右图所示的实验装置,进行一氧化碳还原氧化铜的实验。试回答:
(l)该装置存在的一个主要问题是_____ ,写出你的改进方法。
(2)实验开始时,是先给氧化铜加热,还是先
通入一氧化碳
(3)实验过程中,A处能观察到的实验现象是
发生反应的化学方程式为
B处观察到的实验现象是
缺少尾气的处理装置
在出气口处添加一燃着的酒精灯,把未反应的一氧化碳燃烧掉。
先通一氧化碳。
加热
CuO+CO ==== Cu+CO2
澄清的石灰水变浑浊。
黑色的固体逐渐变成亮红色的固体。
谢 谢 观 看
第 六 单 元 碳和碳的氧化物
第 2 课 时
课 题 3 二氧化碳和一氧化碳
第六单元 碳和碳的氧化物
1.通过生活实例,能说出二氧化碳的用途和自然界中的碳循环。
2.通过小组交流讨论,总结归纳温室效应的原因及危害并能说出防止温室效应进一步增强的措施。
3.通过实验,结合生活实例,记住一氧化碳的性质,能写出相关的化学方程式。
4.认识自然界中二氧化碳的循环及重要性,增强环保意识及人与自然的和谐统一意识;通过全面认识一氧化碳的性质,体会任何事物的两面性。
学 习 目 标
自 主 探 究
阅读教材119-121页,思考:
1. 二氧化碳有哪些用途,利用了二氧化碳的哪些性质?
2. 温室效应增强的原因、危害和对策。
3. 日常生活中怎样做才算是“低碳”?
二氧化碳的主要用途
用途 性质
灭火 不能燃烧一般也不支持燃烧,密度比空气大
汽水、碳酸饮料 可溶于水
温室气体肥料 能够参与光合作用
致冷剂、人工降雨 干冰升华吸热
合作交流
温 室 效 应
(1)改变能源结构,减少使用煤、石油、天然气等化石燃料,更多地利用太阳能、风能等清洁能源。
(2)大力植树造林,严禁乱砍滥伐。
(3)提高能源的生产效率和使用效率。
(4)采用物理或化学的方法,人工吸收二氧化碳。
减缓温室效应的措施
低碳指的是较低的二氧化碳排放量
物理性质 颜色 气味 状态 溶解性 密度
一氧化碳
无色
无味
气体
难溶于水
比空气略小
1.一氧化碳的物理性质
一氧化碳可以用什么方法收集?
可以用排水法收集
自主学习
2.一氧化碳的化学性质
(1)一氧化碳有可燃性。
点燃前要:检验纯度
化学方程式:2CO+O2====2CO2
用途:气体燃料。
燃烧现象:点燃纯净的CO,它能够燃烧,放出大量的热,火焰呈蓝色,生成能使澄清的石灰水变浑浊的气体。
点燃
思考讨论:
1.煤气的主要成分是什么?
2.煤气泄漏为什么不易被发觉?
3.煤气中毒的原因是什么?
4.怎样预防煤气中毒?
5.煤炉上放一壶水能防止煤气中毒吗?
小组合作
冬季用炭火取暖或在浴室内使用燃气热水器,由于环境比较密闭,燃料不充分燃烧,容易产生一氧化碳使人中毒。
小常识
由于一氧化碳无色无味,泄露不易被发现。
(2)一氧化碳有毒性。
一氧化碳极易与血红蛋白结合,从而使血红蛋白不能再与氧气结合,造成生物体缺氧。
预防一氧化碳中毒的措施
发生煤气泄漏应关闭阀门,开窗通风;
不能触动电器开关
一氧化碳与氧化铜反应
一氧化碳还原氧化铜的实验应怎样操作?
探究实验
实验步骤 原因
1.连接装置 ,检查装置的气密性。
2.点燃后面酒精灯。
3.先通入CO。
4.然后加热CuO。 5.停止加热CuO。
6.冷却后停止通入CO。 7 . 停止点燃尾气。
防止尾气中有毒的一氧化碳污染空气。
为了排尽玻璃管内的空气,防止一氧
化碳和氧气混合加热发生爆炸。
为了防止热的铜被氧化,防止石灰水
倒流进玻璃管中,炸裂玻璃管。
一氧化碳与氧化铜反应
黑色粉末变为红色
澄清石灰水变浑浊
有蓝色火焰出现
用途:冶金工业,例如利用一氧化碳还原性炼铁
CO + CuO ==== Cu + CO2
加热
还原剂
具有还原性
被氧化
发生氧化反应
氧化剂
具有氧化性
被还原
发生还原反应
(3)一氧化碳有还原性
总 结
2.一氧化碳的化学性质
(1)一氧化碳具有可燃性 2CO+O2====2CO2
(2)一氧化碳有毒
(3)一氧化碳具有还原性 CO+CuO ==== Cu+ CO2
加热
点燃
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
课 堂 达 标
1.下列二氧化碳的用途,既跟它的物理性质有关,又跟它的化学性质有关的是( )
A.用来灭火 B.制干冰
C.温室内做气体肥料 D.制化肥
A
2.关于C、CO、CO2三种物质,有下列说法:
①三种物质都含有碳元素,都具有还原性
②CO、CO2都是没有颜色、没有气味的气体
③CO2可用于光合作用,CO可用于人工降雨
④CO2能产生温室效应,CO易与血液中的血红蛋白结合引起中毒
⑤CO2可用来灭火,CO可用作燃料
上述说法中正确的是( )
A.①②③ B.②③④ C.②④⑤ D.①③⑤
C
3.某同学设计右图所示的实验装置,进行一氧化碳还原氧化铜的实验。试回答:
(l)该装置存在的一个主要问题是_____ ,写出你的改进方法。
(2)实验开始时,是先给氧化铜加热,还是先
通入一氧化碳
(3)实验过程中,A处能观察到的实验现象是
发生反应的化学方程式为
B处观察到的实验现象是
缺少尾气的处理装置
在出气口处添加一燃着的酒精灯,把未反应的一氧化碳燃烧掉。
先通一氧化碳。
加热
CuO+CO ==== Cu+CO2
澄清的石灰水变浑浊。
黑色的固体逐渐变成亮红色的固体。
谢 谢 观 看
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
