【轻松备课】人教版化学九年级上 第五单元 课题2 如何正确书写化学方程式(第1课时)教学课件
文档属性
| 名称 | 【轻松备课】人教版化学九年级上 第五单元 课题2 如何正确书写化学方程式(第1课时)教学课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
第 五 单 元 化学方程式
第1课时
课 题 2 如何正确书写化学方程式
第五单元 化学方程式
1.通过复习质量守恒定律,知道书写化学方程式遵守的原则。
2.通过分析具体的化学反应,理解化学方程式的含义。
3.通过练习,能正确书写简单的化学方程式。
学 习 目 标
木炭燃烧
红磷燃烧
硫酸铜溶液与氢氧化钠溶液反应
一、书写化学方程式遵循的原则
请同学们阅读教材98页。
自 主 探 究
(1)以客观事实为基础。
(2)遵守质量守恒定律,即等号两边
各原子的种类和数目必须相等。
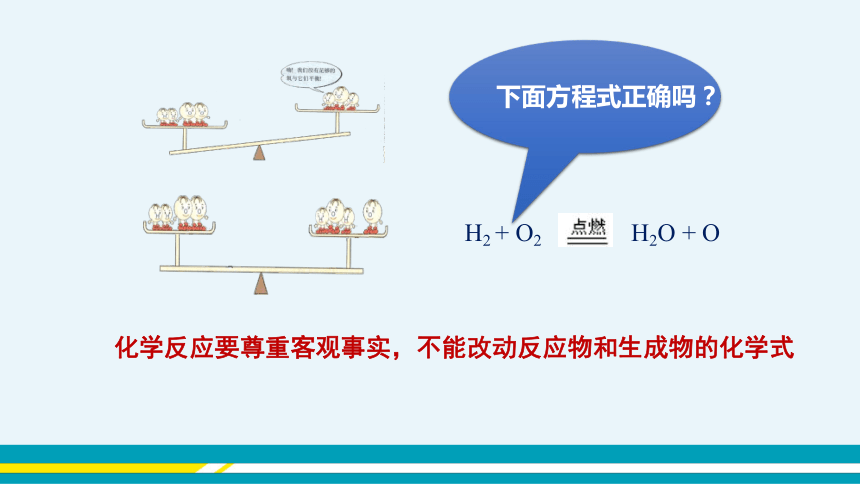
H2 + O2 H2O + O
化学反应要尊重客观事实,不能改动反应物和生成物的化学式
下面方程式正确吗?
点燃
4P + 5O2 2P2O5
点燃
在短线两边写出反应物与生成物的化学式
P + O2 P2O5
在化学式前填数字将两边的原子数目配平
4P + 5O2 2P2O5
将短横线改写成“ ”
4P +5O2 2P2O5
注明反应发生条件以及生成物状态“↑”或“↓”
二、书写化学方程式的步骤
写
配
注
等
根据化合价的规则书写化合物的化学式:
先排列,
后标价;
约最简,
再交叉。
正确书写反应物和生成物的化学式
写出下列物质的化学式
(1)氧气、氢气、氯气、氮气
(2)氧化铝、氯化钾、氧化钙、氧化铁
(3)氢氧化钙、碳酸钠、硫酸铜、锰酸钾
O2 H2 Cl2 N2
Al2O3 KCl CaO Fe2O3
Ca(OH)2 Na2CO3 CuSO4 K2MnO4
就是在各化学式前面配上适当的化学计量数,
使左、右两边各种元素的原子个数相等。
配平时只能在各化学式前加化学计量数,
不能改动元素符号右下方的小数字;
配平化学方程式
1
各化学计量数之间为最简整数比,不能是分数,不能有约数。
2
S + O2 SO2
点燃
C + O2 CO2
点燃
C + O2 CO
点燃
这种方法适合一些
简单的化学方程式,
凑数进行配平。
配平方法一:观察法
2
2
三、化学方程式的配平方法
首先找出其中出现次数较多,且原子个数相差较多的原子作配平起点,求出它们的最小公倍数。反应前、后该(氧)原子个数的最小公倍数是10
P + 5O2 2P2O5
最小公倍数除以化学式中该原子的个数,把得到的数字写到化学式前面。在O2前面配上计量数5,在P2O5前面配上计量数2。
4P + 5O2 2P2O5
再配平其他原子。等号后面磷原子的个数是4,在等号前面P前面配上计量数4。
P + O2 P2O5
配平方法二:最小公倍数法
(1) C + CO2 CO
高温
点燃
点燃
高温
配平下列化学方程式
2
4 3 2
2 2
2 2
(5) KClO3 KCl + O2↑
MnO2
△
3
2
2
(3) CuO + C Cu + CO2
(2) Al + O2 Al2O3
(4) CH4 + O2 CO2 + H2O
加热(△)、点燃、催化剂、一定条件、
800度、催化剂、高温高压等
2
2
H2O
H2
+
O2
通电
液体
气体
气体
注明反应条件,生成物状态
1
气体↑和沉淀↓的标注
只有生成物中有气体时(反应物中没有气体),在气体物质的化学式右边标注“↑”
2
如硫酸铜溶液与氢氧化钠溶液的化学反应方程式:
注意:配平时原子团当成一个整体来考虑
2
+
+
CuSO4
NaOH
Cu(OH)2
Na2SO4
注明反应条件,生成物状态
气体↑和沉淀↓的标注
溶液中的反应 ,只有生成物中有难溶的固体物质时(反应物无难溶性固体),在固体物质的化学式右边标注“↓”。
3
1.S+O2 SO2
加热
2.C+O2 CO2
点燃
3.Fe+CuSO4 Cu +FeSO4
判断下列反应的化学方程式的反应条件、气体符号
和沉淀符号添加是否正确?
×
×
×
1.细铁丝燃烧
2.镁带燃烧
3.实验室用过氧化氢制取氧气
4.高锰酸钾受热分解
点燃
3Fe+2O2 Fe3O4
2Mg+ O2 2MgO
点燃
MnO2
2H2O2 2H2O+O2
Δ
2
KMnO4
K2MnO4
MnO2
+
+
O2
正确书写下列反应的化学方程式:
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
课 堂 达 标
写出下列反应的化学方程式:
1.点燃红磷
2.加热氯酸钾和二氧化锰混合物
3.铝在氧气中燃烧
4.在空气中点燃氢气
5.氧化汞加热分解
点燃
4P+5O2 2P2O5
点燃
4Al+3O2 2Al2O3
点燃
2H2+O2 2H2O
2HgO 2Hg+O2
Δ
↑
2KClO3 2KCl+3O2↑
Δ
MnO2
4. 2KMnO4 K2MnO4+ MnO2+ O2
点燃
生成物的化学式书写错误
没有配平
不应该标生成物的状态
未标明气体的状态
2.指出下列化学方程式的错误并说明原因
不应该在化学式中间配平
化学计量数要化成最简整数比
1. Mg + O2 MgO2
通电
2. H2O H2↑+ O2↑
Δ
3. Fe+CuSO4 Cu +FeSO4
5. Mg+ O2 Mg2O
6. 4H2O2 4H2O+2O2
MnO2
点燃
谢 谢 观 看
第 五 单 元 化学方程式
第1课时
课 题 2 如何正确书写化学方程式
第五单元 化学方程式
1.通过复习质量守恒定律,知道书写化学方程式遵守的原则。
2.通过分析具体的化学反应,理解化学方程式的含义。
3.通过练习,能正确书写简单的化学方程式。
学 习 目 标
木炭燃烧
红磷燃烧
硫酸铜溶液与氢氧化钠溶液反应
一、书写化学方程式遵循的原则
请同学们阅读教材98页。
自 主 探 究
(1)以客观事实为基础。
(2)遵守质量守恒定律,即等号两边
各原子的种类和数目必须相等。
H2 + O2 H2O + O
化学反应要尊重客观事实,不能改动反应物和生成物的化学式
下面方程式正确吗?
点燃
4P + 5O2 2P2O5
点燃
在短线两边写出反应物与生成物的化学式
P + O2 P2O5
在化学式前填数字将两边的原子数目配平
4P + 5O2 2P2O5
将短横线改写成“ ”
4P +5O2 2P2O5
注明反应发生条件以及生成物状态“↑”或“↓”
二、书写化学方程式的步骤
写
配
注
等
根据化合价的规则书写化合物的化学式:
先排列,
后标价;
约最简,
再交叉。
正确书写反应物和生成物的化学式
写出下列物质的化学式
(1)氧气、氢气、氯气、氮气
(2)氧化铝、氯化钾、氧化钙、氧化铁
(3)氢氧化钙、碳酸钠、硫酸铜、锰酸钾
O2 H2 Cl2 N2
Al2O3 KCl CaO Fe2O3
Ca(OH)2 Na2CO3 CuSO4 K2MnO4
就是在各化学式前面配上适当的化学计量数,
使左、右两边各种元素的原子个数相等。
配平时只能在各化学式前加化学计量数,
不能改动元素符号右下方的小数字;
配平化学方程式
1
各化学计量数之间为最简整数比,不能是分数,不能有约数。
2
S + O2 SO2
点燃
C + O2 CO2
点燃
C + O2 CO
点燃
这种方法适合一些
简单的化学方程式,
凑数进行配平。
配平方法一:观察法
2
2
三、化学方程式的配平方法
首先找出其中出现次数较多,且原子个数相差较多的原子作配平起点,求出它们的最小公倍数。反应前、后该(氧)原子个数的最小公倍数是10
P + 5O2 2P2O5
最小公倍数除以化学式中该原子的个数,把得到的数字写到化学式前面。在O2前面配上计量数5,在P2O5前面配上计量数2。
4P + 5O2 2P2O5
再配平其他原子。等号后面磷原子的个数是4,在等号前面P前面配上计量数4。
P + O2 P2O5
配平方法二:最小公倍数法
(1) C + CO2 CO
高温
点燃
点燃
高温
配平下列化学方程式
2
4 3 2
2 2
2 2
(5) KClO3 KCl + O2↑
MnO2
△
3
2
2
(3) CuO + C Cu + CO2
(2) Al + O2 Al2O3
(4) CH4 + O2 CO2 + H2O
加热(△)、点燃、催化剂、一定条件、
800度、催化剂、高温高压等
2
2
H2O
H2
+
O2
通电
液体
气体
气体
注明反应条件,生成物状态
1
气体↑和沉淀↓的标注
只有生成物中有气体时(反应物中没有气体),在气体物质的化学式右边标注“↑”
2
如硫酸铜溶液与氢氧化钠溶液的化学反应方程式:
注意:配平时原子团当成一个整体来考虑
2
+
+
CuSO4
NaOH
Cu(OH)2
Na2SO4
注明反应条件,生成物状态
气体↑和沉淀↓的标注
溶液中的反应 ,只有生成物中有难溶的固体物质时(反应物无难溶性固体),在固体物质的化学式右边标注“↓”。
3
1.S+O2 SO2
加热
2.C+O2 CO2
点燃
3.Fe+CuSO4 Cu +FeSO4
判断下列反应的化学方程式的反应条件、气体符号
和沉淀符号添加是否正确?
×
×
×
1.细铁丝燃烧
2.镁带燃烧
3.实验室用过氧化氢制取氧气
4.高锰酸钾受热分解
点燃
3Fe+2O2 Fe3O4
2Mg+ O2 2MgO
点燃
MnO2
2H2O2 2H2O+O2
Δ
2
KMnO4
K2MnO4
MnO2
+
+
O2
正确书写下列反应的化学方程式:
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
课 堂 达 标
写出下列反应的化学方程式:
1.点燃红磷
2.加热氯酸钾和二氧化锰混合物
3.铝在氧气中燃烧
4.在空气中点燃氢气
5.氧化汞加热分解
点燃
4P+5O2 2P2O5
点燃
4Al+3O2 2Al2O3
点燃
2H2+O2 2H2O
2HgO 2Hg+O2
Δ
↑
2KClO3 2KCl+3O2↑
Δ
MnO2
4. 2KMnO4 K2MnO4+ MnO2+ O2
点燃
生成物的化学式书写错误
没有配平
不应该标生成物的状态
未标明气体的状态
2.指出下列化学方程式的错误并说明原因
不应该在化学式中间配平
化学计量数要化成最简整数比
1. Mg + O2 MgO2
通电
2. H2O H2↑+ O2↑
Δ
3. Fe+CuSO4 Cu +FeSO4
5. Mg+ O2 Mg2O
6. 4H2O2 4H2O+2O2
MnO2
点燃
谢 谢 观 看
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
