2023-2024学年九年级化学鲁教版上册第三单元溶液检测题(无答案)
文档属性
| 名称 | 2023-2024学年九年级化学鲁教版上册第三单元溶液检测题(无答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 339.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览

文档简介
鲁教版第三单元溶液测试题
一.选择题
1.将厨房中的下列物质分别加入适量水中、充分搅拌。能形成溶液的是( )
A. 豆油 B. 奶粉 C. 食盐 D. 花生酱
2.名称中有“水”字的物质可能是溶液,下列有“水”字的物质不属于溶液的是( )
A. 矿泉水B. 食盐水C. 冰水D. 澄清的石灰水
3.“恒大冰泉”是来自长白山的天然矿泉水,判断“恒大冰泉”属于溶液的依据是( )
①无色 ②混合物 ③化合物 ④均一性 ⑤稳定性.
A. ①②④ B. ②④⑤ C. ①③⑤ D. ③④⑤
4.医生常用生理盐水(溶质质量分数为0.9%)给患者输液。下列对生理盐水的理解不正确的是( )
A. 生理盐水中氯化钠是溶质,水是溶剂B. 输液时,输液管中和输液瓶中生理盐水的溶质质量分数相同
C. 每输入100g生理盐水,进入患者体内的氯化钠质量为0.9gD.生理盐水中氯化钠与水的质量比为9:1000
5.如图所示,U型管内a、b两液面高度相同。现将胶头滴管内的少量水挤入锥形瓶内,一会儿后观察到U型管内a液面上升,b液面下降。已知固体X是氢氧化钠、硝酸铵、氯化钠、蔗糖四种固体物质中的一种,则X是( )
A. 氢氧化钠固体
B. 硝酸铵固体
C. 氯化钠固体
D. 蔗糖固体
6.下列有关溶液的相关说法中正确的是( )
A. 物质的溶解过程通常会伴随着能量变化B. 溶液具有均一、稳定、透明的特征
C. 任何溶液都只含有一种溶质D. 不饱和溶液变饱和溶液,溶质质量分数一定变大
7.许多科学知识在逻辑上存在如图所示关系。其中并列关系是由于分类依据的相同而把事物截然分开并列,而交叉关系是对事物分类时,由于采用不同的分类依据,则必然出现交叉关系,下列关于溶液说法正确的是( )
A饱和溶液包含浓溶液 B. 饱和溶液与稀溶液属于并列关系
C. 饱和溶液与不饱和溶液属于交叉关系 D. 不饱和溶液与稀溶液属于交叉关系
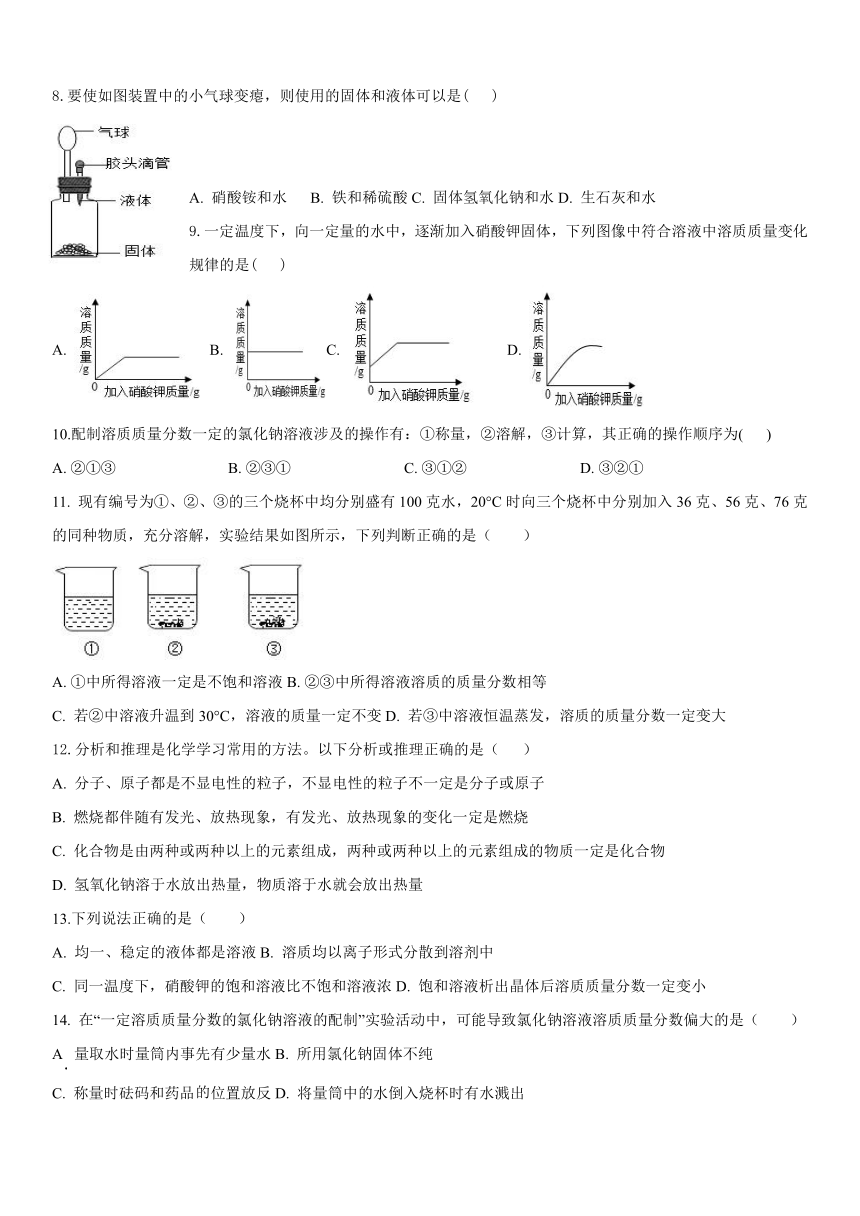
8.要使如图装置中的小气球变瘪,则使用的固体和液体可以是( )
A. 硝酸铵和水 B. 铁和稀硫酸C. 固体氢氧化钠和水D. 生石灰和水
9.一定温度下,向一定量的水中,逐渐加入硝酸钾固体,下列图像中符合溶液中溶质质量变化规律的是( )
A. B. C. D.
10.配制溶质质量分数一定的氯化钠溶液涉及的操作有:①称量,②溶解,③计算,其正确的操作顺序为( )
A. ②①③ B. ②③① C. ③①② D. ③②①
11. 现有编号为①、②、③的三个烧杯中均分别盛有100克水,20°C时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示,下列判断正确的是( )
A. ①中所得溶液一定是不饱和溶液B. ②③中所得溶液溶质的质量分数相等
C. 若②中溶液升温到30°C,溶液的质量一定不变D. 若③中溶液恒温蒸发,溶质的质量分数一定变大
12.分析和推理是化学学习常用的方法。以下分析或推理正确的是( )
A. 分子、原子都是不显电性的粒子,不显电性的粒子不一定是分子或原子
B. 燃烧都伴随有发光、放热现象,有发光、放热现象的变化一定是燃烧
C. 化合物是由两种或两种以上的元素组成,两种或两种以上的元素组成的物质一定是化合物
D. 氢氧化钠溶于水放出热量,物质溶于水就会放出热量
13.下列说法正确的是( )
A. 均一、稳定的液体都是溶液B. 溶质均以离子形式分散到溶剂中
C. 同一温度下,硝酸钾的饱和溶液比不饱和溶液浓D. 饱和溶液析出晶体后溶质质量分数一定变小
14. 在“一定溶质质量分数的氯化钠溶液的配制”实验活动中,可能导致氯化钠溶液溶质质量分数偏大的是( )
A 量取水时量筒内事先有少量水B. 所用氯化钠固体不纯
C. 称量时砝码和药品位置放反D. 将量筒中的水倒入烧杯时有水溅出
15. 实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是( )
①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A. ①② B. ①③ C. ②④ D. ③④
二.填空题
16.如图所示,一物体悬挂在饱和氯化钠溶液中,在恒温条件下向烧杯内溶液中分别加入下列物质(悬挂物不参与反应)。说明弹簧测力计读数变化情况(填“变大”“不变”或“变小”)。
(1)如果加入氯化钠晶体,弹簧测力计读数 。 (2)如果加入蒸馏水,弹簧测力计读数 。
(3)如果加入KNO3晶体,弹簧测力计读数 。
17.A、B、C、D四个烧杯分别盛有质量相等的同种溶剂,在相同的温度下,向4个烧杯中加入20g、15g、10g、5g的某溶质,充分溶解后,如图所示。回答下列各问题(填序号)。
(1)_______中盛的一定是不饱和溶液;
(2)若固体溶质为硝酸钾,四个烧杯中溶液的溶质质量分数最小的是_______。想让溶液变饱和可采用加入同种溶质的方法,除此外还可采用_______方法(填一种即可);
(3)在一定温度下,在A、B中分别加入相同质量的水,B中固体刚好溶解,所得溶液溶质质量分数A___B(填>、=、<)。
18.20℃时,向50g水中加入31.6gKNO3固体并进行如下系列操作,请回答相关问题:
(1)图中烧杯A、C中的溶液一定是饱和溶液,理由是_______。
(2)若烧杯B中的溶液恰好饱和,则烧杯C中剩余固体的质量_______20g(>,<,=)。
(3)操作a可采用的方法是_______(答一条即可)
(4)向B中恰好饱和的硝酸钾溶液中加入少量高锰酸钾固体,充分搅拌后发现溶液变为紫红色,由此可以得出的结论有。
A. 一定温度下硝酸钾的饱和溶液还能继续溶解其它物质B. 溶液不一定都是无色的
C. 相同条件下,高锰酸钾的溶解能力比硝酸钾的溶解能力强D. 一种溶液中可以有多种溶质
三、实验探究题
19.现配制50g溶质质量分数为15%的氯化钠溶液。
(1)配制50g溶质质量分数为15%的氯化钠溶液所需氯化钠的质量为______g;
(2)操作步骤如图所示:
①上述操作步骤的正确顺序是______(填字母序号);
②B操作过程中若天平指针向左偏转,则应______,直至指针指向分度盘中间;
(3)下列错误操作可能导致溶质质量分数小于15%的是______(填序号)。
①所称取的氯化钠固体不纯②向烧杯中倒水溶解时部分水酒出③装瓶时部分溶液洒出④量取水时仰视读数
四、计算题
20. (一)现有90g10%的Na2SO4溶液,经过下列操作后,计算所得溶液的质量分数。
(1)加入110g水:______;
(2)加入10g Na2SO4,完全溶解______;
(3)加入10g20%的Na2SO4溶液后所得溶液的溶质质量分数是多少?(写出计算步骤)
(二)将6克硝酸钾完全溶于54克水中,并将形成的溶液平均分成三份,计算:
(1)根据溶液的均一性,任取其中一份,其溶质的质量分数是__________;
(2)另取一份,使其溶质质量分数增大一倍,需加入硝酸钾__________克;再取一份,欲使其溶质质量分数减小一半,需加水__________克;
(3)现有溶质质量分数为10%的硝酸钾溶液200g,若配制成溶质质量分数为2%的硝酸钾溶液,需要加水的质量是多少?(写出计算过程)
一.选择题
1.将厨房中的下列物质分别加入适量水中、充分搅拌。能形成溶液的是( )
A. 豆油 B. 奶粉 C. 食盐 D. 花生酱
2.名称中有“水”字的物质可能是溶液,下列有“水”字的物质不属于溶液的是( )
A. 矿泉水B. 食盐水C. 冰水D. 澄清的石灰水
3.“恒大冰泉”是来自长白山的天然矿泉水,判断“恒大冰泉”属于溶液的依据是( )
①无色 ②混合物 ③化合物 ④均一性 ⑤稳定性.
A. ①②④ B. ②④⑤ C. ①③⑤ D. ③④⑤
4.医生常用生理盐水(溶质质量分数为0.9%)给患者输液。下列对生理盐水的理解不正确的是( )
A. 生理盐水中氯化钠是溶质,水是溶剂B. 输液时,输液管中和输液瓶中生理盐水的溶质质量分数相同
C. 每输入100g生理盐水,进入患者体内的氯化钠质量为0.9gD.生理盐水中氯化钠与水的质量比为9:1000
5.如图所示,U型管内a、b两液面高度相同。现将胶头滴管内的少量水挤入锥形瓶内,一会儿后观察到U型管内a液面上升,b液面下降。已知固体X是氢氧化钠、硝酸铵、氯化钠、蔗糖四种固体物质中的一种,则X是( )
A. 氢氧化钠固体
B. 硝酸铵固体
C. 氯化钠固体
D. 蔗糖固体
6.下列有关溶液的相关说法中正确的是( )
A. 物质的溶解过程通常会伴随着能量变化B. 溶液具有均一、稳定、透明的特征
C. 任何溶液都只含有一种溶质D. 不饱和溶液变饱和溶液,溶质质量分数一定变大
7.许多科学知识在逻辑上存在如图所示关系。其中并列关系是由于分类依据的相同而把事物截然分开并列,而交叉关系是对事物分类时,由于采用不同的分类依据,则必然出现交叉关系,下列关于溶液说法正确的是( )
A饱和溶液包含浓溶液 B. 饱和溶液与稀溶液属于并列关系
C. 饱和溶液与不饱和溶液属于交叉关系 D. 不饱和溶液与稀溶液属于交叉关系
8.要使如图装置中的小气球变瘪,则使用的固体和液体可以是( )
A. 硝酸铵和水 B. 铁和稀硫酸C. 固体氢氧化钠和水D. 生石灰和水
9.一定温度下,向一定量的水中,逐渐加入硝酸钾固体,下列图像中符合溶液中溶质质量变化规律的是( )
A. B. C. D.
10.配制溶质质量分数一定的氯化钠溶液涉及的操作有:①称量,②溶解,③计算,其正确的操作顺序为( )
A. ②①③ B. ②③① C. ③①② D. ③②①
11. 现有编号为①、②、③的三个烧杯中均分别盛有100克水,20°C时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示,下列判断正确的是( )
A. ①中所得溶液一定是不饱和溶液B. ②③中所得溶液溶质的质量分数相等
C. 若②中溶液升温到30°C,溶液的质量一定不变D. 若③中溶液恒温蒸发,溶质的质量分数一定变大
12.分析和推理是化学学习常用的方法。以下分析或推理正确的是( )
A. 分子、原子都是不显电性的粒子,不显电性的粒子不一定是分子或原子
B. 燃烧都伴随有发光、放热现象,有发光、放热现象的变化一定是燃烧
C. 化合物是由两种或两种以上的元素组成,两种或两种以上的元素组成的物质一定是化合物
D. 氢氧化钠溶于水放出热量,物质溶于水就会放出热量
13.下列说法正确的是( )
A. 均一、稳定的液体都是溶液B. 溶质均以离子形式分散到溶剂中
C. 同一温度下,硝酸钾的饱和溶液比不饱和溶液浓D. 饱和溶液析出晶体后溶质质量分数一定变小
14. 在“一定溶质质量分数的氯化钠溶液的配制”实验活动中,可能导致氯化钠溶液溶质质量分数偏大的是( )
A 量取水时量筒内事先有少量水B. 所用氯化钠固体不纯
C. 称量时砝码和药品位置放反D. 将量筒中的水倒入烧杯时有水溅出
15. 实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏小的是( )
①称量的氯化钠固体中含有不溶性杂质; ②用量筒量取水时仰视读数;
③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。
A. ①② B. ①③ C. ②④ D. ③④
二.填空题
16.如图所示,一物体悬挂在饱和氯化钠溶液中,在恒温条件下向烧杯内溶液中分别加入下列物质(悬挂物不参与反应)。说明弹簧测力计读数变化情况(填“变大”“不变”或“变小”)。
(1)如果加入氯化钠晶体,弹簧测力计读数 。 (2)如果加入蒸馏水,弹簧测力计读数 。
(3)如果加入KNO3晶体,弹簧测力计读数 。
17.A、B、C、D四个烧杯分别盛有质量相等的同种溶剂,在相同的温度下,向4个烧杯中加入20g、15g、10g、5g的某溶质,充分溶解后,如图所示。回答下列各问题(填序号)。
(1)_______中盛的一定是不饱和溶液;
(2)若固体溶质为硝酸钾,四个烧杯中溶液的溶质质量分数最小的是_______。想让溶液变饱和可采用加入同种溶质的方法,除此外还可采用_______方法(填一种即可);
(3)在一定温度下,在A、B中分别加入相同质量的水,B中固体刚好溶解,所得溶液溶质质量分数A___B(填>、=、<)。
18.20℃时,向50g水中加入31.6gKNO3固体并进行如下系列操作,请回答相关问题:
(1)图中烧杯A、C中的溶液一定是饱和溶液,理由是_______。
(2)若烧杯B中的溶液恰好饱和,则烧杯C中剩余固体的质量_______20g(>,<,=)。
(3)操作a可采用的方法是_______(答一条即可)
(4)向B中恰好饱和的硝酸钾溶液中加入少量高锰酸钾固体,充分搅拌后发现溶液变为紫红色,由此可以得出的结论有。
A. 一定温度下硝酸钾的饱和溶液还能继续溶解其它物质B. 溶液不一定都是无色的
C. 相同条件下,高锰酸钾的溶解能力比硝酸钾的溶解能力强D. 一种溶液中可以有多种溶质
三、实验探究题
19.现配制50g溶质质量分数为15%的氯化钠溶液。
(1)配制50g溶质质量分数为15%的氯化钠溶液所需氯化钠的质量为______g;
(2)操作步骤如图所示:
①上述操作步骤的正确顺序是______(填字母序号);
②B操作过程中若天平指针向左偏转,则应______,直至指针指向分度盘中间;
(3)下列错误操作可能导致溶质质量分数小于15%的是______(填序号)。
①所称取的氯化钠固体不纯②向烧杯中倒水溶解时部分水酒出③装瓶时部分溶液洒出④量取水时仰视读数
四、计算题
20. (一)现有90g10%的Na2SO4溶液,经过下列操作后,计算所得溶液的质量分数。
(1)加入110g水:______;
(2)加入10g Na2SO4,完全溶解______;
(3)加入10g20%的Na2SO4溶液后所得溶液的溶质质量分数是多少?(写出计算步骤)
(二)将6克硝酸钾完全溶于54克水中,并将形成的溶液平均分成三份,计算:
(1)根据溶液的均一性,任取其中一份,其溶质的质量分数是__________;
(2)另取一份,使其溶质质量分数增大一倍,需加入硝酸钾__________克;再取一份,欲使其溶质质量分数减小一半,需加水__________克;
(3)现有溶质质量分数为10%的硝酸钾溶液200g,若配制成溶质质量分数为2%的硝酸钾溶液,需要加水的质量是多少?(写出计算过程)
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
