【轻松备课】沪教版(全国)化学九年级上 第3章 第2节 组成物质的化学元素 第1课时 教学课件
文档属性
| 名称 | 【轻松备课】沪教版(全国)化学九年级上 第3章 第2节 组成物质的化学元素 第1课时 教学课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.8MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
第3章 物质构成的奥秘
第2节 组成物质的化学元素
第3章 物质构成的奥秘
第 1 课 时
学 习 目 标
1.知道元素的定义及其简单分类。
2.记住并能书写常见元素的名称和符号。
3.能根据元素的原子序数在元素周期表中找到指定的元素。
4.培养学生利用课外时间查阅资料,培养学生收集信息、处理信息的能力。
这里的钙、镁、钾、钠指的是元素。
这里的钙、镁、钾、钠指的是什么呢?
一、元素与元素符号
自 主 探 究
1.元素
(1)物质由元素组成
①物质是由元素组成的,如水是由氢元素和氧元素组成的,氧气是由氧元素组成的,氧气和水中都含有氧元素。
②我们生产、生活中使用的农药、化肥、日用品、食品、医药等物质都是由元素组成的。我们生命活动所必需的元素,如钙、碘、氟、铁等对人体健康有显著影响。
(2)元素的定义
元素是具有相同核电荷数(即质子数)的同一类原子的总称。
规律总结
这里所说的同一类原子包括:质子数相同、中子数不同的原子,如质子数为17、中子数为18的氯原子和质子数为17、中子数为20的氯原子,质子数为17的Cl-。上述原子或离子的核电荷数(即质子数)都是17,所以它们都是氯元素,属于氯元素的不同原子或离子。
(3)元素与原子的比较
元素 原子
概念 具有相同核电荷数(即质子数)的同一类原子的总称。一种元素可包含几种原子,如氢元素包含 11H、21H、31H(元素符号左上角的数字是近似相对原子质量,左下角的数字是核电荷数) 化学变化中的最小粒子。同种元素的原子,质子数相同;不同种元素的原子,质子数不同
区别 宏观概念,只讲种类,不讲个数 微观概念,既讲种类,又讲个数
使用范围 描述物质宏观组成,如水是由氢元素和氧元素组成的 描述物质的微观构成,如铁是由铁原子构成的
联系 核电荷数相同的一类原子属于同一种元素。原子是元素的最小单位,元素则是原子的一个归类集体,即元素和原子是总体和个体的关系
教师点拨
①不同的物质可能含有相同的元素[如氧气(O2)和臭氧(O3)均是由氧元素组成的,水(H2O)和双氧水(H2O2)均含有氢、氧两种元素]。
②不同的物质也可能含有不同的元素[如高锰酸钾(KMnO4)含有钾、锰、氧三种元素,而二氧化碳(CO2)含有碳、氧两种元素]。
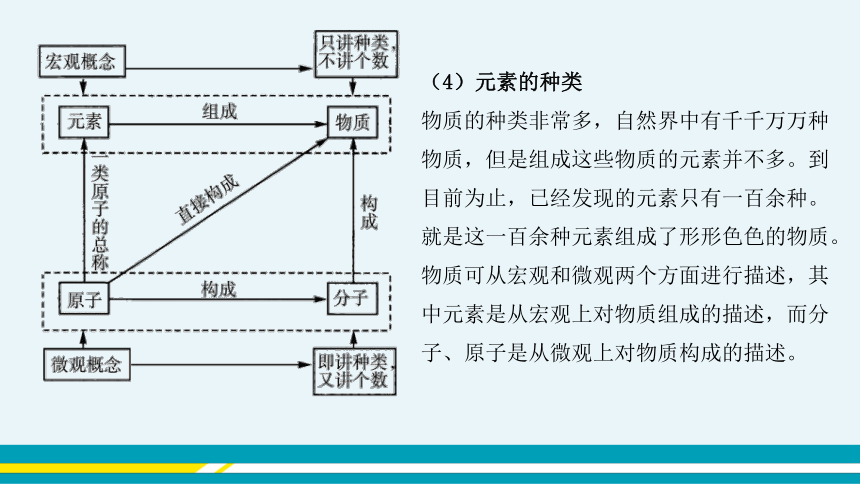
(4)元素的种类
物质的种类非常多,自然界中有千千万万种物质,但是组成这些物质的元素并不多。到目前为止,已经发现的元素只有一百余种。就是这一百余种元素组成了形形色色的物质。
物质可从宏观和微观两个方面进行描述,其中元素是从宏观上对物质组成的描述,而分子、原子是从微观上对物质构成的描述。
2.物质的组成与构成
(1)元素是宏观概念,只有种类之分,没有数量之别。在讨论物质的组成时,一般用“某物质由什么元素组成”来描述,其中只涉及类别而没有数量多少的含义;而分子、原子、离子等是微观概念,既有种类之分,又有数量之别,当讨论物质的微观构成时,一般用“某物质由什么分子(或原子、离子)构成”“每个某分子是由多少个某原子构成的”。一般“元素与组成”匹配,而“分子(或原子、离子)与构成”匹配。
(2)注意物质的描述过程中“宏观与宏观”“微观与微观”对应。
1个水分子由2个氢原子和1个氧原子构成。
水由氢元素和氧元素组成。
宏观
宏观
宏观
如:
微观
微观
微观
个数
个数
个数
世界上现在已经发现了一百多种元素,为了方便的表示它们,世界各国的化学工作者制定了国际统一的符号来表示不同的元素。这种符号就叫做化学元素符号。
3.元素符号
(1)元素符号的规定
国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,如果几种元素拉丁文名称的第一个字母相同时,就附加一个小写字母来区别,如N表示氮元素,Na表示钠元素。
(2)元素符号的写法
①由一个字母表示的元素符号要大写,如H、C、K、S等。
②由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如Na、Mg、Cu等。书写这类元素符号时,特别注意辨清第一个字母相同的一些类似的元素符号,如Cu、Ca、Cl等。
第一个字母大写,第二个字母小写可简记为“一大二小”。
③常见元素符号规范写法如下:
(3)元素符号的含义
①意义
宏观:表示一种元素
微观:表示这种元素的一个原子
②对于由原子直接构成的单质,元素符号还表示一种物质。例如,Fe的含义:表示铁元素、一个铁原子、铁这种物质。
③元素符号前面加数字时,表示原子个数,如2N表示两个氮原子,而不表示氮元素。
4.元素的分类
分类 分类标准
金属 元素 汉字名称中有“钅”字旁(金、汞除外),如铁、铜等
非金属元素 汉字名称中不带“钅”字旁的元素,如氧、溴、碘等元素。
元素可分为金属元素和非金属元素。分类标准如下。
元素的分类由原子的最外层电子数决定。
注意:汞、金元素的汉字名称中无“钅”字旁,但它们不是非金属元素,而是金属元素
俄国科学家门捷列夫在总结前人工作的基础上,对元素及其性质进行了系统研究,根据元素的相对原子质量大小将当时发现的所有元素依次排列成一个表格,这就是现代元素周期表的雏形。
5.元素周期表
(1)概念
根据元素的原子结构和性质,将已知的100多种元素按原子序数(数值上等于核电荷数)科学有序地排列起来所得的表,叫元素周期表。
(2)元素周期表的结构
①横行(周期):元素周期表每一横行代表一个周期,共有7个横行,即7个周期。
②纵列(族):元素周期表共有18个纵列,每1个纵列叫做一个族,第8、9、10三个纵列共同组成一个族,所以有16个族。
③每一格:在元素周期表中,每一种元素均占据一格,即元素在周期表中的位置,每一格的信息包括元素的原子序数、元素符号、元素名称、相对原子质量等内容。
规律总结
元素周期表中的相等规律
①电子层数=周期数。
②最外层电子数=族序数(Ⅷ、0族除外)。
③原子序数=核电荷数=质子数=核外电子数。
(3)元素周期表的意义
①为寻找新元素提供了理论依据。
②由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。
下面是核电荷数1~18的元素原子结构示意图。根据表格,你能找到哪些规律?
(4)元素周期表的编排规律
①每一周期从左至右原子序数(或核电荷数或质子数)依次增加,最外层电子数依次增加,电子层数相同。
②同一族从上到下电子层数依次增加,最外层电子数相同(He除外)。
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
课 堂 达 标
1. 元素观是化学的重要观念之一。下列有关元素的说法错误的是( )
A.物质都是由元素组成的
B.同种元素的原子核内中子数相同
C.在化学变化中元素的种类不发生改变
D.决定元素种类的是质子数
B
2.下列说法正确的是( )
A.二氧化硫(SO2)由一个硫原子和两个氧原子构成
B.二氧化硫由硫和氧气组成
C.二氧化硫由一个硫元素和两个氧元素组成
D.二氧化硫由硫元素和氧元素组成
3.下列符号既能表示某种元素,又能表示该元素的一个原子,还能表示一种物质的是( )
A. SO2 B. H2 C. O D. Cu
D
D
4. 下列元素中,属于金属元素的是( )
A.氖 B.氧 C.锌 D.磷
C
5.我国著名化学家徐光宪因在稀土元素等研究领域做出杰出贡献,荣获“国家最高科学技术奖”。铈(Ce)是一种常见的稀土元素,如图 所示,下列关于铈的说法错误的是( )
A.原子序数是58
B.相对原子质量是140.1
C.质子数为58
D.铈元素是非金属元素
D
6.下表为元素周期表的一部分,A~E代表五种不同的元素。下列说法不正确的是( )
B
A.原子序数:C>B
B.核内质子数:A=E
C. B、C同周期
D. A、D同主族
谢 谢 观 看
第3章 物质构成的奥秘
第2节 组成物质的化学元素
第3章 物质构成的奥秘
第 1 课 时
学 习 目 标
1.知道元素的定义及其简单分类。
2.记住并能书写常见元素的名称和符号。
3.能根据元素的原子序数在元素周期表中找到指定的元素。
4.培养学生利用课外时间查阅资料,培养学生收集信息、处理信息的能力。
这里的钙、镁、钾、钠指的是元素。
这里的钙、镁、钾、钠指的是什么呢?
一、元素与元素符号
自 主 探 究
1.元素
(1)物质由元素组成
①物质是由元素组成的,如水是由氢元素和氧元素组成的,氧气是由氧元素组成的,氧气和水中都含有氧元素。
②我们生产、生活中使用的农药、化肥、日用品、食品、医药等物质都是由元素组成的。我们生命活动所必需的元素,如钙、碘、氟、铁等对人体健康有显著影响。
(2)元素的定义
元素是具有相同核电荷数(即质子数)的同一类原子的总称。
规律总结
这里所说的同一类原子包括:质子数相同、中子数不同的原子,如质子数为17、中子数为18的氯原子和质子数为17、中子数为20的氯原子,质子数为17的Cl-。上述原子或离子的核电荷数(即质子数)都是17,所以它们都是氯元素,属于氯元素的不同原子或离子。
(3)元素与原子的比较
元素 原子
概念 具有相同核电荷数(即质子数)的同一类原子的总称。一种元素可包含几种原子,如氢元素包含 11H、21H、31H(元素符号左上角的数字是近似相对原子质量,左下角的数字是核电荷数) 化学变化中的最小粒子。同种元素的原子,质子数相同;不同种元素的原子,质子数不同
区别 宏观概念,只讲种类,不讲个数 微观概念,既讲种类,又讲个数
使用范围 描述物质宏观组成,如水是由氢元素和氧元素组成的 描述物质的微观构成,如铁是由铁原子构成的
联系 核电荷数相同的一类原子属于同一种元素。原子是元素的最小单位,元素则是原子的一个归类集体,即元素和原子是总体和个体的关系
教师点拨
①不同的物质可能含有相同的元素[如氧气(O2)和臭氧(O3)均是由氧元素组成的,水(H2O)和双氧水(H2O2)均含有氢、氧两种元素]。
②不同的物质也可能含有不同的元素[如高锰酸钾(KMnO4)含有钾、锰、氧三种元素,而二氧化碳(CO2)含有碳、氧两种元素]。
(4)元素的种类
物质的种类非常多,自然界中有千千万万种物质,但是组成这些物质的元素并不多。到目前为止,已经发现的元素只有一百余种。就是这一百余种元素组成了形形色色的物质。
物质可从宏观和微观两个方面进行描述,其中元素是从宏观上对物质组成的描述,而分子、原子是从微观上对物质构成的描述。
2.物质的组成与构成
(1)元素是宏观概念,只有种类之分,没有数量之别。在讨论物质的组成时,一般用“某物质由什么元素组成”来描述,其中只涉及类别而没有数量多少的含义;而分子、原子、离子等是微观概念,既有种类之分,又有数量之别,当讨论物质的微观构成时,一般用“某物质由什么分子(或原子、离子)构成”“每个某分子是由多少个某原子构成的”。一般“元素与组成”匹配,而“分子(或原子、离子)与构成”匹配。
(2)注意物质的描述过程中“宏观与宏观”“微观与微观”对应。
1个水分子由2个氢原子和1个氧原子构成。
水由氢元素和氧元素组成。
宏观
宏观
宏观
如:
微观
微观
微观
个数
个数
个数
世界上现在已经发现了一百多种元素,为了方便的表示它们,世界各国的化学工作者制定了国际统一的符号来表示不同的元素。这种符号就叫做化学元素符号。
3.元素符号
(1)元素符号的规定
国际上统一采用元素拉丁文名称的第一个字母(大写)来表示元素,如果几种元素拉丁文名称的第一个字母相同时,就附加一个小写字母来区别,如N表示氮元素,Na表示钠元素。
(2)元素符号的写法
①由一个字母表示的元素符号要大写,如H、C、K、S等。
②由两个字母表示的元素符号,第一个字母大写,第二个字母小写,如Na、Mg、Cu等。书写这类元素符号时,特别注意辨清第一个字母相同的一些类似的元素符号,如Cu、Ca、Cl等。
第一个字母大写,第二个字母小写可简记为“一大二小”。
③常见元素符号规范写法如下:
(3)元素符号的含义
①意义
宏观:表示一种元素
微观:表示这种元素的一个原子
②对于由原子直接构成的单质,元素符号还表示一种物质。例如,Fe的含义:表示铁元素、一个铁原子、铁这种物质。
③元素符号前面加数字时,表示原子个数,如2N表示两个氮原子,而不表示氮元素。
4.元素的分类
分类 分类标准
金属 元素 汉字名称中有“钅”字旁(金、汞除外),如铁、铜等
非金属元素 汉字名称中不带“钅”字旁的元素,如氧、溴、碘等元素。
元素可分为金属元素和非金属元素。分类标准如下。
元素的分类由原子的最外层电子数决定。
注意:汞、金元素的汉字名称中无“钅”字旁,但它们不是非金属元素,而是金属元素
俄国科学家门捷列夫在总结前人工作的基础上,对元素及其性质进行了系统研究,根据元素的相对原子质量大小将当时发现的所有元素依次排列成一个表格,这就是现代元素周期表的雏形。
5.元素周期表
(1)概念
根据元素的原子结构和性质,将已知的100多种元素按原子序数(数值上等于核电荷数)科学有序地排列起来所得的表,叫元素周期表。
(2)元素周期表的结构
①横行(周期):元素周期表每一横行代表一个周期,共有7个横行,即7个周期。
②纵列(族):元素周期表共有18个纵列,每1个纵列叫做一个族,第8、9、10三个纵列共同组成一个族,所以有16个族。
③每一格:在元素周期表中,每一种元素均占据一格,即元素在周期表中的位置,每一格的信息包括元素的原子序数、元素符号、元素名称、相对原子质量等内容。
规律总结
元素周期表中的相等规律
①电子层数=周期数。
②最外层电子数=族序数(Ⅷ、0族除外)。
③原子序数=核电荷数=质子数=核外电子数。
(3)元素周期表的意义
①为寻找新元素提供了理论依据。
②由于元素周期表中位置越靠近的元素性质越相似,启发人们在元素周期表的一定区域内寻找新物质(如半导体材料、农药、催化剂等)。
下面是核电荷数1~18的元素原子结构示意图。根据表格,你能找到哪些规律?
(4)元素周期表的编排规律
①每一周期从左至右原子序数(或核电荷数或质子数)依次增加,最外层电子数依次增加,电子层数相同。
②同一族从上到下电子层数依次增加,最外层电子数相同(He除外)。
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
课 堂 达 标
1. 元素观是化学的重要观念之一。下列有关元素的说法错误的是( )
A.物质都是由元素组成的
B.同种元素的原子核内中子数相同
C.在化学变化中元素的种类不发生改变
D.决定元素种类的是质子数
B
2.下列说法正确的是( )
A.二氧化硫(SO2)由一个硫原子和两个氧原子构成
B.二氧化硫由硫和氧气组成
C.二氧化硫由一个硫元素和两个氧元素组成
D.二氧化硫由硫元素和氧元素组成
3.下列符号既能表示某种元素,又能表示该元素的一个原子,还能表示一种物质的是( )
A. SO2 B. H2 C. O D. Cu
D
D
4. 下列元素中,属于金属元素的是( )
A.氖 B.氧 C.锌 D.磷
C
5.我国著名化学家徐光宪因在稀土元素等研究领域做出杰出贡献,荣获“国家最高科学技术奖”。铈(Ce)是一种常见的稀土元素,如图 所示,下列关于铈的说法错误的是( )
A.原子序数是58
B.相对原子质量是140.1
C.质子数为58
D.铈元素是非金属元素
D
6.下表为元素周期表的一部分,A~E代表五种不同的元素。下列说法不正确的是( )
B
A.原子序数:C>B
B.核内质子数:A=E
C. B、C同周期
D. A、D同主族
谢 谢 观 看
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
