【轻松备课】沪教版(全国)化学九年级上 第5章 第1节 金属的性质和利用 第1课时 教学课件
文档属性
| 名称 | 【轻松备课】沪教版(全国)化学九年级上 第5章 第1节 金属的性质和利用 第1课时 教学课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
第5章 金属的冶炼与利用
第1节 金属的性质和利用
第5章 金属的冶炼与利用
第 1 课 时
1.了解金属的物理性质及其应用。
2.认识常见的金属与氧气、酸、某些金属化合物溶液的反应。
3.初步认识置换反应的概念,能够判断常见的化学反应是否属于置换反应。
4.认识金属材料在生产、生活和社会发展中的重要作用。
学 习 目 标
金属是一类重要的材料,人类的生活和生产都离不开金属。了解金属的性质,对科学地利用金属材料是十分重要的。你对金属有哪些了解呢?
自 主 探 究
一、金属的性质
暖气片
镁铝合金
金项链
铜导线
门锁
汞
说一说:
你知道哪些
金属?它们
在生产生活
中的用途分
别体现了哪
些物理性质呢?
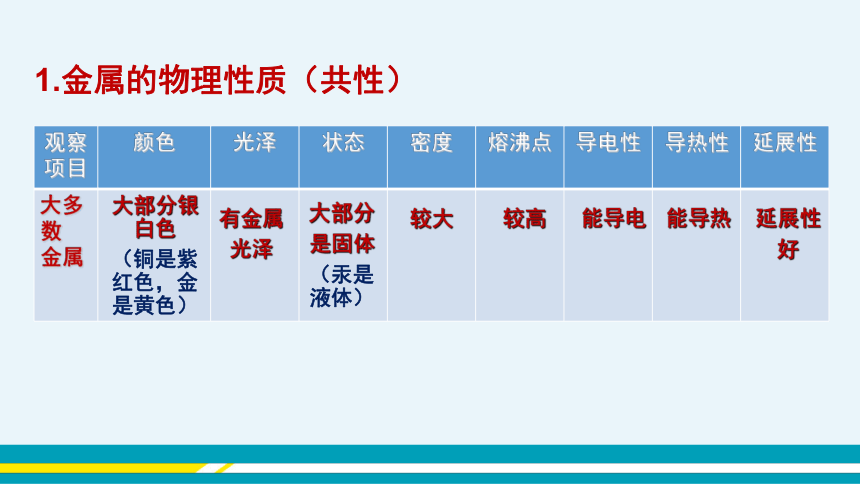
1.金属的物理性质(共性)
观察 项目 颜色 光泽 状态 密度 熔沸点 导电性 导热性 延展性
大多数 金属
有金属
光泽
大部分银白色
(铜是紫红色,金是黄色)
大部分
是固体
(汞是液体)
较大
较高
能导电
能导热
延展性
好
铁粉
铝粉:
俗称“银粉”
银白色
不同的金属也有本身的特性
不同的金属导电性、导热性、密度、熔点、硬度等物理性质,差别也较大。
(1)为什么铁制锅铲需要加上木柄或塑料柄?
(2)银的导电性比铜好,一般情况下为什么不用银制造电线电缆?
(3)选择铸造硬币的金属材料需要考虑哪些因素?
请同学们结合生活实际讨论下列问题
铁易导热,加上导热性弱的木柄等以防烫手
银的价格比铜高许多
资源丰富
无毒轻便
耐磨耐腐蚀
美观、易加工
有一定的硬度……
联想与
启示
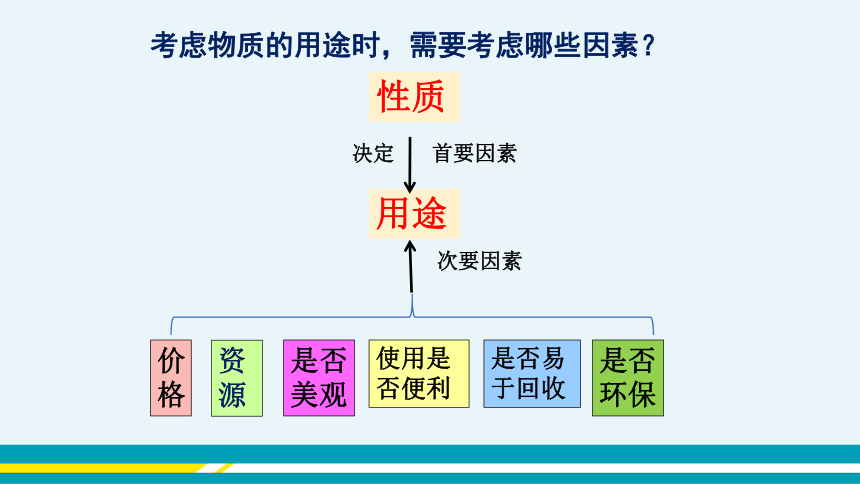
性质
用途
首要因素
决定
次要因素
是否易于回收
是否环保
使用是否便利
是否美观
资源
价格
考虑物质的用途时,需要考虑哪些因素?
同样是金属,差别怎么这样大呢?
2.常见金属的化学性质
回忆并描述镁在空气中燃烧,铁丝在氧气中燃烧
的现象,写出反应的化学方程式。
观察
与
思考
1.镁条在空气中燃烧;(略)
2.铁丝在氧气中点燃;(略)
3.铝片在空气中加热;
4.铜片在空气中加热。
观察完后,请将观察到的现象填入课本第115页《观察与思考》的表格中。
活动
与
探究
演示实验
镁在空气中点燃 铁在氧气中点燃 铝在空气中加热 铜在空气中加热
实验 现象
化学方程式
结论 剧烈燃烧,火星四射,放热,生成黑色固体
表面变暗,失去金属光泽
表面由红色变成黑色
剧烈燃烧,发出耀眼的白光,放热,生成白色固体
4Al+3O2==2Al2O3
Mg 、 Fe 、 Al、Cu能与氧气反应
3Fe+2O2 ==Fe3O4
点燃
2Mg+O2==2MgO
点燃
(1)金属与氧气反应—化合反应
2Cu+O2 2CuO
结论: ①许多金属都能与氧气反应,但反应的难易和剧烈程度是不同的,如镁、铝等在常温下就能与氧气反应。铝在空气中与氧气反应,在其表面生成一层致密的氧化铝(Al2O3)膜,从而阻止铝进一步被氧化,因此,铝具有很好的抗腐蚀性能。
②铜等在常温下几乎不与氧气反应,但在点燃或加热时能与氧气反应。
③金在高温条件下也不与氧气反应。
(2)金属与盐酸、稀硫酸的反应
分别把镁条、铁片和铜片(或铜丝)的表面用砂纸擦亮,放入稀盐酸(或稀硫酸)中,观察实验现象,比较反应的剧烈程度。若能反应,写出反应的化学方程式。
活动
与
探究
交流
与
讨论
金属 实验现象 化学方程式 稀盐酸 稀硫酸 稀盐酸 稀硫酸
镁 金属表面产生气泡非常快 金属表面产生气泡非常快 Mg+2HCl= MgCl2+H2↑ Mg+H2SO4=
MgSO4+H2 ↑
铁 产生气泡较慢,溶液由无色变为浅绿色 产生气泡较慢,溶液由无色变为浅绿色 Fe+2HCl= FeCl2+H2↑ Fe+H2SO4=
FeSO4+H2↑
铜 无现象 无现象 — —
结论:很多金属能与盐酸或稀硫酸反应,但是反应的剧烈程度不同。
应用:判断金属活动性的方法二,根据金属与盐酸或稀硫酸能否反应以及反应的剧烈程度判断金属活动性
活动性:镁>铁>铜
(3)铁钉与硫酸铜溶液的反应
在试管中加入少量硫酸铜溶液,把2-3枚无锈的新铁钉浸入硫酸铜溶液中,观察实验现象,写出反应的化学方程式。
活动
与
探究
交流
与
讨论
实验 实验现象 化学方程式
铁钉浸入硫酸铜溶液中 铁丝表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色
Fe+CuSO4=FeSO4+Cu
--《淮南万毕术》
曾青得铁则化为铜
古代湿法冶金的原理
(4)请大家从反应物和生成物的物质类别的角度分析,金属与盐酸、稀硫酸的反应有什么特点?
置换反应:一种单质和一种化合物反应,生成另一种单质和另一化合物的反应
观察
与
思考
(1)药品和反应原理: 锌粒和稀硫酸
Zn+H2SO4=ZnSO4 +H2
(2)发生装置和收集装置
(3)操作步骤:查、装、定、加、收
3.氢气的实验室制法
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
1.把一支洁净的铁钉放入稀硫酸中,下列说法错误的是( )
A.铁钉表面产生气泡 B.溶液由无色变成浅绿色
C.铁钉质量变轻 D.液体质量变轻
2.下列关于金属与氧气反应的观点中不正确的是( )
A.大多数金属都能与氧气反应
B.镁在点燃时能与空气中的氧气反应
C.“真金不怕火炼”说明金即使在高温下也不与氧气反应
D.铁在氧气中燃烧生成氧化铁
D
D
课 堂 达 标
3.下列各组物质,由金属跟同一种稀酸直接作用生成的是( )
A.ZnCl2 和ZnSO4 B. ZnSO4和 FeSO4
C.FeCl2 和 FeCl3 D. ZnSO4 和 CuSO4
4.生铁和足量的稀盐酸充分反应后,总会有一些残渣剩余,残渣的成分主要是( )
A.铁 B.氯化铁 C.氯化亚铁 D.碳
B
D
C
5.为了适应火车提速,我国铁路线上的短轨(25m)已经链接为长轨,一方面火车得到了提速,另一方面降低了火车经过时的噪音。铁路部门的技术工人用下列反应焊接原钢轨间的缝隙:
该反应的基本类型是( )
A.分解反应 B.化合反应 C.置换反应
2Al+Fe2O3 2Fe +Al2O3
高温
6.黄金是一种贵重金属,在人类漫长的历史中,素有“沙里淘金”“真金不怕火炼”之说。 这说明黄金在自然界中主要是以 (填“单质”或“化合物”)形式存在,也说明黄金的化学性质在自然条件下非常 。
7.铝的金属活动性比较强,但铝制品却比较耐用,请用化学方程式解释原因。
单质
稳定
谢 谢 观 看
第5章 金属的冶炼与利用
第1节 金属的性质和利用
第5章 金属的冶炼与利用
第 1 课 时
1.了解金属的物理性质及其应用。
2.认识常见的金属与氧气、酸、某些金属化合物溶液的反应。
3.初步认识置换反应的概念,能够判断常见的化学反应是否属于置换反应。
4.认识金属材料在生产、生活和社会发展中的重要作用。
学 习 目 标
金属是一类重要的材料,人类的生活和生产都离不开金属。了解金属的性质,对科学地利用金属材料是十分重要的。你对金属有哪些了解呢?
自 主 探 究
一、金属的性质
暖气片
镁铝合金
金项链
铜导线
门锁
汞
说一说:
你知道哪些
金属?它们
在生产生活
中的用途分
别体现了哪
些物理性质呢?
1.金属的物理性质(共性)
观察 项目 颜色 光泽 状态 密度 熔沸点 导电性 导热性 延展性
大多数 金属
有金属
光泽
大部分银白色
(铜是紫红色,金是黄色)
大部分
是固体
(汞是液体)
较大
较高
能导电
能导热
延展性
好
铁粉
铝粉:
俗称“银粉”
银白色
不同的金属也有本身的特性
不同的金属导电性、导热性、密度、熔点、硬度等物理性质,差别也较大。
(1)为什么铁制锅铲需要加上木柄或塑料柄?
(2)银的导电性比铜好,一般情况下为什么不用银制造电线电缆?
(3)选择铸造硬币的金属材料需要考虑哪些因素?
请同学们结合生活实际讨论下列问题
铁易导热,加上导热性弱的木柄等以防烫手
银的价格比铜高许多
资源丰富
无毒轻便
耐磨耐腐蚀
美观、易加工
有一定的硬度……
联想与
启示
性质
用途
首要因素
决定
次要因素
是否易于回收
是否环保
使用是否便利
是否美观
资源
价格
考虑物质的用途时,需要考虑哪些因素?
同样是金属,差别怎么这样大呢?
2.常见金属的化学性质
回忆并描述镁在空气中燃烧,铁丝在氧气中燃烧
的现象,写出反应的化学方程式。
观察
与
思考
1.镁条在空气中燃烧;(略)
2.铁丝在氧气中点燃;(略)
3.铝片在空气中加热;
4.铜片在空气中加热。
观察完后,请将观察到的现象填入课本第115页《观察与思考》的表格中。
活动
与
探究
演示实验
镁在空气中点燃 铁在氧气中点燃 铝在空气中加热 铜在空气中加热
实验 现象
化学方程式
结论 剧烈燃烧,火星四射,放热,生成黑色固体
表面变暗,失去金属光泽
表面由红色变成黑色
剧烈燃烧,发出耀眼的白光,放热,生成白色固体
4Al+3O2==2Al2O3
Mg 、 Fe 、 Al、Cu能与氧气反应
3Fe+2O2 ==Fe3O4
点燃
2Mg+O2==2MgO
点燃
(1)金属与氧气反应—化合反应
2Cu+O2 2CuO
结论: ①许多金属都能与氧气反应,但反应的难易和剧烈程度是不同的,如镁、铝等在常温下就能与氧气反应。铝在空气中与氧气反应,在其表面生成一层致密的氧化铝(Al2O3)膜,从而阻止铝进一步被氧化,因此,铝具有很好的抗腐蚀性能。
②铜等在常温下几乎不与氧气反应,但在点燃或加热时能与氧气反应。
③金在高温条件下也不与氧气反应。
(2)金属与盐酸、稀硫酸的反应
分别把镁条、铁片和铜片(或铜丝)的表面用砂纸擦亮,放入稀盐酸(或稀硫酸)中,观察实验现象,比较反应的剧烈程度。若能反应,写出反应的化学方程式。
活动
与
探究
交流
与
讨论
金属 实验现象 化学方程式 稀盐酸 稀硫酸 稀盐酸 稀硫酸
镁 金属表面产生气泡非常快 金属表面产生气泡非常快 Mg+2HCl= MgCl2+H2↑ Mg+H2SO4=
MgSO4+H2 ↑
铁 产生气泡较慢,溶液由无色变为浅绿色 产生气泡较慢,溶液由无色变为浅绿色 Fe+2HCl= FeCl2+H2↑ Fe+H2SO4=
FeSO4+H2↑
铜 无现象 无现象 — —
结论:很多金属能与盐酸或稀硫酸反应,但是反应的剧烈程度不同。
应用:判断金属活动性的方法二,根据金属与盐酸或稀硫酸能否反应以及反应的剧烈程度判断金属活动性
活动性:镁>铁>铜
(3)铁钉与硫酸铜溶液的反应
在试管中加入少量硫酸铜溶液,把2-3枚无锈的新铁钉浸入硫酸铜溶液中,观察实验现象,写出反应的化学方程式。
活动
与
探究
交流
与
讨论
实验 实验现象 化学方程式
铁钉浸入硫酸铜溶液中 铁丝表面覆盖一层红色物质,溶液由蓝色逐渐变为浅绿色
Fe+CuSO4=FeSO4+Cu
--《淮南万毕术》
曾青得铁则化为铜
古代湿法冶金的原理
(4)请大家从反应物和生成物的物质类别的角度分析,金属与盐酸、稀硫酸的反应有什么特点?
置换反应:一种单质和一种化合物反应,生成另一种单质和另一化合物的反应
观察
与
思考
(1)药品和反应原理: 锌粒和稀硫酸
Zn+H2SO4=ZnSO4 +H2
(2)发生装置和收集装置
(3)操作步骤:查、装、定、加、收
3.氢气的实验室制法
本节课你学会了哪些知识?
收获了什么方法?
还有什么疑惑吗?
1.把一支洁净的铁钉放入稀硫酸中,下列说法错误的是( )
A.铁钉表面产生气泡 B.溶液由无色变成浅绿色
C.铁钉质量变轻 D.液体质量变轻
2.下列关于金属与氧气反应的观点中不正确的是( )
A.大多数金属都能与氧气反应
B.镁在点燃时能与空气中的氧气反应
C.“真金不怕火炼”说明金即使在高温下也不与氧气反应
D.铁在氧气中燃烧生成氧化铁
D
D
课 堂 达 标
3.下列各组物质,由金属跟同一种稀酸直接作用生成的是( )
A.ZnCl2 和ZnSO4 B. ZnSO4和 FeSO4
C.FeCl2 和 FeCl3 D. ZnSO4 和 CuSO4
4.生铁和足量的稀盐酸充分反应后,总会有一些残渣剩余,残渣的成分主要是( )
A.铁 B.氯化铁 C.氯化亚铁 D.碳
B
D
C
5.为了适应火车提速,我国铁路线上的短轨(25m)已经链接为长轨,一方面火车得到了提速,另一方面降低了火车经过时的噪音。铁路部门的技术工人用下列反应焊接原钢轨间的缝隙:
该反应的基本类型是( )
A.分解反应 B.化合反应 C.置换反应
2Al+Fe2O3 2Fe +Al2O3
高温
6.黄金是一种贵重金属,在人类漫长的历史中,素有“沙里淘金”“真金不怕火炼”之说。 这说明黄金在自然界中主要是以 (填“单质”或“化合物”)形式存在,也说明黄金的化学性质在自然条件下非常 。
7.铝的金属活动性比较强,但铝制品却比较耐用,请用化学方程式解释原因。
单质
稳定
谢 谢 观 看
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
