2024年高三化学专题复习 大概念统领下的高中化学物质结构与性质单元复习——以水的共价键为辐射中心 课件(共22张PPT)
文档属性
| 名称 | 2024年高三化学专题复习 大概念统领下的高中化学物质结构与性质单元复习——以水的共价键为辐射中心 课件(共22张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览






文档简介
(共22张PPT)
大概念统领下的物质结构与性质单元复习
—以水中的共价键为辐射中心
【素养目标】
通过核心概念思维导图的构建,培养学生证据推理与模型认知、变化观念与平衡思想、科学探究与创新意识的化学学科核心素养。
【课程目标】
1. 以水中化学键为中心构建核心概念---共价键的思维导图;
2. 以共价晶体为中心构建核心概念---晶体的思维导图;
3. 通过思维导图的构建,使学生总体上对结构知识有宏观的大局把控,细节上对具
体知识有微观的区分与联系。
教学与评价目标
水,生命之源,你了解它吗 ?
(1)H2O是生命之源
(2)H2O是由2个H和1个O组成的3原子分子
(3)H2O键长0.94 A,键角104°45′
(4)H2O是极性分子
(5)H2O分子之间可以形成氢键
(6)H2O中的化学键是极性共价键
问题1:从视频中你获取到了哪些信息?
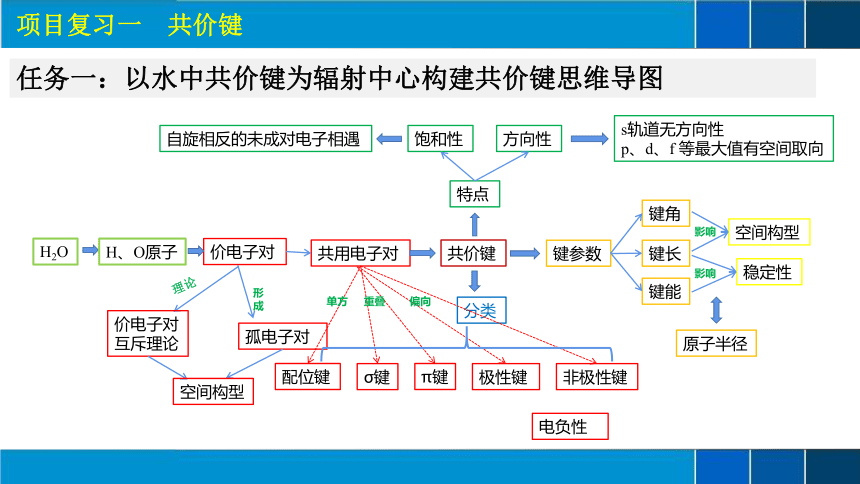
任务一:以水中共价键为辐射中心构建共价键思维导图
H2O
共价键
特点
方向性
饱和性
配位键
极性键
非极性键
σ键
π键
键长
键角
键能
键参数
空间构型
稳定性
分类
s轨道无方向性
p、d、f 等最大值有空间取向
共用电子对
孤电子对
价电子对
H、O原子
形
成
单方
重叠
偏向
影响
影响
原子半径
电负性
自旋相反的未成对电子相遇
项目复习一 共价键
价电子对互斥理论
理论
空间构型
年份省份 情境素材 核心考点
22山东 半导体、钠离子电池材料 晶体性质、共价键类型、杂化、配位数、晶胞结构
笼形包合物四方晶胞 电子排布式、配位数、杂化、成键轨道、分子性质、互斥理论
22全国甲 透光气囊材料 电子排布图、电离能、杂化轨道、晶胞结构、核间距
22全国乙 卤族元素 电子排布式、能量比较、杂化轨道、成键轨道、键长、键能、物质性质、晶胞体积
22北京 铁精粉 电子排布式、键角、作用力、核间距、晶体密度
22湖南 微量元素铁和硒 电子排布式、键角、共价键类型、电负性、杂化轨道、等电子体、配位数、晶体密度
22广东 微量元素硒、热电材料 电子排布式、氢键、孤对电子、立体构型、晶胞组成、核间距
22海南 半导体材料、酞菁 电子排布式、金属键、杂化、物质熔点、配位反应、离子键、晶胞结构
22河北 四元半导体化合物 自旋电子、电离能、几何构型、杂化、化合价、晶胞组成、原子坐标
21山东 、 、 分子极性、空间构型、熔沸点、杂化
非金属氟化物 电子运动状态、电负性、空间构型、熔沸点、杂化、晶胞组成、核间距、原子坐标
21全国甲 太阳能电池、合成甲醇 电子排布式、晶体类型、杂化、共价键类型、熔沸点、配位数、晶体密度、晶胞组成
21全国乙 过渡金属元素铬 电子排布式、电负性、配位键、杂化、沸点、键角、晶胞结构、空间占有率
21广东 汞的解毒剂 电子排布式、氢键、电负性、键角、杂化、键能、溶解性、晶胞组成、结构、密度
21河北 晶体 核外电子排布、自旋量子数、键能、杂化、等电子体、晶体密度、晶胞投影图
21海南 金属羰基配位化合物 电子排布式、配位数、电离能、杂化、熔沸点、原子坐标
21湖南 硅锗及其化合物 电子排布式、熔沸点、空间构型、杂化、电负性、共价键类型、晶胞组成、密度
20山东 碳硅及其化合物 键能、晶体性质、电负性、成键特点
新型热电材料 空间构型、晶体类型、熔沸点、键角、配位键、杂化、晶胞组成、原子坐标
20全国Ⅰ 锂离子电池及钴酸锂、磷酸铁锂等正极材料 未成对电子、电离能、空间构型、价层电子对、杂化轨道、晶胞组成
20全国Ⅱ 钙钛矿型化合物 电子排布式、熔沸点、电负性、配位数、晶胞结构、杂化轨道、晶体密度
20全国Ⅲ 氨硼烷 原子半径、成键特点、杂化轨道、电负性、等电子体、熔沸点、晶体密度
20海南 储氢物质 电子排布式、杂化轨道、键能、溶解性、配位数、晶胞结构
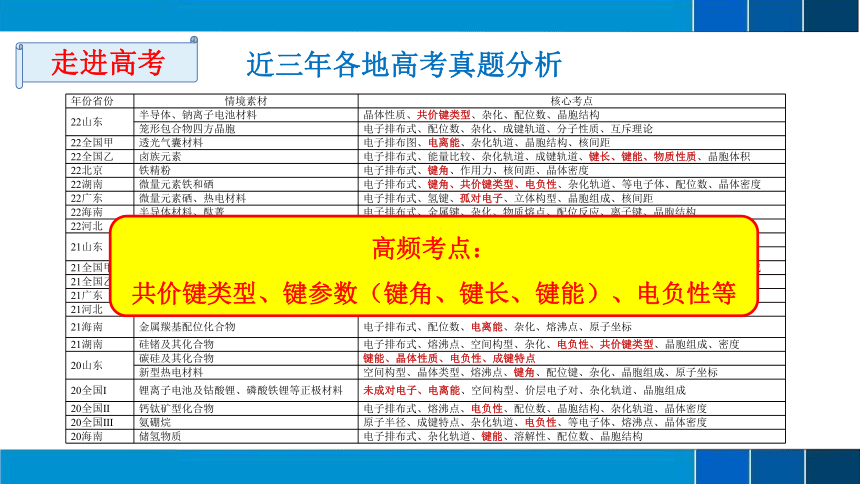
近三年各地高考真题分析
走进高考
高频考点:
共价键类型、键参数(键角、键长、键能)、电负性等
1. (2022.辽宁)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是( )
A.X能与多种元素形成共价键 B.简单氢化物沸点:Z<Q
C.第一电离能:Y>Z D.电负性:W<Z
走进高考1
B
2.(2022.北京)由键能数据大小,不能解释下列事实的是( )
化学键 C﹣H Si﹣H C=O C﹣O Si﹣O C﹣C Si﹣Si
键能/kJ mol﹣1 411 318 799 358 452 346 222
A.稳定性:CH4>SiH4 B.键长:C=O<C﹣O
C.熔点:CO2<SiO2 D.硬度:金刚石>晶体硅
C
S
O
C
N
Al
3. (2020.山东)NH3、PH3、AsH3的沸点由高到低的顺序为 ( 填化学式,下同),还原性由强到弱的顺序为 ,键角由大到小的顺序为 。
NH3、AsH3、PH3
AsH3、PH3、NH3
NH3、PH3、AsH3
对于分子晶体,若存在分子间氢键,熔沸点升高,若不存在分子间氢键,相对分子质量越大,分子间作用力越大,熔沸点越高。
原子得电子能力N>P>As,对应阴离子的失电子能力As3+>P3+>N3+,故氢化物的还原性AsH3>PH3>NH3 。
中心原子电负性越大,与H原子之间的共用电子对离中心原子越近,成键电子对之间斥力越大,键角越大。
走进高考
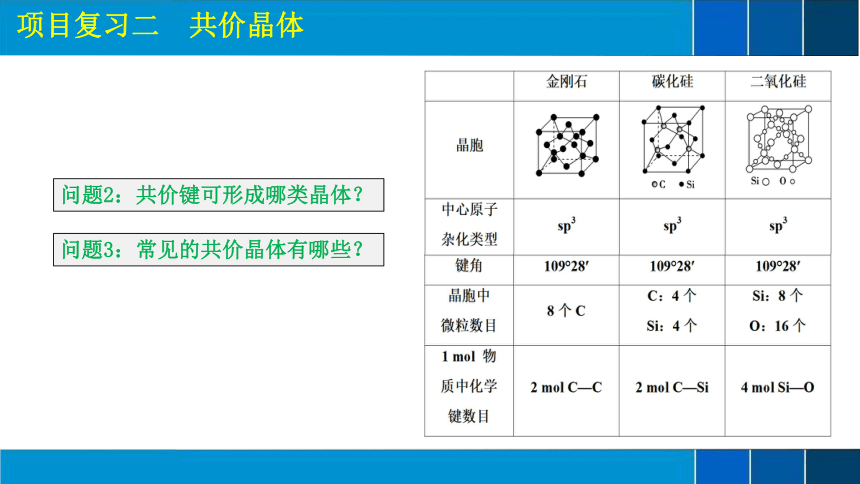
项目复习二 共价晶体
问题2:共价键可形成哪类晶体?
问题3:常见的共价晶体有哪些?
1.在金刚石晶体中每个碳原子周围紧邻的碳原子有多少个?
2.在金刚石晶体中每个碳原子连接有几个共价键?
3.碳原子的配位数是多少?
4.在金刚石晶体中碳原子个数与C-C共价键个数之比是多少?
5.1mol金刚石中含有的共价键数目是多少?
4
1 :2
金刚石晶胞
4
4
2 NA
再探金刚石
6. 1个碳原子形成几个六元环?
12
任意一个C原子,形成4根共价键,任取2根共价键,有C 4种组合,且2根共价键仅共存于2个六元环中:2× C 4=12
再探金刚石
7. 金刚石晶胞含有____个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=____a,密度=________(列出计算式,下同),表示碳原子在晶胞中的空间占有率____
8
再探金刚石
1
2
3
a
1
3
2
8r=
a
r=
8r
有关晶胞计算的思维流程
单位统一:确定晶胞参数时就转化好长度单位!
1nm=10-7cm=10 -9m 1pm=10-10cm=10-12m
知识
回顾
理解晶胞结构
确定晶胞组成
计算晶胞质量
确定晶胞体积
计算晶体密度
理解晶胞结构
确定晶胞组成
计算微粒体积
确定晶胞体积
计算空间占有率
【交流研讨】
观察二氧化硅的晶体结构,思考下列问题:
(1)每个二氧化硅晶胞中有几个硅原子和氧原子?
(4)二氧化硅晶体每个12元环中有几个原子?
(2)每个二氧化硅晶胞中有多少个Si-O共价键?
8个硅原子,16氧原子
硅原子数为0.5个,氧原子数1个
由于每个硅原子被12个环共有,因此每个环只占有该硅原子的1/12,又因为每个最小环上有6个硅原子,所以每个最小环平均拥有的硅原子数为:6×(1/12)=0.5个。又因为SiO2晶体是由硅原子和氧原子按1:2的比例所组成,因此氧原子的数目为0.5×2=1个,每个最小环平均拥有1个氧原子。
16×2 =32
(3) 1个硅原子形成几个12元环?
12 个
类型项目 金属晶体 共价晶体 分子晶体 离子晶体
构成晶体的微粒 金属阳离子和“自由电子” 原子 分子 阴、阳
微粒间作用 金属键 共价键 分子间作用力(范德华力或氢键) 离子键
作用力强弱(一般地) 一般较强,有的较弱 很强 弱 较强
确定作用力强弱的一般判断方法 离子半径、价电子数 键长(原子半径) 组成结构相似时比较相对分子质量 离子所带电荷
熔、沸点 差别较大(汞常温下为液态,钨熔点为3 410 ℃) 高 低 较高
硬度 差别较大 大 较小 略硬而脆
导热和导电性 良导体 不良导体 不良导体(部分溶于水发生电离后导电) 不良导体(熔化后或溶于水导电)
溶解性(水) 一般不溶于水,少数与水反应 一般不溶 相似相溶 多数易溶
问题5:共价晶体与其他晶体有哪些区别与联系?
问题4:常见晶体类型还有哪些?
离子晶体、金属晶体、分子晶体
项目复习二 共价晶体
年份省份 情境素材 核心考点
22山东 Ni(CN)x.Zn(NH3)y.zC6H6 配位数、微粒个数
22全国甲 CaF2 离子的确定、微粒间的距离
22全国乙 a-AgI晶体中I-体心立方晶胞 晶体的摩尔体积
22湖南 K、Fe、Se形成的超导体 化学式的确定、配位数、晶体的密度
22广东 晶体X 化学式的确定、微粒间的距离求算
21山东 XeF2四方晶胞 晶胞中分子个数的确定、分数坐标、原子间距离的求算
21全国甲 ZrO2四方晶胞 配位数、晶体密度、化学式的确定
21全国乙 AlCr2体心四方晶胞 原子位置确定、原子空间占有率
21广东 Hg、Ge、Sb形成的晶胞 配位数、晶胞中微粒比、晶体密度
21河北 KHPO4四方晶胞 晶体的密度、晶胞投影图
21湖南 Mg、Ge、O形成的晶胞 原子位置的确定、化学式的确定、晶体的密度
20山东 CdSnAs2四方晶胞 微粒数的确定、分数坐标、配位数
20全国Ⅰ LiFePO4 晶胞中单元数的确定、化学式的确定
20全国Ⅱ 金属卤化物 微粒位置的确定、晶体密度
20全国Ⅲ 氨硼烷 晶体的密度
近三年各地高考真题分析
走进高考
高频考点:
晶胞化学式的确定、晶体的密度、配位数、微粒间的距离、分数坐标等
1.(2021全国甲)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数 ,晶胞参数为apm、apm、cpm,该晶体密度为 g cm﹣3(写出表达式)。在ZrO2中掺杂少量ZnO后形成的催化剂,化学式可表示为
ZnxZr1﹣xOy,则y= (用x表达)。
8
2﹣x
走进高考2
2.(2021全国乙)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,, )已知Xe—F键长为rpm,则B点原子的分数坐标为 ;晶胞中A、B间距离d= pm。
走进高考2
2
r
o
m
n
任务二:以共价键为中心构建晶体核心概念群的思维导图
共价键
共价晶体
共价化合物
晶体
分子晶体
金属晶体
离子晶体
晶胞
基本
单元
面心立方
六方
体心立方
简单立方
包
括
包
括
配位数
决定
聚集
非晶体
固体
分为
共用电子对
原子间
通过
形成
只含
离子化合物
可能含有
化合物
分为
键参数
键
长
键
角
键
能
空间
构型
稳定性
包含
影响
影响
配位键
极性键
非极性键
σ键
π键
单方
重叠
偏向
分为
晶胞中微粒个数的确定
化学式的确定
微粒半径与晶胞参数的关系
晶胞密度的求算
空间占有率的求算
微粒间距离的求算
项目复习二 共价晶体
课堂总结
1.已知SiC的熔点为2 830 ℃,晶胞结构如图所示。下列说法错误的是( )
A.SiC晶体中碳原子和硅原子均采用sp3杂化
B.硅单质的熔点高于2 830 ℃
C.距离硅原子最近且距离相等的碳原子数为4
D.若晶胞参数为a pm,则该晶体的密度为 g·cm-3
B
当堂检测
当堂检测
利用皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管可以合成T-碳,T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)替代,图a、b分别为T-碳的晶胞和俯视图,图c为金刚石晶胞。
一个T-碳晶胞中含有_______个碳原子,T-碳的密度为金刚石的一半,则T-碳晶胞和金刚石晶胞的棱长之比为_______。
2:1
32
课后作业
1.查阅资料,进一步了解认识水分子中共价键,理解水是生命之源的内涵。
2.强化以共价键为中心构建核心概念群。
大概念统领下的物质结构与性质单元复习
—以水中的共价键为辐射中心
【素养目标】
通过核心概念思维导图的构建,培养学生证据推理与模型认知、变化观念与平衡思想、科学探究与创新意识的化学学科核心素养。
【课程目标】
1. 以水中化学键为中心构建核心概念---共价键的思维导图;
2. 以共价晶体为中心构建核心概念---晶体的思维导图;
3. 通过思维导图的构建,使学生总体上对结构知识有宏观的大局把控,细节上对具
体知识有微观的区分与联系。
教学与评价目标
水,生命之源,你了解它吗 ?
(1)H2O是生命之源
(2)H2O是由2个H和1个O组成的3原子分子
(3)H2O键长0.94 A,键角104°45′
(4)H2O是极性分子
(5)H2O分子之间可以形成氢键
(6)H2O中的化学键是极性共价键
问题1:从视频中你获取到了哪些信息?
任务一:以水中共价键为辐射中心构建共价键思维导图
H2O
共价键
特点
方向性
饱和性
配位键
极性键
非极性键
σ键
π键
键长
键角
键能
键参数
空间构型
稳定性
分类
s轨道无方向性
p、d、f 等最大值有空间取向
共用电子对
孤电子对
价电子对
H、O原子
形
成
单方
重叠
偏向
影响
影响
原子半径
电负性
自旋相反的未成对电子相遇
项目复习一 共价键
价电子对互斥理论
理论
空间构型
年份省份 情境素材 核心考点
22山东 半导体、钠离子电池材料 晶体性质、共价键类型、杂化、配位数、晶胞结构
笼形包合物四方晶胞 电子排布式、配位数、杂化、成键轨道、分子性质、互斥理论
22全国甲 透光气囊材料 电子排布图、电离能、杂化轨道、晶胞结构、核间距
22全国乙 卤族元素 电子排布式、能量比较、杂化轨道、成键轨道、键长、键能、物质性质、晶胞体积
22北京 铁精粉 电子排布式、键角、作用力、核间距、晶体密度
22湖南 微量元素铁和硒 电子排布式、键角、共价键类型、电负性、杂化轨道、等电子体、配位数、晶体密度
22广东 微量元素硒、热电材料 电子排布式、氢键、孤对电子、立体构型、晶胞组成、核间距
22海南 半导体材料、酞菁 电子排布式、金属键、杂化、物质熔点、配位反应、离子键、晶胞结构
22河北 四元半导体化合物 自旋电子、电离能、几何构型、杂化、化合价、晶胞组成、原子坐标
21山东 、 、 分子极性、空间构型、熔沸点、杂化
非金属氟化物 电子运动状态、电负性、空间构型、熔沸点、杂化、晶胞组成、核间距、原子坐标
21全国甲 太阳能电池、合成甲醇 电子排布式、晶体类型、杂化、共价键类型、熔沸点、配位数、晶体密度、晶胞组成
21全国乙 过渡金属元素铬 电子排布式、电负性、配位键、杂化、沸点、键角、晶胞结构、空间占有率
21广东 汞的解毒剂 电子排布式、氢键、电负性、键角、杂化、键能、溶解性、晶胞组成、结构、密度
21河北 晶体 核外电子排布、自旋量子数、键能、杂化、等电子体、晶体密度、晶胞投影图
21海南 金属羰基配位化合物 电子排布式、配位数、电离能、杂化、熔沸点、原子坐标
21湖南 硅锗及其化合物 电子排布式、熔沸点、空间构型、杂化、电负性、共价键类型、晶胞组成、密度
20山东 碳硅及其化合物 键能、晶体性质、电负性、成键特点
新型热电材料 空间构型、晶体类型、熔沸点、键角、配位键、杂化、晶胞组成、原子坐标
20全国Ⅰ 锂离子电池及钴酸锂、磷酸铁锂等正极材料 未成对电子、电离能、空间构型、价层电子对、杂化轨道、晶胞组成
20全国Ⅱ 钙钛矿型化合物 电子排布式、熔沸点、电负性、配位数、晶胞结构、杂化轨道、晶体密度
20全国Ⅲ 氨硼烷 原子半径、成键特点、杂化轨道、电负性、等电子体、熔沸点、晶体密度
20海南 储氢物质 电子排布式、杂化轨道、键能、溶解性、配位数、晶胞结构
近三年各地高考真题分析
走进高考
高频考点:
共价键类型、键参数(键角、键长、键能)、电负性等
1. (2022.辽宁)短周期元素X、Y、Z、W、Q原子序数依次增大。基态X、Z、Q原子均有两个单电子,W简单离子在同周期离子中半径最小,Q与Z同主族。下列说法错误的是( )
A.X能与多种元素形成共价键 B.简单氢化物沸点:Z<Q
C.第一电离能:Y>Z D.电负性:W<Z
走进高考1
B
2.(2022.北京)由键能数据大小,不能解释下列事实的是( )
化学键 C﹣H Si﹣H C=O C﹣O Si﹣O C﹣C Si﹣Si
键能/kJ mol﹣1 411 318 799 358 452 346 222
A.稳定性:CH4>SiH4 B.键长:C=O<C﹣O
C.熔点:CO2<SiO2 D.硬度:金刚石>晶体硅
C
S
O
C
N
Al
3. (2020.山东)NH3、PH3、AsH3的沸点由高到低的顺序为 ( 填化学式,下同),还原性由强到弱的顺序为 ,键角由大到小的顺序为 。
NH3、AsH3、PH3
AsH3、PH3、NH3
NH3、PH3、AsH3
对于分子晶体,若存在分子间氢键,熔沸点升高,若不存在分子间氢键,相对分子质量越大,分子间作用力越大,熔沸点越高。
原子得电子能力N>P>As,对应阴离子的失电子能力As3+>P3+>N3+,故氢化物的还原性AsH3>PH3>NH3 。
中心原子电负性越大,与H原子之间的共用电子对离中心原子越近,成键电子对之间斥力越大,键角越大。
走进高考
项目复习二 共价晶体
问题2:共价键可形成哪类晶体?
问题3:常见的共价晶体有哪些?
1.在金刚石晶体中每个碳原子周围紧邻的碳原子有多少个?
2.在金刚石晶体中每个碳原子连接有几个共价键?
3.碳原子的配位数是多少?
4.在金刚石晶体中碳原子个数与C-C共价键个数之比是多少?
5.1mol金刚石中含有的共价键数目是多少?
4
1 :2
金刚石晶胞
4
4
2 NA
再探金刚石
6. 1个碳原子形成几个六元环?
12
任意一个C原子,形成4根共价键,任取2根共价键,有C 4种组合,且2根共价键仅共存于2个六元环中:2× C 4=12
再探金刚石
7. 金刚石晶胞含有____个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=____a,密度=________(列出计算式,下同),表示碳原子在晶胞中的空间占有率____
8
再探金刚石
1
2
3
a
1
3
2
8r=
a
r=
8r
有关晶胞计算的思维流程
单位统一:确定晶胞参数时就转化好长度单位!
1nm=10-7cm=10 -9m 1pm=10-10cm=10-12m
知识
回顾
理解晶胞结构
确定晶胞组成
计算晶胞质量
确定晶胞体积
计算晶体密度
理解晶胞结构
确定晶胞组成
计算微粒体积
确定晶胞体积
计算空间占有率
【交流研讨】
观察二氧化硅的晶体结构,思考下列问题:
(1)每个二氧化硅晶胞中有几个硅原子和氧原子?
(4)二氧化硅晶体每个12元环中有几个原子?
(2)每个二氧化硅晶胞中有多少个Si-O共价键?
8个硅原子,16氧原子
硅原子数为0.5个,氧原子数1个
由于每个硅原子被12个环共有,因此每个环只占有该硅原子的1/12,又因为每个最小环上有6个硅原子,所以每个最小环平均拥有的硅原子数为:6×(1/12)=0.5个。又因为SiO2晶体是由硅原子和氧原子按1:2的比例所组成,因此氧原子的数目为0.5×2=1个,每个最小环平均拥有1个氧原子。
16×2 =32
(3) 1个硅原子形成几个12元环?
12 个
类型项目 金属晶体 共价晶体 分子晶体 离子晶体
构成晶体的微粒 金属阳离子和“自由电子” 原子 分子 阴、阳
微粒间作用 金属键 共价键 分子间作用力(范德华力或氢键) 离子键
作用力强弱(一般地) 一般较强,有的较弱 很强 弱 较强
确定作用力强弱的一般判断方法 离子半径、价电子数 键长(原子半径) 组成结构相似时比较相对分子质量 离子所带电荷
熔、沸点 差别较大(汞常温下为液态,钨熔点为3 410 ℃) 高 低 较高
硬度 差别较大 大 较小 略硬而脆
导热和导电性 良导体 不良导体 不良导体(部分溶于水发生电离后导电) 不良导体(熔化后或溶于水导电)
溶解性(水) 一般不溶于水,少数与水反应 一般不溶 相似相溶 多数易溶
问题5:共价晶体与其他晶体有哪些区别与联系?
问题4:常见晶体类型还有哪些?
离子晶体、金属晶体、分子晶体
项目复习二 共价晶体
年份省份 情境素材 核心考点
22山东 Ni(CN)x.Zn(NH3)y.zC6H6 配位数、微粒个数
22全国甲 CaF2 离子的确定、微粒间的距离
22全国乙 a-AgI晶体中I-体心立方晶胞 晶体的摩尔体积
22湖南 K、Fe、Se形成的超导体 化学式的确定、配位数、晶体的密度
22广东 晶体X 化学式的确定、微粒间的距离求算
21山东 XeF2四方晶胞 晶胞中分子个数的确定、分数坐标、原子间距离的求算
21全国甲 ZrO2四方晶胞 配位数、晶体密度、化学式的确定
21全国乙 AlCr2体心四方晶胞 原子位置确定、原子空间占有率
21广东 Hg、Ge、Sb形成的晶胞 配位数、晶胞中微粒比、晶体密度
21河北 KHPO4四方晶胞 晶体的密度、晶胞投影图
21湖南 Mg、Ge、O形成的晶胞 原子位置的确定、化学式的确定、晶体的密度
20山东 CdSnAs2四方晶胞 微粒数的确定、分数坐标、配位数
20全国Ⅰ LiFePO4 晶胞中单元数的确定、化学式的确定
20全国Ⅱ 金属卤化物 微粒位置的确定、晶体密度
20全国Ⅲ 氨硼烷 晶体的密度
近三年各地高考真题分析
走进高考
高频考点:
晶胞化学式的确定、晶体的密度、配位数、微粒间的距离、分数坐标等
1.(2021全国甲)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为ZnO/ZrO2固溶体。四方ZrO2晶胞如图所示。Zr4+离子在晶胞中的配位数 ,晶胞参数为apm、apm、cpm,该晶体密度为 g cm﹣3(写出表达式)。在ZrO2中掺杂少量ZnO后形成的催化剂,化学式可表示为
ZnxZr1﹣xOy,则y= (用x表达)。
8
2﹣x
走进高考2
2.(2021全国乙)XeF2晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,该晶胞中有 个XeF2分子。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点原子的分数坐标为( ,, )已知Xe—F键长为rpm,则B点原子的分数坐标为 ;晶胞中A、B间距离d= pm。
走进高考2
2
r
o
m
n
任务二:以共价键为中心构建晶体核心概念群的思维导图
共价键
共价晶体
共价化合物
晶体
分子晶体
金属晶体
离子晶体
晶胞
基本
单元
面心立方
六方
体心立方
简单立方
包
括
包
括
配位数
决定
聚集
非晶体
固体
分为
共用电子对
原子间
通过
形成
只含
离子化合物
可能含有
化合物
分为
键参数
键
长
键
角
键
能
空间
构型
稳定性
包含
影响
影响
配位键
极性键
非极性键
σ键
π键
单方
重叠
偏向
分为
晶胞中微粒个数的确定
化学式的确定
微粒半径与晶胞参数的关系
晶胞密度的求算
空间占有率的求算
微粒间距离的求算
项目复习二 共价晶体
课堂总结
1.已知SiC的熔点为2 830 ℃,晶胞结构如图所示。下列说法错误的是( )
A.SiC晶体中碳原子和硅原子均采用sp3杂化
B.硅单质的熔点高于2 830 ℃
C.距离硅原子最近且距离相等的碳原子数为4
D.若晶胞参数为a pm,则该晶体的密度为 g·cm-3
B
当堂检测
当堂检测
利用皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管可以合成T-碳,T-碳的晶体结构可看成金刚石晶体中每个碳原子被正四面体结构单元(由四个碳原子组成)替代,图a、b分别为T-碳的晶胞和俯视图,图c为金刚石晶胞。
一个T-碳晶胞中含有_______个碳原子,T-碳的密度为金刚石的一半,则T-碳晶胞和金刚石晶胞的棱长之比为_______。
2:1
32
课后作业
1.查阅资料,进一步了解认识水分子中共价键,理解水是生命之源的内涵。
2.强化以共价键为中心构建核心概念群。
同课章节目录
