第一章微项目探秘膨松剂讲义2023-2024学年高一上学期化学鲁科版(2019)必修第一册
文档属性
| 名称 | 第一章微项目探秘膨松剂讲义2023-2024学年高一上学期化学鲁科版(2019)必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览



文档简介
微项目 探秘膨松剂
[核心素养发展目标]
1、运用研究物质性质的基本方法(观察、实验、分类、比较等)和基本程序,对碳酸氢钠的蓬松原理进行实验探究,促使“科学探究与创新意识”核心素养的发展。
2、了解复合膨松剂的组成,学会在真实情景中分析、解决实际问题,探究陌生物质的性质,促进“科学态度与社会责任”核心素养的发展。
项目活动1 探究碳酸氢钠用作膨松剂的作用原理
1.膨松剂及其类别
(1)概念
膨松剂是在食品加工过程中加入的,能使面胚发起形成多孔组织,从而使食品具有柔软或蓬松特点的一类物质。
(2)分类
膨松剂
(3)化学膨松剂中基本上都含有一种化学物质——碳酸氢钠。
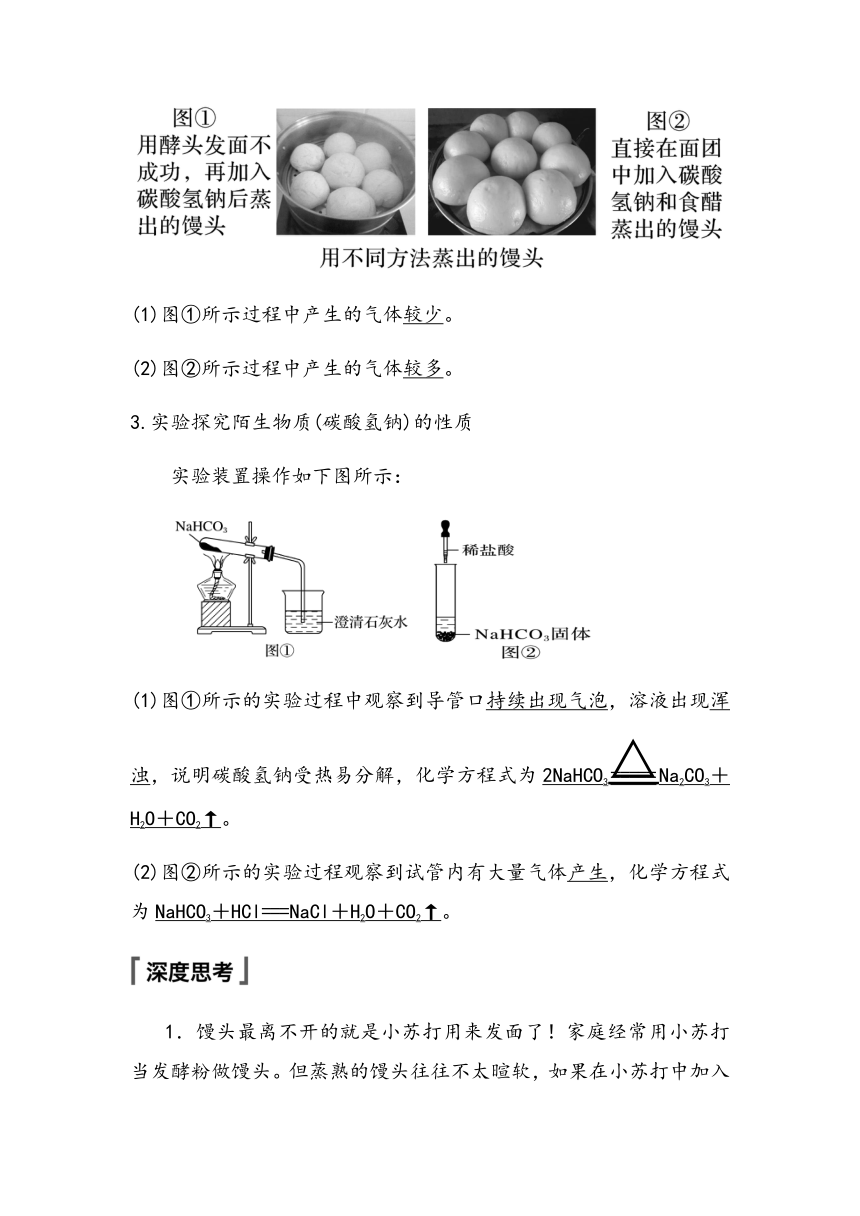
2.观察不同方法蒸出的馒头
(1)图①所示过程中产生的气体较少。
(2)图②所示过程中产生的气体较多。
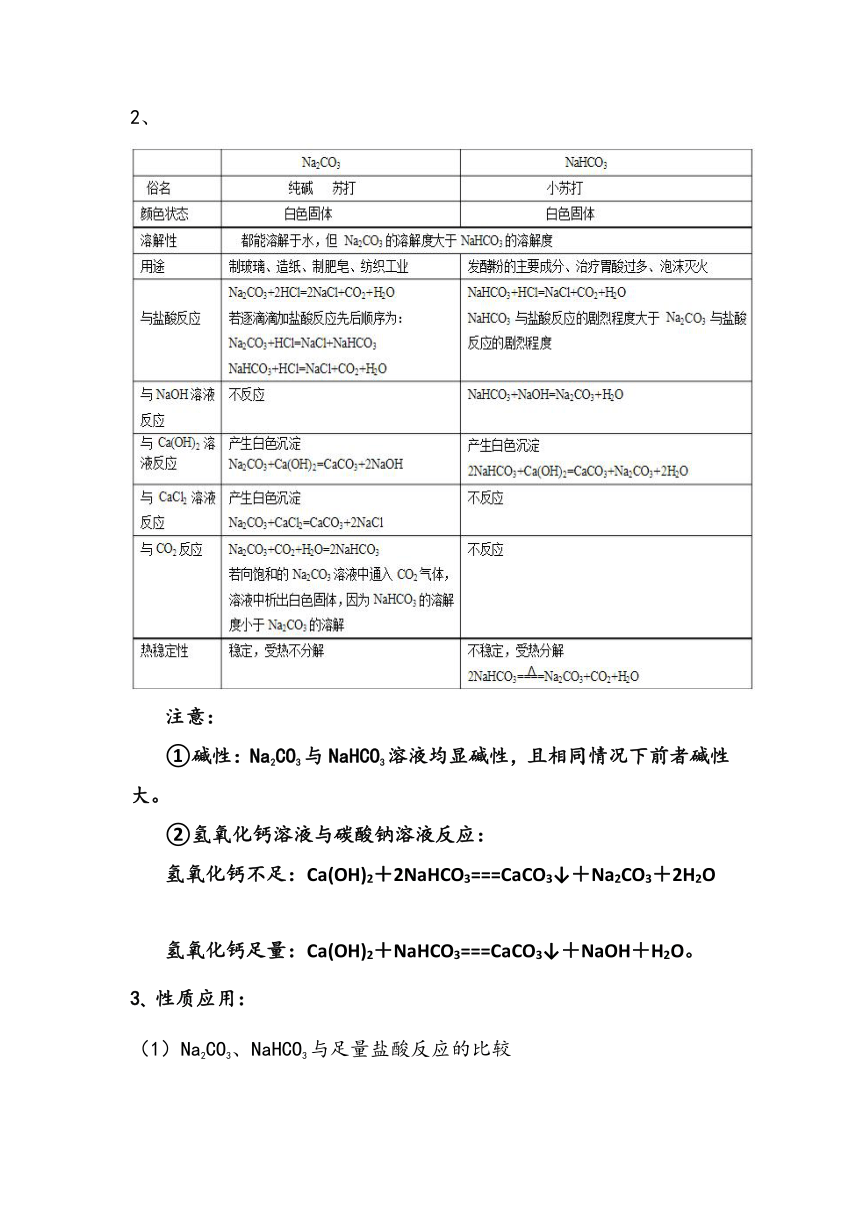
3.实验探究陌生物质(碳酸氢钠)的性质
实验装置操作如下图所示:
(1)图①所示的实验过程中观察到导管口持续出现气泡,溶液出现浑浊,说明碳酸氢钠受热易分解,化学方程式为2NaHCO3Na2CO3+H2O+CO2↑。
(2)图②所示的实验过程观察到试管内有大量气体产生,化学方程式为NaHCO3+HCl===NaCl+H2O+CO2↑。
1.馒头最离不开的就是小苏打用来发面了!家庭经常用小苏打当发酵粉做馒头。但蒸熟的馒头往往不太暄软,如果在小苏打中加入一定量的醋酸,发出的馒头会非常松软,这是为什么?
[提示] 这是因为小苏打遇热放出的二氧化碳气体不多,馒头中产生的小气孔少,面发的不好。另一方面小苏打本身是碱性物质,如用量稍多,馒头就会产生碱味,色泽发黄,维生素被破坏,效果很不理想。如果在小苏打中加入一定量的醋酸(食醋)就可弥补以上的不足。不仅可产生大量的二氧化碳气体,而且也不会有很大的碱味。
2.当酵头发面面团发的不够好,为什么不用碳酸钠,而是添加了碳酸氢钠进行调节?
[提示] 碳酸氢钠分解产生CO2,从而可作膨松剂,但是碳酸钠受热不分解,故不用碳酸钠。
3.如果面团发酵过头,会有酸味,可以加入碱性物质,如碳酸钠,为什么?
[提示] 面团发酵时产生的乳酸、醋酸等与Na2CO3反应,可以减轻酸味,产生的CO2还可以使面团变得更加松软。
[反思归纳]
1、碳酸氢钠的性质
(1)易溶于水,水溶液呈碱性。
(2)不稳定,受热易分解。
(3)能与酸反应,放出二氧化碳。
(4)能与碱溶液反应
NaOH+NaHCO3===Na2CO3+H2O,
Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O或Ca(OH)2+NaHCO3===CaCO3↓+NaOH+H2O。
2、
注意:
①碱性:Na2CO3与NaHCO3溶液均显碱性,且相同情况下前者碱性大。
②氢氧化钙溶液与碳酸钠溶液反应:
氢氧化钙不足:Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O
氢氧化钙足量:Ca(OH)2+NaHCO3===CaCO3↓+NaOH+H2O。
3、性质应用:
(1)Na2CO3、NaHCO3与足量盐酸反应的比较
(2)Na2CO3、NaHCO3与盐酸反应的反应原理及现象
①Na2CO3溶液与盐酸反应
Na2CO3溶液与盐酸反应时,滴加顺序不同,实验现象不同,产生的CO2的量也可能不同。
滴加顺序 反应现象 离子方程式
滴加Na2CO3溶液,马上有气体放出后 CO+2H+===CO2↑+H2O
开始无明显现象,后来有气体放出 开始:CO+H+===HCO 后来:HCO+H+===CO2↑+H2O
②无论将NaHCO3溶液滴入盐酸中,还是将盐酸滴入NaHCO3溶液中,都只发生反应:HCO+H+===CO2↑+H2O,即开始滴加就会有CO2气体生成。
(3)Na2CO3、NaHCO3的鉴别方法
(4)Na2CO3、NaHCO3的提纯方法(括号内为杂质)
固体 Na2CO3(NaHCO3):加热 2NaHCO3Na2CO3+CO2↑+H2O,加热至恒重 ②NaHCO3(Na2CO3):加水溶解制成饱和溶液,通入足量CO2气体,结晶、过滤
溶液 Na2CO3(NaHCO3):加适量NaOH溶液 NaHCO3+NaOH===Na2CO3+H2O NaHCO3(Na2CO3):通入足量CO2 Na2CO3+H2O+CO2===2NaHCO3
(5)Na2CO3与NaHCO3的相互转化
[能力达成]
1.为使以面粉为原料的面包松软可口,通常用碳酸氢钠作膨松剂,其原因是( )
①热稳定性差 ②增加甜味 ③产生二氧化碳 ④提供钠离子
A.②③ B.①③ C.①④ D.③④
B [碳酸氢钠不稳定,加热易分解生成二氧化碳气体,不能增加甜味,与是否提供钠离子无关,可使面包疏松多孔而导致松软可口。故选B。]
2.纯碱和小苏打都是白色晶体,在日常生活中很常见。若要在家中将它们区分开来,下面的方法中可行的是( )
A.分别放在炒锅中加热,观察是否有残留物
B.分别向纯碱溶液和小苏打溶液中加入食盐水
C.分别向纯碱溶液和小苏打溶液中加入石灰水
D.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度
D [NaHCO3不稳定,受热易分解:2NaHCO3Na2CO3+CO2↑+H2O,但分解后仍有固体剩余;Na2CO3稳定性好,不分解,A错误。Na2CO3溶液、NaHCO3溶液与NaCl溶液均不反应,B错误。澄清石灰水与NaHCO3、Na2CO3溶液均能生成白色沉淀,C错误。相同质量的NaHCO3与Na2CO3分别与白醋反应,反应较剧烈的是NaHCO3,D正确。]
3.胃酸过多又称作胃酸过高,是胃肠疾病的常见症状之一。适度的胃酸可以帮助消化,但如果胃酸过多就会伤及胃、十二指肠黏膜,造成胃溃疡或十二指肠溃疡等疾病,治疗胃酸过多可以用碳酸氢钠。
请用化学方程式解释碳酸氢钠可以治疗胃酸过多的原因。
[答案] NaHCO3+HCl===NaCl+CO2↑+H2O。
项目活动2 设计并使用复合膨松剂
[项目情境]
用碳酸氢钠蒸的馒头呈淡黄色,口感差一些,如何使馒头又白又松软,口味更好呢?
[探究问题]
1.如果用碳酸氢钠制作复合膨松剂的主材料,另一种主材料需具有什么性质?
[提示]酸性。所选材料必须能与碳酸氢钠反应产生CO2。
2.用复合膨松剂NaHCO3和食醋蒸馒头时,从用量(或物质比例)的角度应注意什么问题?为什么?
[提示]尽量使NaHCO3与食醋恰好完全反应;若NaHCO3相对食醋过量过多,过量的NaHCO3受热分解产生Na2CO3,导致馒头发黄、有碱味;若食醋相对NaHCO3过量过多,馒头会有酸味。
3.如果用碳酸氢钠制作复合膨松剂的主材料,另一种主材料用白醋和柠檬酸哪一个更合适?并说出你的理由。
[提示] 柠檬酸。常温下柠檬酸为固体,白醋是液体,白醋和碳酸氢钠混合会直接发生反应,故柠檬酸更合适。
[反思归纳]
1、复合膨松剂的组成
碳酸盐类 如碳酸氢钠通常用量30%~50% 作用是反应产生二氧化碳
酸性物质 如柠檬酸通常用量30%~40% 作用是与碳酸盐反应,控制反应速率和提升膨松剂的作用效果,调节产品酸碱度
助剂 指的是淀粉、脂肪酸等,通常用量10%~30% 作用是防止膨松剂吸潮结块而失效,调节气体产生速率或使气体均匀产生
2、常见的酸性物质
酸性物质 化学式 色态 气味 溶解性 挥发性
白醋 CH3COOH 无色液体 刺激性 易溶于水 易挥发
柠檬酸 C6H8O7·H2O 无色晶体 无臭 易溶于水 难挥发
[能力达成]
1.在下列膨松剂中,属于复合膨松剂的是( )
A.泡打粉 B.碳酸钠
C.碳酸氢钠 D.碳酸氢铵
A [泡打粉是由碱性物质、酸式盐和填充物按一定比例混合而成的化学复合膨松剂。]
2.膨松剂是一种食品添加剂,它受热分解产生的气体,能使面胚在焙烤过程中变得松软、多孔。碳酸氢钠(NaHCO3)受热后发生分解反应生成二氧化碳、水和碳酸钠,是常用的膨松剂之一。它既可以作为碱性膨松剂单独使用,也可以与酒石酸氢钾、淀粉按一定比例混合制成复合膨松剂。复合膨松剂遇水会产生二氧化碳,起到膨松作用。下列说法正确的是( )
A.任何受热分解能产生气体的物质都可以做食品膨松剂
B.碳酸氢钠受热分解的化学方程式为NaHCO3CO2↑+H2O+Na2CO3
C.碳酸氢钠做膨松剂时,必须与酒石酸氢钾、淀粉混合使用
D.复合膨松剂应在干燥的环境中保存
D [碳酸氢钠在加热的条件下会生成碳酸钠、水和二氧化碳,碳酸氢钠与酸反应也会生成二氧化碳,二氧化碳可以使食品变得松软、多孔。任何受热分解能产生无毒气体的物质才可以做食品膨松剂,故A错误;碳酸氢钠受热分解的化学方程式为2NaHCO3CO2↑+H2O+Na2CO3,故B错误;碳酸氢钠做膨松剂时,也可以与有机酸反应,故C错误;复合膨松剂遇水会产生二氧化碳,起到膨松作用,所以复合膨松剂应在干燥的环境中保存,故D正确。]
【课堂小结】
探究碳酸氢钠用作膨松剂的作用原理
2、设计并使用复合膨松剂
[核心素养发展目标]
1、运用研究物质性质的基本方法(观察、实验、分类、比较等)和基本程序,对碳酸氢钠的蓬松原理进行实验探究,促使“科学探究与创新意识”核心素养的发展。
2、了解复合膨松剂的组成,学会在真实情景中分析、解决实际问题,探究陌生物质的性质,促进“科学态度与社会责任”核心素养的发展。
项目活动1 探究碳酸氢钠用作膨松剂的作用原理
1.膨松剂及其类别
(1)概念
膨松剂是在食品加工过程中加入的,能使面胚发起形成多孔组织,从而使食品具有柔软或蓬松特点的一类物质。
(2)分类
膨松剂
(3)化学膨松剂中基本上都含有一种化学物质——碳酸氢钠。
2.观察不同方法蒸出的馒头
(1)图①所示过程中产生的气体较少。
(2)图②所示过程中产生的气体较多。
3.实验探究陌生物质(碳酸氢钠)的性质
实验装置操作如下图所示:
(1)图①所示的实验过程中观察到导管口持续出现气泡,溶液出现浑浊,说明碳酸氢钠受热易分解,化学方程式为2NaHCO3Na2CO3+H2O+CO2↑。
(2)图②所示的实验过程观察到试管内有大量气体产生,化学方程式为NaHCO3+HCl===NaCl+H2O+CO2↑。
1.馒头最离不开的就是小苏打用来发面了!家庭经常用小苏打当发酵粉做馒头。但蒸熟的馒头往往不太暄软,如果在小苏打中加入一定量的醋酸,发出的馒头会非常松软,这是为什么?
[提示] 这是因为小苏打遇热放出的二氧化碳气体不多,馒头中产生的小气孔少,面发的不好。另一方面小苏打本身是碱性物质,如用量稍多,馒头就会产生碱味,色泽发黄,维生素被破坏,效果很不理想。如果在小苏打中加入一定量的醋酸(食醋)就可弥补以上的不足。不仅可产生大量的二氧化碳气体,而且也不会有很大的碱味。
2.当酵头发面面团发的不够好,为什么不用碳酸钠,而是添加了碳酸氢钠进行调节?
[提示] 碳酸氢钠分解产生CO2,从而可作膨松剂,但是碳酸钠受热不分解,故不用碳酸钠。
3.如果面团发酵过头,会有酸味,可以加入碱性物质,如碳酸钠,为什么?
[提示] 面团发酵时产生的乳酸、醋酸等与Na2CO3反应,可以减轻酸味,产生的CO2还可以使面团变得更加松软。
[反思归纳]
1、碳酸氢钠的性质
(1)易溶于水,水溶液呈碱性。
(2)不稳定,受热易分解。
(3)能与酸反应,放出二氧化碳。
(4)能与碱溶液反应
NaOH+NaHCO3===Na2CO3+H2O,
Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O或Ca(OH)2+NaHCO3===CaCO3↓+NaOH+H2O。
2、
注意:
①碱性:Na2CO3与NaHCO3溶液均显碱性,且相同情况下前者碱性大。
②氢氧化钙溶液与碳酸钠溶液反应:
氢氧化钙不足:Ca(OH)2+2NaHCO3===CaCO3↓+Na2CO3+2H2O
氢氧化钙足量:Ca(OH)2+NaHCO3===CaCO3↓+NaOH+H2O。
3、性质应用:
(1)Na2CO3、NaHCO3与足量盐酸反应的比较
(2)Na2CO3、NaHCO3与盐酸反应的反应原理及现象
①Na2CO3溶液与盐酸反应
Na2CO3溶液与盐酸反应时,滴加顺序不同,实验现象不同,产生的CO2的量也可能不同。
滴加顺序 反应现象 离子方程式
滴加Na2CO3溶液,马上有气体放出后 CO+2H+===CO2↑+H2O
开始无明显现象,后来有气体放出 开始:CO+H+===HCO 后来:HCO+H+===CO2↑+H2O
②无论将NaHCO3溶液滴入盐酸中,还是将盐酸滴入NaHCO3溶液中,都只发生反应:HCO+H+===CO2↑+H2O,即开始滴加就会有CO2气体生成。
(3)Na2CO3、NaHCO3的鉴别方法
(4)Na2CO3、NaHCO3的提纯方法(括号内为杂质)
固体 Na2CO3(NaHCO3):加热 2NaHCO3Na2CO3+CO2↑+H2O,加热至恒重 ②NaHCO3(Na2CO3):加水溶解制成饱和溶液,通入足量CO2气体,结晶、过滤
溶液 Na2CO3(NaHCO3):加适量NaOH溶液 NaHCO3+NaOH===Na2CO3+H2O NaHCO3(Na2CO3):通入足量CO2 Na2CO3+H2O+CO2===2NaHCO3
(5)Na2CO3与NaHCO3的相互转化
[能力达成]
1.为使以面粉为原料的面包松软可口,通常用碳酸氢钠作膨松剂,其原因是( )
①热稳定性差 ②增加甜味 ③产生二氧化碳 ④提供钠离子
A.②③ B.①③ C.①④ D.③④
B [碳酸氢钠不稳定,加热易分解生成二氧化碳气体,不能增加甜味,与是否提供钠离子无关,可使面包疏松多孔而导致松软可口。故选B。]
2.纯碱和小苏打都是白色晶体,在日常生活中很常见。若要在家中将它们区分开来,下面的方法中可行的是( )
A.分别放在炒锅中加热,观察是否有残留物
B.分别向纯碱溶液和小苏打溶液中加入食盐水
C.分别向纯碱溶液和小苏打溶液中加入石灰水
D.在水杯中各盛相同质量的样品,分别加入等体积的白醋,观察反应的剧烈程度
D [NaHCO3不稳定,受热易分解:2NaHCO3Na2CO3+CO2↑+H2O,但分解后仍有固体剩余;Na2CO3稳定性好,不分解,A错误。Na2CO3溶液、NaHCO3溶液与NaCl溶液均不反应,B错误。澄清石灰水与NaHCO3、Na2CO3溶液均能生成白色沉淀,C错误。相同质量的NaHCO3与Na2CO3分别与白醋反应,反应较剧烈的是NaHCO3,D正确。]
3.胃酸过多又称作胃酸过高,是胃肠疾病的常见症状之一。适度的胃酸可以帮助消化,但如果胃酸过多就会伤及胃、十二指肠黏膜,造成胃溃疡或十二指肠溃疡等疾病,治疗胃酸过多可以用碳酸氢钠。
请用化学方程式解释碳酸氢钠可以治疗胃酸过多的原因。
[答案] NaHCO3+HCl===NaCl+CO2↑+H2O。
项目活动2 设计并使用复合膨松剂
[项目情境]
用碳酸氢钠蒸的馒头呈淡黄色,口感差一些,如何使馒头又白又松软,口味更好呢?
[探究问题]
1.如果用碳酸氢钠制作复合膨松剂的主材料,另一种主材料需具有什么性质?
[提示]酸性。所选材料必须能与碳酸氢钠反应产生CO2。
2.用复合膨松剂NaHCO3和食醋蒸馒头时,从用量(或物质比例)的角度应注意什么问题?为什么?
[提示]尽量使NaHCO3与食醋恰好完全反应;若NaHCO3相对食醋过量过多,过量的NaHCO3受热分解产生Na2CO3,导致馒头发黄、有碱味;若食醋相对NaHCO3过量过多,馒头会有酸味。
3.如果用碳酸氢钠制作复合膨松剂的主材料,另一种主材料用白醋和柠檬酸哪一个更合适?并说出你的理由。
[提示] 柠檬酸。常温下柠檬酸为固体,白醋是液体,白醋和碳酸氢钠混合会直接发生反应,故柠檬酸更合适。
[反思归纳]
1、复合膨松剂的组成
碳酸盐类 如碳酸氢钠通常用量30%~50% 作用是反应产生二氧化碳
酸性物质 如柠檬酸通常用量30%~40% 作用是与碳酸盐反应,控制反应速率和提升膨松剂的作用效果,调节产品酸碱度
助剂 指的是淀粉、脂肪酸等,通常用量10%~30% 作用是防止膨松剂吸潮结块而失效,调节气体产生速率或使气体均匀产生
2、常见的酸性物质
酸性物质 化学式 色态 气味 溶解性 挥发性
白醋 CH3COOH 无色液体 刺激性 易溶于水 易挥发
柠檬酸 C6H8O7·H2O 无色晶体 无臭 易溶于水 难挥发
[能力达成]
1.在下列膨松剂中,属于复合膨松剂的是( )
A.泡打粉 B.碳酸钠
C.碳酸氢钠 D.碳酸氢铵
A [泡打粉是由碱性物质、酸式盐和填充物按一定比例混合而成的化学复合膨松剂。]
2.膨松剂是一种食品添加剂,它受热分解产生的气体,能使面胚在焙烤过程中变得松软、多孔。碳酸氢钠(NaHCO3)受热后发生分解反应生成二氧化碳、水和碳酸钠,是常用的膨松剂之一。它既可以作为碱性膨松剂单独使用,也可以与酒石酸氢钾、淀粉按一定比例混合制成复合膨松剂。复合膨松剂遇水会产生二氧化碳,起到膨松作用。下列说法正确的是( )
A.任何受热分解能产生气体的物质都可以做食品膨松剂
B.碳酸氢钠受热分解的化学方程式为NaHCO3CO2↑+H2O+Na2CO3
C.碳酸氢钠做膨松剂时,必须与酒石酸氢钾、淀粉混合使用
D.复合膨松剂应在干燥的环境中保存
D [碳酸氢钠在加热的条件下会生成碳酸钠、水和二氧化碳,碳酸氢钠与酸反应也会生成二氧化碳,二氧化碳可以使食品变得松软、多孔。任何受热分解能产生无毒气体的物质才可以做食品膨松剂,故A错误;碳酸氢钠受热分解的化学方程式为2NaHCO3CO2↑+H2O+Na2CO3,故B错误;碳酸氢钠做膨松剂时,也可以与有机酸反应,故C错误;复合膨松剂遇水会产生二氧化碳,起到膨松作用,所以复合膨松剂应在干燥的环境中保存,故D正确。]
【课堂小结】
探究碳酸氢钠用作膨松剂的作用原理
2、设计并使用复合膨松剂
