2024年高三化学实验专题复习 深入探究氢氧化亚铁的制备 说课课件(共25张PPT)
文档属性
| 名称 | 2024年高三化学实验专题复习 深入探究氢氧化亚铁的制备 说课课件(共25张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 54.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2023-10-12 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
深入探究氢氧化亚铁的制备
目录
01
03
02
实验设计依据
实验教学目标
实验方案设计
04
05
实验数据处理
实验操作要领
06
教学评价与反思
实验设计依据
01
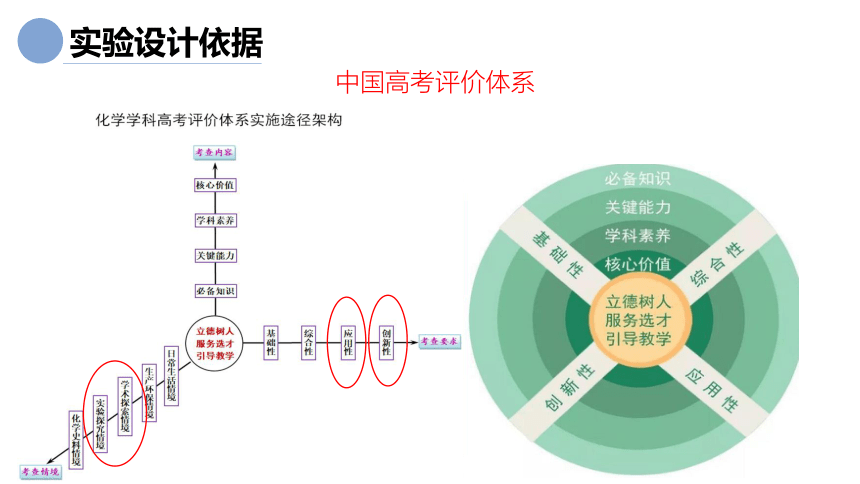
实验设计依据
中国高考评价体系
实验设计依据
主题1:化学科学与实验探究
【内容要求】
1.2 理解从问题和假设出发确定研究目的、依据研究目的设计方案、基于证据进行分析和推理等对于科学探究的重要性。
1.3 体会实验条件控制对完成科学实验及探究活动的作用。
1.4发展对化学实验探究活动的好奇心和兴趣,养成注重实证、严谨求实的科学态度,增强合作探究意识,养成独立思考、敢于质疑和勇于创新的精神。
【学业要求】
1.具有较强的问题意识,能提出化学探究问题,能作出预测和假设。能依据实验目的和假设,设计解决简单问题的实验方案,能对实验方案进行评价。
2.能运用实验基本操作实施实验方案,能观察并如实记录实验现象和数据,进行分析和推理,得出合理的结论,能对实验过程和结果进行反思。
3.能根据不同类型实验的特点,设计并实施实验,能运用变量控制的思想初步探究反应规律。
课标考查要求
实验设计依据
主题2:常见的无机物及其应用
【内容要求】
2.4结合真实情境中的应用实例或者通过实验探究,了解铁及其化合物的主要性质。
教学策略:重视开展高水平的实验探究活动。
学生活动建议:氢氧化亚铁的制备
课标考查要求
实验设计依据
本实验为鲁科版必修一第三章第1节铁的多样性内容,教材实验很难观察到白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色。
近几年山东高考题着重考察探究意识和深度思维,对于实验的考察也越来越重视情境下信息的提取能力以及学生探究能力。
教材实验分析
新高考命题趋势
实验设计依据
文献资料分析
研究文献发现,目前大部分改进实验主要从避氧、创造还原性条件等角度出发,没有让学生了解灰绿色物质出现的本质原因。
实验设计依据
实验设计思路
为适应新高考模式,从熟悉氢氧化亚铁制备实验出发,结合陌生的实验探究情境和学术探索情境,从本实验中最大的吸引点入手,解决学生存在的疑问,灰绿色沉淀是什么,引起学生的探究欲望,通过提供文献资料支持,学生自主设计实验并进行实验探究,对氢氧化亚铁白色沉淀的制备进行方案的优化,充分落实了“素养为本”的实验教学。
结合现有研究成果,认为Fe(OH)2 沉淀物吸附反应体系中绿色的Fe2+ 是Fe(OH)2 白色沉淀变为灰绿色沉淀的真正原因。
实验教学目标
02
实验教学目标
基于资料卡片,找出制备氢氧化亚铁白色沉淀的影响因素,运用变量控制思想设计实验方案初步探索,提升“科学探究与创新意识”化学学科核心素养。
2. 通过实验探究活动,促进学生建立实验目的、实验证据、实验结果之间的关
系,提升“证据推理与模型认知”化学学科核心素养。
3. 通过实验探究活动,评价学生:提取情境信息的能力水平(部分/全部);选
取试剂设计实验方案的能力水平(选取的试剂不合适/正确选取试剂);实验
目的、实验证据、实验结论之间的推理分析能力水平(三者之间的系统证据
推理/局部的证据推理/缺少证据的推理过程)
实验方案设计
03
实验方案设计
阅读资料卡片
找出影响因素
设计实验方案
进行实验探究
优化制备方法
资料卡片1:根据调色原理可知,白色和红褐色的调和色不可能是浅绿色、灰绿色,即灰绿色沉淀不可能是氢氧化亚铁和氢氧化铁的混合物。
资料卡片2:现有研究成果表明, Fe(OH)2 沉淀物吸附反应体系中绿色的Fe2+ 是Fe(OH)2 白色沉淀变为灰绿色沉淀的真正原因。
资料卡片3:氧气的和Fe3+的存在会使形成的Fe(OH)2沉淀不纯净,更容易吸附Fe2+ 而使沉淀颜色变化。
资料卡片4:实验还发现采用FeCl2 与FeSO4 溶液分别制备Fe(OH)2 沉淀也有所差异,前者得到Fe(OH)2 保持白色的时间更久。
【问题1】选择哪两种试剂进行反应?
【问题2】灰绿色沉淀形成原因是什么?
【问题3】影响灰绿色沉淀产生的因素有哪些?
设计意图:在实验目的的引领下,培养学生对情境中信息的提取和理解能力,启发学生进行深度思考,培养学生的深度思维,充分挖掘学生潜力。
实验方案设计
阅读资料卡片
找出影响因素
设计实验方案
进行实验探究
优化制备方法
设计意图:能根据实验特点设计实验方案,并对实验方案进行评价反思,在不断优化过程中,发现自己存在的问题,进一步体会变量控制的重要作用。
实验方案设计
阅读资料卡片
找出影响因素
设计实验方案
进行实验探究
优化制备方法
实验数据处理
04
实验数据处理
滴加顺序(FeCl2溶液浓度为0.1 mol/L,NaOH溶液浓度为8mol/L )
FeCl2
FeCl2
FeCl2
NaOH
NaOH
5min后
√
实验结论:FeCl2溶液中存在大量Fe2+,容易吸附到白色沉淀表面,滴加顺序应选择在NaOH溶液中滴加FeCl2溶液。
实验现象:在 NaOH溶液中滴加FeCl2溶液时,生成白色沉淀悬浮在溶液中,一段时间后仍为白色。
在FeCl2溶液中滴加NaOH溶液时,生成白色沉淀迅速变为灰绿色,最后变为深绿色。
设计意图:通过对比现象,引导学生找出现象背后的原因,引发深度思考,实现能力进阶。
FeCl2
NaOH
实验数据处理
FeCl2溶液浓度(在10mL 饱和NaOH溶液中滴加5mL不同浓度的FeCl2溶液)
0.05 mol/L
0.1 mol/L
0.4 mol/L
√
实验现象:0.4 mol/L:产生灰绿色沉淀且一段时间后沉淀上层变为深绿色,0.2mol/L:产生浅灰绿色沉淀;0.1 mol/L:产生白色沉淀;0.05 mol/L:产生白色沉淀,量少。
实验结论:FeCl2浓度越小,越容易制得白色沉淀,但浓度小生成的沉淀少,且结构不紧密,不利于观察,最终选择FeCl2浓度为0.1mol/L。
0.2 mol/L
实验数据处理
NaOH溶液浓度(在10mL 不同浓度的NaOH溶液中滴加5mL 0.2mol/L的FeCl2溶液)
饱和
8mol/L
4 mol/L
1min
5min
√
实验现象:饱和溶液:产生白色沉淀;8mol/L:产生白色沉淀;4 mol/L:产生浅灰绿色沉淀。
实验结论:氢氧化钠浓度越大,越容易制得白色沉淀,且结构紧密,最终选择氢氧化钠饱和溶液。
实验数据处理
条件选择
实验探究发现,制备氢氧化亚铁的最佳条件为:在10mL 饱和NaOH溶液中滴加5mL 0.1mol/L FeCl2溶液。
1min
5min
实验数据处理
优化制备方法
实验数据处理
优化制备方法
时间t/min
教学评价与反思
05
教学评价与反思
锻炼了学生对情境中信息的提取和处理能力,自主设计实验方案,并进行实验探究,深度参与学习过程,深刻体会了实验条件控制对完成实验探究活动的作用。
1
已有
技能
使学生从本质上明白了灰绿色物质形成的原因,控制变量的唯一找出制备白色沉淀的方法,不仅落实了学科知识,还充分发挥了探究性实验的育人功能,培养了学生化学核心素养。
2
应该更加注重问题的引导,让学生自主思考回答,重视学生的探究过程,引导学生深入思考。
3
汇报完毕
敬请批评指正
深入探究氢氧化亚铁的制备
目录
01
03
02
实验设计依据
实验教学目标
实验方案设计
04
05
实验数据处理
实验操作要领
06
教学评价与反思
实验设计依据
01
实验设计依据
中国高考评价体系
实验设计依据
主题1:化学科学与实验探究
【内容要求】
1.2 理解从问题和假设出发确定研究目的、依据研究目的设计方案、基于证据进行分析和推理等对于科学探究的重要性。
1.3 体会实验条件控制对完成科学实验及探究活动的作用。
1.4发展对化学实验探究活动的好奇心和兴趣,养成注重实证、严谨求实的科学态度,增强合作探究意识,养成独立思考、敢于质疑和勇于创新的精神。
【学业要求】
1.具有较强的问题意识,能提出化学探究问题,能作出预测和假设。能依据实验目的和假设,设计解决简单问题的实验方案,能对实验方案进行评价。
2.能运用实验基本操作实施实验方案,能观察并如实记录实验现象和数据,进行分析和推理,得出合理的结论,能对实验过程和结果进行反思。
3.能根据不同类型实验的特点,设计并实施实验,能运用变量控制的思想初步探究反应规律。
课标考查要求
实验设计依据
主题2:常见的无机物及其应用
【内容要求】
2.4结合真实情境中的应用实例或者通过实验探究,了解铁及其化合物的主要性质。
教学策略:重视开展高水平的实验探究活动。
学生活动建议:氢氧化亚铁的制备
课标考查要求
实验设计依据
本实验为鲁科版必修一第三章第1节铁的多样性内容,教材实验很难观察到白色沉淀,白色沉淀迅速变为灰绿色,最终变为红褐色。
近几年山东高考题着重考察探究意识和深度思维,对于实验的考察也越来越重视情境下信息的提取能力以及学生探究能力。
教材实验分析
新高考命题趋势
实验设计依据
文献资料分析
研究文献发现,目前大部分改进实验主要从避氧、创造还原性条件等角度出发,没有让学生了解灰绿色物质出现的本质原因。
实验设计依据
实验设计思路
为适应新高考模式,从熟悉氢氧化亚铁制备实验出发,结合陌生的实验探究情境和学术探索情境,从本实验中最大的吸引点入手,解决学生存在的疑问,灰绿色沉淀是什么,引起学生的探究欲望,通过提供文献资料支持,学生自主设计实验并进行实验探究,对氢氧化亚铁白色沉淀的制备进行方案的优化,充分落实了“素养为本”的实验教学。
结合现有研究成果,认为Fe(OH)2 沉淀物吸附反应体系中绿色的Fe2+ 是Fe(OH)2 白色沉淀变为灰绿色沉淀的真正原因。
实验教学目标
02
实验教学目标
基于资料卡片,找出制备氢氧化亚铁白色沉淀的影响因素,运用变量控制思想设计实验方案初步探索,提升“科学探究与创新意识”化学学科核心素养。
2. 通过实验探究活动,促进学生建立实验目的、实验证据、实验结果之间的关
系,提升“证据推理与模型认知”化学学科核心素养。
3. 通过实验探究活动,评价学生:提取情境信息的能力水平(部分/全部);选
取试剂设计实验方案的能力水平(选取的试剂不合适/正确选取试剂);实验
目的、实验证据、实验结论之间的推理分析能力水平(三者之间的系统证据
推理/局部的证据推理/缺少证据的推理过程)
实验方案设计
03
实验方案设计
阅读资料卡片
找出影响因素
设计实验方案
进行实验探究
优化制备方法
资料卡片1:根据调色原理可知,白色和红褐色的调和色不可能是浅绿色、灰绿色,即灰绿色沉淀不可能是氢氧化亚铁和氢氧化铁的混合物。
资料卡片2:现有研究成果表明, Fe(OH)2 沉淀物吸附反应体系中绿色的Fe2+ 是Fe(OH)2 白色沉淀变为灰绿色沉淀的真正原因。
资料卡片3:氧气的和Fe3+的存在会使形成的Fe(OH)2沉淀不纯净,更容易吸附Fe2+ 而使沉淀颜色变化。
资料卡片4:实验还发现采用FeCl2 与FeSO4 溶液分别制备Fe(OH)2 沉淀也有所差异,前者得到Fe(OH)2 保持白色的时间更久。
【问题1】选择哪两种试剂进行反应?
【问题2】灰绿色沉淀形成原因是什么?
【问题3】影响灰绿色沉淀产生的因素有哪些?
设计意图:在实验目的的引领下,培养学生对情境中信息的提取和理解能力,启发学生进行深度思考,培养学生的深度思维,充分挖掘学生潜力。
实验方案设计
阅读资料卡片
找出影响因素
设计实验方案
进行实验探究
优化制备方法
设计意图:能根据实验特点设计实验方案,并对实验方案进行评价反思,在不断优化过程中,发现自己存在的问题,进一步体会变量控制的重要作用。
实验方案设计
阅读资料卡片
找出影响因素
设计实验方案
进行实验探究
优化制备方法
实验数据处理
04
实验数据处理
滴加顺序(FeCl2溶液浓度为0.1 mol/L,NaOH溶液浓度为8mol/L )
FeCl2
FeCl2
FeCl2
NaOH
NaOH
5min后
√
实验结论:FeCl2溶液中存在大量Fe2+,容易吸附到白色沉淀表面,滴加顺序应选择在NaOH溶液中滴加FeCl2溶液。
实验现象:在 NaOH溶液中滴加FeCl2溶液时,生成白色沉淀悬浮在溶液中,一段时间后仍为白色。
在FeCl2溶液中滴加NaOH溶液时,生成白色沉淀迅速变为灰绿色,最后变为深绿色。
设计意图:通过对比现象,引导学生找出现象背后的原因,引发深度思考,实现能力进阶。
FeCl2
NaOH
实验数据处理
FeCl2溶液浓度(在10mL 饱和NaOH溶液中滴加5mL不同浓度的FeCl2溶液)
0.05 mol/L
0.1 mol/L
0.4 mol/L
√
实验现象:0.4 mol/L:产生灰绿色沉淀且一段时间后沉淀上层变为深绿色,0.2mol/L:产生浅灰绿色沉淀;0.1 mol/L:产生白色沉淀;0.05 mol/L:产生白色沉淀,量少。
实验结论:FeCl2浓度越小,越容易制得白色沉淀,但浓度小生成的沉淀少,且结构不紧密,不利于观察,最终选择FeCl2浓度为0.1mol/L。
0.2 mol/L
实验数据处理
NaOH溶液浓度(在10mL 不同浓度的NaOH溶液中滴加5mL 0.2mol/L的FeCl2溶液)
饱和
8mol/L
4 mol/L
1min
5min
√
实验现象:饱和溶液:产生白色沉淀;8mol/L:产生白色沉淀;4 mol/L:产生浅灰绿色沉淀。
实验结论:氢氧化钠浓度越大,越容易制得白色沉淀,且结构紧密,最终选择氢氧化钠饱和溶液。
实验数据处理
条件选择
实验探究发现,制备氢氧化亚铁的最佳条件为:在10mL 饱和NaOH溶液中滴加5mL 0.1mol/L FeCl2溶液。
1min
5min
实验数据处理
优化制备方法
实验数据处理
优化制备方法
时间t/min
教学评价与反思
05
教学评价与反思
锻炼了学生对情境中信息的提取和处理能力,自主设计实验方案,并进行实验探究,深度参与学习过程,深刻体会了实验条件控制对完成实验探究活动的作用。
1
已有
技能
使学生从本质上明白了灰绿色物质形成的原因,控制变量的唯一找出制备白色沉淀的方法,不仅落实了学科知识,还充分发挥了探究性实验的育人功能,培养了学生化学核心素养。
2
应该更加注重问题的引导,让学生自主思考回答,重视学生的探究过程,引导学生深入思考。
3
汇报完毕
敬请批评指正
同课章节目录
